文档内容
通关 14 有机合成与推断
目录
【高考预测】预测考向,总结常考点及应对的策略
【技法必备】提供方法技巧,解决问题策略
【误区点拨】点拨常见的易错点
【抢分通关】分析命题热点,把握解题技巧,精选名校模拟题
概率预测 ☆ ☆ ☆ ☆ ☆
题型预测 主观填空题 ☆ ☆ ☆ ☆ ☆
考向预测 有机物的推断、有机物的合成的综合分析及应用
有机化学的结构与性质是有机化学的基础知识,涉及有机物的基本概念,有机物的组成与结构、有机反应
类型、同分异构体的书写及判断,官能团的结构与性质、常见有机物的检验与鉴别等。在近几年的高考中
题型主要为选择题,通常以药物、材料、新物质的合成为载体考查有机化学的核心知识。涉及的常见考点
如下:有机物结构简式的确定、官能团的名称、反应类型的判断、有机物的命名、化学方程式的书写、同
分异构体的分析和书写等,但知识点覆盖面广,侧重考查对知识的理解及综合运用能力。高考非选择题通
常以药物、材料、新物质的合成为背景,根据合成路线命题形式总体可分为三类:第一类是有机推断型,
即在合成路线中各物质的结构简式是未知的,需要结合反应条件、分子式、目标产物、题给信息等进行推
断;第二类是结构已知型,即合成路线中各物质的结构简式是已知的,此类试题中所涉及的有机物大多是
陌生且比较复杂的,需要根据前后的变化来分析其反应特点;第三类是“半推半知”型,即合成路线中部分
有机物的结构简式是已知的,部分是未知的,审题时需要结合条件及已知结构去推断未知有机物的结构。
考查的知识点相对比较稳定,有结构简式的推断、官能团的名称、有机物命名、反应类型的判断、有机化
学方程式的书写、同分异构体数目的判断、结合核磁共振氢谱书写指定有机物的结构简式、合成路线设计
等。
技法1 有机推断题的突破口——题眼
有机推断解题的突破口也叫做题眼,题眼可以是一种特殊的现象、反应、性质、用途或反应条件,或在框
图推断试题中,有几条线同时经过一种物质,往往这就是题眼。
题眼1、有机反应条件
条件1、 这是烷烃和烷基中的氢被取代的反应条件。如: 烷烃的取代;芳香烃或芳香族化合物侧链烷基的取代;
不饱和烃中烷基的取代。
①
③
条件2、 这是乙醇脱水生成乙烯的反应条件。条件3、 或 为不饱和键加氢反应的条件,包括:-C=C-、=C=O、-C≡C-的加成。
条件4、 是 醇消去H2O生成烯烃或炔烃; 醇分子间脱水生成醚的反应; 酯
① ② ③
化反应的反应条件。
条件5、 是 卤代烃水解生成醇; 酯类水解反应的条件。
① ②
条件6、 是卤代烃消去HX生成不饱和烃的反应条件。
条件7、 是 酯类水解(包括油脂的酸性水解); 糖类的水解
① ②
条件8、 或 是醇氧化的条件。
条件9、 或 是不饱和烃加成反应的条件。
条件10、 是苯的同系物侧链氧化的反应条件(侧链烃基被氧化成-COOH)。
条件11、显色现象:苯酚遇FeCl3 溶液显紫色;与新制Cu(OH)
2
悬浊液反应的现象:1、沉淀溶解,出
现深蓝色溶液则有多羟基存在;2、沉淀溶解,出现蓝色溶液则有羧基存在;3、加热后有红色沉淀出现则
有醛基存在。
题眼2、有机物的性质
1、能使溴水褪色的有机物通常含有“—C=C—”、“—C≡C—”或“—CHO”。
2、能使酸性高锰酸钾溶液褪色的有机物通常含有“—C=C—”或“—C≡C—”、“—CHO”或为“苯的同系
物”、
醇类、酚类。
3、能发生加成反应的有机物通常含有“—C=C—”、“—C≡C—”、“—CHO”或“苯环”,其中“—
CHO”和“苯环”只能与H2 发生加成反应。
4、能发生银镜反应或能与新制的Cu(OH)2 悬浊液反应的有机物必含有“—CHO”。
5、能与钠反应放出H2 的有机物必含有“—OH”、“—COOH”。
6、能与Na2CO3 或NaHCO3 溶液反应放出CO2 或使石蕊试液变红的有机物中必含有-COOH。
7、能发生消去反应的有机物为醇或卤代烃。
8、能发生水解反应的有机物为卤代烃、酯、糖或蛋白质。9、遇FeCl3 溶液显紫色的有机物必含有酚羟基。
10、能发生连续氧化的有机物是伯醇或乙烯,即具有“—CH2OH”的醇。比如有机物A能发生如下反应:
A→B→C,则A应是具有“—CH2OH”的醇,B就是醛,C应是酸。
11 、 加 入 浓 溴 水 出 现 白 色 沉 淀 的 有 机 物 含 有 酚 羟 基 、 遇 碘 变 蓝 的 有 机 物 为 淀 粉
遇浓硝酸变黄的有机物为蛋白质
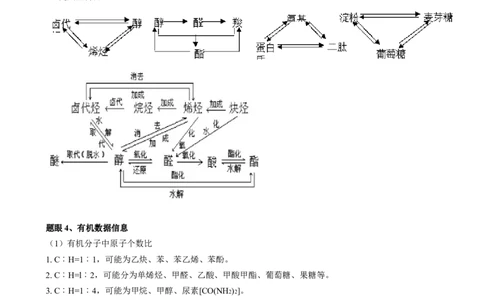
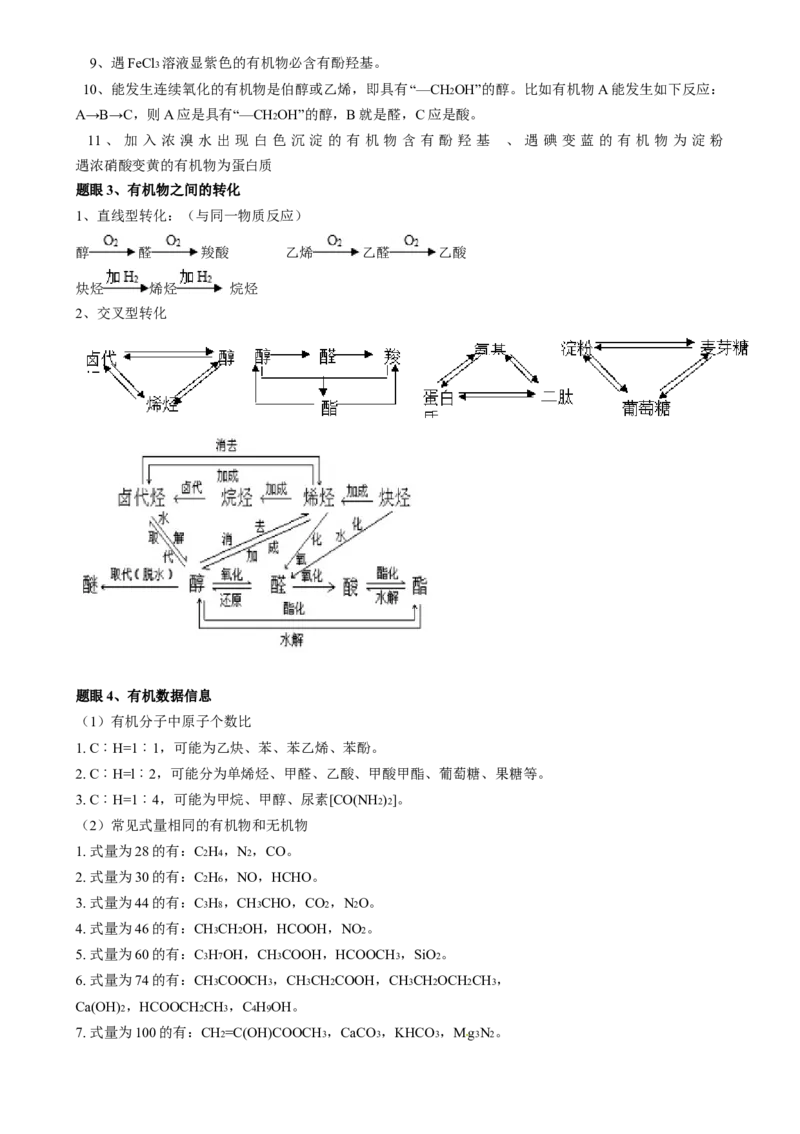
题眼3、有机物之间的转化
1、直线型转化:(与同一物质反应)
醇 醛 羧酸 乙烯 乙醛 乙酸
炔烃 烯烃 烷烃
2、交叉型转化
题眼4、有机数据信息
(1)有机分子中原子个数比
1. C︰H=1︰1,可能为乙炔、苯、苯乙烯、苯酚。
2. C︰H=l︰2,可能分为单烯烃、甲醛、乙酸、甲酸甲酯、葡萄糖、果糖等。
3. C︰H=1︰4,可能为甲烷、甲醇、尿素[CO(NH2)2]。
(2)常见式量相同的有机物和无机物
1. 式量为28的有:C2H4 ,N2 ,CO。
2. 式量为30的有:C2H6 ,NO,HCHO。
3. 式量为44的有:C3H8 ,CH3CHO,CO2 ,N2O。
4. 式量为46的有:CH3CH2OH,HCOOH,NO2 。
5. 式量为60的有:C3H7OH,CH3COOH,HCOOCH3 ,SiO2 。
6. 式量为74的有:CH3COOCH3 ,CH3CH2COOH,CH3CH2OCH2CH3 ,
Ca(OH)2 ,HCOOCH2CH3 ,C4H9OH。
7. 式量为100的有:CH2=C(OH)COOCH3 ,CaCO3 ,KHCO3 ,Mg3N2 。8. 式量为120的有: C9H12(丙苯或三甲苯或甲乙苯),MgSO4 ,NaHSO4 ,KHSO3 ,CaSO3 ,NaH2PO4 ,
MgHPO4 ,FeS2 。
9. 式量为128的有:C9H20(壬烷),C10H8(萘)。
(3)有机反应数据信息
1、根据与H2 加成时所消耗H2 的物质的量进行突破:1mol=C=C=加成时需1molH2 ,1molHX,1mol—
C≡C—完全加成时需2molH2 ,1mol—CHO加成时需1molH2 ,而1mol苯环加成时需3molH2 。
2、含1mol—OH或1mol—COOH的有机物与活泼金属反应放出0.5molH2 。
3、含1mol—COOH的有机物与碳酸氢钠溶液反应放出1molCO2 。
4、1mol一元醇与足量乙酸反应生成1mol酯时,其相对分子质量将增加42。
1mol二元醇与足量乙酸反应生成酯时,其相对分子质量将增加84。
1mol一元酸与足量乙醇反应生成1mol酯时,其相对分子质量将增加28。
1mol二元酸与足量乙醇反应生成酯时,其相对分子质量将增加56。
5、1mol某酯A发生水解反应生成B和乙酸时,若A与B的相对分子质量相差42,则生成1mol乙酸。
6、由—CHO变为—COOH时,相对分子质量将增加16。
7、分子中与饱和链烃相比,若每少2个氢原子,则分子中可能含双键。
8、烃和卤素单质的取代:取代1 mol 氢原子,消耗1 mol 卤素单质(X2)。
9、1 mol —CHO对应2 mol Ag;或1 mol —CHO对应1 mol Cu2O。
题眼5 反应类型与官能团的关系:
反应类型 可能官能团
加成反应 C=C、C≡C、-CHO、羰基、苯环
加聚反应 C=C、C≡C
酯化反应 羟基或羧基
水解反应 -X、酯基、肽键 、多糖等
单一物质能发生缩聚
分子中同时含有羟基和羧基或羧基和胺基
反应
题眼6 特征反应现象:
反应的试剂 有机物 现象
(1)烯烃、二烯烃(2)炔烃 溴水褪色,且产物分层
与溴水反应 (3)醛 溴水褪色,且产物不分层
(4)苯酚 有白色沉淀生成
与酸性高 (1)烯烃、二烯烃(2)炔烃 高锰酸钾溶液均褪色
锰酸钾反应 (3)苯的同系物(4)醇(5)醛
(1)醇 放出气体,反应缓和
与金属钠反应 (2)苯酚 放出气体,反应速度较快
(3)羧酸 放出气体,反应速度更快
与氢氧化钠 (1)卤代烃 分层消失,生成一种有机物(2)苯酚 浑浊变澄清
反应 (3)羧酸 无明显现象
(4)酯 分层消失,生成两种有机物
与碳酸氢钠反应 羧酸 放出气体且能使石灰水变浑浊
(1)醛 有银镜或红色沉淀产生
银氨溶液或
(2)甲酸或甲酸钠 加碱中和后有银镜或红色沉淀产生
新制氢氧化铜
(3)甲酸酯 有银镜或红色沉淀生成
技法2 官能团的引入、消除与保护:
1、引入常见的官能团
引入官能团 有关反应
羟基-OH 烯烃与水加成,醛/酮加氢,卤代烃水解,酯的水解、醛的氧化
卤素原子(- 烃与X2取代,不饱和烃与HX或X2加成,醇与HX取代
X)
碳碳双键C=C 某些醇或卤代烃的消去,炔烃加氢
醛基-CHO 某些醇(-CH2OH)氧化,烯氧化,糖类水解,(炔水化)
羧基-COOH 醛氧化, 酯酸性水解, 羧酸盐酸化,(苯的同系物被强氧化剂氧化)
酯基-COO- 酯化反应
2、有机合成中的成环反应
加成成环:不饱和烃小分子加成(信息题);
二元醇分子间或分子内脱水成环;
①
二元醇和二元酸酯化成环;
②
羟基酸、氨基酸通过分子内或分子间脱去小分子的成环。
③
3、有机合成中的增减碳链的反应
④
⑴增加碳链的反应:
有机合成题中碳链的增长,一般会以信息形式给出,常见方式为有机物与 HCN反应或者不饱和化合物间
的聚合、 酯化反应 、 加聚反应、 缩聚反应
⑵减少碳链的反应:
① ② ③
水解反应:酯的水解,糖类、蛋白质的水解;
裂化和裂解反应;
①
氧化反应:燃烧,烯催化氧化(信息题),脱羧反应(信息题)。
②
4、官能团的消除
通过加成消除不饱和键;
通过加成或氧化等消除醛基(—CHO);
①
通过消去、氧化或酯化反应等消除羟基(—OH)
②
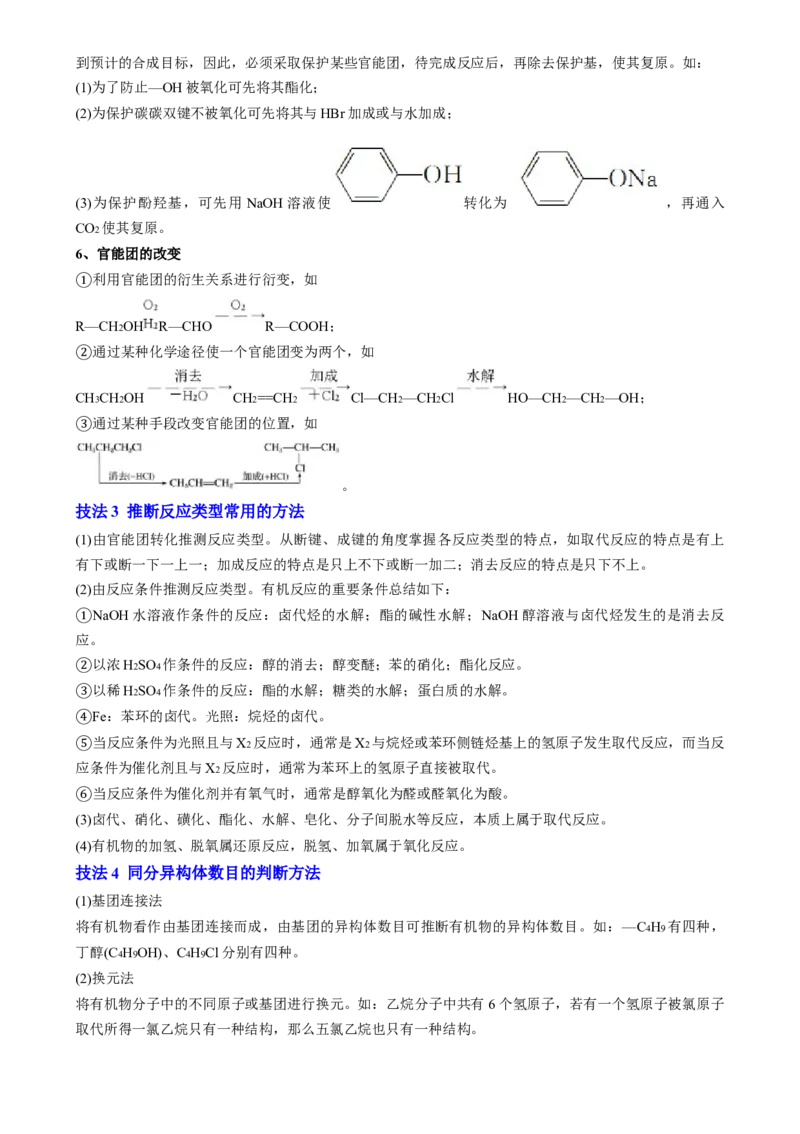
5、官能团的保护
③
在有机合成中,某些不希望起反应的官能团,在反应试剂或反应条件的影响下发生副反应,这样就不能达到预计的合成目标,因此,必须采取保护某些官能团,待完成反应后,再除去保护基,使其复原。如:
(1)为了防止—OH被氧化可先将其酯化;
(2)为保护碳碳双键不被氧化可先将其与HBr加成或与水加成;
(3)为保护酚羟基,可先用NaOH溶液使 转化为 ,再通入
CO2 使其复原。
6、官能团的改变
利用官能团的衍生关系进行衍变,如
①
R—CH2OH R—CHO R—COOH;
通过某种化学途径使一个官能团变为两个,如
②
CH3CH2OH CH2==CH2 Cl—CH2—CH2Cl HO—CH2—CH2—OH;
通过某种手段改变官能团的位置,如
③
。
技法3 推断反应类型常用的方法
(1)由官能团转化推测反应类型。从断键、成键的角度掌握各反应类型的特点,如取代反应的特点是有上
有下或断一下一上一;加成反应的特点是只上不下或断一加二;消去反应的特点是只下不上。
(2)由反应条件推测反应类型。有机反应的重要条件总结如下:
NaOH水溶液作条件的反应:卤代烃的水解;酯的碱性水解;NaOH醇溶液与卤代烃发生的是消去反
应。
①
以浓H2SO4 作条件的反应:醇的消去;醇变醚;苯的硝化;酯化反应。
②
以稀H2SO4 作条件的反应:酯的水解;糖类的水解;蛋白质的水解。
Fe:苯环的卤代。光照:烷烃的卤代。
③
④
当反应条件为光照且与X2 反应时,通常是X2 与烷烃或苯环侧链烃基上的氢原子发生取代反应,而当反
⑤
应条件为催化剂且与X2 反应时,通常为苯环上的氢原子直接被取代。
当反应条件为催化剂并有氧气时,通常是醇氧化为醛或醛氧化为酸。
(3)卤代、硝化、磺化、酯化、水解、皂化、分子间脱水等反应,本质上属于取代反应。
⑥
(4)有机物的加氢、脱氧属还原反应,脱氢、加氧属于氧化反应。
技法4 同分异构体数目的判断方法
(1)基团连接法
将有机物看作由基团连接而成,由基团的异构体数目可推断有机物的异构体数目。如:—C4H9 有四种,
丁醇(C4H9OH)、C4H9Cl分别有四种。
(2)换元法
将有机物分子中的不同原子或基团进行换元。如:乙烷分子中共有6个氢原子,若有一个氢原子被氯原子
取代所得一氯乙烷只有一种结构,那么五氯乙烷也只有一种结构。(3)等效氢原子法(又称对称法)
有机物分子中有多少种等效氢原子,其一元取代物就有多少种,从而确定同分异构体数目的方法。
分子中等效氢原子有如下情况:
分子中同一个碳上的氢原子等效;
同一个碳上的甲基氢原子等效;
①
分子中处于镜面对称位置(相当于平面镜成像时)上的氢原子是等效的。
②
(4)定1移2法
③
分析二元取代物的方法,先固定一个取代基的位置,再移动另一取代基的位置,从而可确定同分异构体的
数目。如分析C3H6Cl2 的同分异构体,先固定其中一个氯原子的位置,移动另外一个氯原子。
同分异构体数目的判断,可固定一个取代基的位置,再移动另一取代基的位置以确定同分异构体的数目。
技法5 限定条件下同分异构体的书写技巧
1)确定基团
明确书写什么物质的同分异构体,该物质的组成情况怎么样。解读限制条件,从性质联想结构,将物质分
裂成一个个基团,基团可以是官能团,也可是烃基(尤其是官能团之外的饱和碳原子)。
2)组装分子
要关注分子的结构特点,包括几何特征和化学特征。几何特征指所组装的分子是空间结构还是平面结构,
有无对称性。化学特征包括等效氢。
3)含苯环同分异构体数目的确定技巧
(1)若苯环上连有2个取代基,其结构有邻、间、对3种。
(2)若苯环上连有3个相同的取代基,其结构有3种。
(3)若苯环上连有—X、—X、—Y 3个取代基,其结构有6种。
(4)若苯环上连有—X、—Y、—Z 3个不同的取代基,其结构有10种。
4)酯( )的同分异构体书写:
(1)按—R中所含碳原子数由少到多,—R′中所含碳原子数由多到少的顺序书写。
(2)用组合法推断
先确定一基团同分异构体的数目,再确定另一基团同分异构体的数目,从而确定两基团组合后同分异构体
数目的方法。如饱和一元酯 ,—R1 有m种结构,—R2 有n种结构,共有m×n种酯的结构。
实例:分子式为C9H18O2 的酯在酸性条件下水解得到的两种有机物的相对分子质量相等,则形成该酯的酸
为C3H7COOH(2种结构),醇为C5H11OH(8种结构),故该酯的结构共有2×8=16种。
技法6 常用的合成路线
有机合成往往要经过多步反应才能完成,因此确定有机合成的途径和路线时,要进行合理选择。
(1)一元合成路线
R—CH=CH2 卤代烃 一元醇 一元醛 一元羧酸 酯
(2)二元合成路线
CH2 CH2 CH2X—CH2X CH2OH—CH2OHHOOC—COOH 链酯、环酯、聚酯
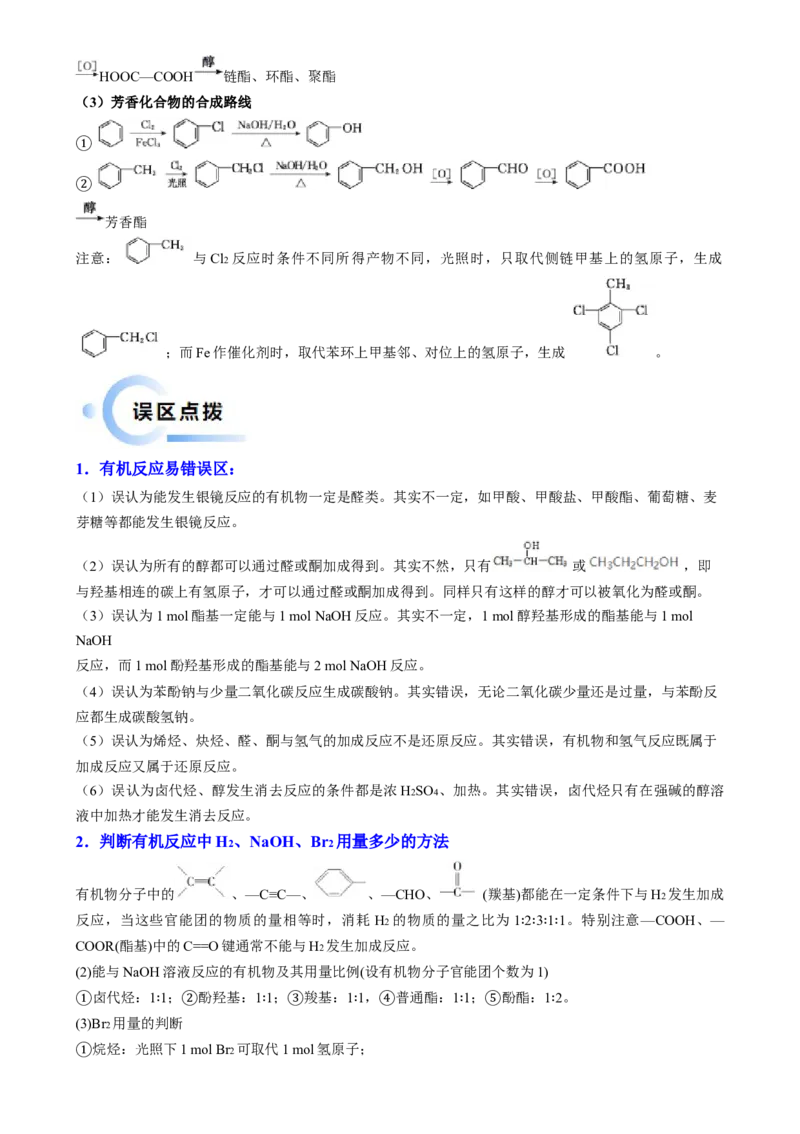
(3)芳香化合物的合成路线
①
②
芳香酯
注意: 与Cl2 反应时条件不同所得产物不同,光照时,只取代侧链甲基上的氢原子,生成
;而Fe作催化剂时,取代苯环上甲基邻、对位上的氢原子,生成 。
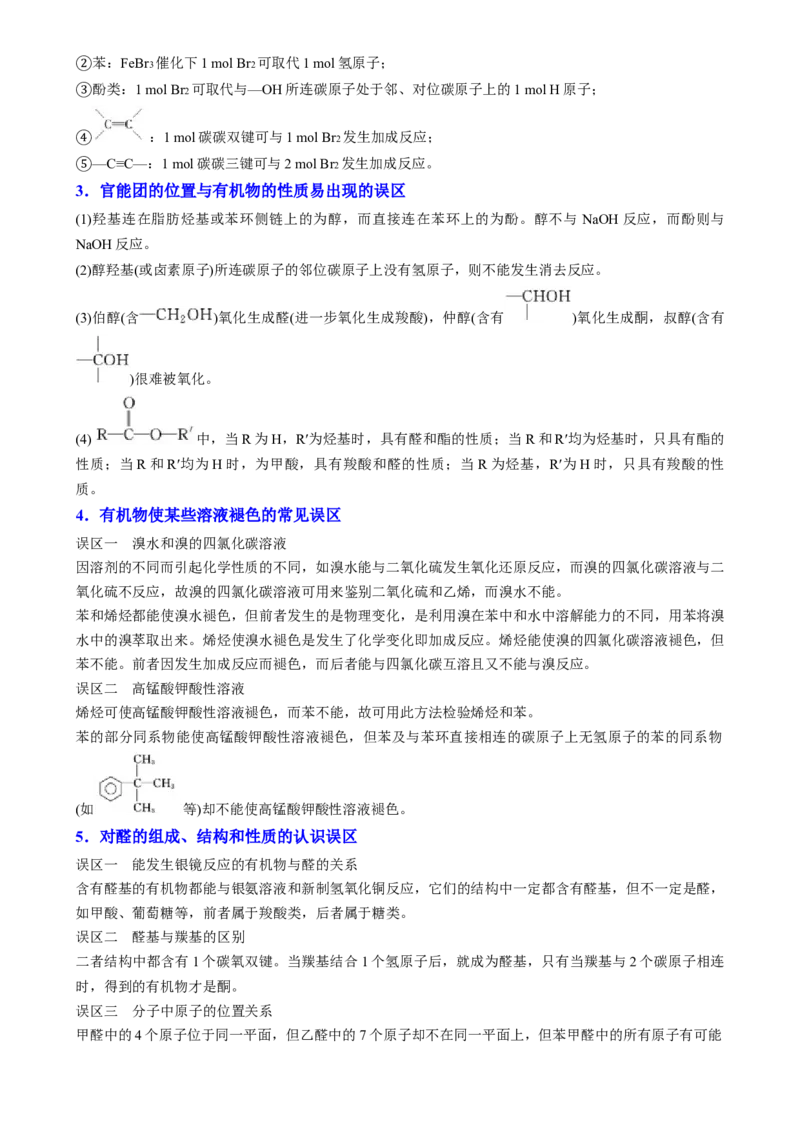
1.有机反应易错误区:
(1)误认为能发生银镜反应的有机物一定是醛类。其实不一定,如甲酸、甲酸盐、甲酸酯、葡萄糖、麦
芽糖等都能发生银镜反应。
(2)误认为所有的醇都可以通过醛或酮加成得到。其实不然,只有 或 ,即
与羟基相连的碳上有氢原子,才可以通过醛或酮加成得到。同样只有这样的醇才可以被氧化为醛或酮。
(3)误认为1 mol酯基一定能与1 mol NaOH反应。其实不一定,1 mol醇羟基形成的酯基能与1 mol
NaOH
反应,而1 mol酚羟基形成的酯基能与2 mol NaOH反应。
(4)误认为苯酚钠与少量二氧化碳反应生成碳酸钠。其实错误,无论二氧化碳少量还是过量,与苯酚反
应都生成碳酸氢钠。
(5)误认为烯烃、炔烃、醛、酮与氢气的加成反应不是还原反应。其实错误,有机物和氢气反应既属于
加成反应又属于还原反应。
(6)误认为卤代烃、醇发生消去反应的条件都是浓H2SO4 、加热。其实错误,卤代烃只有在强碱的醇溶
液中加热才能发生消去反应。
2.判断有机反应中H 、NaOH、Br 用量多少的方法
2 2
有机物分子中的 、—C≡C—、 、—CHO、 (羰基)都能在一定条件下与H2 发生加成
反应,当这些官能团的物质的量相等时,消耗 H2 的物质的量之比为1 2 3 1 1。特别注意—COOH、—
COOR(酯基)中的C==O键通常不能与H2 发生加成反应。
∶ ∶ ∶ ∶
(2)能与NaOH溶液反应的有机物及其用量比例(设有机物分子官能团个数为1)
卤代烃:1 1; 酚羟基:1 1; 羧基:1 1, 普通酯:1 1; 酚酯:1 2。
①
(3)Br2 用量的判
∶
断
② ∶ ③ ∶ ④ ∶ ⑤ ∶
烷烃:光照下1 mol Br2 可取代1 mol氢原子;
①苯:FeBr3 催化下1 mol Br2 可取代1 mol氢原子;
②
酚类:1 mol Br2 可取代与—OH所连碳原子处于邻、对位碳原子上的1 mol H原子;
③
:1 mol碳碳双键可与1 mol Br2 发生加成反应;
④
—C≡C—:1 mol碳碳三键可与2 mol Br2 发生加成反应。
3.官能团的位置与有机物的性质易出现的误区
⑤
(1)羟基连在脂肪烃基或苯环侧链上的为醇,而直接连在苯环上的为酚。醇不与 NaOH反应,而酚则与
NaOH反应。
(2)醇羟基(或卤素原子)所连碳原子的邻位碳原子上没有氢原子,则不能发生消去反应。
(3)伯醇(含 )氧化生成醛(进一步氧化生成羧酸),仲醇(含有 )氧化生成酮,叔醇(含有
)很难被氧化。
(4) 中,当R为H,R′为烃基时,具有醛和酯的性质;当R和R′均为烃基时,只具有酯的
性质;当R和R′均为H时,为甲酸,具有羧酸和醛的性质;当R为烃基,R′为H时,只具有羧酸的性
质。
4.有机物使某些溶液褪色的常见误区
误区一 溴水和溴的四氯化碳溶液
因溶剂的不同而引起化学性质的不同,如溴水能与二氧化硫发生氧化还原反应,而溴的四氯化碳溶液与二
氧化硫不反应,故溴的四氯化碳溶液可用来鉴别二氧化硫和乙烯,而溴水不能。
苯和烯烃都能使溴水褪色,但前者发生的是物理变化,是利用溴在苯中和水中溶解能力的不同,用苯将溴
水中的溴萃取出来。烯烃使溴水褪色是发生了化学变化即加成反应。烯烃能使溴的四氯化碳溶液褪色,但
苯不能。前者因发生加成反应而褪色,而后者能与四氯化碳互溶且又不能与溴反应。
误区二 高锰酸钾酸性溶液
烯烃可使高锰酸钾酸性溶液褪色,而苯不能,故可用此方法检验烯烃和苯。
苯的部分同系物能使高锰酸钾酸性溶液褪色,但苯及与苯环直接相连的碳原子上无氢原子的苯的同系物
(如 等)却不能使高锰酸钾酸性溶液褪色。
5.对醛的组成、结构和性质的认识误区
误区一 能发生银镜反应的有机物与醛的关系
含有醛基的有机物都能与银氨溶液和新制氢氧化铜反应,它们的结构中一定都含有醛基,但不一定是醛,
如甲酸、葡萄糖等,前者属于羧酸类,后者属于糖类。
误区二 醛基与羰基的区别
二者结构中都含有1个碳氧双键。当羰基结合1个氢原子后,就成为醛基,只有当羰基与2个碳原子相连
时,得到的有机物才是酮。
误区三 分子中原子的位置关系
甲醛中的4个原子位于同一平面,但乙醛中的7个原子却不在同一平面上,但苯甲醛中的所有原子有可能在一个平面上。
误区四 醛也能与硝酸银溶液反应
醛能与银氨溶液反应,往往认为其一定能与硝酸银溶液反应,因为硝酸银溶液中c(Ag+)更大,氧化性应该
更强。但是忽略了银镜反应必须在碱性条件下进行。另外,醛能与新制氢氧化铜悬浊液反应,但却不能与
硫酸铜溶液反应,也不能与长久放置的氢氧化铜反应。
6.巧辨同分异构体,避免限误区
(1)判断取代产物同分异构体的数目。其分析方法是分析有机物的结构特点,确定有机物中氢原子的种
类,再确定取代产物同分异构体的数目。
(2)判断有机物是否互为同分异构体。紧扣定义: “同分”指的是分子式必须相同,而不是相对分子质
量相同,相对分子质量相同的化合物不一定互为同分异构体。 “结构不同”指的是碳链骨架不同,或官
①
能团在碳链上的位置不同,或官能团种类不同。在解题时对“结构不同”的判断显得更为关键。
②
(3)限定条件(或范围)书写或补写同分异构体。解题时要看清所限定的条件(或范围),分析给定的
有机物的结构,对其碳链进行调整,或对官能团位置进行调整,或对官能团类别进行调整,进而写出同分
异构体。如果是补写同分异构体,则要分析已知的同分异构体的结构特点,通过对比联想找出规律后再进
行补写,同时要注意碳原子的四价原则和对官能团存在位置的要求等。
(4)在书写同分异构体时务必注意常见原子的价键数,例如在有机物分子中碳原子的价键数为 4,氧原
子的价键数为2,氮原子的价键数为3,卤原子、氢原子的价键数为1,不足或超过这些价键数的结构都
是不存在的。
(5)书写要有序进行,如书写酯类物质的同分异构体时,可采用逐一增加碳原子的方法。如C8H8O2 含苯
环的属于酯类的同分异构体为甲酸某酯: (邻、间、对);
乙酸某酯:
。
7.有机合成综合题中的常见误区
误区一 转化缺乏依据
在所给合成路线中,有时存在一步或两步的变化是中学有机化学中未曾学习过的,此时推断过程往往难以
进行下去。在这种情况下,应该结合变化前后两种有机物在碳链结构、官能团等方面的差异去寻找突破
口,切勿主观臆造化学反应使转化缺乏依据。
误区二 混淆反应条件
有机化学反应大多需要在一定条件下才能进行,有些条件只是在浓度上的差异,如酯化反应一般用浓硫
酸,而酯的水解一般用稀硫酸即可;卤代烃的取代反应需在氢氧化钠水溶液中进行,而卤代烃的消去反应
则需
在氢氧化钠醇溶液中进行等。有些催化剂可能是与反应物发生反应的生成物,如苯的卤代反应,一般加入
铁作催化剂,而实际起催化作用的是卤化铁,有时题目给出了卤化铁,但学生由于思维定势,就会出现
错误。
误区三 忽视相对分子质量的变化
化学反应一定遵守质量守恒(原子守恒)定律。有机化学反应中常有无机小分子(如水分子)参加或生成,若忽视反应前后有机物相对分子质量变化这一重要条件,就会使问题的解决变得困难。
误区四 忽视题给隐含信息
解决题目问题的某些条件往往隐含在合成路线中或在题给的需要学生解决的问题中,由于没有认真审题而
忽略了这些信息,往往导致题目的问题不能解决。
【热点一】结构未知型有机推断的综合考查
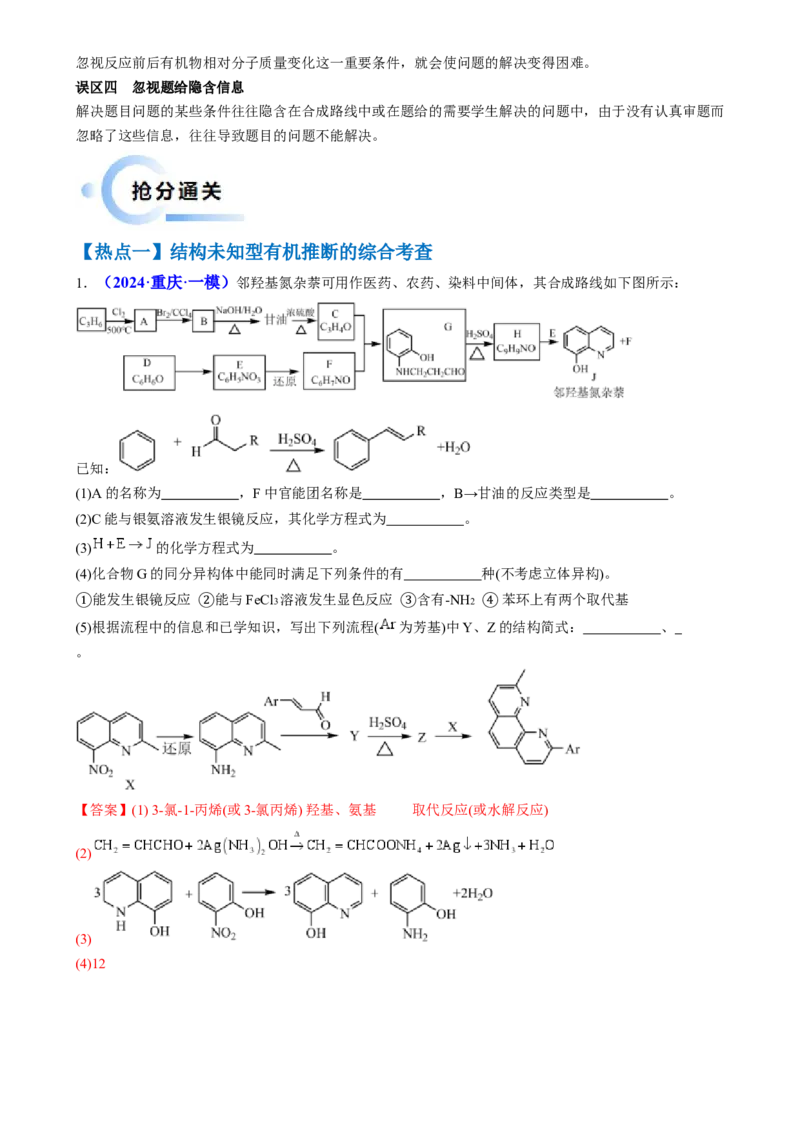
1.(2024·重庆·一模)邻羟基氮杂萘可用作医药、农药、染料中间体,其合成路线如下图所示:
已知:
(1)A的名称为 ,F中官能团名称是 ,B→甘油的反应类型是 。
(2)C能与银氨溶液发生银镜反应,其化学方程式为 。
(3) 的化学方程式为 。
(4)化合物G的同分异构体中能同时满足下列条件的有 种(不考虑立体异构)。
能发生银镜反应 能与FeCl3 溶液发生显色反应 含有-NH2 苯环上有两个取代基
①(5)根据流程中的信息
②
和已学知识,写出下列流程( 为
③
芳基)中Y、 ④Z的结构简式: 、
。
【答案】(1) 3-氯-1-丙烯(或3-氯丙烯) 羟基、氨基 取代反应(或水解反应)
(2)
(3)
(4)12(5) 【分析】C3H6 为CH2=CHCH3 ,与Cl2 在500 下发生取
代反应,生成A为CH2=CHCH2Cl和HCl,CH2=CHCH2Cl与Br2 的CCl4 溶液发生加成反应,生
℃
成B为
BrCH2CHBrCH2Cl,在NaOH水溶液中发生水解反应,生成甘油HOCH2CH(OH)CH2OH,甘油在浓硫酸、
∆条件下发生消去反应,生成C的分子式为C3H4O,由G的结构简式,可确定C为CH2=CHCHO;由G的
结构简式,可确定D为 ,E为 ,F为 ;由G的结构简式,参照H的
分子式,可确定H为 。
【解析】(1)A为CH2=CHCH2Cl,名称为3-氯-1-丙烯(或3-氯丙烯),F为 ,官能团名称是
羟基、氨基;B为BrCH2CHBrCH2Cl,在NaOH水溶液中发生水解反应,生成甘油HOCH2CH(OH)CH2OH
等,则B→甘油的反应类型是取代反应(或水解反应)。
(2)C为CH2=CHCHO,能与银氨溶液发生银镜反应,其化学方程式为
。
(3)H为 ,E为 ,J为 ,F为 ,则 的化学
方程式为 。
(4)化合物G为 ,同时满足下列条件:“ 能发生银镜反应 能与FeCl3 溶液发生
显色反应 含有-NH2 苯环上有两个取代基”的同分异构体
①
,分子中含有苯环、
②
酚-OH、-NH2 、-
CHO,则苯
③
环上的两个取
④
代基中,一个为酚-OH,另一个为-CH2CH(NH2)CHO、-CH(NH2)CH2CHO、-CH(CHO)CH2NH2 、 ,两个取代基可分别位于苯环的邻、间、对位,共有4×3=12种。
(5)根据流程中C+E→G的信息和已学知识,可推出Y的结构简式: ,再依据
G→H的信息,可确定Z的结构简式为 。
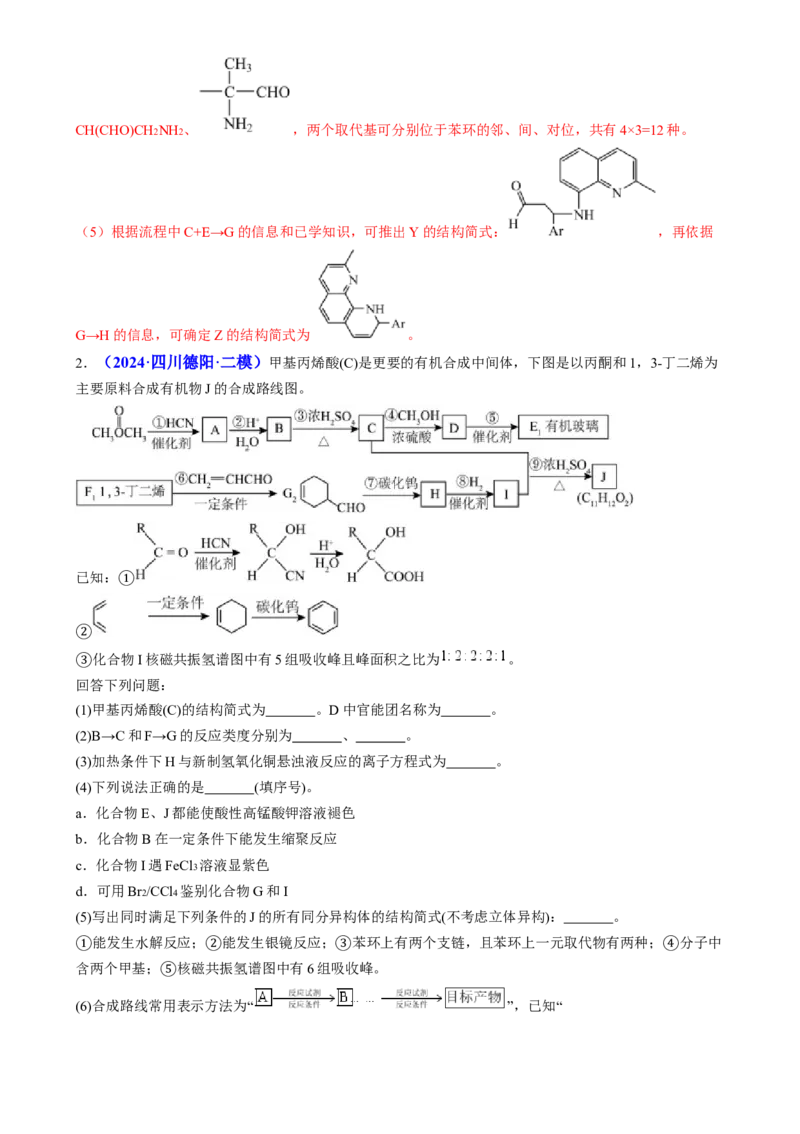
2.(2024·四川德阳·二模)甲基丙烯酸(C)是更要的有机合成中间体,下图是以丙酮和1,3-丁二烯为
主要原料合成有机物J的合成路线图。
已知:
①
②
化合物I核磁共振氢谱图中有5组吸收峰且峰面积之比为 。
回答下列问题:
③
(1)甲基丙烯酸(C)的结构简式为 。D中官能团名称为 。
(2)B→C和F→G的反应类度分别为 、 。
(3)加热条件下H与新制氢氧化铜悬浊液反应的离子方程式为 。
(4)下列说法正确的是 (填序号)。
a.化合物E、J都能使酸性高锰酸钾溶液褪色
b.化合物B在一定条件下能发生缩聚反应
c.化合物I遇FeCl3 溶液显紫色
d.可用Br2/CCl4 鉴别化合物G和I
(5)写出同时满足下列条件的J的所有同分异构体的结构简式(不考虑立体异构): 。
能发生水解反应; 能发生银镜反应; 苯环上有两个支链,且苯环上一元取代物有两种; 分子中
含两个甲基; 核磁共振氢谱图中有6组吸收峰。
① ② ③ ④
⑤
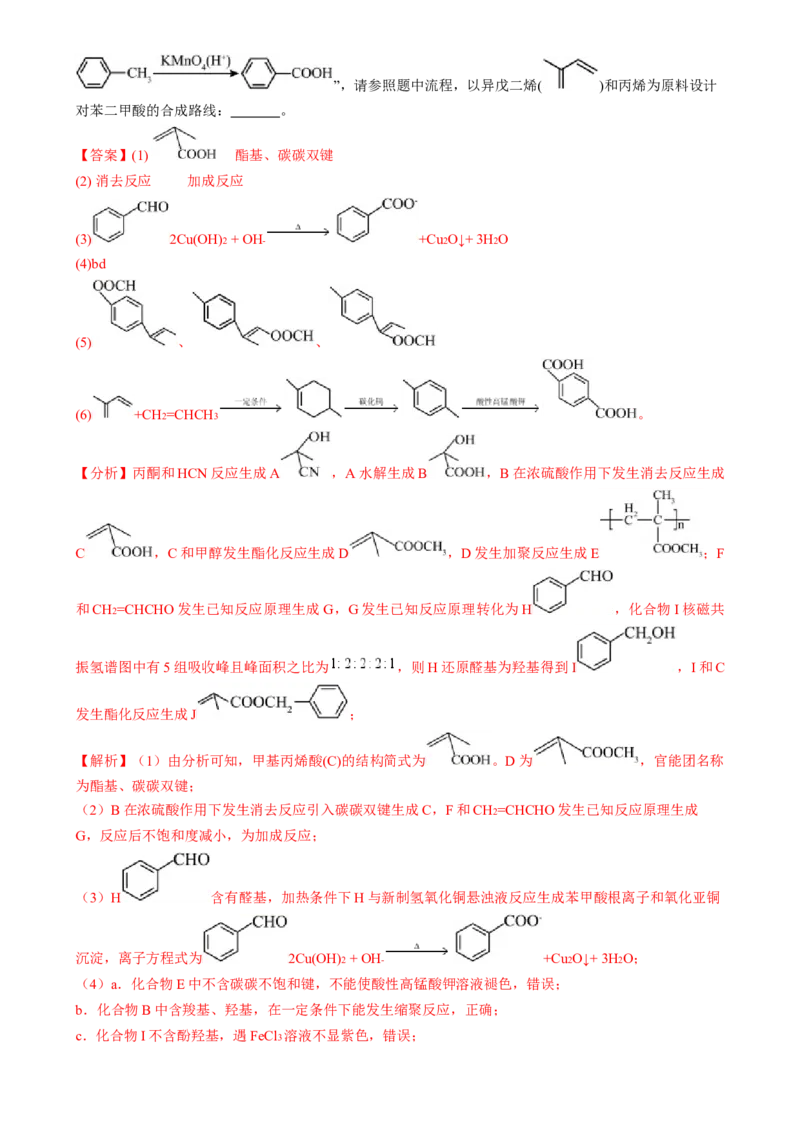
(6)合成路线常用表示方法为“ ”,已知“”,请参照题中流程,以异戊二烯( )和丙烯为原料设计
对苯二甲酸的合成路线: 。
【答案】(1) 酯基、碳碳双键
(2) 消去反应 加成反应
(3) 2Cu(OH)2 + OH- +Cu2O↓+ 3H2O
(4)bd
(5) 、 、
(6) +CH2=CHCH3 。
【分析】丙酮和HCN反应生成A ,A水解生成B ,B在浓硫酸作用下发生消去反应生成
C ,C和甲醇发生酯化反应生成D ,D发生加聚反应生成E ;F
和CH2=CHCHO发生已知反应原理生成G,G发生已知反应原理转化为H ,化合物I核磁共
振氢谱图中有5组吸收峰且峰面积之比为 ,则H还原醛基为羟基得到I ,I和C
发生酯化反应生成J ;
【解析】(1)由分析可知,甲基丙烯酸(C)的结构简式为 。D为 ,官能团名称
为酯基、碳碳双键;
(2)B在浓硫酸作用下发生消去反应引入碳碳双键生成C,F和CH2=CHCHO发生已知反应原理生成
G,反应后不饱和度减小,为加成反应;
(3)H 含有醛基,加热条件下H与新制氢氧化铜悬浊液反应生成苯甲酸根离子和氧化亚铜
沉淀,离子方程式为 2Cu(OH)2 + OH- +Cu2O↓+ 3H2O;
(4)a.化合物E中不含碳碳不饱和键,不能使酸性高锰酸钾溶液褪色,错误;
b.化合物B中含羧基、羟基,在一定条件下能发生缩聚反应,正确;
c.化合物I不含酚羟基,遇FeCl3 溶液不显紫色,错误;d.G含醛基、碳碳双键,能和溴的四氯化碳溶液反应使得溶液褪色,I含羟基不和溴的四氯化碳溶液反
应,可用Br2/CCl4 鉴别化合物G和I,正确;
故选bd;
(5)J ,除苯环外含有5个碳、2个氧、2个不饱和度,同时满足下列条件的J的所
有同分异构体的结构简式(不考虑立体异构):
能发生水解反应,则含有酯基; 能发生银镜反应,含有醛基; 苯环上有两个支链,且苯环上一元
取代物有两种,则两个取代基处于对位; 分子中含两个甲基; 核磁共振氢谱图中有6组吸收峰,则
① ② ③
④ ⑤
存在6种氢。故结构可以为: 、 、 ;
(6) 和丙烯发生已知反应原理生成 ,在碳化钨作用下转化为 ,甲基被酸性高
锰酸钾氧化为羧基得到 ,故流程为: +CH2=CHCH3
。
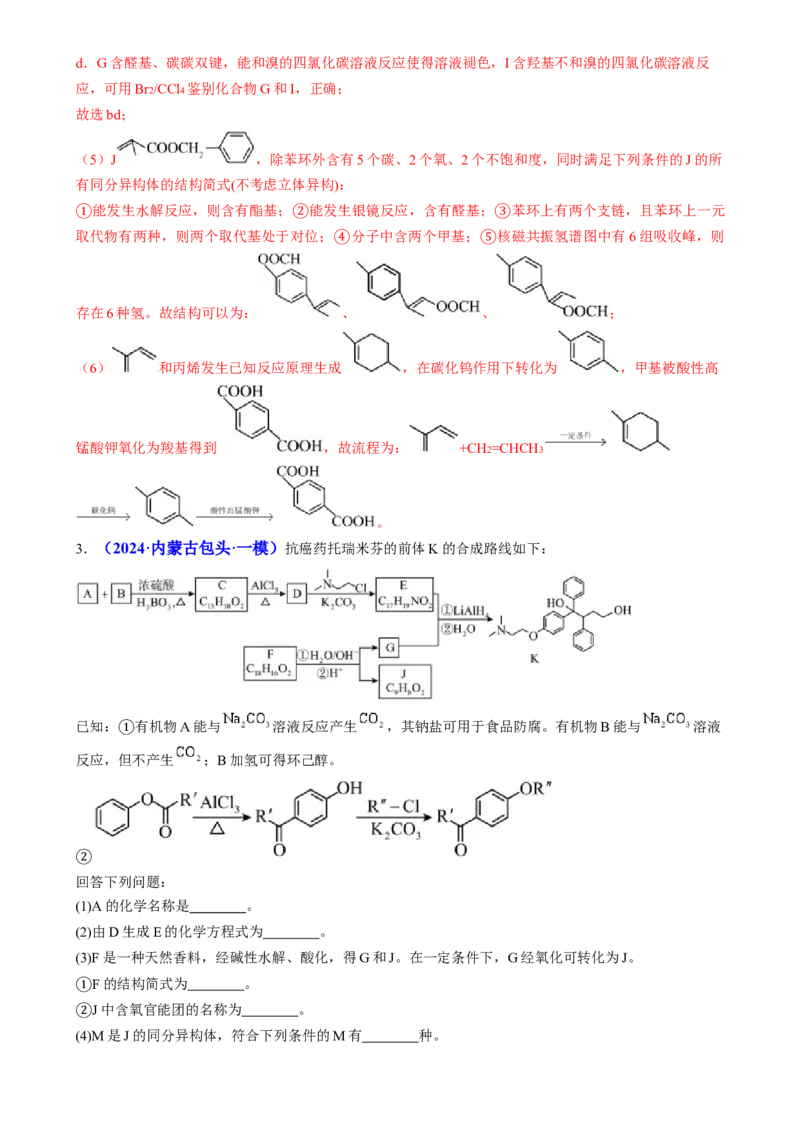
3.(2024·内蒙古包头·一模)抗癌药托瑞米芬的前体K的合成路线如下:
已知: 有机物A能与 溶液反应产生 ,其钠盐可用于食品防腐。有机物B能与 溶液
反应,①但不产生 ;B加氢可得环己醇。
回答下列问题:
②
(1)A的化学名称是 。
(2)由D生成E的化学方程式为 。
(3)F是一种天然香料,经碱性水解、酸化,得G和J。在一定条件下,G经氧化可转化为J。
F的结构简式为 。
J中含氧官能团的名称为 。
①
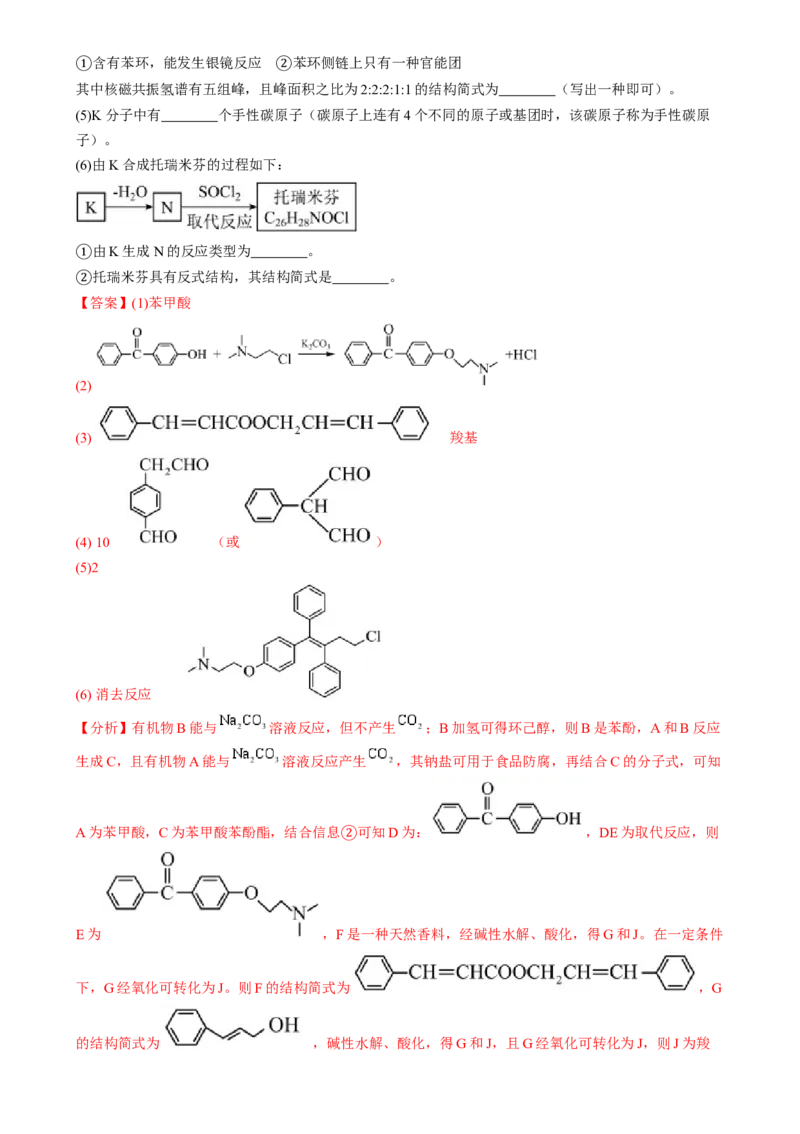
(4)M是J的同分异构体,符合下列条件的M有 种。
②含有苯环,能发生银镜反应 苯环侧链上只有一种官能团
其中核磁共振氢谱有五组峰,且峰面积之比为2:2:2:1:1的结构简式为 (写出一种即可)。
① ②
(5)K分子中有 个手性碳原子(碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳原
子)。
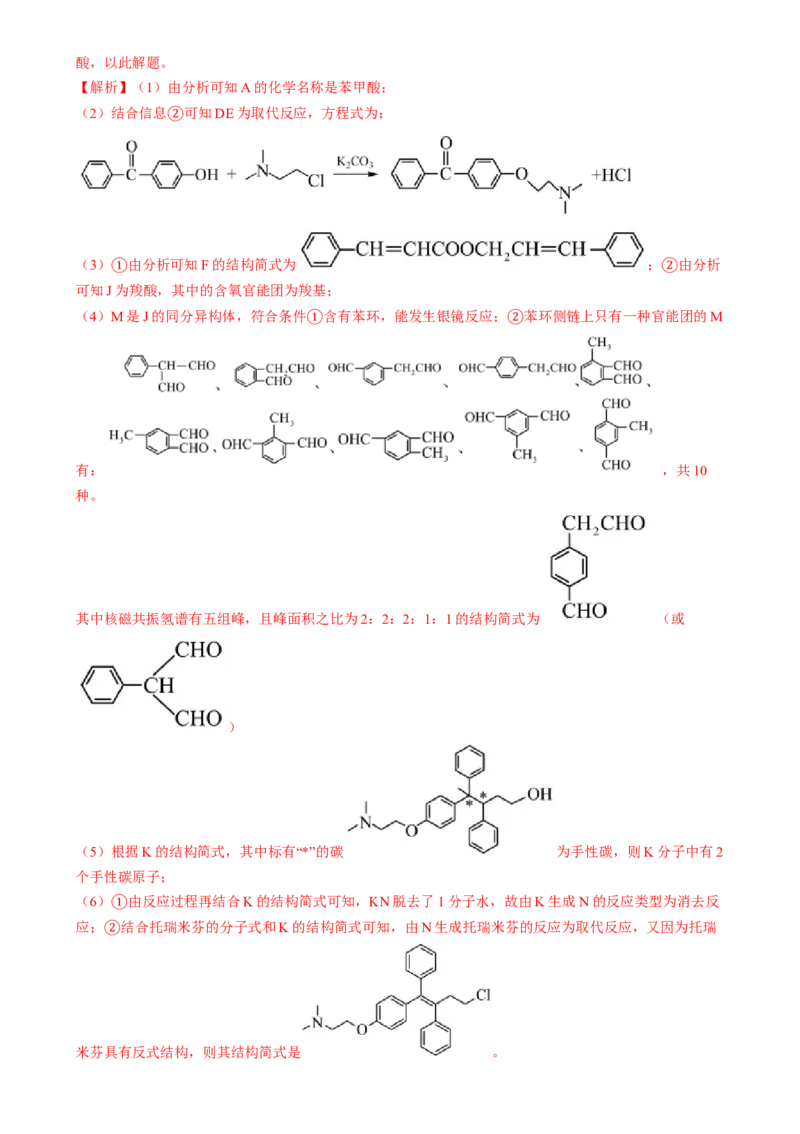
(6)由K合成托瑞米芬的过程如下:
由K生成N的反应类型为 。
托瑞米芬具有反式结构,其结构简式是 。
①
【答案】(1)苯甲酸
②
(2)
(3) 羧基
(4) 10 (或 )
(5)2
(6) 消去反应
【分析】有机物B能与 溶液反应,但不产生 ;B加氢可得环己醇,则B是苯酚,A和B反应
生成C,且有机物A能与 溶液反应产生 ,其钠盐可用于食品防腐,再结合C的分子式,可知
A为苯甲酸,C为苯甲酸苯酚酯,结合信息 可知D为: ,DE为取代反应,则
②
E为 ,F是一种天然香料,经碱性水解、酸化,得G和J。在一定条件
下,G经氧化可转化为J。则F的结构简式为 ,G
的结构简式为 ,碱性水解、酸化,得G和J,且G经氧化可转化为J,则J为羧酸,以此解题。
【解析】(1)由分析可知A的化学名称是苯甲酸;
(2)结合信息 可知DE为取代反应,方程式为:
②
(3) 由分析可知F的结构简式为 ; 由分析
可知J为羧酸,其中的含氧官能团为羧基;
① ②
(4)M是J的同分异构体,符合条件 含有苯环,能发生银镜反应; 苯环侧链上只有一种官能团的M
① ②
有: ,共10
种。
其中核磁共振氢谱有五组峰,且峰面积之比为2:2:2:1:1的结构简式为 (或
)
(5)根据K的结构简式,其中标有“*”的碳 为手性碳,则K分子中有2
个手性碳原子;
(6) 由反应过程再结合K的结构简式可知,KN脱去了1分子水,故由K生成N的反应类型为消去反
应; 结合托瑞米芬的分子式和K的结构简式可知,由N生成托瑞米芬的反应为取代反应,又因为托瑞
①
②
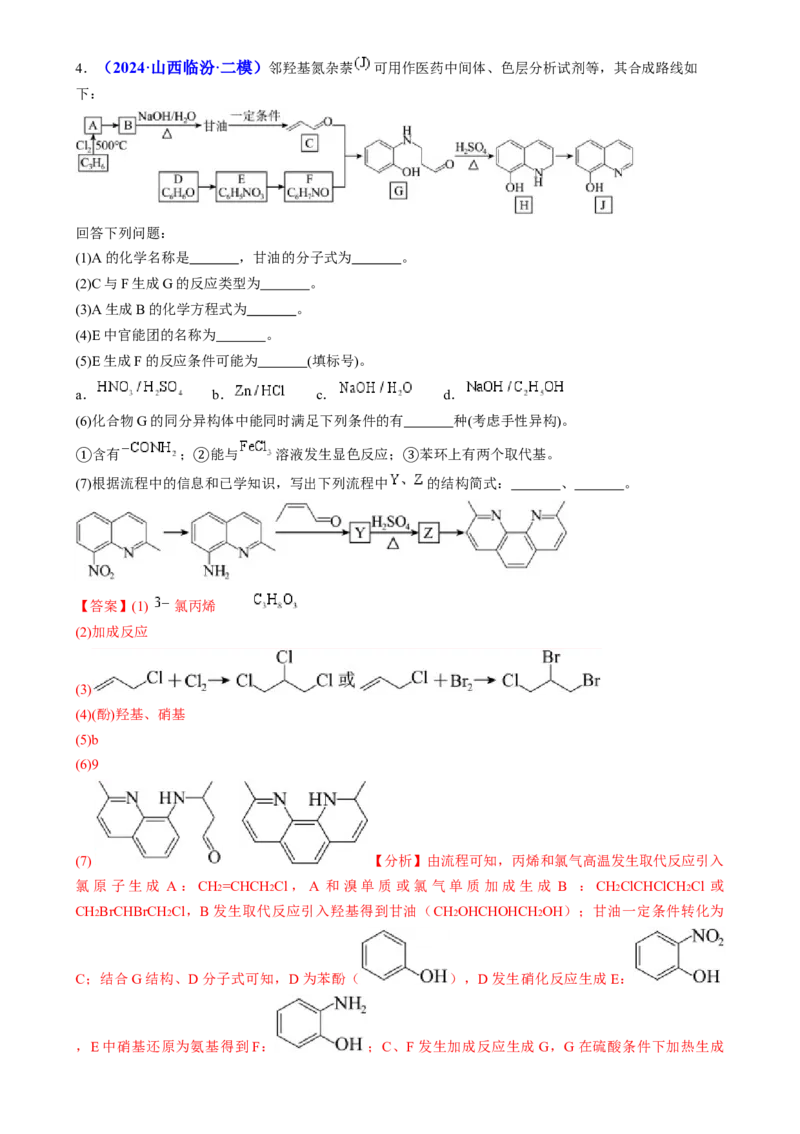
米芬具有反式结构,则其结构简式是 。4.(2024·山西临汾·二模)邻羟基氮杂萘 可用作医药中间体、色层分析试剂等,其合成路线如
下:
回答下列问题:
(1)A的化学名称是 ,甘油的分子式为 。
(2)C与F生成G的反应类型为 。
(3)A生成B的化学方程式为 。
(4)E中官能团的名称为 。
(5)E生成F的反应条件可能为 (填标号)。
a. b. c. d.
(6)化合物G的同分异构体中能同时满足下列条件的有 种(考虑手性异构)。
含有 ; 能与 溶液发生显色反应; 苯环上有两个取代基。
①(7)根据流程中的信息②和已学知识,写出下列流程中 ③ 的结构简式: 、 。
【答案】(1) 氯丙烯
(2)加成反应
(3)
(4)(酚)羟基、硝基
(5)b
(6)9
(7) 【分析】由流程可知,丙烯和氯气高温发生取代反应引入
氯原子生成 A:CH2=CHCH2Cl,A 和溴单质或氯气单质加成生成 B :CH2ClCHClCH2Cl 或
CH2BrCHBrCH2Cl,B发生取代反应引入羟基得到甘油(CH2OHCHOHCH2OH);甘油一定条件转化为
C;结合G结构、D分子式可知,D为苯酚( ),D发生硝化反应生成E:
,E中硝基还原为氨基得到F: ;C、F发生加成反应生成G,G在硫酸条件下加热生成H,H生成J。
【解析】(1)由分析可知,A为CH2=CHCH2Cl,化学名称是 氯丙烯,甘油为CH2OHCHOHCH2OH,
分子式为 ;
(2)由分析可知,C、F发生生成G,反应后不饱和度减小,为加成反应;
(3)A和溴单质或氯气单质加成生成B :CH2ClCHClCH2Cl或CH2BrCHBrCH2Cl,反应为:
;
(4)由分析可知,E为 ,含有酚羟基、硝基;
(5)E中硝基还原为氨基得到F,需要加入还原剂,故选b;
(6)化合物G的同分异构体中能同时满足下列条件 (考虑手性异构):
含有 ; 能与 溶液发生显色反应,则含有酚羟基; 苯环上有两个取代基;则除酚羟
①
基外还含有一个取代
②
基,若为-CH2CH2CONH2 ,则存在邻间对3种;若
③
为-CH(CH3)CONH2 ,存在邻间对3
种,由于连接甲基的碳为手性碳,则存在3×2=6种;共9种;
(7) 中氨基和 发生C、F生成G的反应原理生成Y: ,
Y成环得到Z: 。
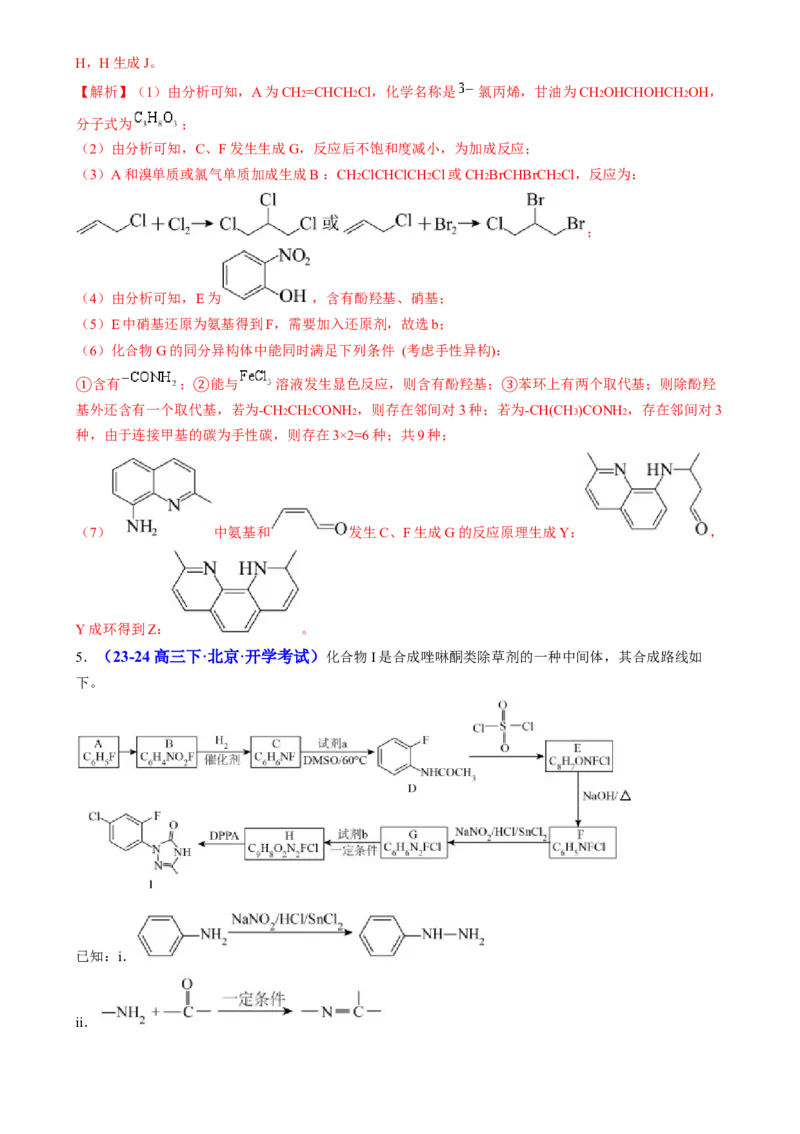
5.(23-24高三下·北京·开学考试)化合物I是合成唑啉酮类除草剂的一种中间体,其合成路线如
下。
已知:i.
ii.iii.R1-COOH+ R2NH2
(1)A→B反应所需的试剂和条件是 。
(2)已知:2CH3COOH→a+H2O。C→D的化学方程式为 。
(3)E→F的反应类型是 。
(4)由C合成F的过程中,C→D的目的是 。
(5)G→H的化学方程式为 。
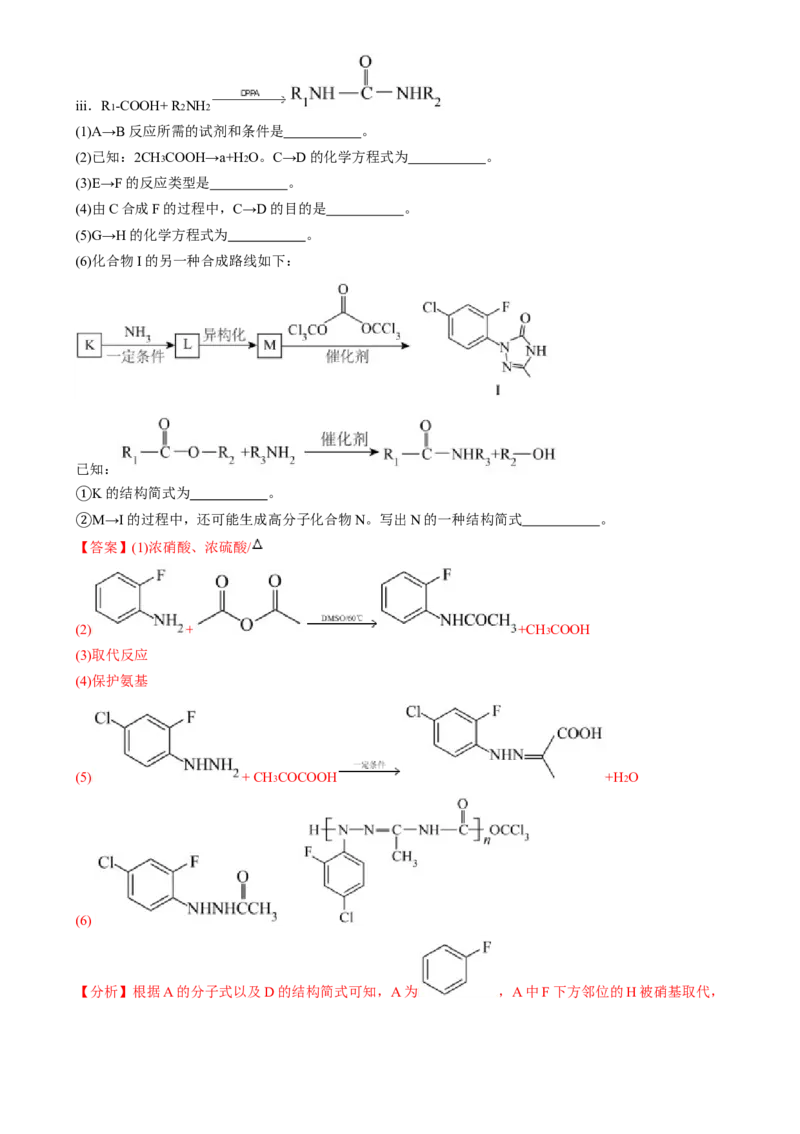
(6)化合物I的另一种合成路线如下:
已知:
K的结构简式为 。
M→I的过程中,还可能生成高分子化合物N。写出N的一种结构简式 。
①
②
【答案】(1)浓硝酸、浓硫酸/
(2) + +CH3COOH
(3)取代反应
(4)保护氨基
(5) + CH3COCOOH +H2O
(6)
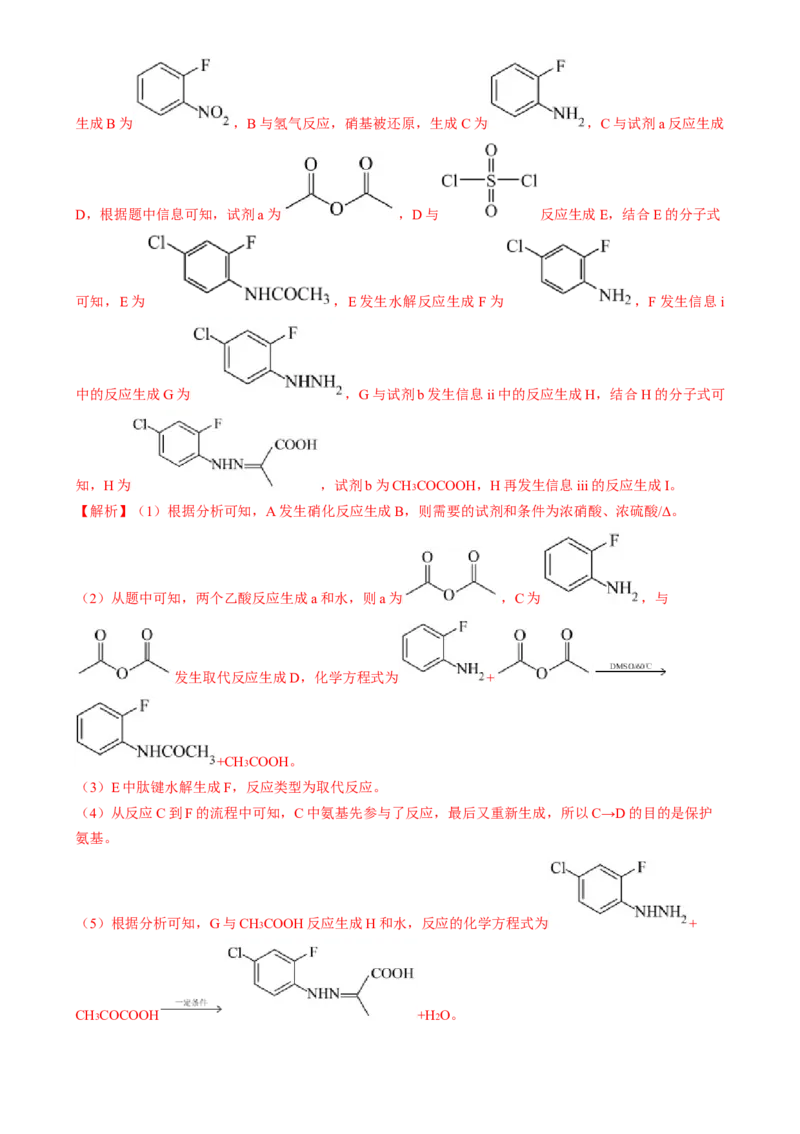
【分析】根据A的分子式以及D的结构简式可知,A为 ,A中F下方邻位的H被硝基取代,生成B为 ,B与氢气反应,硝基被还原,生成C为 ,C与试剂a反应生成
D,根据题中信息可知,试剂a为 ,D与 反应生成E,结合E的分子式
可知,E为 ,E发生水解反应生成F为 ,F发生信息i
中的反应生成G为 ,G与试剂b发生信息ii中的反应生成H,结合H的分子式可
知,H为 ,试剂b为CH3COCOOH,H再发生信息iii的反应生成I。
【解析】(1)根据分析可知,A发生硝化反应生成B,则需要的试剂和条件为浓硝酸、浓硫酸/Δ。
(2)从题中可知,两个乙酸反应生成a和水,则a为 ,C为 ,与
发生取代反应生成D,化学方程式为 +
+CH3COOH。
(3)E中肽键水解生成F,反应类型为取代反应。
(4)从反应C到F的流程中可知,C中氨基先参与了反应,最后又重新生成,所以C→D的目的是保护
氨基。
(5)根据分析可知,G与CH3COOH反应生成H和水,反应的化学方程式为 +
CH3COCOOH +H2O。(6) M与 发生已知信息的反应生成I,则M为 ,L异
①
构化得到M,K与NH3 先发生加成反应再发生消去反应生成L,则K为 。
M生成I的过程中先生成 ,
②
可以发生缩聚反应生成高分子化合物 。
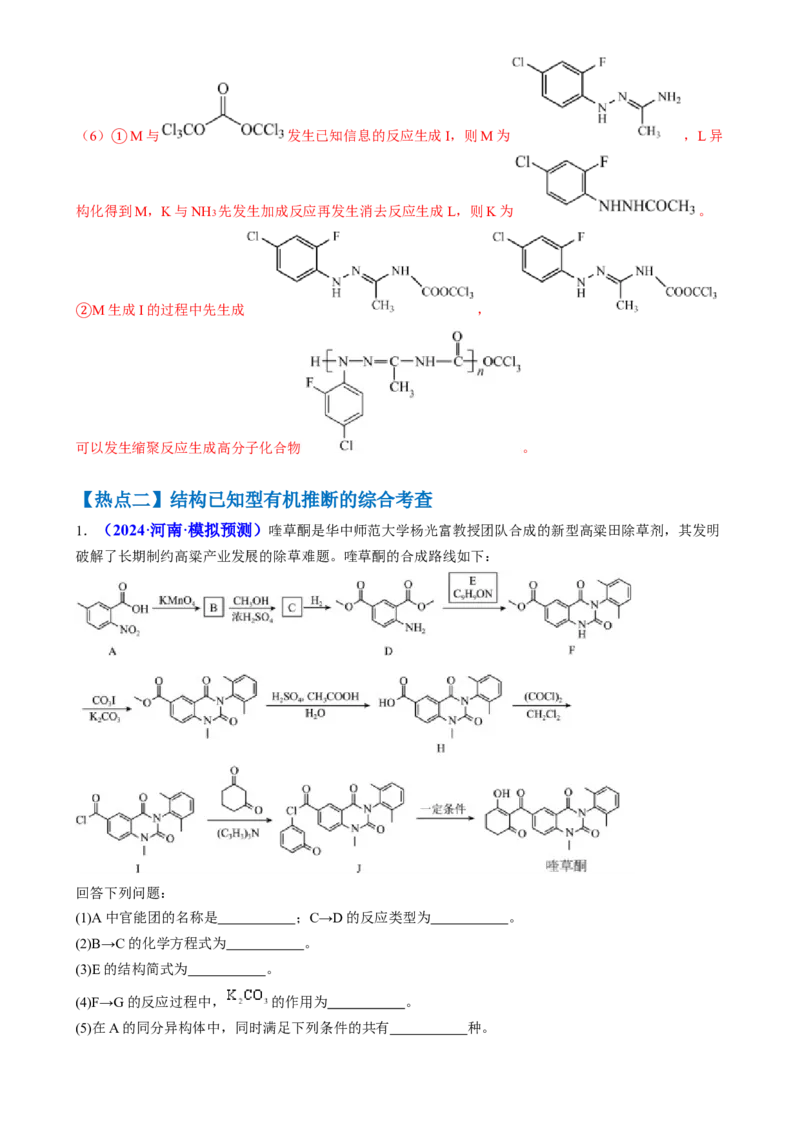
【热点二】结构已知型有机推断的综合考查
1.(2024·河南·模拟预测)喹草酮是华中师范大学杨光富教授团队合成的新型高粱田除草剂,其发明
破解了长期制约高粱产业发展的除草难题。喹草酮的合成路线如下:
回答下列问题:
(1)A中官能团的名称是 ;C→D的反应类型为 。
(2)B→C的化学方程式为 。
(3)E的结构简式为 。
(4)F→G的反应过程中, 的作用为 。
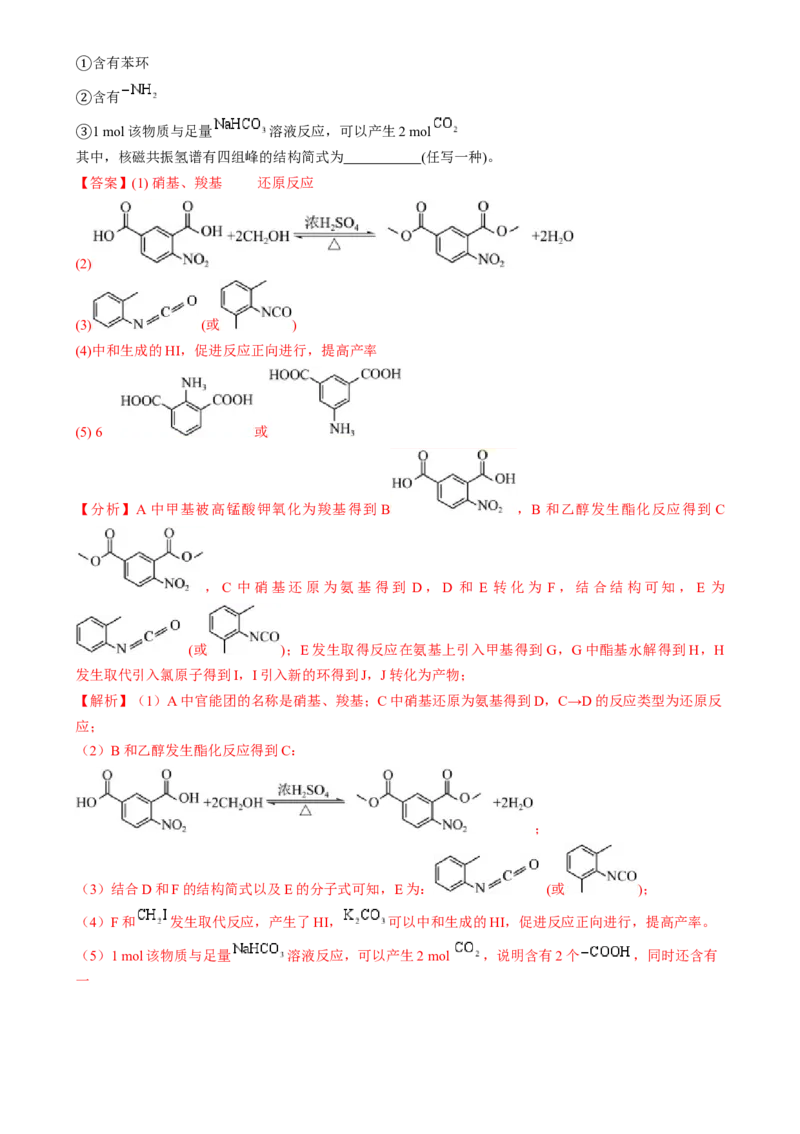
(5)在A的同分异构体中,同时满足下列条件的共有 种。含有苯环
①含有
②1 mol该物质与足量 溶液反应,可以产生2 mol
其中,核磁共振氢谱有四组峰的结构简式为 (任写一种)。
③
【答案】(1) 硝基、羧基 还原反应
(2)
(3) (或 )
(4)中和生成的HI,促进反应正向进行,提高产率
(5) 6 或
【分析】A中甲基被高锰酸钾氧化为羧基得到 B ,B和乙醇发生酯化反应得到 C
,C 中硝基还原为氨基得到 D,D 和 E 转化为 F,结合结构可知,E 为
(或 );E发生取得反应在氨基上引入甲基得到 G,G中酯基水解得到H,H
发生取代引入氯原子得到I,I引入新的环得到J,J转化为产物;
【解析】(1)A中官能团的名称是硝基、羧基;C中硝基还原为氨基得到D,C→D的反应类型为还原反
应;
(2)B和乙醇发生酯化反应得到C:
;
(3)结合D和F的结构简式以及E的分子式可知,E为: (或 );
(4)F和 发生取代反应,产生了HI, 可以中和生成的HI,促进反应正向进行,提高产率。
(5)1 mol该物质与足量 溶液反应,可以产生2 mol ,说明含有2个 ,同时还含有
一个 。具体结构如下: ,共6种。其中,核
磁共振氢谱有四组峰的结构简式为 和 。
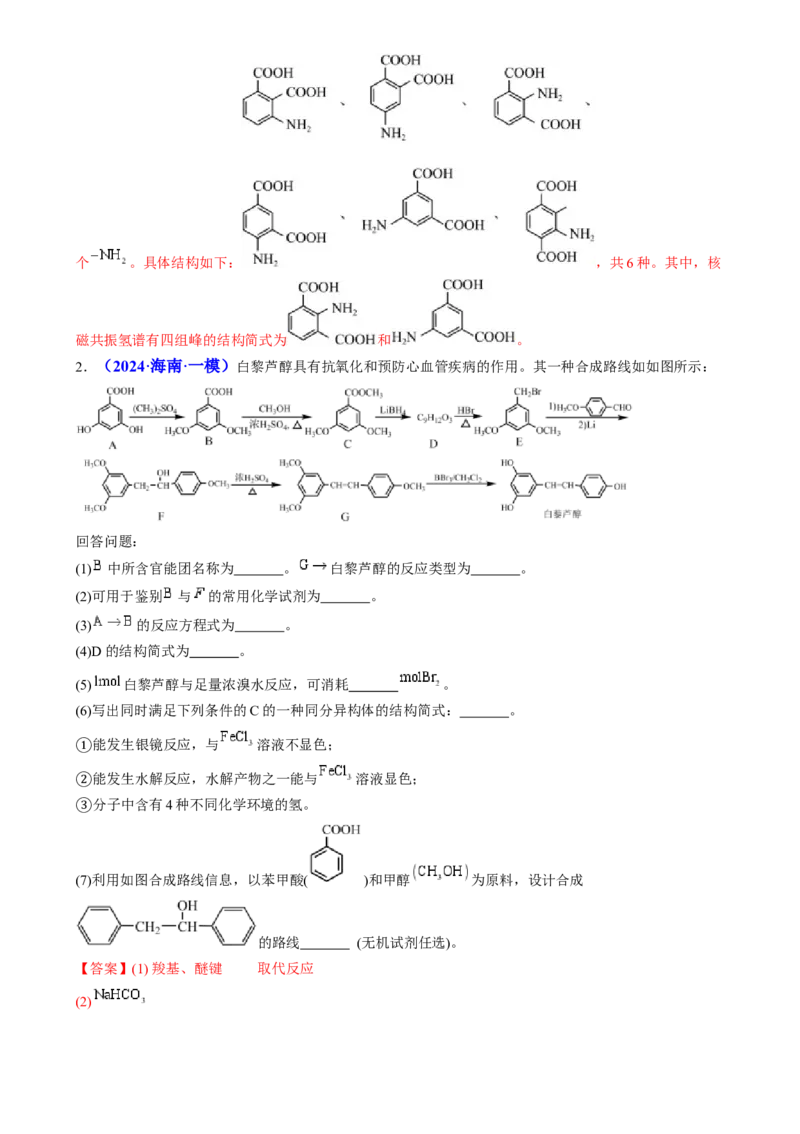
2.(2024·海南·一模)白黎芦醇具有抗氧化和预防心血管疾病的作用。其一种合成路线如如图所示:
回答问题:
(1) 中所含官能团名称为 。 白黎芦醇的反应类型为 。
(2)可用于鉴别 与 的常用化学试剂为 。
(3) 的反应方程式为 。
(4)D的结构简式为 。
(5) 白黎芦醇与足量浓溴水反应,可消耗 。
(6)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
能发生银镜反应,与 溶液不显色;
①能发生水解反应,水解产物之一能与 溶液显色;
分子中含有4种不同化学环境的氢。
②
③
(7)利用如图合成路线信息,以苯甲酸( )和甲醇 为原料,设计合成
的路线 (无机试剂任选)。
【答案】(1) 羧基、醚键 取代反应
(2)(3)
(4) 6
(5)
(6)
【分析】A发生取代反应生成B,B和甲醇发生酯化反应生成C,C发生还原反应生成D,结合E的结
构、 D 到 E 的反应条件以及 D 分子式可以推断 D 的结构是 ,E 和
发生加成反应生成F,F发生消去反应生成G,G发生取代反应生成白藜芦醇。
【解析】(1)根据B的结构,可以看出B中所含的官能团为醚键、羧基。对比G和白藜芦醇的结构,可
以看出G→白藜芦醇的反应类型是取代反应。
(2)观察B和F的结构,B中有羧基,F中有羟基,所以鉴别B和F的试剂可以选择碳酸氢钠,碳酸氢
钠会与B反应产生气泡,与F不反应无现象。
(3)对比A和B的结构可知,A→B的方程式为:
。
(4)结合D到E的反应条件以及D的分子式,可以推断出D的结构简式为 。
(5)观察白藜芦醇的结构,能与溴发生反应的有碳碳双键、苯环上与酚羟基相邻、相对位置的氢原子,所以1mol白黎芦醇与足量浓溴水反应,可消耗6molBr2 。
(6)能发生银镜反应,说明含有醛基,与 溶液不显色,说明不含酚羟基;能发生水解反应,水解
产物之一能与 溶液显色,说明含有酯基且水解能生成酚羟基;分子中含有4种不同化学环境的氢。
结合以上条件,符合条件的同分异构体为 。
(7)根据给出的合成路线可知,苯甲酸可先与甲醇发生酯化反应生成苯甲酸甲酯,然后在LiBH4 作用下
发生还原反应生成苯甲醇,再与HBr发生取代反应生成 ,同时苯甲醇与氧气发生催化
氧化生成苯甲醛,最后根据E到F的合成思路制备所需目标产物,具体合成路线为
。
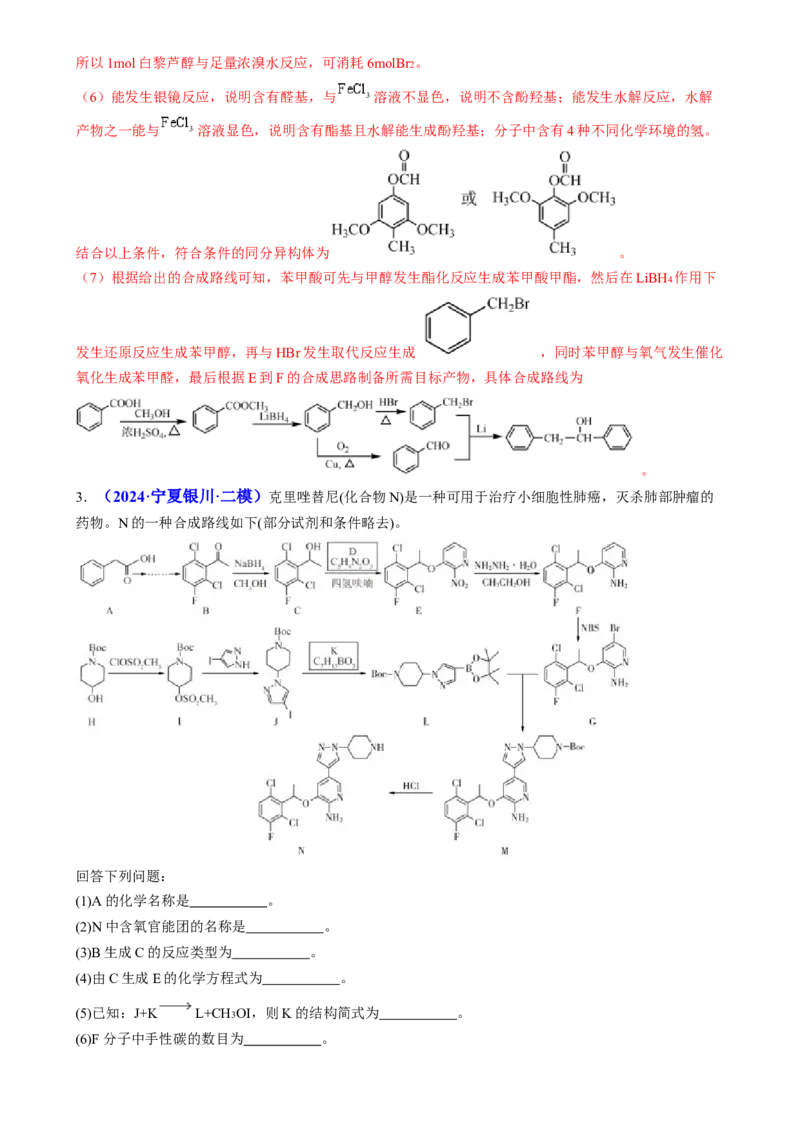
3.(2024·宁夏银川·二模)克里唑替尼(化合物N)是一种可用于治疗小细胞性肺癌,灭杀肺部肿瘤的
药物。N的一种合成路线如下(部分试剂和条件略去)。
回答下列问题:
(1)A的化学名称是 。
(2)N中含氧官能团的名称是 。
(3)B生成C的反应类型为 。
(4)由C生成E的化学方程式为 。
(5)已知:J+K L+CH3OI,则K的结构简式为 。
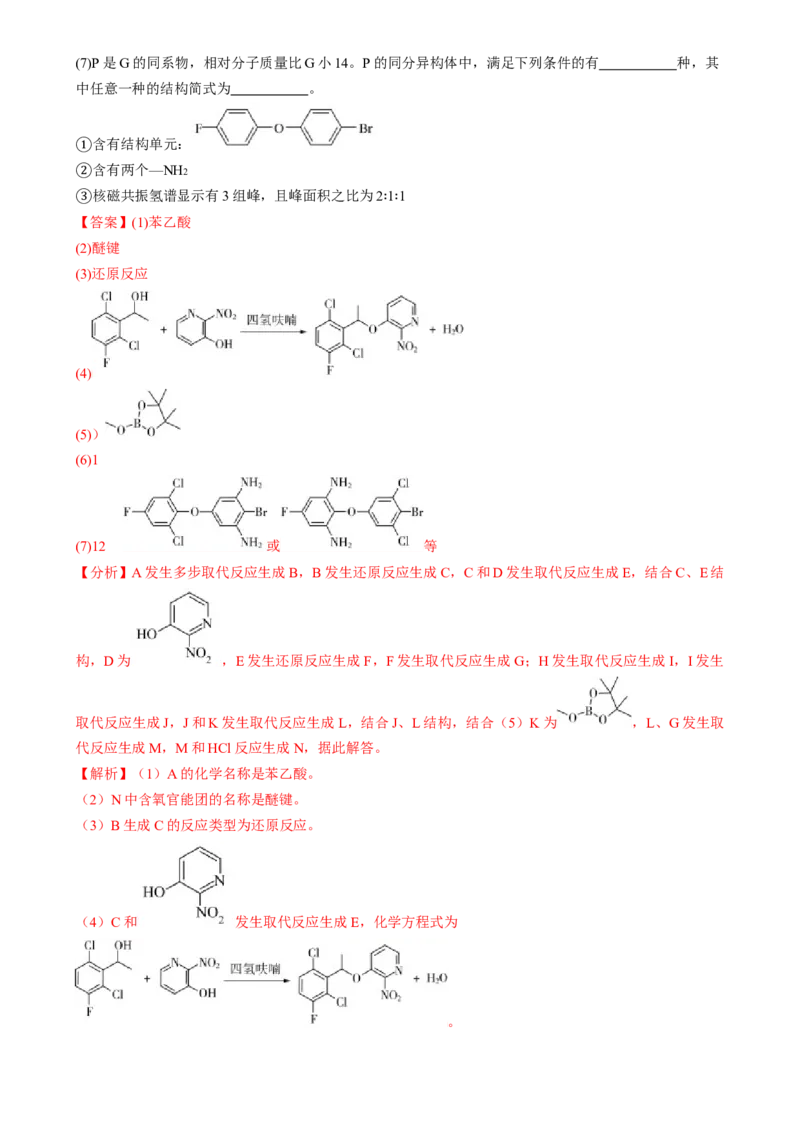
(6)F分子中手性碳的数目为 。(7)P是G的同系物,相对分子质量比G小14。P的同分异构体中,满足下列条件的有 种,其
中任意一种的结构简式为 。
含有结构单元:
①
含有两个—NH2
核磁共振氢谱显示有3组峰,且峰面积之比为2 1 1
②
【答案】(1)苯乙酸
③ ∶ ∶
(2)醚键
(3)还原反应
(4)
(5))
(6)1
(7)12 或 等
【分析】A发生多步取代反应生成B,B发生还原反应生成C,C和D发生取代反应生成E,结合C、E结
构,D为 ,E发生还原反应生成F,F发生取代反应生成G;H发生取代反应生成I,I发生
取代反应生成J,J和K发生取代反应生成L,结合J、L结构,结合(5)K为 ,L、G发生取
代反应生成M,M和HCl反应生成N,据此解答。
【解析】(1)A的化学名称是苯乙酸。
(2)N中含氧官能团的名称是醚键。
(3)B生成C的反应类型为还原反应。
(4)C和 发生取代反应生成E,化学方程式为
。(5)已知:J+K L+CH3OI,则K的结构简式为 。
(6)F分子中手性碳如图星号所示 ,数目为1。
(7)G为 ,P是G的同系物,相对分子质量比G小14。P的同分异构体中, 含
①
有结构单元: ,该结构上下对称, 含有两个—NH2 , 核磁共振氢谱显示有3
② ③
组峰,其中且峰面积之比为2 1 1, 可以存在取代基的为如图8个位置,其中
、 、 、 必
∶ ∶
须满足有一组没有取代基,故-Cl、-Cl、-NH2 、-NH2 四个取代基每个可以
在上部或下部3个位置,且每个有4种结构,故满足条件的有3×4=12种,满足条件的结构为
①⑤ ②⑥ ③⑦ ④⑧
或 等。
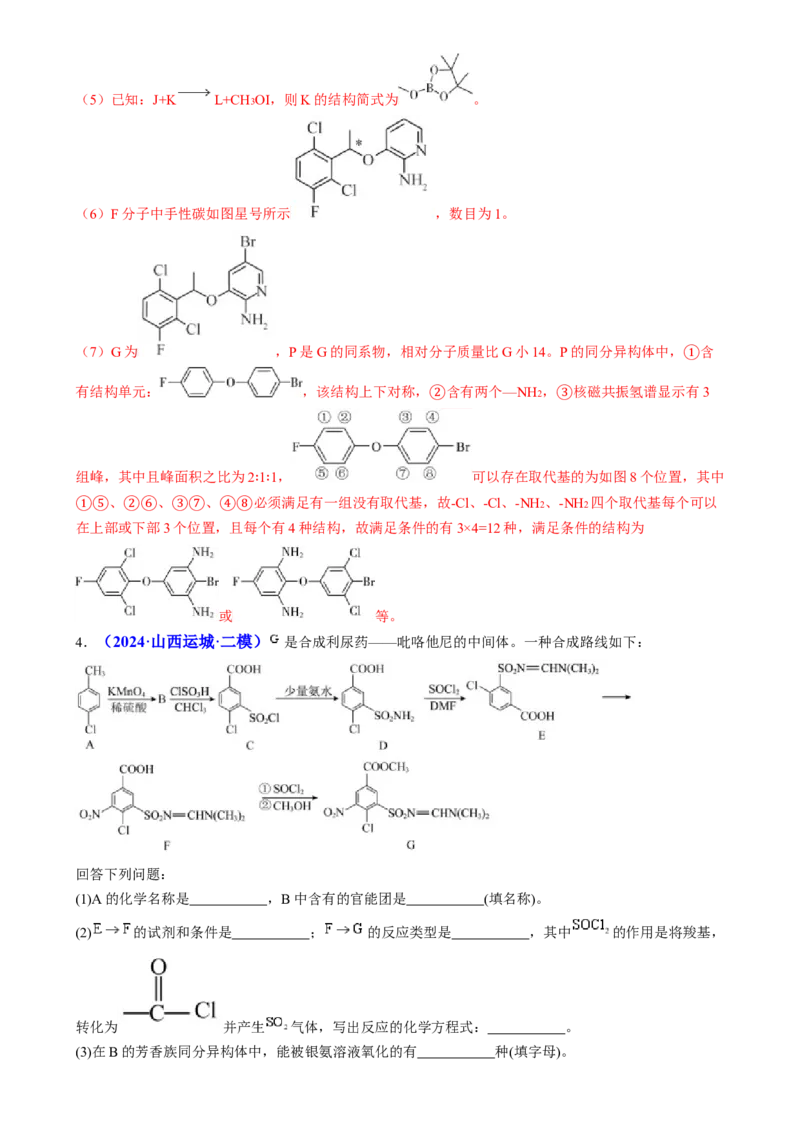
4.(2024·山西运城·二模) 是合成利尿药——吡咯他尼的中间体。一种合成路线如下:
回答下列问题:
(1)A的化学名称是 ,B中含有的官能团是 (填名称)。
(2) 的试剂和条件是 ; 的反应类型是 ,其中 的作用是将羧基,
转化为 并产生 气体,写出反应的化学方程式: 。
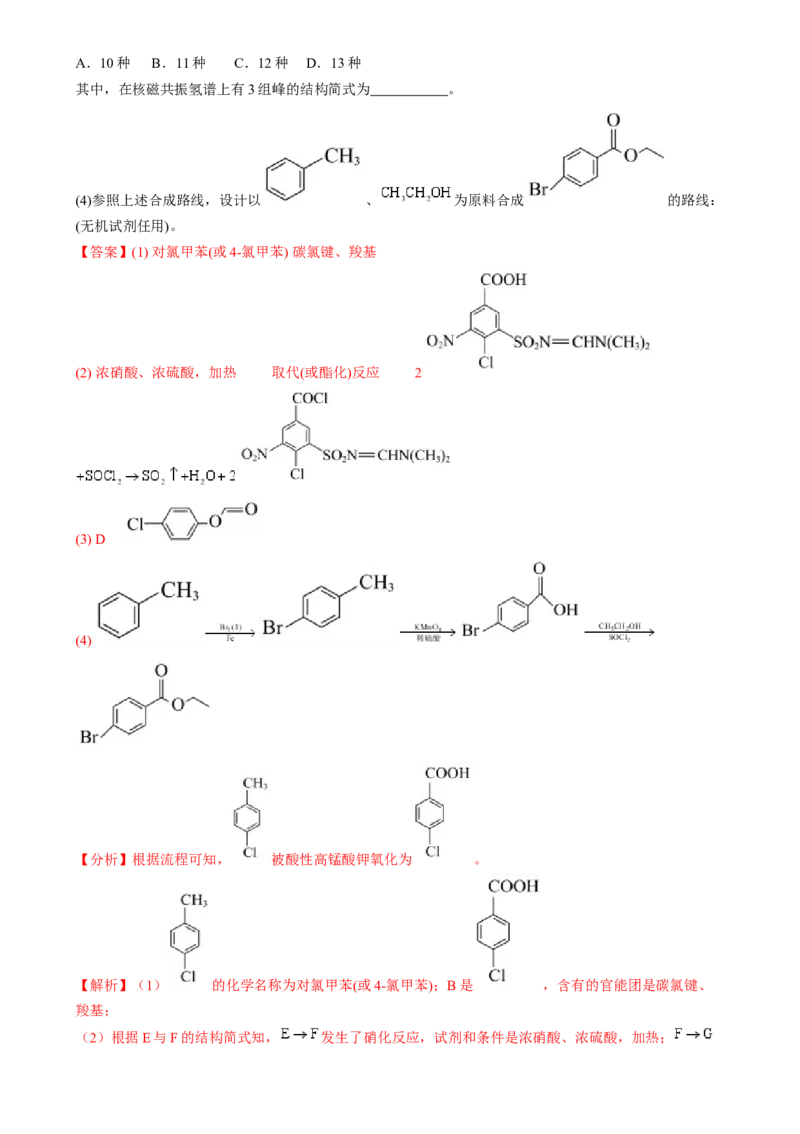
(3)在B的芳香族同分异构体中,能被银氨溶液氧化的有 种(填字母)。A.10种 B.11种 C.12种 D.13种
其中,在核磁共振氢谱上有3组峰的结构简式为 。
(4)参照上述合成路线,设计以 、 为原料合成 的路线:
(无机试剂任用)。
【答案】(1) 对氯甲苯(或4-氯甲苯) 碳氯键、羧基
(2) 浓硝酸、浓硫酸,加热 取代(或酯化)反应 2
(3) D
(4)
【分析】根据流程可知, 被酸性高锰酸钾氧化为 。
【解析】(1) 的化学名称为对氯甲苯(或4-氯甲苯);B是 ,含有的官能团是碳氯键、
羧基;
(2)根据E与F的结构简式知, 发生了硝化反应,试剂和条件是浓硝酸、浓硫酸,加热;是羧基与醇羟基发生了取代(或酯化)反应;根据原子守恒以及 的作用是将羧基转化为
并产生 气体得到化学方程式为:2
;
(3)能被银氨溶液氧化,说明有醛基,如果苯环上有两个取代基,即 与 ,有邻
间对三种同分异构体,如果苯环上有三个取代基,即 、 与 ,则有10种同分异构体,即共有
13
种同分异构体,故选D;其中在核磁共振氢谱上有3组峰的结构简式为 ;
(4)根据逆推法,需要制取 ,再结合流程可得:
。
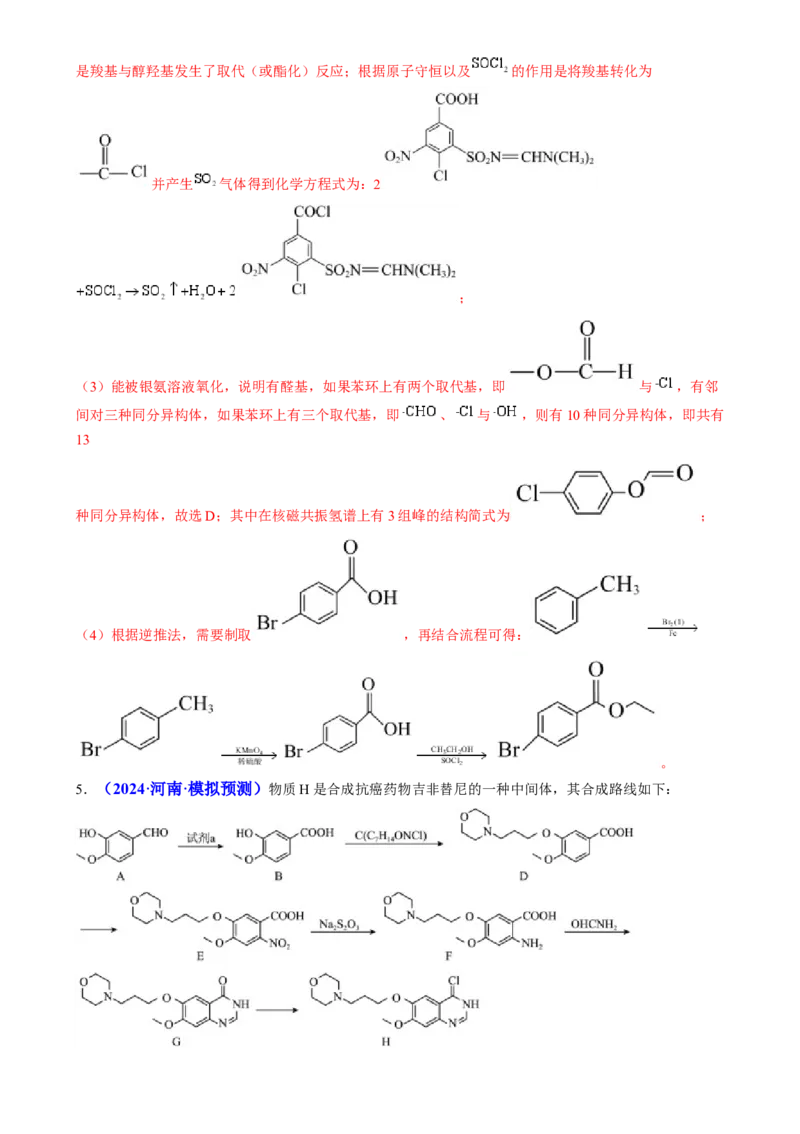
5.(2024·河南·模拟预测)物质H是合成抗癌药物吉非替尼的一种中间体,其合成路线如下:回答下列问题:
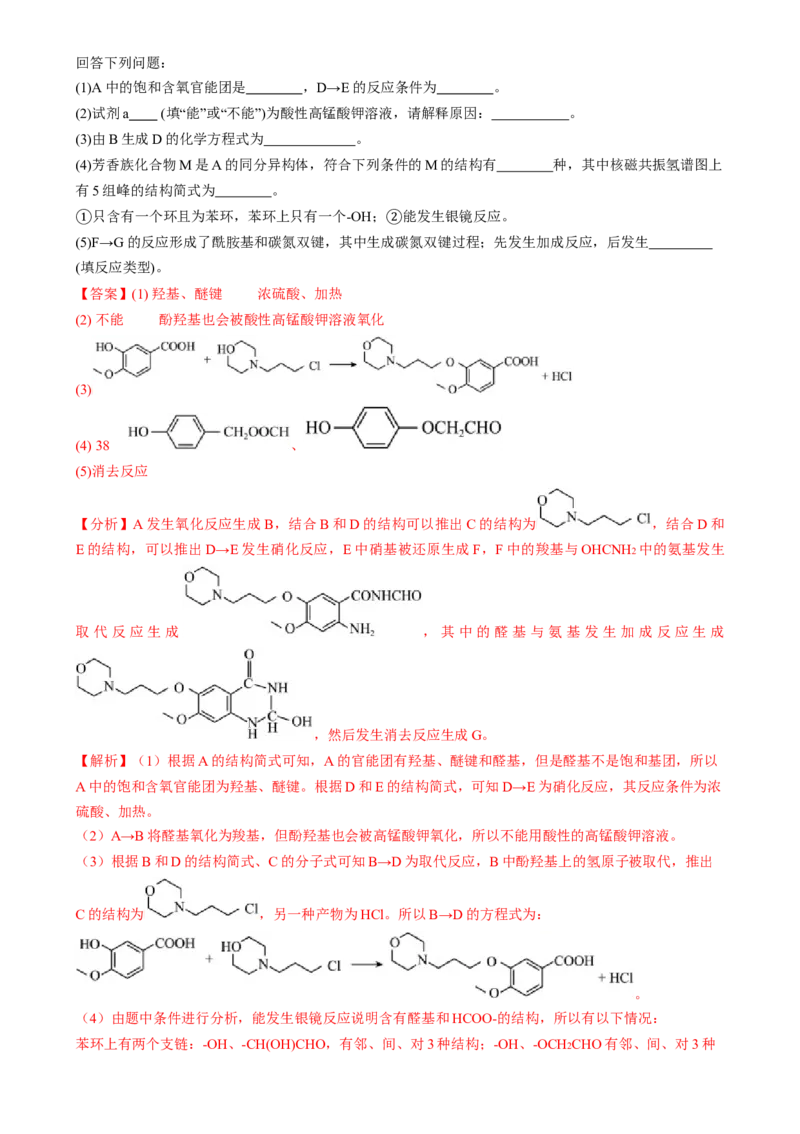
(1)A中的饱和含氧官能团是 ,D→E的反应条件为 。
(2)试剂a (填“能”或“不能”)为酸性高锰酸钾溶液,请解释原因: 。
(3)由B生成D的化学方程式为 。
(4)芳香族化合物M是A的同分异构体,符合下列条件的M的结构有 种,其中核磁共振氢谱图上
有5组峰的结构简式为 。
只含有一个环且为苯环,苯环上只有一个-OH; 能发生银镜反应。
(5)F→G的反应形成了酰胺基和碳氮双键,其中生成碳氮双键过程;先发生加成反应,后发生
① ②
(填反应类型)。
【答案】(1) 羟基、醚键 浓硫酸、加热
(2) 不能 酚羟基也会被酸性高锰酸钾溶液氧化
(3)
(4) 38 、
(5)消去反应
【分析】A发生氧化反应生成B,结合B和D的结构可以推出C的结构为 ,结合D和
E的结构,可以推出D→E发生硝化反应,E中硝基被还原生成F,F中的羧基与OHCNH2 中的氨基发生
取代反应生成 ,其中的醛基与氨基发生加成反应生成
,然后发生消去反应生成G。
【解析】(1)根据A的结构简式可知,A的官能团有羟基、醚键和醛基,但是醛基不是饱和基团,所以
A中的饱和含氧官能团为羟基、醚键。根据D和E的结构简式,可知D→E为硝化反应,其反应条件为浓
硫酸、加热。
(2)A→B将醛基氧化为羧基,但酚羟基也会被高锰酸钾氧化,所以不能用酸性的高锰酸钾溶液。
(3)根据B和D的结构简式、C的分子式可知B→D为取代反应,B中酚羟基上的氢原子被取代,推出
C的结构为 ,另一种产物为HCl。所以B→D的方程式为:
。
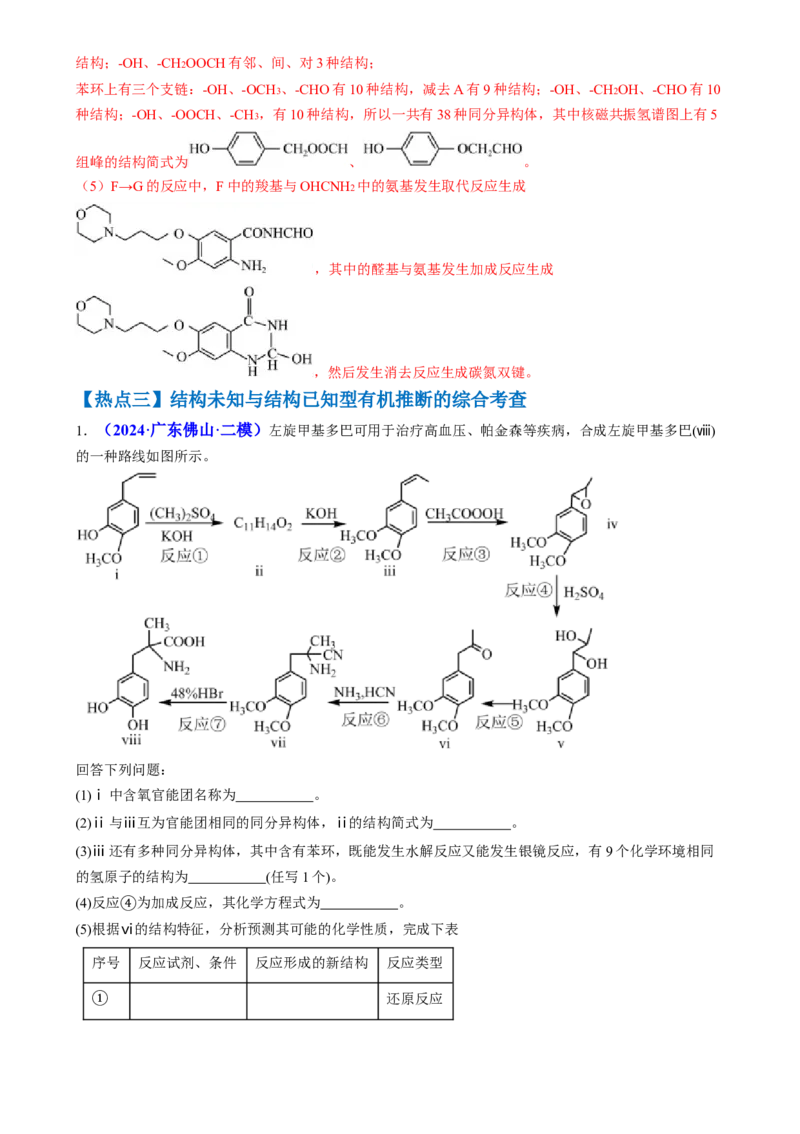
(4)由题中条件进行分析,能发生银镜反应说明含有醛基和HCOO-的结构,所以有以下情况:
苯环上有两个支链:-OH、-CH(OH)CHO,有邻、间、对3种结构;-OH、-OCH2CHO有邻、间、对3种结构;-OH、-CH2OOCH有邻、间、对3种结构;
苯环上有三个支链:-OH、-OCH3 、-CHO有10种结构,减去A有9种结构;-OH、-CH2OH、-CHO有10
种结构;-OH、-OOCH、-CH3 ,有10种结构,所以一共有38种同分异构体,其中核磁共振氢谱图上有5
组峰的结构简式为 、 。
(5)F→G的反应中,F中的羧基与OHCNH2 中的氨基发生取代反应生成
,其中的醛基与氨基发生加成反应生成
,然后发生消去反应生成碳氮双键。
【热点三】结构未知与结构已知型有机推断的综合考查
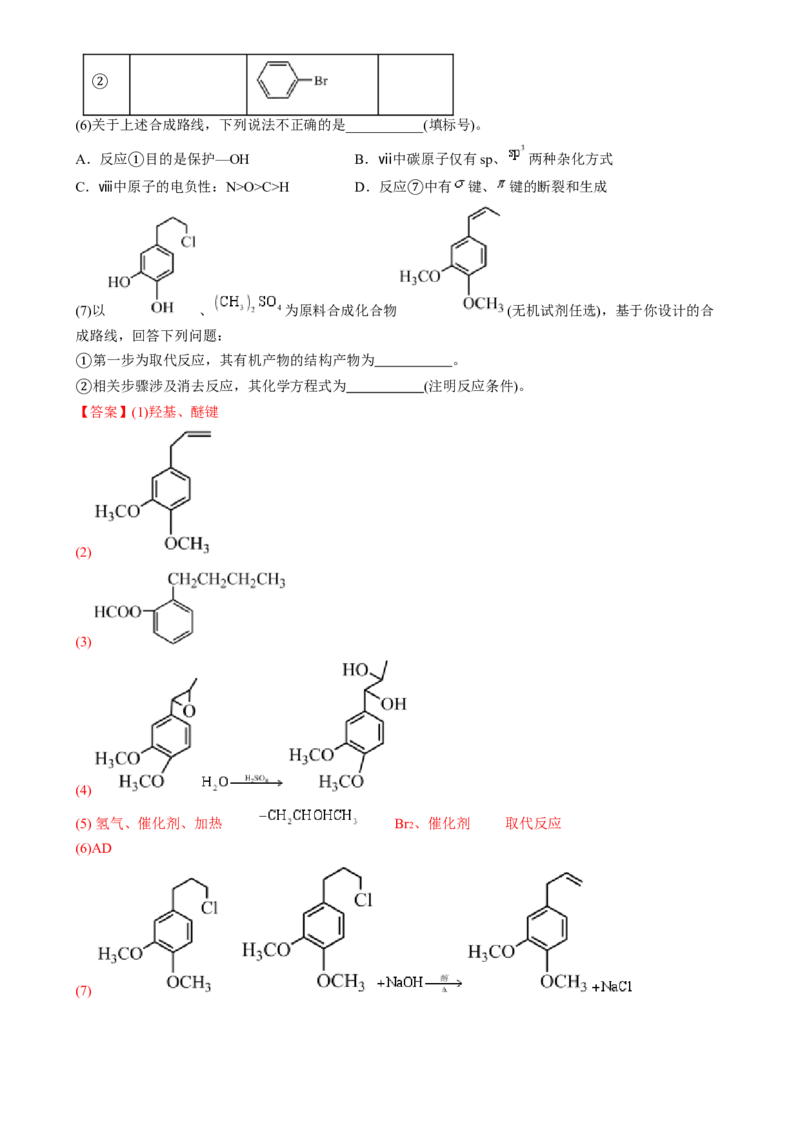
1.(2024·广东佛山·二模)左旋甲基多巴可用于治疗高血压、帕金森等疾病,合成左旋甲基多巴(ⅷ)
的一种路线如图所示。
回答下列问题:
(1)ⅰ中含氧官能团名称为 。
(2)ⅱ与ⅲ互为官能团相同的同分异构体,ⅱ的结构简式为 。
(3)ⅲ还有多种同分异构体,其中含有苯环,既能发生水解反应又能发生银镜反应,有9个化学环境相同
的氢原子的结构为 (任写1个)。
(4)反应 为加成反应,其化学方程式为 。
(5)根据ⅵ的结构特征,分析预测其可能的化学性质,完成下表
④
序号 反应试剂、条件 反应形成的新结构 反应类型
还原反应
①②
(6)关于上述合成路线,下列说法不正确的是___________(填标号)。
A.反应 目的是保护—OH B.ⅶ中碳原子仅有sp、 两种杂化方式
C.ⅷ中原
①
子的电负性:N>O>C>H D.反应 中有 键、 键的断裂和生成
⑦
(7)以 、 为原料合成化合物 (无机试剂任选),基于你设计的合
成路线,回答下列问题:
第一步为取代反应,其有机产物的结构产物为 。
相关步骤涉及消去反应,其化学方程式为 (注明反应条件)。
①
【答案】(1)羟基、醚键
②
(2)
(3)
(4)
(5) 氢气、催化剂、加热 Br2 、催化剂 取代反应
(6)AD
(7)【分析】结合i和iii结构以及对比i和ii分子式可知,i发生取代反应生成ii ,在KOH作
用下ii反应生成iii,iii发生反应成环生成iv,iv在酸性条件下开环生成v,v被氧化生成vi,vi发生加成
生成vii,vii发生反应生成viii。
【解析】(1)ⅰ中含氧官能团名称:羟基、醚键;
(2)ⅱ与ⅲ互为官能团相同的同分异构体,结合分析,ⅱ的结构简式: ;
(3)ⅲ同分异构体满足:含有苯环,既能发生水解反应又能发生银镜反应,说明含甲酸某酯基,其中有
9个化学环境相同的氢原子,说明对称性很低,满足要求的结构: ;
(4)反应 为加成反应,其化学方程式: ;
(5)物质④vi含官能团酮羰基,在催化剂、加热条件下可与氢气发生加成反应形成 ;苯环
上的氢在催化剂作用下可被卤素取代;
(6)A.对比反应物i和最终产物viii可知,反应 目的是保护—OH,A正确;B.vii中C原子成键形
式有单键、双键和三键,杂化类型有sp、sp2 和sp3① ,B错误;C.同周期元素从左到右元素电负性逐渐增
强,所以电负性: ,C错误;D.反应 中有碳氮三键的断裂,涉及 键和 的断裂,有羧基
的形成,涉及 键和 的形成,D正确;
⑦
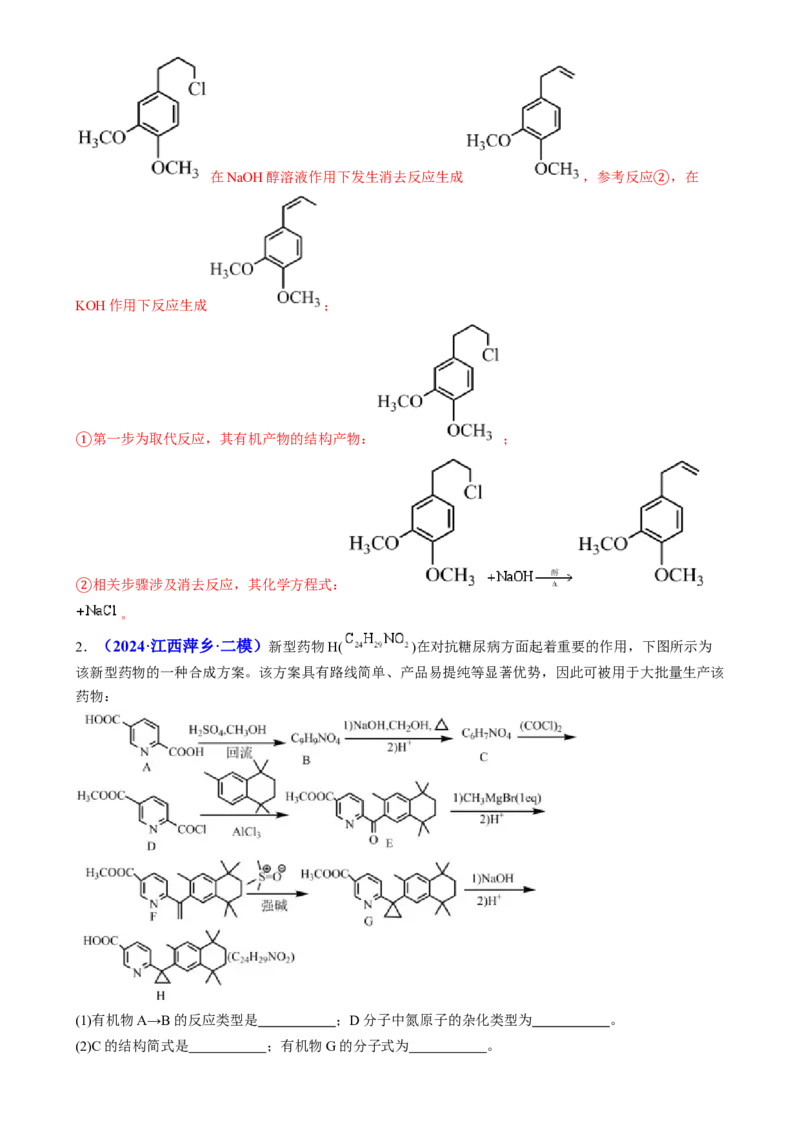
(7)参考反应 与 反应生成 ,
①在NaOH醇溶液作用下发生消去反应生成 ,参考反应 ,在
②
KOH作用下反应生成 ;
第一步为取代反应,其有机产物的结构产物: ;
①
相关步骤涉及消去反应,其化学方程式:
② 。
2.(2024·江西萍乡·二模)新型药物H( )在对抗糖尿病方面起着重要的作用,下图所示为
该新型药物的一种合成方案。该方案具有路线简单、产品易提纯等显著优势,因此可被用于大批量生产该
药物:
(1)有机物A→B的反应类型是 ;D分子中氮原子的杂化类型为 。
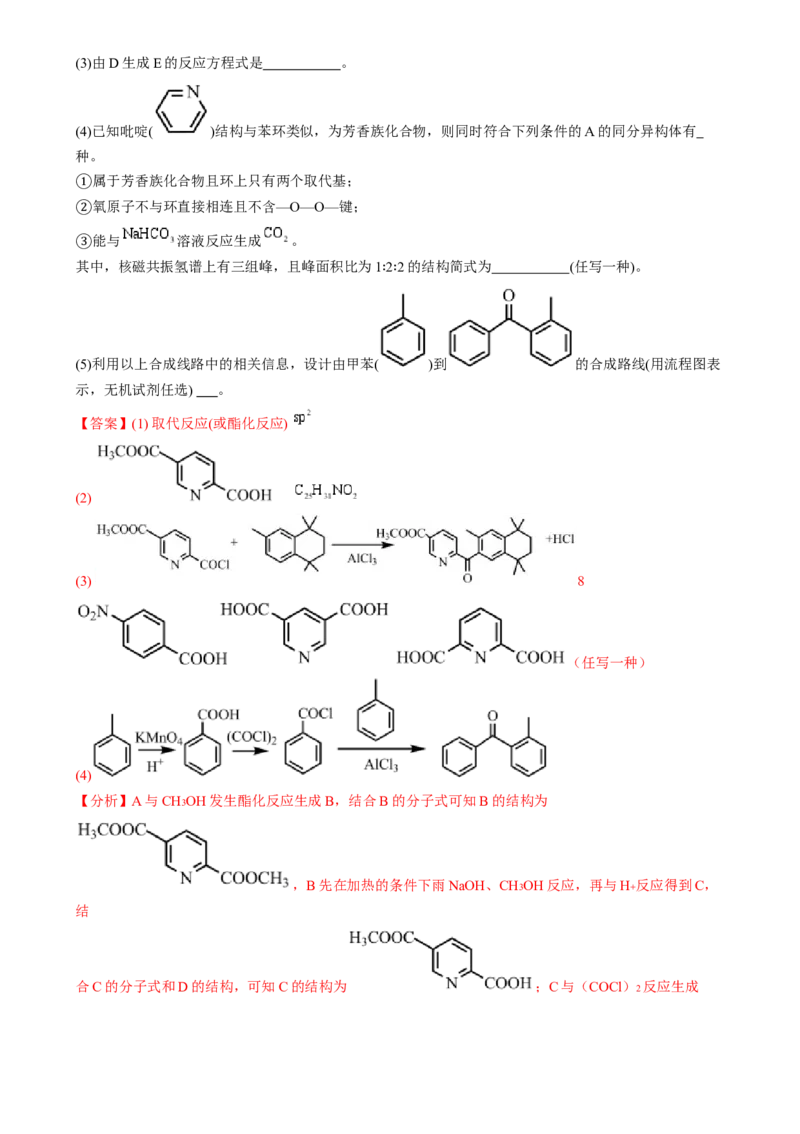
(2)C的结构简式是 ;有机物G的分子式为 。(3)由D生成E的反应方程式是 。
(4)已知吡啶( )结构与苯环类似,为芳香族化合物,则同时符合下列条件的A的同分异构体有
种。
属于芳香族化合物且环上只有两个取代基;
氧原子不与环直接相连且不含—O—O—键;
①
②能与 溶液反应生成 。
其中,核磁共振氢谱上有三组峰,且峰面积比为1 2 2的结构简式为 (任写一种)。
③
∶ ∶
(5)利用以上合成线路中的相关信息,设计由甲苯( )到 的合成路线(用流程图表
示,无机试剂任选) 。
【答案】(1) 取代反应(或酯化反应)
(2)
(3) 8
(任写一种)
(4)
【分析】A与CH3OH发生酯化反应生成B,结合B的分子式可知B的结构为
,B先在加热的条件下雨NaOH、CH3OH反应,再与H+ 反应得到C,
结
合C的分子式和D的结构,可知C的结构为 ;C与(COCl)
2
反应生成D,D与 在AlCl3 作催化剂的条件下反应生成E,E先与CH3MgBr(1eq)反应,再与H+ 反应
生成F,F与 在强碱下反应生成G,G先水解再与H+ 反应得到H。
【解析】(1)A与CH3OH发生酯化反应生成B;D中含有2个σ键,1个孤电子对,属于sp2 杂化;
(2)由分析得,C的结构简式为 ;由G的结构简式可得G的分子式
为 ;
(3)D与 在AlCl3 作催化剂的条件下反应生成E,化学方程式为:
;
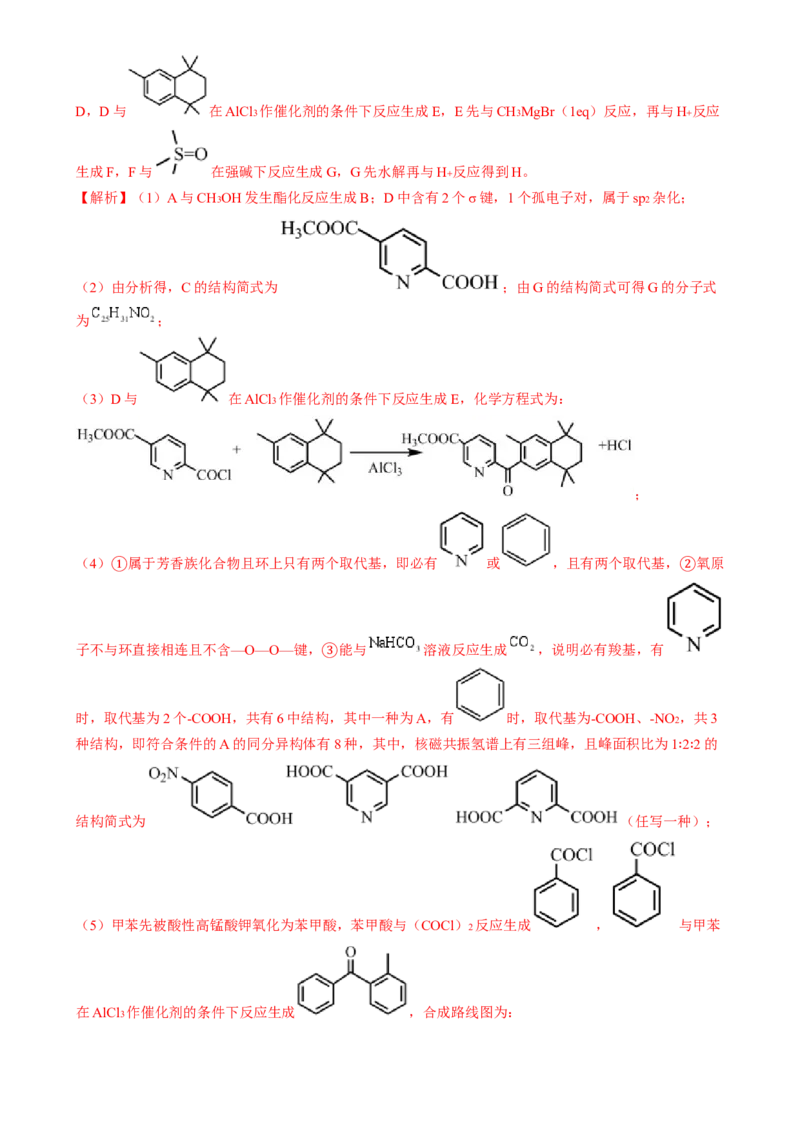
(4) 属于芳香族化合物且环上只有两个取代基,即必有 或 ,且有两个取代基, 氧原
① ②
子不与环直接相连且不含—O—O—键, 能与 溶液反应生成 ,说明必有羧基,有
③
时,取代基为2个-COOH,共有6中结构,其中一种为A,有 时,取代基为-COOH、-NO2 ,共3
种结构,即符合条件的A的同分异构体有8种,其中,核磁共振氢谱上有三组峰,且峰面积比为1 2 2的
∶ ∶
结构简式为 (任写一种);
(5)甲苯先被酸性高锰酸钾氧化为苯甲酸,苯甲酸与(COCl)
2
反应生成 , 与甲苯
在AlCl3 作催化剂的条件下反应生成 ,合成路线图为:。
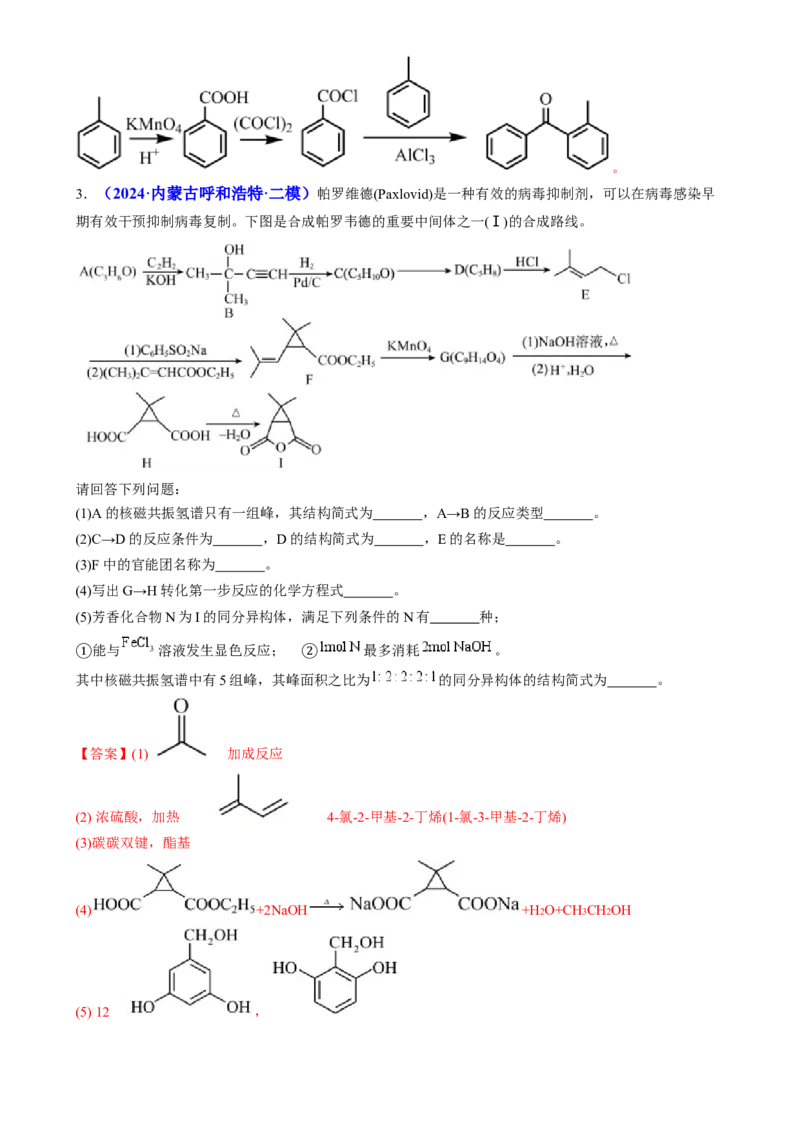
3.(2024·内蒙古呼和浩特·二模)帕罗维德(Paxlovid)是一种有效的病毒抑制剂,可以在病毒感染早
期有效干预抑制病毒复制。下图是合成帕罗韦德的重要中间体之一(Ⅰ)的合成路线。
请回答下列问题:
(1)A的核磁共振氢谱只有一组峰,其结构简式为 ,A→B的反应类型 。
(2)C→D的反应条件为 ,D的结构简式为 ,E的名称是 。
(3)F中的官能团名称为 。
(4)写出G→H转化第一步反应的化学方程式 。
(5)芳香化合物N为I的同分异构体,满足下列条件的N有 种;
能与 溶液发生显色反应; 最多消耗 。
①其中核磁共振氢谱中有5组峰,其峰面②积之比为 的同分异构体的结构简式为 。
【答案】(1) 加成反应
(2) 浓硫酸,加热 4-氯-2-甲基-2-丁烯(1-氯-3-甲基-2-丁烯)
(3)碳碳双键,酯基
(4) +2NaOH +H2O+CH3CH2OH
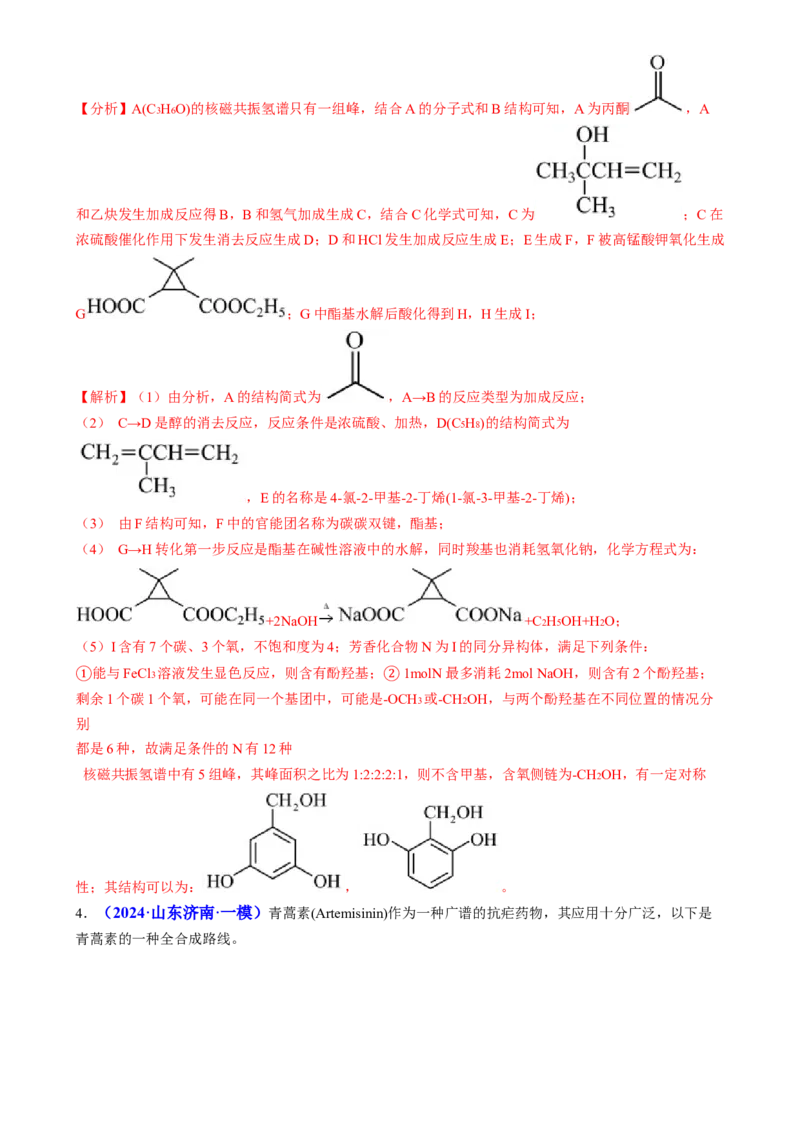
(5) 12 ,【分析】A(C3H6O)的核磁共振氢谱只有一组峰,结合A的分子式和B结构可知,A为丙酮 ,A
和乙炔发生加成反应得B,B和氢气加成生成C,结合C化学式可知,C为 ;C在
浓硫酸催化作用下发生消去反应生成D;D和HCl发生加成反应生成E;E生成F,F被高锰酸钾氧化生成
G ;G中酯基水解后酸化得到H,H生成I;
【解析】(1)由分析,A的结构简式为 ,A→B的反应类型为加成反应;
(2) C→D是醇的消去反应,反应条件是浓硫酸、加热,D(C5H8)的结构简式为
,E的名称是4-氯-2-甲基-2-丁烯(1-氯-3-甲基-2-丁烯);
(3) 由F结构可知,F中的官能团名称为碳碳双键,酯基;
(4) G→H转化第一步反应是酯基在碱性溶液中的水解,同时羧基也消耗氢氧化钠,化学方程式为:
+2NaOH +C2H5OH+H2O;
(5)I含有7个碳、3个氧,不饱和度为4;芳香化合物N为I的同分异构体,满足下列条件:
能与FeCl3 溶液发生显色反应,则含有酚羟基; 1molN最多消耗2mol NaOH,则含有2个酚羟基;
①
剩余1个碳1个氧,可能在同一个基团中,可能是-
②
OCH3 或-CH2OH,与两个酚羟基在不同位置的情况分
别
都是6种,故满足条件的N有12种
核磁共振氢谱中有5组峰,其峰面积之比为1:2:2:2:1,则不含甲基,含氧侧链为-CH2OH,有一定对称
性;其结构可以为: , 。
4.(2024·山东济南·一模)青蒿素(Artemisinin)作为一种广谱的抗疟药物,其应用十分广泛,以下是
青蒿素的一种全合成路线。已知:
I.
Ⅱ.
Ⅲ.
Ⅳ.
Ⅴ.R,R1 ,R2 ,R3 ,R4=H或烷基。
回答下列问题:
(1)A中含氧官能团的名称为 ,青蒿素的分子式为 。
(2)化合物 有多种同分异构体,写出满足以下条件的同分异构体结构简式 。
能与银氨溶液发生反应; 核磁共振氢谱中共含有三组吸收峰。
(3)化合物C的结构简式为 。
① ②
(4)由F生成G的反应类型为 ,稍过量K2CO3 时,由G生成H的反应方程式为 。
(5)参照以上合成路线,设计 为原料合成 的合成路线 (无机试剂任选)。
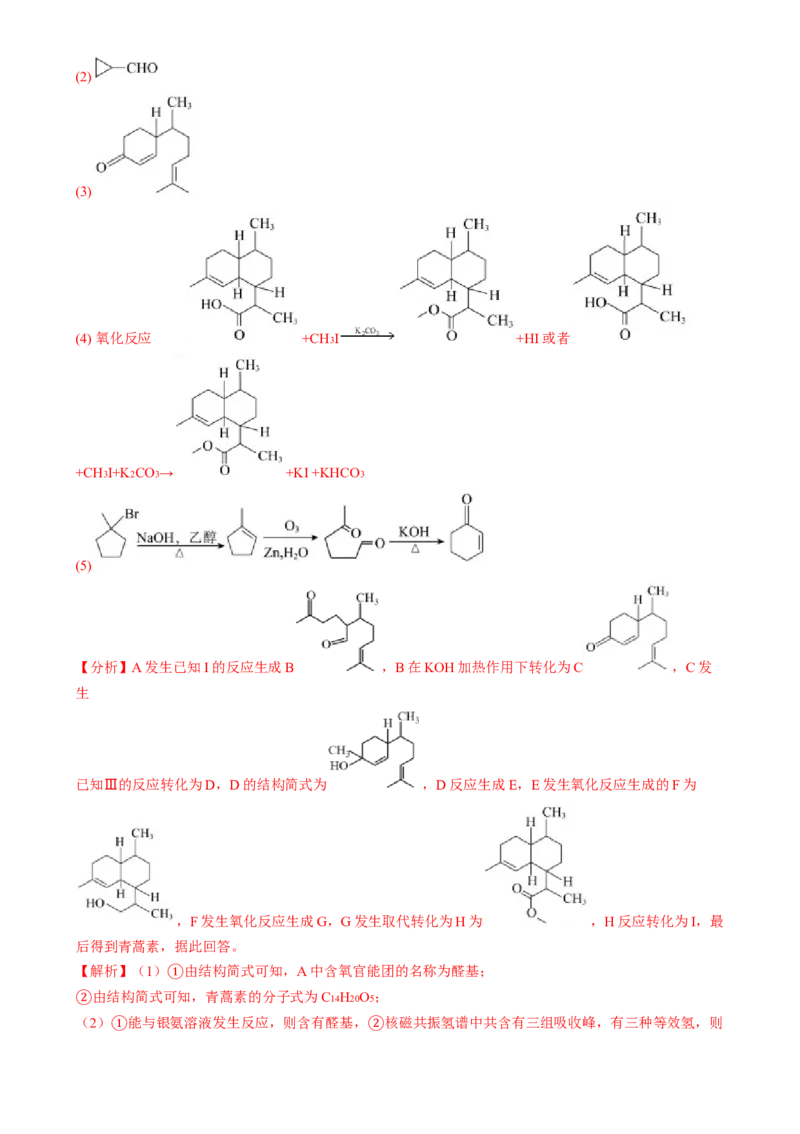
【答案】(1) 醛基 C14H20O5(2)
(3)
(4) 氧化反应 +CH3I +HI或者
+CH3I+K2CO3→ +KI +KHCO3
(5)
【分析】A发生已知I的反应生成B ,B在KOH加热作用下转化为C ,C发
生
已知Ⅲ的反应转化为D,D的结构简式为 ,D反应生成E,E发生氧化反应生成的F为
,F发生氧化反应生成G,G发生取代转化为H为 ,H反应转化为I,最
后得到青蒿素,据此回答。
【解析】(1) 由结构简式可知,A中含氧官能团的名称为醛基;
由结构简式可
①
知,青蒿素的分子式为C14H20O5 ;
(2) 能与银氨溶液发生反应,则含有醛基, 核磁共振氢谱中共含有三组吸收峰,有三种等效氢,则
②
① ②符合条件的同分异构体为: ;
(3)根据分析可知,化合物C的结构简式为: ;
(4) 对比F、G的结构简式知,F生成G的反应类型为氧化反应;
①
过量K2CO3 时,由G生成H的反应方程式为: +CH3I +HI或
②
者 +CH3I+K2CO3 +KI +KHCO3 ;
(5) 合成 首先 发生消去反应生成 ,接着被氧化为 ,最后在
KOH
加热的情况下转化为 ,路线如下:
。
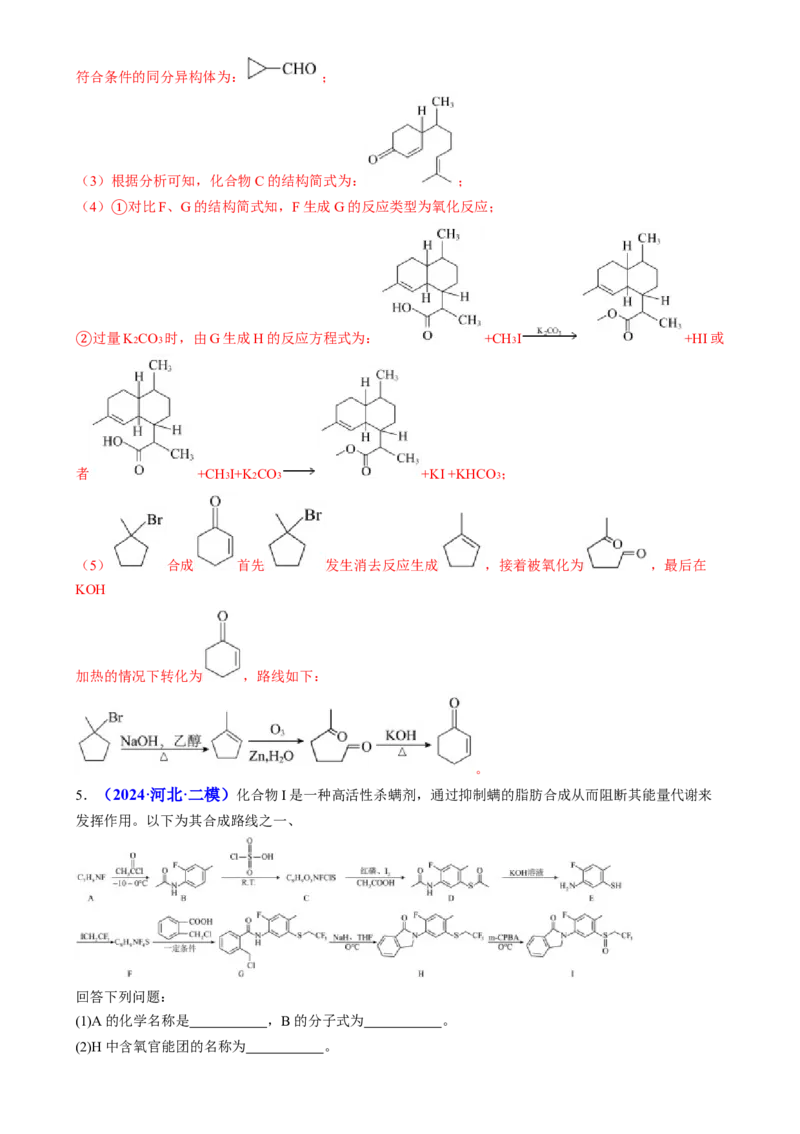
5.(2024·河北·二模)化合物I是一种高活性杀螨剂,通过抑制螨的脂肪合成从而阻断其能量代谢来
发挥作用。以下为其合成路线之一、
回答下列问题:
(1)A的化学名称是 ,B的分子式为 。
(2)H中含氧官能团的名称为 。(3)C的结构简式为 。
(4)E→F的反应类型为 。
(5)F→G的化学方程式为 。
(6)化合物ICH2CF3 中,碘原子与碳原子形成 键(填写轨道重叠方式)。
(7)在B的同分异构体中,同时满足下列条件的共有 种(不考虑立体异构)。
含有苯环
能发生银镜反应
①
②
苯环上有两个取代基,其中一个取代基为氨基(-NH2)与苯环直接相连
其中,核磁共振氢谱显示为5组峰,且峰面积之比为3:2:2:2:1的同分异构体的结构简式为
③
。
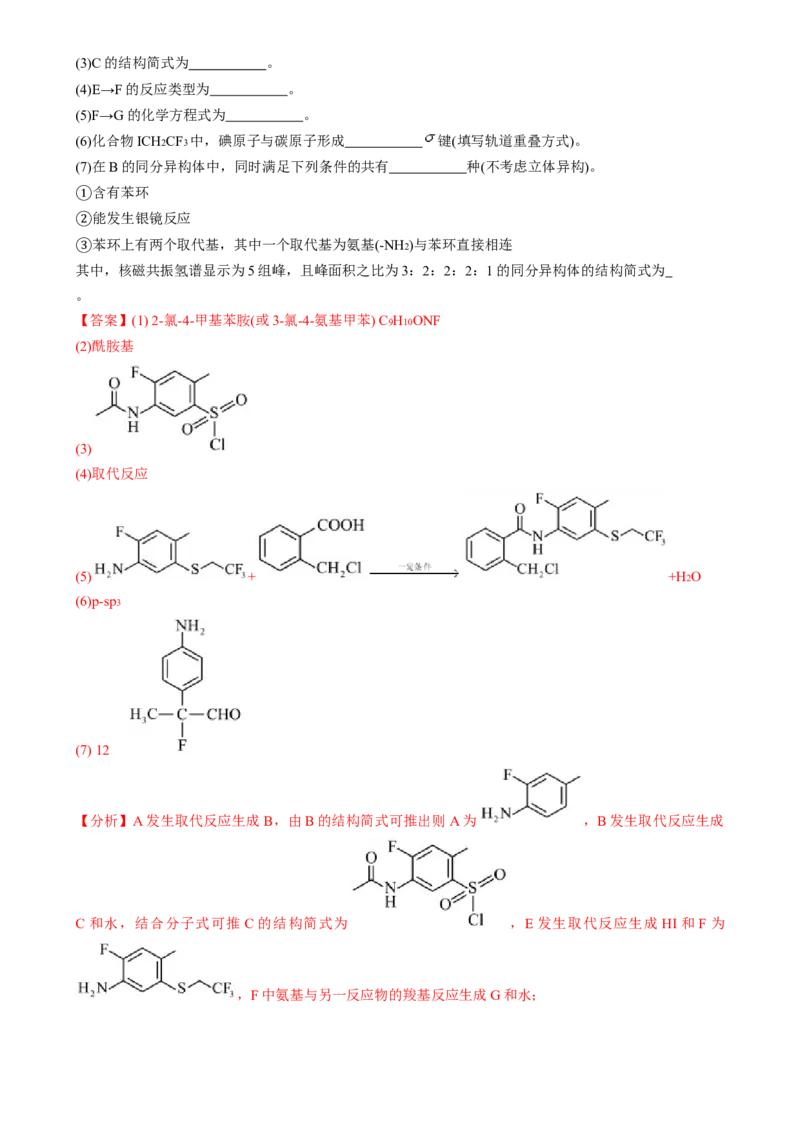
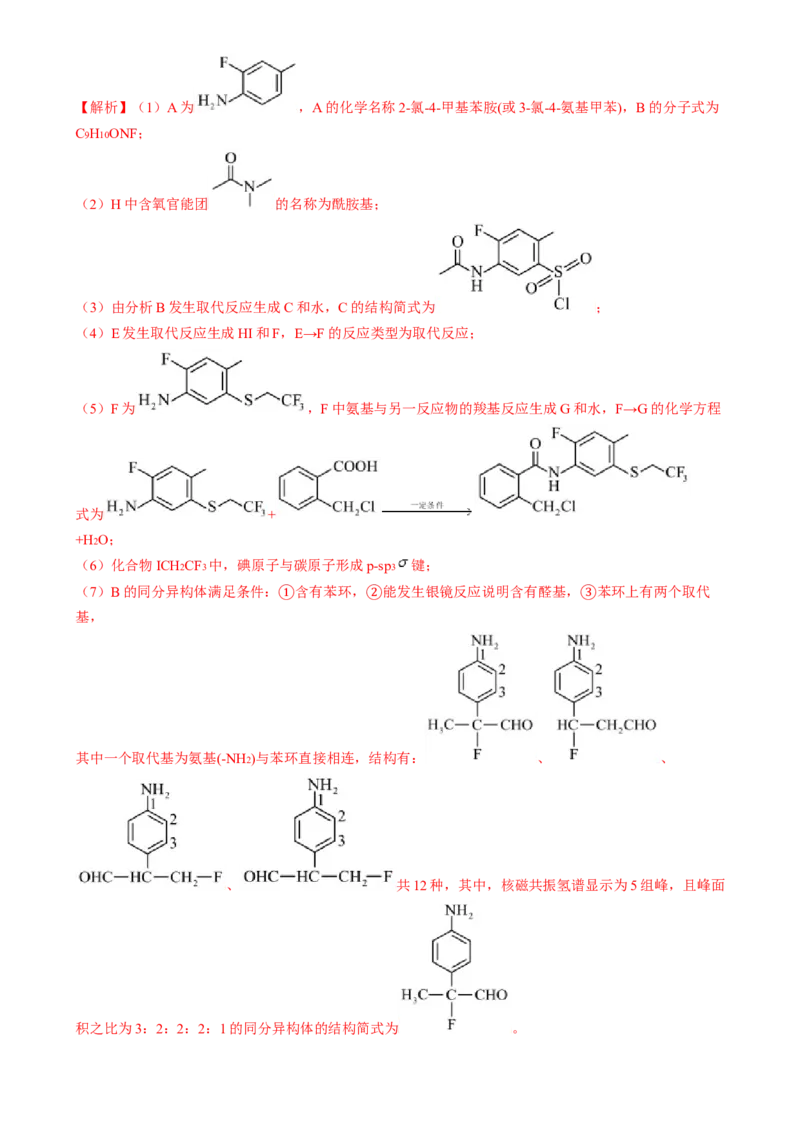
【答案】(1) 2-氯-4-甲基苯胺(或3-氯-4-氨基甲苯) C9H10ONF
(2)酰胺基
(3)
(4)取代反应
(5) + +H2O
(6)p-sp3
(7) 12
【分析】A发生取代反应生成B,由B的结构简式可推出则A为 ,B发生取代反应生成
C和水,结合分子式可推 C的结构简式为 ,E发生取代反应生成 HI和F为
,F中氨基与另一反应物的羧基反应生成G和水;【解析】(1)A为 ,A的化学名称2-氯-4-甲基苯胺(或3-氯-4-氨基甲苯),B的分子式为
C9H10ONF;
(2)H中含氧官能团 的名称为酰胺基;
(3)由分析B发生取代反应生成C和水,C的结构简式为 ;
(4)E发生取代反应生成HI和F,E→F的反应类型为取代反应;
(5)F为 ,F中氨基与另一反应物的羧基反应生成G和水,F→G的化学方程
式为 +
+H2O;
(6)化合物ICH2CF3 中,碘原子与碳原子形成p-sp3 键;
(7)B的同分异构体满足条件: 含有苯环, 能发生银镜反应说明含有醛基, 苯环上有两个取代
基,
① ② ③
其中一个取代基为氨基(-NH2)与苯环直接相连,结构有: 、 、
、 共12种,其中,核磁共振氢谱显示为5组峰,且峰面
积之比为3:2:2:2:1的同分异构体的结构简式为 。