文档内容
2023年重庆一中高2023届3月月考
化学试题卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.化学与生活生产密切相关,下列说法错误的是( )
A.用 与 两种溶液制作泡沫灭火剂
B. 与 溶液可用作焊接金属的除锈剂
C. 常用作医学上肠胃X射线检查的造影剂
D.带有强亲水基团的聚丙烯酸钠常用作高吸水性树脂
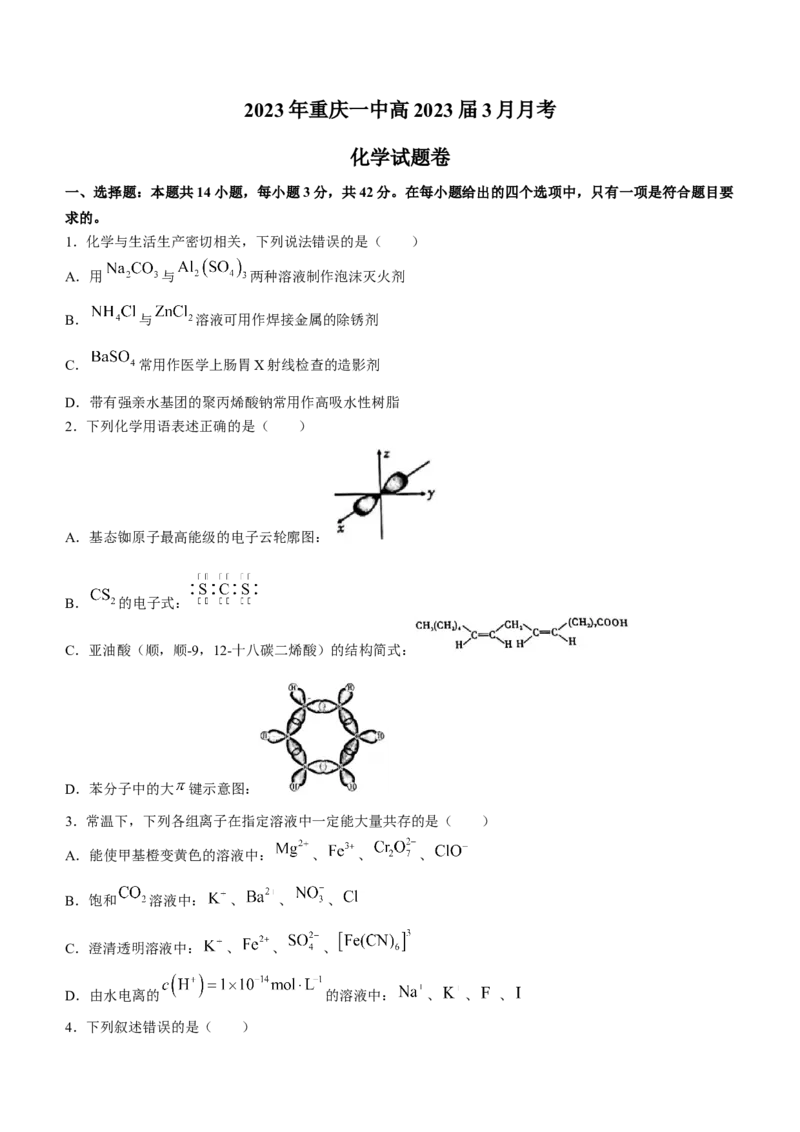
2.下列化学用语表述正确的是( )
A.基态铷原子最高能级的电子云轮廓图:
B. 的电子式:
C.亚油酸(顺,顺-9,12-十八碳二烯酸)的结构简式:
D.苯分子中的大 键示意图:
3.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.能使甲基橙变黄色的溶液中: 、 、 、
B.饱和 溶液中: 、 、 、
C.澄清透明溶液中: 、 、 、
D.由水电离的 的溶液中: 、 、 、
4.下列叙述错误的是( )
学科网(北京)股份有限公司A.向 固体中分别通入 和 气体,均能得到大量
B.过量 分别通入 溶液和 溶液中,均可看到溶液先浑浊后澄清
C. 使溴水褪色与乙烯使 溶液褪色的原型相同
D.饱和 溶液和浓硝酸均可使鸡蛋清溶液产生沉淀,但原理不同
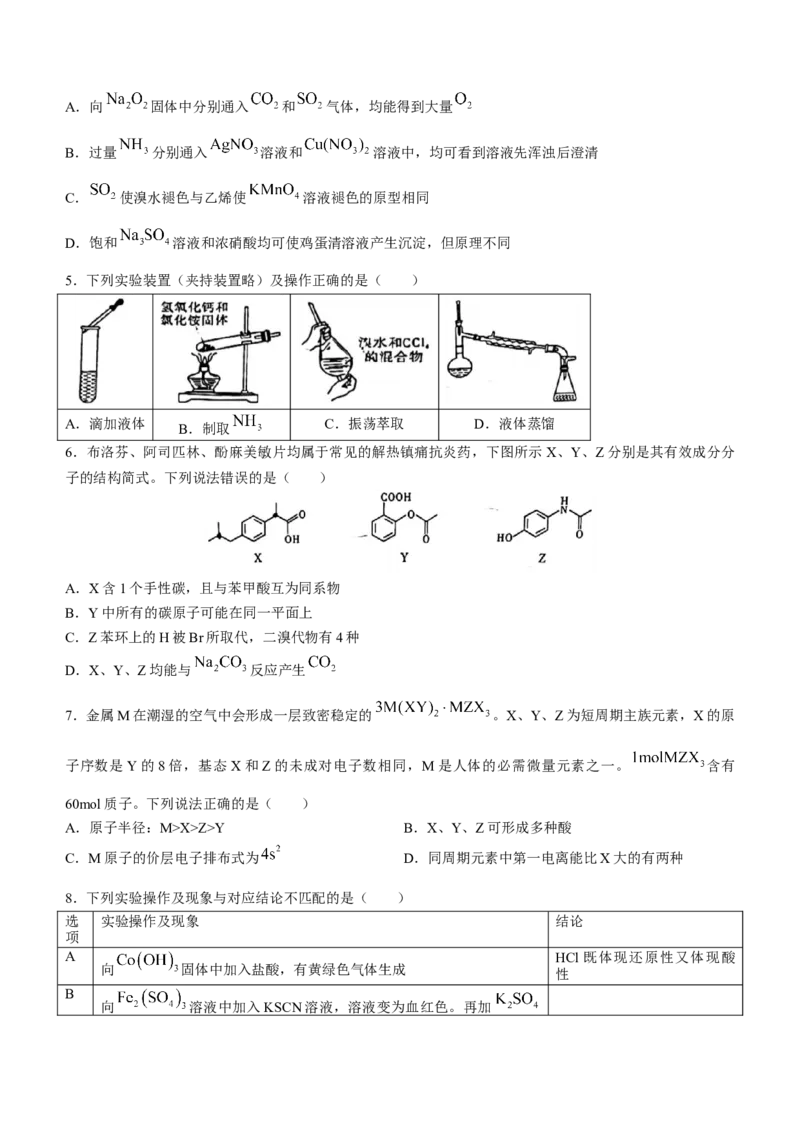
5.下列实验装置(夹持装置略)及操作正确的是( )
A.滴加液体
B.制取
C.振荡萃取 D.液体蒸馏
6.布洛芬、阿司匹林、酚麻美敏片均属于常见的解热镇痛抗炎药,下图所示X、Y、Z分别是其有效成分分
子的结构简式。下列说法错误的是( )
A.X含1个手性碳,且与苯甲酸互为同系物
B.Y中所有的碳原子可能在同一平面上
C.Z苯环上的H被Br所取代,二溴代物有4种
D.X、Y、Z均能与 反应产生
7.金属M在潮湿的空气中会形成一层致密稳定的 。X、Y、Z为短周期主族元素,X的原
子序数是Y的8倍,基态X和Z的未成对电子数相同,M是人体的必需微量元素之一。 含有
60mol质子。下列说法正确的是( )
A.原子半径:M>X>Z>Y B.X、Y、Z可形成多种酸
C.M原子的价层电子排布式为 D.同周期元素中第一电离能比X大的有两种
8.下列实验操作及现象与对应结论不匹配的是( )
选 实验操作及现象 结论
项
A HCl 既体现还原性又体现酸
向 固体中加入盐酸,有黄绿色气体生成
性
B
向 溶液中加入KSCN溶液,溶液变为血红色。再加
学科网(北京)股份有限公司固体,无明显现象。 与KSCN的反应具有不可逆性
C
向 溶液中通入 气体有黑色沉淀生成 结合 的能力:
D 相同条件下Na分别与水和无水乙醇反应,前者产生气体的速率更快
结 合 的 能 力 :
9. 代表阿伏加德罗常数的值。下列说法正确的是( )
A.密闭容器中 与 反应制备 ,增加的P-Cl位数目小于
B.12g石墨烯(单层石墨)中含有六元环的数目与12g金刚石中所含有化学键的数目均为
C.8.96L氢气、一氧化碳的混合气体完全燃烧,消耗氧分子的数目为
D. 反应中,生成 时,转移的电子数目为
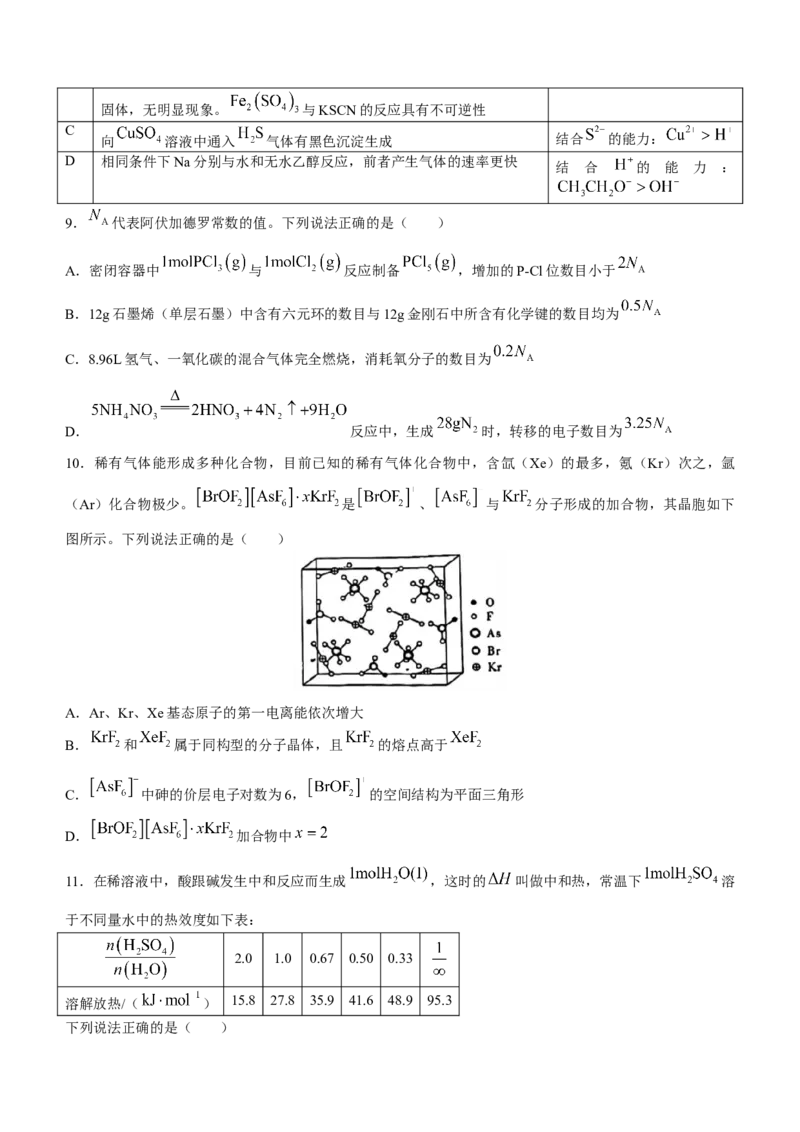
10.稀有气体能形成多种化合物,目前已知的稀有气体化合物中,含氙(Xe)的最多,氪(Kr)次之,氩
(Ar)化合物极少。 是 、 与 分子形成的加合物,其晶胞如下
图所示。下列说法正确的是( )
A.Ar、Kr、Xe基态原子的第一电离能依次增大
B. 和 属于同构型的分子晶体,且 的熔点高于
C. 中砷的价层电子对数为6, 的空间结构为平面三角形
D. 加合物中
11.在稀溶液中,酸跟碱发生中和反应而生成 ,这时的 叫做中和热,常温下 溶
于不同量水中的热效度如下表:
2.0 1.0 0.67 0.50 0.33
溶解放热/( ) 15.8 27.8 35.9 41.6 48.9 95.3
下列说法正确的是( )
学科网(北京)股份有限公司A.硫酸溶于水时破坏范德华力、氢键、离子键和共价键
B.当 时,溶解放热
C.向 的溶液中加入9g水,放出热量6.9kJ
D.用 的溶液测定中和热会使结果偏大
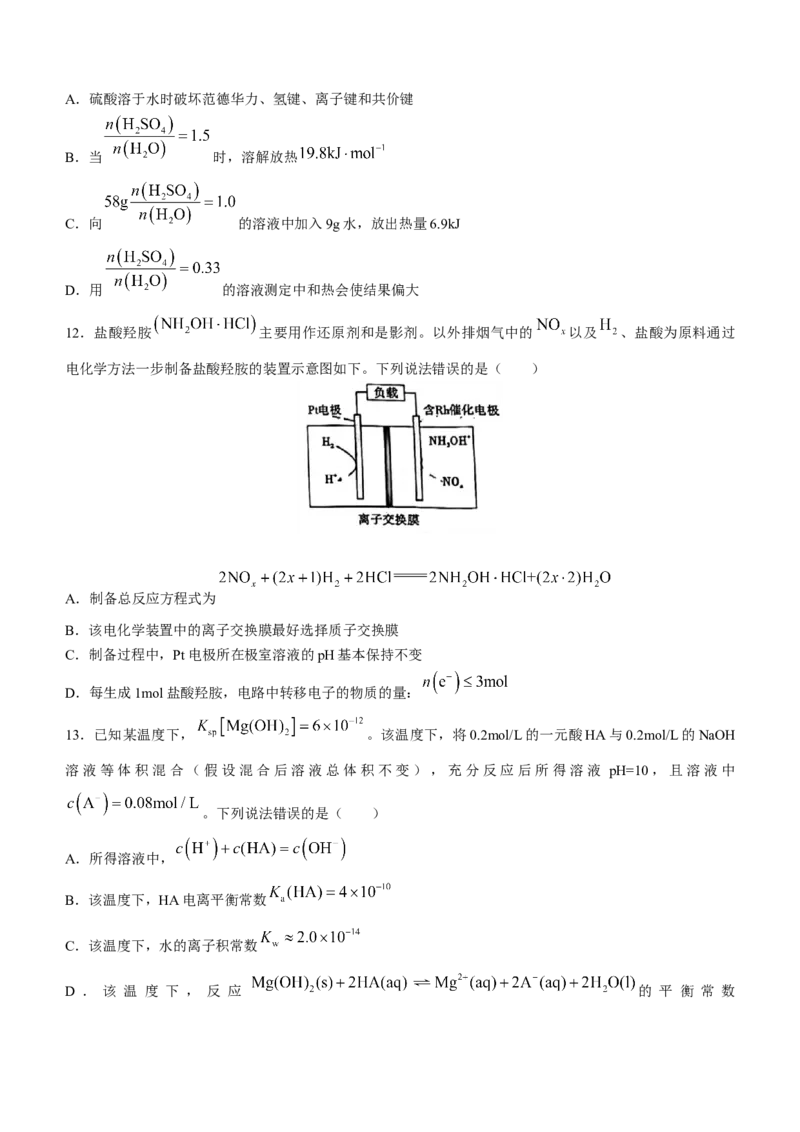
12.盐酸羟胺 主要用作还原剂和是影剂。以外排烟气中的 以及 、盐酸为原料通过
电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是( )
A.制备总反应方程式为
B.该电化学装置中的离子交换膜最好选择质子交换膜
C.制备过程中,Pt电极所在极室溶液的pH基本保持不变
D.每生成1mol盐酸羟胺,电路中转移电子的物质的量:
13.已知某温度下, 。该温度下,将0.2mol/L的一元酸HA与0.2mol/L的NaOH
溶液等体积混合(假设混合后溶液总体积不变),充分反应后所得溶液 pH=10,且溶液中
。下列说法错误的是( )
A.所得溶液中,
B.该温度下,HA电离平衡常数
C.该温度下,水的离子积常数
D . 该 温 度 下 , 反 应 的 平 衡 常 数
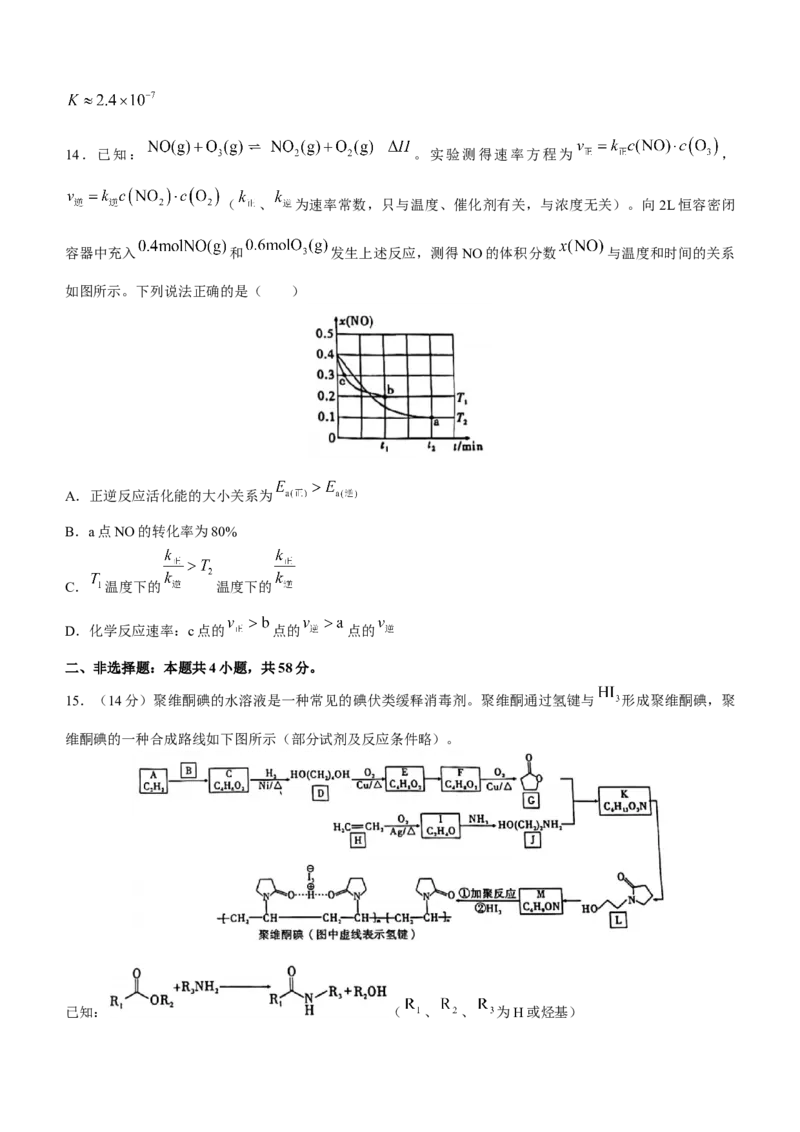
学科网(北京)股份有限公司14.已知: 。实验测得速率方程为 ,
( 、 为速率常数,只与温度、催化剂有关,与浓度无关)。向2L恒容密闭
容器中充入 和 发生上述反应,测得NO的体积分数 与温度和时间的关系
如图所示。下列说法正确的是( )
A.正逆反应活化能的大小关系为
B.a点NO的转化率为80%
C. 温度下的 温度下的
D.化学反应速率:c点的 点的 点的
二、非选择题:本题共4小题,共58分。
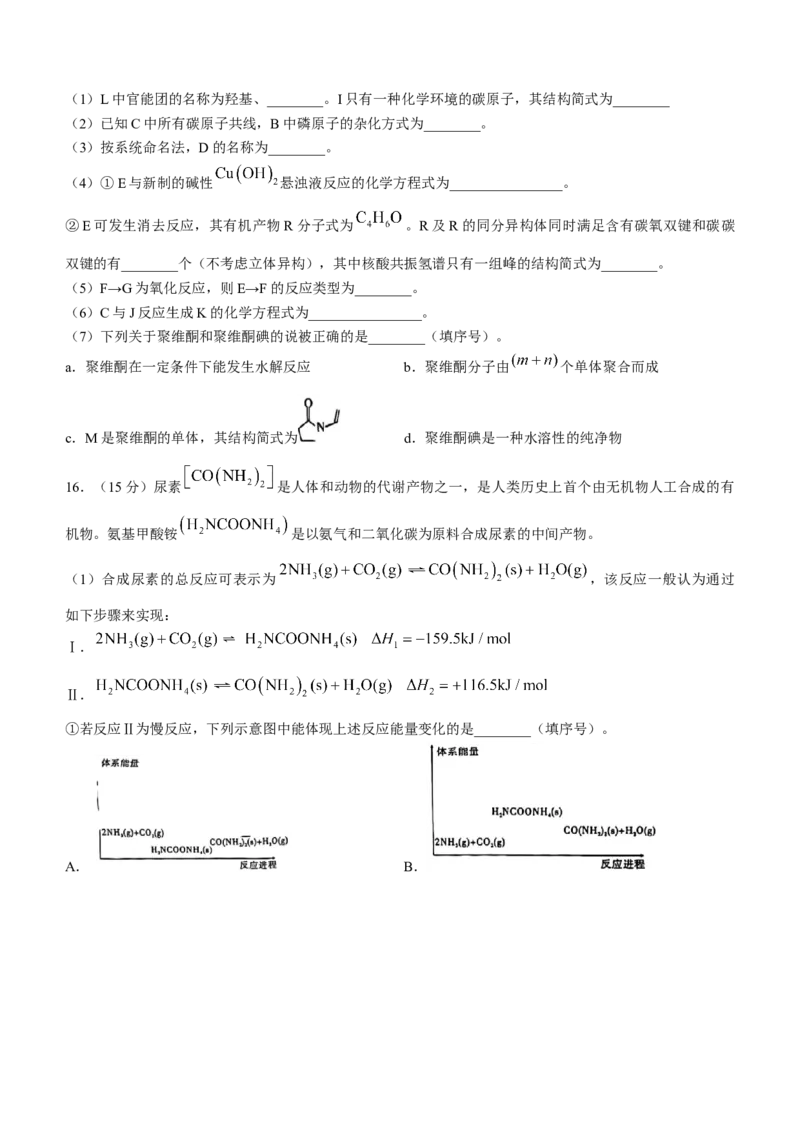
15.(14分)聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂。聚维酮通过氢键与 形成聚维酮碘,聚
维酮碘的一种合成路线如下图所示(部分试剂及反应条件略)。
已知: ( 、 、 为H或烃基)
学科网(北京)股份有限公司(1)L中官能团的名称为羟基、________。I只有一种化学环境的碳原子,其结构简式为________
(2)已知C中所有碳原子共线,B中磷原子的杂化方式为________。
(3)按系统命名法,D的名称为________。
(4)①E与新制的碱性 悬浊液反应的化学方程式为________________。
②E可发生消去反应,其有机产物R分子式为 。R及R的同分异构体同时满足含有碳氧双键和碳碳
双键的有________个(不考虑立体异构),其中核酸共振氢谱只有一组峰的结构简式为________。
(5)F→G为氧化反应,则E→F的反应类型为________。
(6)C与J反应生成K的化学方程式为________________。
(7)下列关于聚维酮和聚维酮碘的说被正确的是________(填序号)。
a.聚维酮在一定条件下能发生水解反应 b.聚维酮分子由 个单体聚合而成
c.M是聚维酮的单体,其结构简式为 d.聚维酮碘是一种水溶性的纯净物
16.(15分)尿素 是人体和动物的代谢产物之一,是人类历史上首个由无机物人工合成的有
机物。氨基甲酸铵 是以氨气和二氧化碳为原料合成尿素的中间产物。
(1)合成尿素的总反应可表示为 ,该反应一般认为通过
如下步骤来实现:
Ⅰ.
Ⅱ.
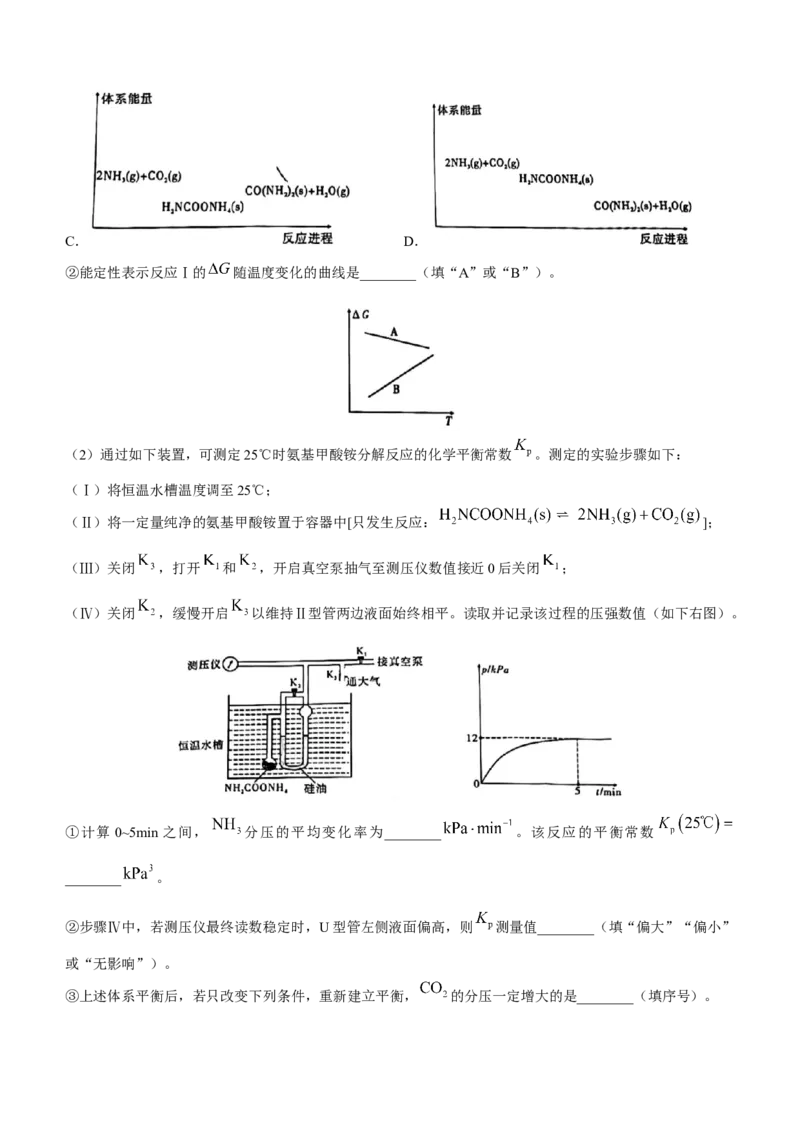
①若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是________(填序号)。
A. B.
学科网(北京)股份有限公司C. D.
②能定性表示反应Ⅰ的 随温度变化的曲线是________(填“A”或“B”)。
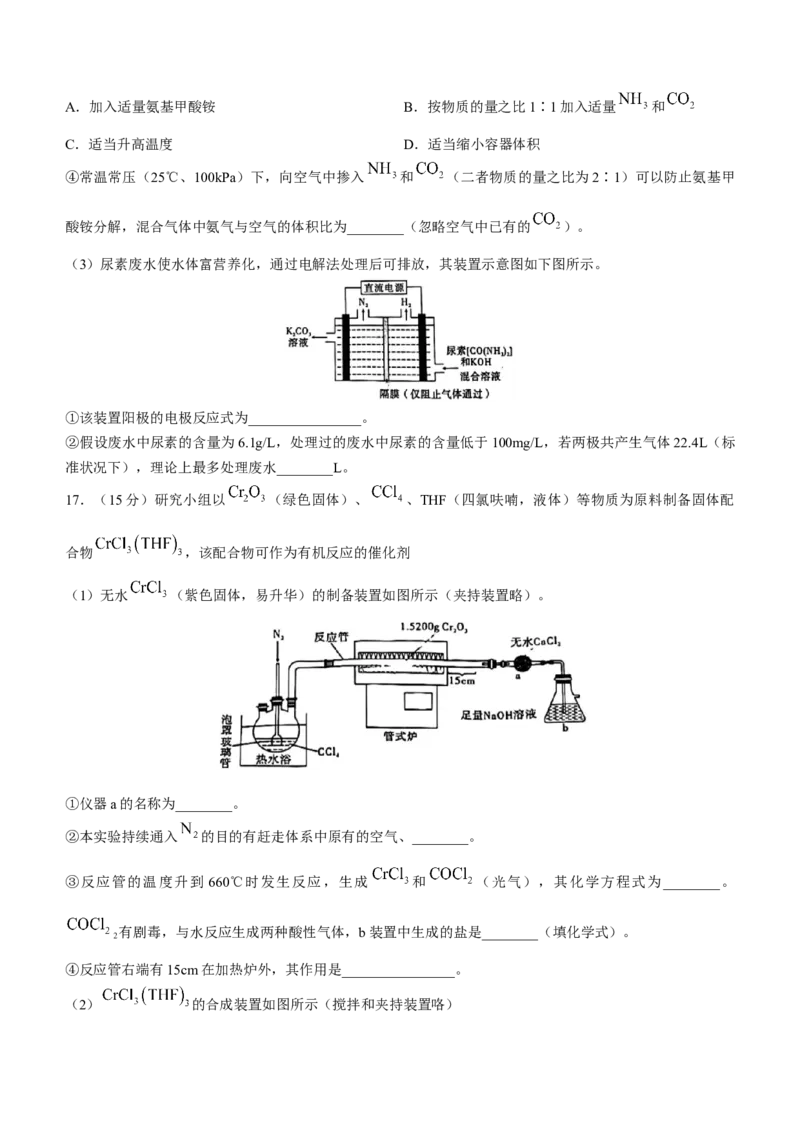
(2)通过如下装置,可测定25℃时氨基甲酸铵分解反应的化学平衡常数 。测定的实验步骤如下:
(Ⅰ)将恒温水槽温度调至25℃;
(Ⅱ)将一定量纯净的氨基甲酸铵置于容器中[只发生反应: ];
(Ⅲ)关闭 ,打开 和 ,开启真空泵抽气至测压仪数值接近0后关闭 ;
(Ⅳ)关闭 ,缓慢开启 以维持Ⅱ型管两边液面始终相平。读取并记录该过程的压强数值(如下右图)。
①计算 0~5min 之间, 分压的平均变化率为________ 。该反应的平衡常数
________ 。
②步骤Ⅳ中,若测压仪最终读数稳定时,U型管左侧液面偏高,则 测量值________(填“偏大”“偏小”
或“无影响”)。
③上述体系平衡后,若只改变下列条件,重新建立平衡, 的分压一定增大的是________(填序号)。
学科网(北京)股份有限公司A.加入适量氨基甲酸铵 B.按物质的量之比1∶1加入适量 和
C.适当升高温度 D.适当缩小容器体积
④常温常压(25℃、100kPa)下,向空气中掺入 和 (二者物质的量之比为2∶1)可以防止氨基甲
酸铵分解,混合气体中氨气与空气的体积比为________(忽略空气中已有的 )。
(3)尿素废水使水体富营养化,通过电解法处理后可排放,其装置示意图如下图所示。
①该装置阳极的电极反应式为________________。
②假设废水中尿素的含量为6.1g/L,处理过的废水中尿素的含量低于100mg/L,若两极共产生气体22.4L(标
准状况下),理论上最多处理废水________L。
17.(15分)研究小组以 (绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配
合物 ,该配合物可作为有机反应的催化剂
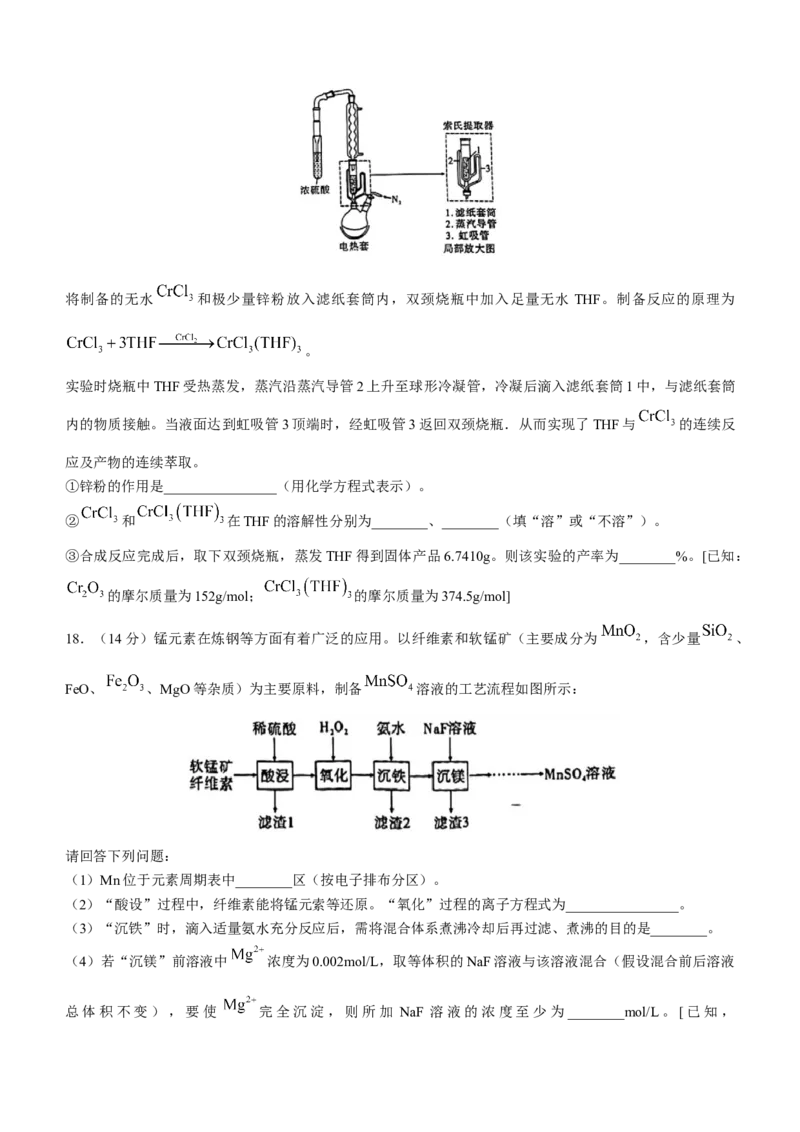
(1)无水 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
①仪器a的名称为________。
②本实验持续通入 的目的有赶走体系中原有的空气、________。
③反应管的温度升到 660℃时发生反应,生成 和 (光气),其化学方程式为________。
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是________(填化学式)。
2
④反应管右端有15cm在加热炉外,其作用是________________。
(2) 的合成装置如图所示(搅拌和夹持装置咯)
学科网(北京)股份有限公司将制备的无水 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水 THF。制备反应的原理为
。
实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒
内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与 的连续反
应及产物的连续萃取。
①锌粉的作用是________________(用化学方程式表示)。
② 和 在THF的溶解性分别为________、________(填“溶”或“不溶”)。
③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为________%。[已知:
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
18.(14分)锰元素在炼钢等方面有着广泛的应用。以纤维素和软锰矿(主要成分为 ,含少量 、
FeO、 、MgO等杂质)为主要原料,制备 溶液的工艺流程如图所示:
请回答下列问题:
(1)Mn位于元素周期表中________区(按电子排布分区)。
(2)“酸设”过程中,纤维素能将锰元索等还原。“氧化”过程的离子方程式为________________。
(3)“沉铁”时,滴入适量氨水充分反应后,需将混合体系煮沸冷却后再过滤、煮沸的目的是________。
(4)若“沉镁”前溶液中 浓度为0.002mol/L,取等体积的NaF溶液与该溶液混合(假设混合前后溶液
总体积不变),要使 完全沉淀,则所加 NaF 溶液的浓度至少为________mol/L。[已知,
学科网(北京)股份有限公司, ]
(5) 溶液中锰元素含量的测定:取 溶液于锥形瓶中,滴加2~3滴铬黑 作指
示剂,用 标准液滴定至终点,消耗标准液15.00mL.
滴定原理如下: (蓝色) (红色)
(无色) (无色)
①滴定终点的颜色变化为________________。
② 溶液中锰元素含量为________g/L。
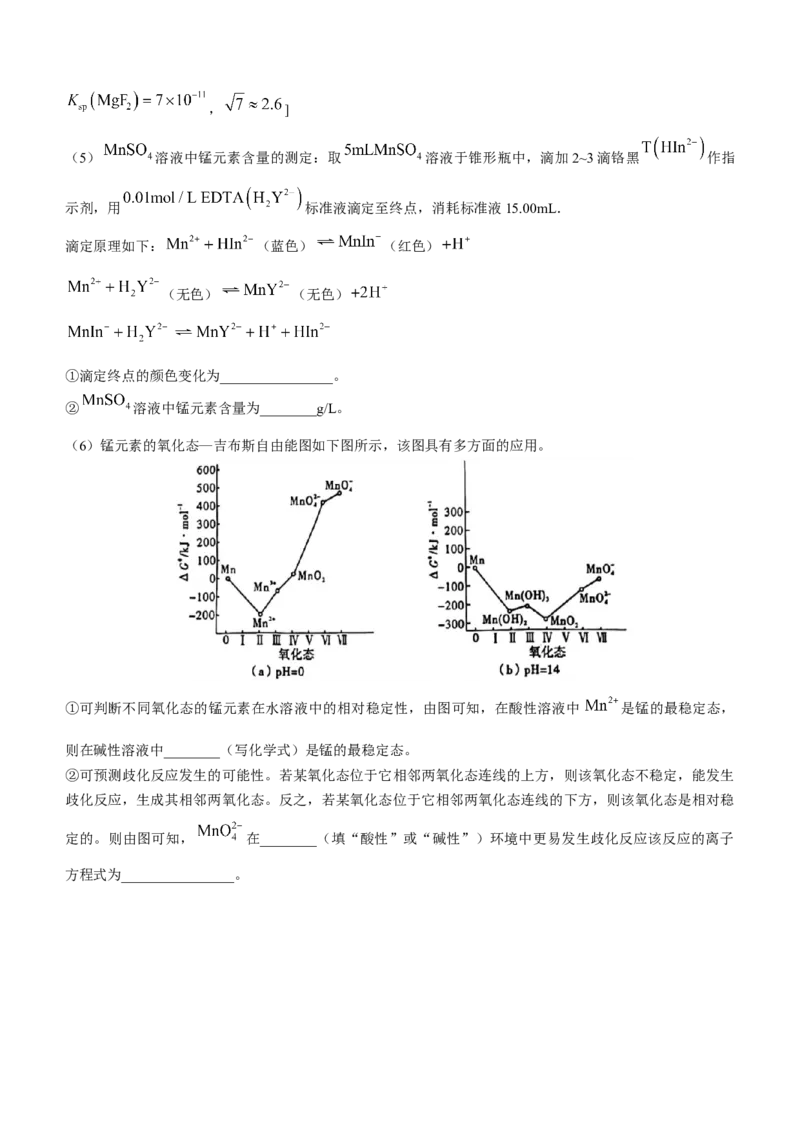
(6)锰元素的氧化态—吉布斯自由能图如下图所示,该图具有多方面的应用。
①可判断不同氧化态的锰元素在水溶液中的相对稳定性,由图可知,在酸性溶液中 是锰的最稳定态,
则在碱性溶液中________(写化学式)是锰的最稳定态。
②可预测歧化反应发生的可能性。若某氧化态位于它相邻两氧化态连线的上方,则该氧化态不稳定,能发生
歧化反应,生成其相邻两氧化态。反之,若某氧化态位于它相邻两氧化态连线的下方,则该氧化态是相对稳
定的。则由图可知, 在________(填“酸性”或“碱性”)环境中更易发生歧化反应该反应的离子
方程式为________________。
学科网(北京)股份有限公司学科网(北京)股份有限公司