文档内容
重庆市高 2023 届高三第一次质量检测
化学试题
命审单位:重庆南开中学
考生注意:
1.本试卷满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。必须在题号所指示的答题区域作答,超出答题区域
书写的答案无效,在试题卷、草稿纸上答题无效。
可能用到的相对原子质量:
一、选择题:本题共 14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
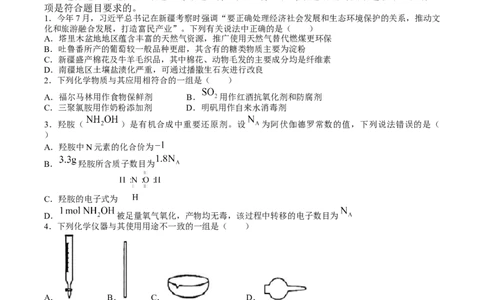
1.今年7月,习近平总书记在新疆考察时强调“要正确处理经济社会发展和生态环境保护的关系,推动文
化和旅游融合发展,打造富民产业”。下列有关说法中正确的是( )
A.塔里木盆地地区蕴含丰富的天然气资源,推广使用天然气替代燃煤更环保
B.吐鲁番所产的葡萄较一般品种更甜,其含有的糖类物质主要为淀粉
C.新疆盛产棉花及牛羊毛织品,其中棉花、动物毛发的主要成分均是纤维素
D.南疆地区土壤盐渍化严重,可通过播撒生石灰进行改良
2.下列化学物质与其应用相符合的一组是( )
A.福尔马林用作食物保鲜剂 B. 用作红酒抗氧化剂和防腐剂
C.三聚氯胺用作奶粉添加剂 D.明矾用作自来水消毒剂
3.羟胺( )是有机合成中重要还原剂。设 为阿伏伽德罗常数的值,下列说法错误的是(
)
A.羟胺中N元素的化合价为
B. 羟胺所含质子数目为
C.羟胺的电子式为
D. 被足量氧气氧化,产物均无毒,该过程中转移的电子数目为
4.下列化学仪器与其使用用途不一致的一组是( )
A. B. C. D.
A.盛装酸性高锰酸钾标准溶液
B.蘸取 溶液置于酒精灯上灼烧以观察 焰色
C. 溶液蒸发浓缩、冷却结晶
D.吸收氯气防止污染环境
5.不能正确表示下列变化的离子方程式的是( )
A.在漂白液中滴加少量稀硫酸以增强漂白性:
B.少量铁粉溶解在稀硝酸中:
C . 向 硫 酸 铝 溶 液 中 加 入 少 量 的 氢 氧 化 钡 溶 液 :D.自来水长期煮沸时生成水垢:
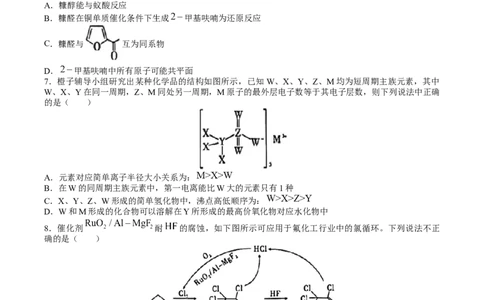
6.如图所示:糠醛可在不同催化剂作用下转化为糠醇或 甲基呋喃。下列说法正确的是( )
A.糠醇能与蚁酸反应
B.糠醛在铜单质催化条件下生成 甲基呋喃为还原反应
C.糠醛与 互为同系物
D. 甲基呋喃中所有原子可能共平面
7.橙子辅导小组研究出某种化学品的结构如图所示,已知W、X、Y、Z、M均为短周期主族元素,其中
W、X、Y在同一周期,Z、M同处另一周期,M原子的最外层电子数等于其电子层数,则下列说法中正确
的是( )
A.元素对应简单离子半径大小关系为:
B.在W的同周期主族元素中,第一电离能比W大的元素只有1种
C.X、Y、Z、W形成的简单氢化物中,沸点高低顺序为:
D.W和M形成的化合物可以溶解在Y所形成的最高价氧化物对应水化物中
8.催化剂 耐 的腐蚀,如下图所示可应用于氟化工行业中的氯循环。下列说法不正
确的是( )
A.若 的价电子排布式为 ,则该元素位于Ⅷ族
B.上述转化过程中涉及的有机反应类型有加成反应、消去反应
C.可通过液化分离出 中大多数的
D.上述循环中有水生成
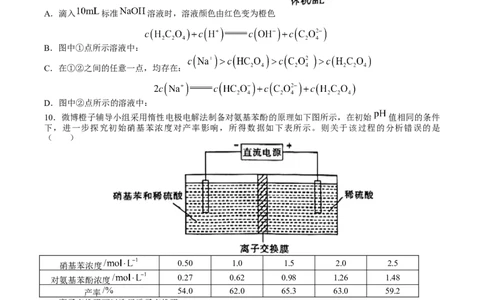
9.常温下,向 的草酸( )溶液中逐滴滴入等浓度的 溶液至过量,用
甲基橙(变色范围的 值为3.1~4.4)作指示剂,并用 计测定滴定过程的溶液 值变化,其滴定曲
线如图所示,则下列分析正确的是( )A.滴入 标准 溶液时,溶液颜色由红色变为橙色
B.图中①点所示溶液中:
C.在①②之间的任意一点,均存在:
D.图中②点所示的溶液中:
10.微博橙子辅导小组采用惰性电极电解法制备对氨基苯酚的原理如下图所示,在初始 值相同的条件
下,进一步探究初始硝基苯浓度对产率影响,所得数据如下表所示。则关于该过程的分析错误的是
( )
硝基苯浓度 0.50 1.0 1.5 2.0 2.5
对氨基苯酚浓度 0.27 0.62 0.98 1.26 1.48
产率 54.0 62.0 65.3 63.0 59.2
A.离子交换膜可以选择质子交换膜
B.阴极的电极反应式为:
C.当硝基苯初始浓度高于 ,产品产率反而降低,其原因可能是受产物溶解度的限制造成的
D.反应结束后,去掉离子交换膜,混匀两极室中溶液,溶液 值不变
11.硫元素的含氧酸根离子,有如下转化关系。下列说法正确的是( )
① ②③ ④
A.上述反应中 都只表现了还原性 B.反应④中表现了 价硫元素的强氧化性
C.反应③中消耗 同时生成 D.反应②中每消耗 转移电子数为
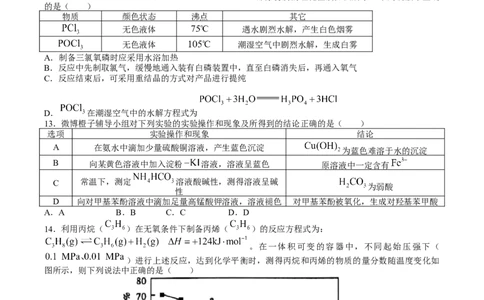
12.三氯氧磷( )是一种重要的化工原料,实验室采用加热条件下,用以下反应制备,
, 。部分物质的理化性质如图所示。下列说法不正确
的是( )
物质 颜色状态 沸点 其它
无色液体 遇水剧烈水解,产生白色烟雾
无色液体 潮湿空气中剧烈水解,生成白雾
A.制备三氯氧磷时应采用水浴加热
B.反应中先制取氯气,缓慢地通入装有白磷装置中,直至白磷消失后,再通入氧气
C.反应结束后,可采用重结晶的方式对产品进行提纯
D. 在潮湿空气中的水解方程式为
13.微博橙子辅导小组对下列实验的实验操作和现象及所得到的结论正确的是( )
选项 实验操作和现象 结论
A 在氨水中滴加少量硫酸铜溶液,产生蓝色沉淀
为蓝色难溶于水的沉淀
B 向某黄色溶液中加入淀粉 溶液,溶液呈蓝色 原溶液中一定含有
C 常温下,测定 溶液酸碱性,测得溶液呈碱
为弱酸
性
D 向对甲基苯酚溶液中滴加足量高锰酸钾溶液,溶液褪色 对甲基苯酚被氧化,生成对羟基苯甲酸
A.A B.B C.C D.D
14.利用丙烷( )在无氧条件下制备丙烯( )的反应方程式为:
。在一体积可变的容器中,不同起始压强下(
)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如
图所示,则下列说法中正确的是( )
A.c曲线表示的是 压强下丙烯随温度变化的物质的量分数B.A点对应的该反应平衡常数 ( 为以分压表示的平衡常数)
C.B点丙烷的平衡转化率为
D.实际生产过程中需通入一定量水蒸气,其目的是稀释原料气,增大丙烯的平衡产率
二、非选择题:共58分。
15.(14分)铬盐是一种重要的战略资源,广泛用于电镀、涂料、木材防腐等领域。其中,红矾钠(即重
铬酸钠晶体 )作为铬盐的母系产品,常用于制造其他铬系产品。铬的主要自然资源则是
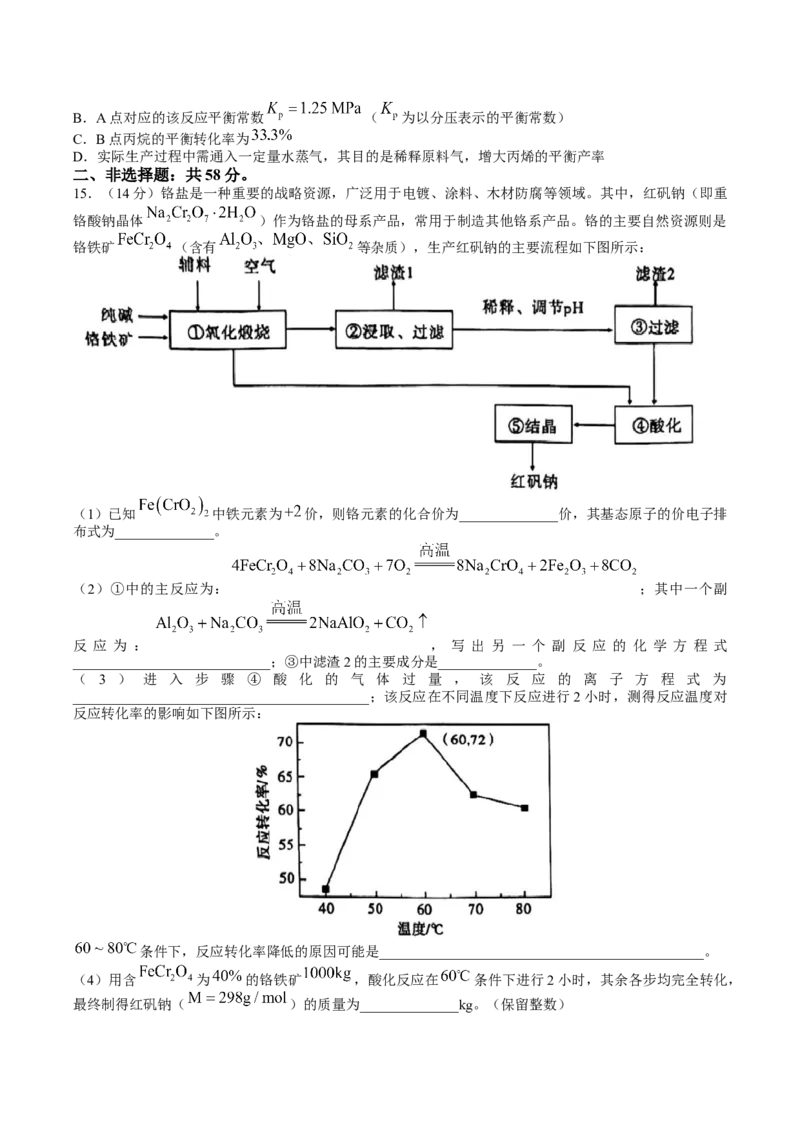
铬铁矿 (含有 等杂质),生产红矾钠的主要流程如下图所示:
(1)已知 中铁元素为 价,则铬元素的化合价为______________价,其基态原子的价电子排
布式为______________。
(2)①中的主反应为: ;其中一个副
反 应 为 : , 写 出 另 一 个 副 反 应 的 化 学 方 程 式
____________________________;③中滤渣2的主要成分是______________。
( 3 ) 进 入 步 骤 ④ 酸 化 的 气 体 过 量 , 该 反 应 的 离 子 方 程 式 为
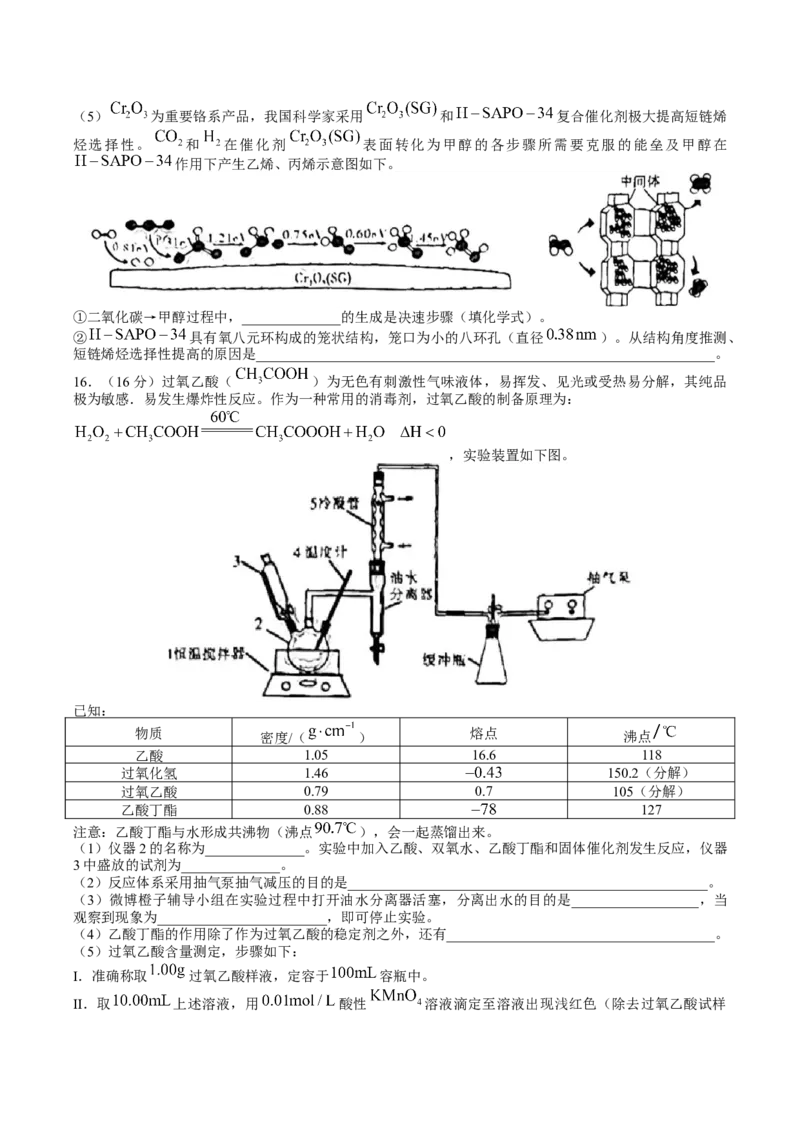
__________________________________________;该反应在不同温度下反应进行2小时,测得反应温度对
反应转化率的影响如下图所示:
条件下,反应转化率降低的原因可能是______________________________________________。
(4)用含 为 的铬铁矿 ,酸化反应在 条件下进行2小时,其余各步均完全转化,
最终制得红矾钠( )的质量为______________kg。(保留整数)(5) 为重要铬系产品,我国科学家采用 和 复合催化剂极大提高短链烯
烃选择性。 和 在催化剂 表面转化为甲醇的各步骤所需要克服的能垒及甲醇在
作用下产生乙烯、丙烯示意图如下。
①二氧化碳→甲醇过程中,______________的生成是决速步骤(填化学式)。
② 具有氧八元环构成的笼状结构,笼口为小的八环孔(直径 )。从结构角度推测、
短链烯烃选择性提高的原因是_________________________________________________________________。
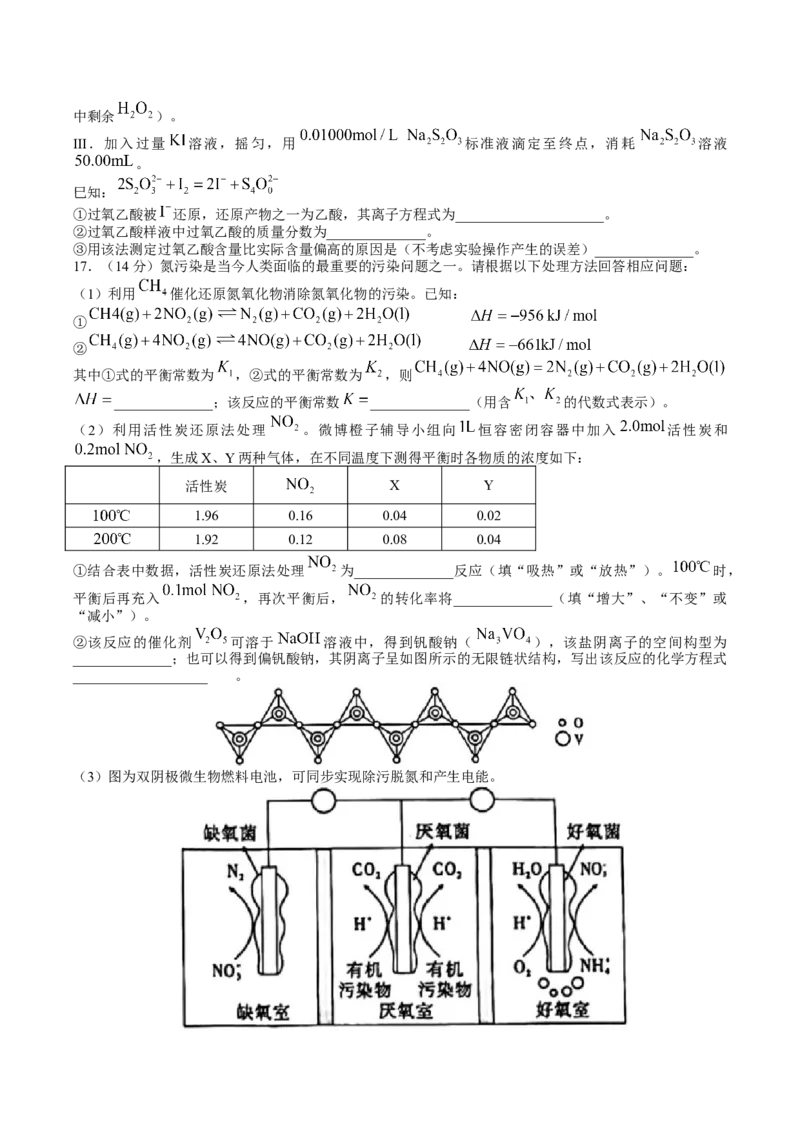
16.(16分)过氧乙酸( )为无色有刺激性气味液体,易挥发、见光或受热易分解,其纯品
极为敏感.易发生爆炸性反应。作为一种常用的消毒剂,过氧乙酸的制备原理为:
,实验装置如下图。
已知:
物质 密度/( ) 熔点 沸点
乙酸 1.05 16.6 118
过氧化氢 1.46 150.2(分解)
过氧乙酸 0.79 0.7 105(分解)
乙酸丁酯 0.88 127
注意:乙酸丁酯与水形成共沸物(沸点 ),会一起蒸馏出来。
(1)仪器2的名称为______________。实验中加入乙酸、双氧水、乙酸丁酯和固体催化剂发生反应,仪器
3中盛放的试剂为______________。
(2)反应体系采用抽气泵抽气减压的目的是___________________________________________________。
(3)微博橙子辅导小组在实验过程中打开油水分离器活塞,分离出水的目的是__________________,当
观察到现象为________________________,即可停止实验。
(4)乙酸丁酯的作用除了作为过氧乙酸的稳定剂之外,还有______________________________________。
(5)过氧乙酸含量测定,步骤如下:
I.准确称取 过氧乙酸样液,定容于 容瓶中。
II.取 上述溶液,用 酸性 溶液滴定至溶液出现浅红色(除去过氧乙酸试样中剩余 )。
III.加入过量 溶液,摇匀,用 标准液滴定至终点,消耗 溶液
。
巳知:
①过氧乙酸被 还原,还原产物之一为乙酸,其离子方程式为_____________________。
②过氧乙酸样液中过氧乙酸的质量分数为______________。
③用该法测定过氧乙酸含量比实际含量偏高的原因是(不考虑实验操作产生的误差)______________。
17.(14分)氮污染是当今人类面临的最重要的污染问题之一。请根据以下处理方法回答相应问题:
(1)利用 催化还原氮氧化物消除氮氧化物的污染。已知:
①
②
其中①式的平衡常数为 ,②式的平衡常数为 ,则
______________;该反应的平衡常数 ______________(用含 的代数式表示)。
(2)利用活性炭还原法处理 。微博橙子辅导小组向 恒容密闭容器中加入 活性炭和
,生成X、Y两种气体,在不同温度下测得平衡时各物质的浓度如下:
活性炭 X Y
1.96 0.16 0.04 0.02
1.92 0.12 0.08 0.04
①结合表中数据,活性炭还原法处理 为______________反应(填“吸热”或“放热”)。 时,
平衡后再充入 ,再次平衡后, 的转化率将______________(填“增大”、“不变”或
“减小”)。
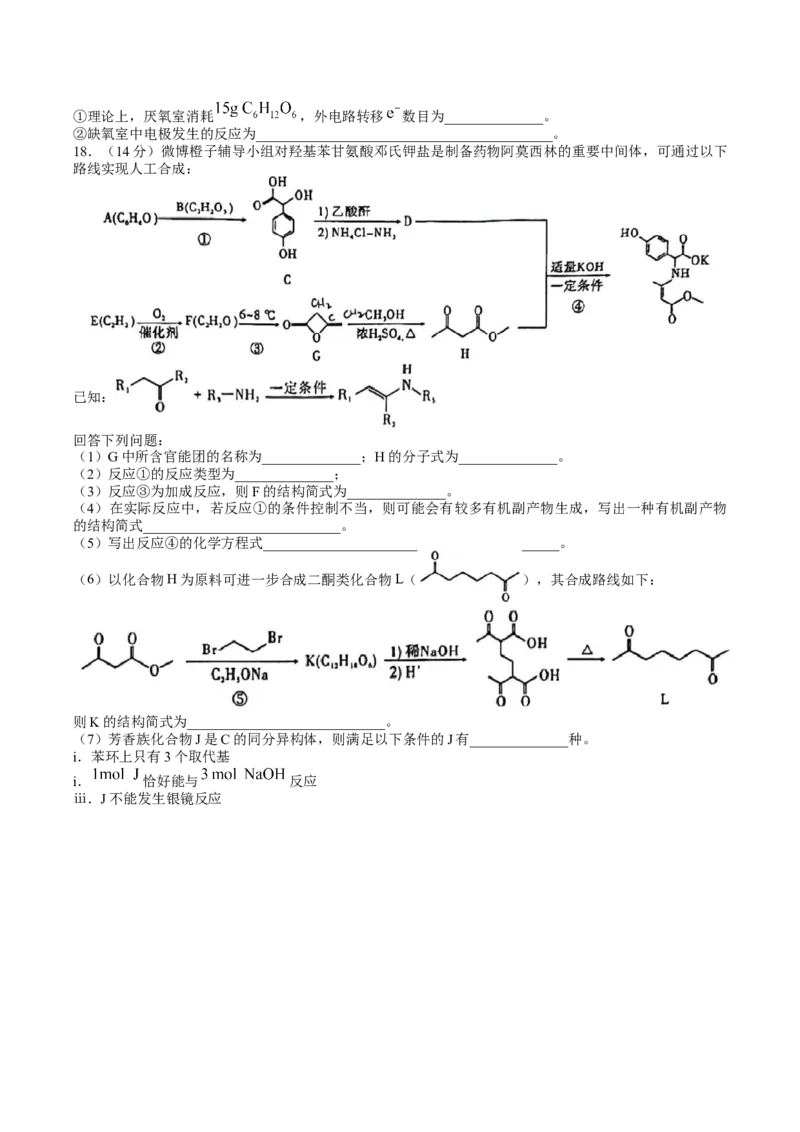
②该反应的催化剂 可溶于 溶液中,得到钒酸钠( ),该盐阴离子的空间构型为
______________;也可以得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,写出该反应的化学方程式
_______________________。
(3)图为双阴极微生物燃料电池,可同步实现除污脱氮和产生电能。①理论上,厌氧室消耗 ,外电路转移 数目为______________。
②缺氧室中电极发生的反应为__________________________________________。
18.(14分)微博橙子辅导小组对羟基苯甘氨酸邓氏钾盐是制备药物阿莫西林的重要中间体,可通过以下
路线实现人工合成:
已知:
回答下列问题:
(1)G中所含官能团的名称为______________;H的分子式为______________。
(2)反应①的反应类型为______________;
(3)反应③为加成反应,则F的结构简式为______________。
(4)在实际反应中,若反应①的条件控制不当,则可能会有较多有机副产物生成,写出一种有机副产物
的结构简式____________________________。
(5)写出反应④的化学方程式__________________________________________。
(6)以化合物H为原料可进一步合成二酮类化合物L( ),其合成路线如下:
则K的结构简式为____________________________。
(7)芳香族化合物J是C的同分异构体,则满足以下条件的J有______________种。
i.苯环上只有3个取代基
i. 恰好能与 反应
ⅲ.J不能发生银镜反应下载最新免费模拟卷,到公众号:一枚试卷君