文档内容
安康中学高2020级高三第一次检测性考试化学试题
可能用到的相对原子质量:H﹣1 C﹣12 O﹣14 S﹣32 Na﹣23 Ba﹣137 Cl﹣35.5 K﹣39 I﹣127
一、单项选择题(本共16小题,每小题3分,共48分)
1.2022年2月4日,第二十四届冬奥会在北京开幕,北京成为世界上首个“双奥之城”。本届冬奥会背后蕴
含了很多科技成果,下列说法正确的是( )
A.颁奖礼服内添加了石墨烯发热材料,石墨烯和 是同位
B.吉祥物冰墩墩的外壳使用了有机硅橡胶材料,属于硅酸盐材料
C.冬奥火炬“飞扬”使用氢气作为燃料,氢能属于新能源
D.国家速滑馆的冰面是采用超临界二氧化碳流体跨临界直冷制冰技术打造的,该过程是化学变化
2. 表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化
钠的一种制备方法是 。下列有关说法正确的是( )
A.12g石墨晶体含碳碳键数
B.1L 溶液中含阴离子的数目小于
C.生成1mol氧化产物时转移电子数为
D.通常状况下 中含质子的数目为
3.氯乙烷(沸点:12.5℃,熔点:﹣138.7℃)有如下转化关系:
设 表示阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,22.4L氯乙烷所含分子数为
B.25℃时, 的NaOH溶液中阴阳离子总数为
C.若有46g乙醇转化为乙醛时,乙醇得到的电子数为
D.若38g乙醛和甲醇的混合物中含有4g氢元素,则碳原子数目为
4.有机物M、N常用作合成香料的原料,结构如图。下列关于M、N的说法错误的是( )A.两者互为同系物
B.M能发生消去反应,且所得产物均存在顺反异构
C.N的分子式为
D.M、N均可以通过聚合反应生成可降解的高分子化合物
5.W、X、Y、Z四种短周期元素,在元素周期表中的位置如图所示,其中W元素的原子序数为Z元素原子
序数的两倍,则下列说法正确的是( )
Y Z
X W
A.X位于元素周期表中的第3周期第ⅥA族
B.X、Y、Z三种元素对应原子的半径依次减小
C. 和 的结构和化学性质相似
D.利用Y的含氧酸酸性强于W的含氧酸酸性,可证明非金属性W强于Y
6.下列有关实验操作与结论都正确的是( )
选项 实验操作及现象 实验结论
用洁净的铂丝蘸取某食盐试样,在酒精灯
A
火焰上灼烧,火焰显黄色 说明该食盐不含
向某无色溶液中滴加NaOH溶液,先产生 该无色溶液中一定有 ,无
B
白色沉淀,后沉淀又会全部消失
C 向尿液中加入新制 悬浊液,没 说明尿液中不含有葡萄糖
有砖红色沉淀生成
某待测液中先滴入氯水无明显现象,后滴
D 该待测液中一定含有
入硫氰化钾溶液出现血红色
7.通过实验得出的结论正确的是( )
A.将某固体试样完全溶于盐酸,再滴加 溶液,出现白色沉淀,则该固体试样中存在
B.将某固体试样完全溶于盐酸,再滴加KSCN溶液,没有出现血红色,则该固体试样中不存在
C.在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体试
样中仍可能存在
D.在某固体试样加水后的上层溶液中,滴加盐酸出现白色沉淀,再加 NaOH溶液沉淀溶解,则该固体试样中存在
8.某固体可能含有 、 、 、 、 、 中的几种离子,取等质量的两份该固体,进
行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量 溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍
有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体 0.672L(标
准状况)。下列说法正确的是( )
A.该固体中一定含有 、 、 、
B.该固体中一定没有 、 、
C.该固体中只含有 、 、 、
D.根据以上实验,无法确定该固体中有
9.关于反应 ,下列说法正确的是( )
A. 发生氧化反应 B.KI是还原产物
C.生成12.7g 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7:1
10.氢氧化铈 是一种重要的稀土氢氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉
末(含 、 、 ),某课题组以此粉末为原料回收铈,设计实验流程如下:
下列说法错误的是( )
A.滤渣A中主要含有 、
B.过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒
C.过程②中发生反应的离子方程式为D.过程④中消耗11.2L (已折合成标准状况),转移电子数为
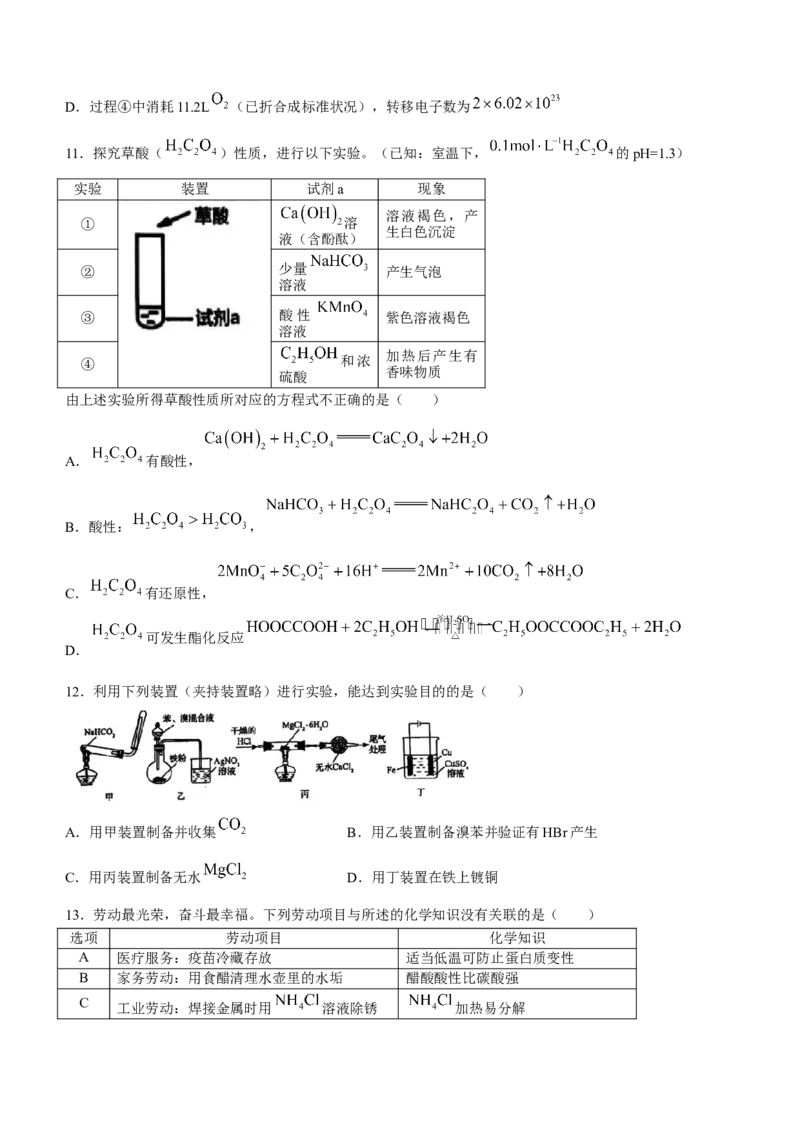
11.探究草酸( )性质,进行以下实验。(已知:室温下, 的pH=1.3)
实验 装置 试剂a 现象
溶液褐色,产
① 溶
生白色沉淀
液(含酚酞)
② 少量 产生气泡
溶液
③ 酸性 紫色溶液褐色
溶液
加热后产生有
④ 和浓
香味物质
硫酸
由上述实验所得草酸性质所对应的方程式不正确的是( )
A. 有酸性,
B.酸性: ,
C. 有还原性,
可发生酯化反应
D.
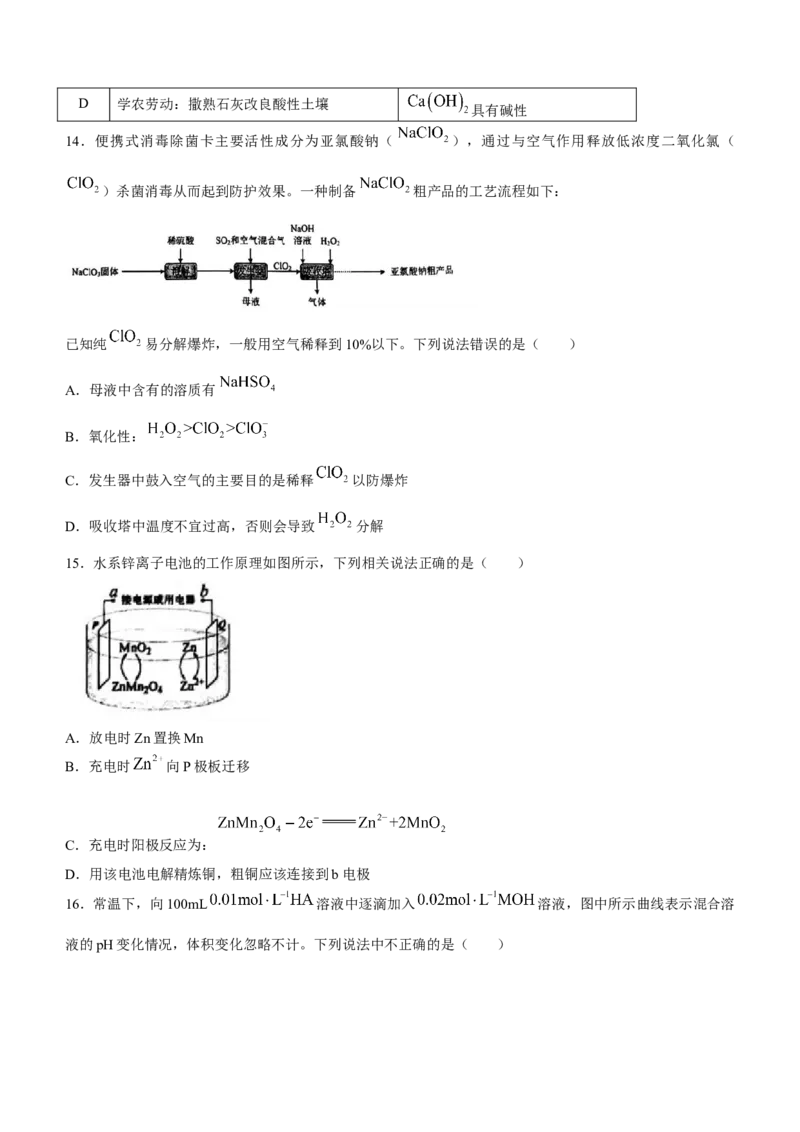
12.利用下列装置(夹持装置略)进行实验,能达到实验目的的是( )
A.用甲装置制备并收集 B.用乙装置制备溴苯并验证有HBr产生
C.用丙装置制备无水 D.用丁装置在铁上镀铜
13.劳动最光荣,奋斗最幸福。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 医疗服务:疫苗冷藏存放 适当低温可防止蛋白质变性
B 家务劳动:用食醋清理水壶里的水垢 醋酸酸性比碳酸强
C
工业劳动:焊接金属时用 溶液除锈 加热易分解D 学农劳动:撒熟石灰改良酸性土壤
具有碱性
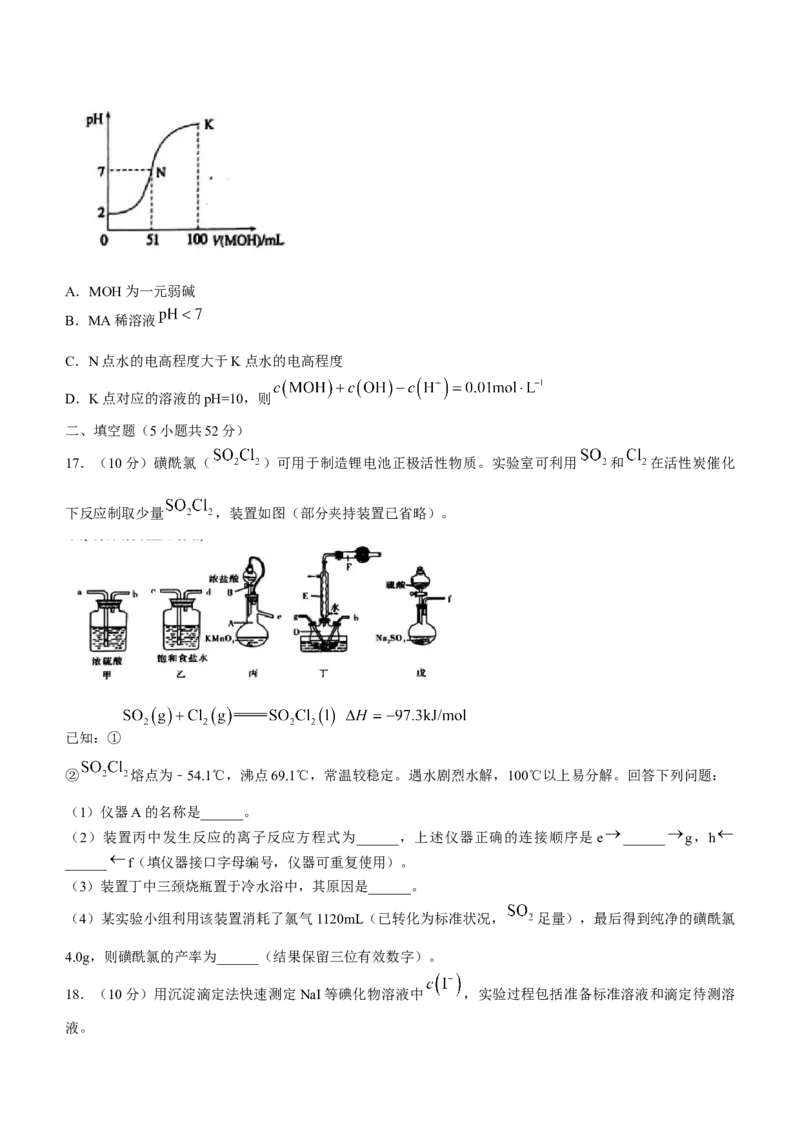
14.便携式消毒除菌卡主要活性成分为亚氯酸钠( ),通过与空气作用释放低浓度二氧化氯(
)杀菌消毒从而起到防护效果。一种制备 粗产品的工艺流程如下:
已知纯 易分解爆炸,一般用空气稀释到10%以下。下列说法错误的是( )
A.母液中含有的溶质有
B.氧化性:
C.发生器中鼓入空气的主要目的是稀释 以防爆炸
D.吸收塔中温度不宜过高,否则会导致 分解
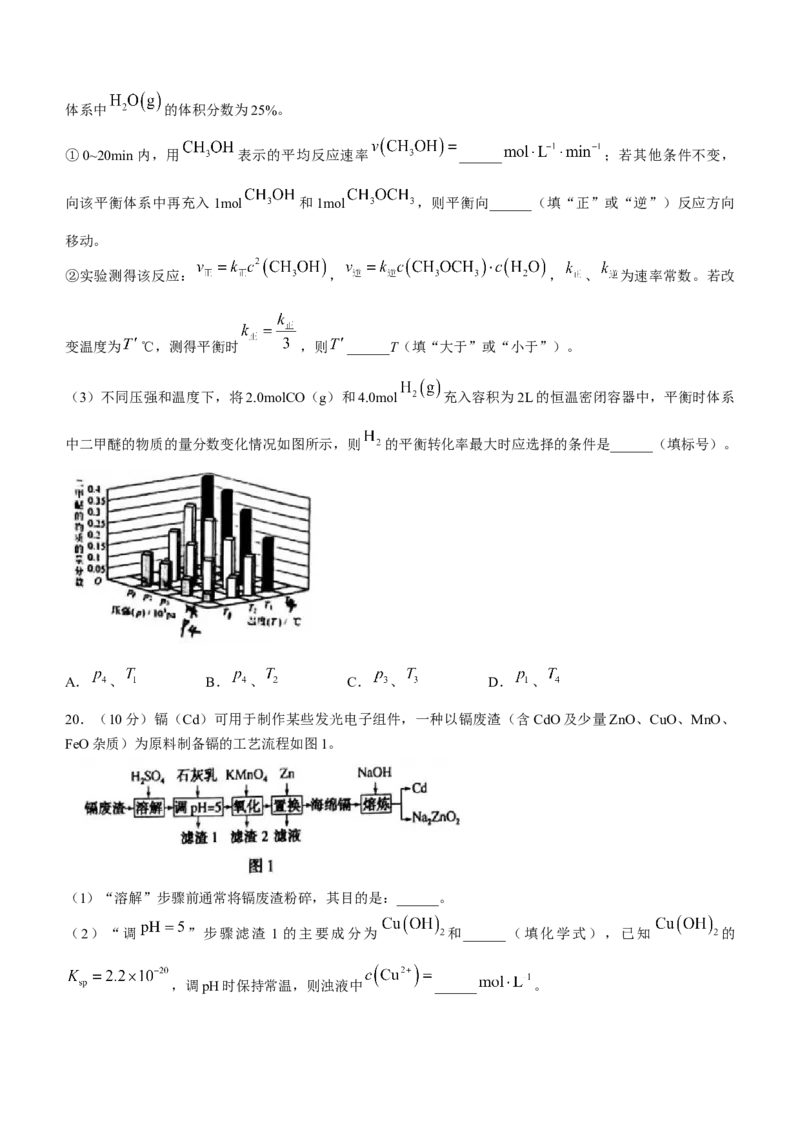
15.水系锌离子电池的工作原理如图所示,下列相关说法正确的是( )
A.放电时Zn置换Mn
B.充电时 向P极板迁移
C.充电时阳极反应为:
D.用该电池电解精炼铜,粗铜应该连接到b电极
16.常温下,向100mL 溶液中逐滴加入 溶液,图中所示曲线表示混合溶
液的pH变化情况,体积变化忽略不计。下列说法中不正确的是( )A.MOH为一元弱碱
B.MA稀溶液
C.N点水的电高程度大于K点水的电高程度
D.K点对应的溶液的pH=10,则
二、填空题(5小题共52分)
17.(10分)磺酰氯( )可用于制造锂电池正极活性物质。实验室可利用 和 在活性炭催化
下反应制取少量 ,装置如图(部分夹持装置已省略)。
已知:①
② 熔点为﹣54.1℃,沸点69.1℃,常温较稳定。遇水剧烈水解,100℃以上易分解。回答下列问题:
(1)仪器A的名称是______。
(2)装置丙中发生反应的离子反应方程式为______,上述仪器正确的连接顺序是e ______ g,h
______ f(填仪器接口字母编号,仪器可重复使用)。
(3)装置丁中三颈烧瓶置于冷水浴中,其原因是______。
(4)某实验小组利用该装置消耗了氯气1120mL(已转化为标准状况, 足量),最后得到纯净的磺酰氯
4.0g,则磺酰氯的产率为______(结果保留三位有效数字)。
18.(10分)用沉淀滴定法快速测定NaI等碘化物溶液中 ,实验过程包括准备标准溶液和滴定待测溶
液。Ⅰ.准备标准溶液
a.准确称取 (0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备
用。
b.配制并标定100mL 标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL 溶液(过量),使 完全转化为AgI沉淀。
c.加入 溶液作指示剂。
d.用 溶液滴定过量的 ,使其恰好完全转化为AgSCN沉淀后,体系出现淡红
色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号 1 2 3
10.24 10.02 9.98
消耗 标准溶液体积/mL
f.数据处理。回答下列问题:
(1)滴定应在 的条件下进行,其原因是______。
(2)b和c两步操作不能颠倒,说明理由______。
(3)计算 ______ 。
(4)判断下列操作对 测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制 标准溶液时,烧杯中的溶液有少量溅出,则测定结果______。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果______。
19.(10分)二甲酸( )是一种性能优良的汽车燃料,工业上可利用CO和 来合成二甲醚,
发生的反应为:
Ⅰ.
Ⅱ. 回答下列问题:
(1)由CO和 直接合成 的热化学反应方程式为______。
(2)T℃下,向体积为2L的恒容密闭容器中充入2mol 发生反应Ⅱ。20min时反应达平衡,测得体系中 的体积分数为25%。
①0~20min内,用 表示的平均反应速率 ______ ;若其他条件不变,
向该平衡体系中再充入1mol 和1mol ,则平衡向______(填“正”或“逆”)反应方向
移动。
②实验测得该反应: , , 、 为速率常数。若改
变温度为 ℃,测得平衡时 ,则 ______T(填“大于”或“小于”)。
(3)不同压强和温度下,将2.0molCO(g)和4.0mol 充入容积为2L的恒温密闭容器中,平衡时体系
中二甲醚的物质的量分数变化情况如图所示,则 的平衡转化率最大时应选择的条件是______(填标号)。
A. 、 B. 、 C. 、 D. 、
20.(10分)镉(Cd)可用于制作某些发光电子组件,一种以镉废渣(含CdO及少量ZnO、CuO、MnO、
FeO杂质)为原料制备镉的工艺流程如图1。
(1)“溶解”步骤前通常将镉废渣粉碎,其目的是:______。
(2)“调 ”步骤滤渣 1 的主要成分为 和______(填化学式),已知 的
,调pH时保持常温,则浊液中 ______ 。(3)“氧化”步骤的目的是除铁、除锰,已知 的还原产物是 ,则除锰的离子方程式为
______。
(4)“熔炼”时,将海绵镉(含Cd和Zn)与NaOH混合,在较高温度下反应,反应的化学方程式是______。
当观察到反应釜中______现象时,停止加热,利用Cd与 的密度不同,将Cd从反应釜下口放出,
以达到分离的目的。
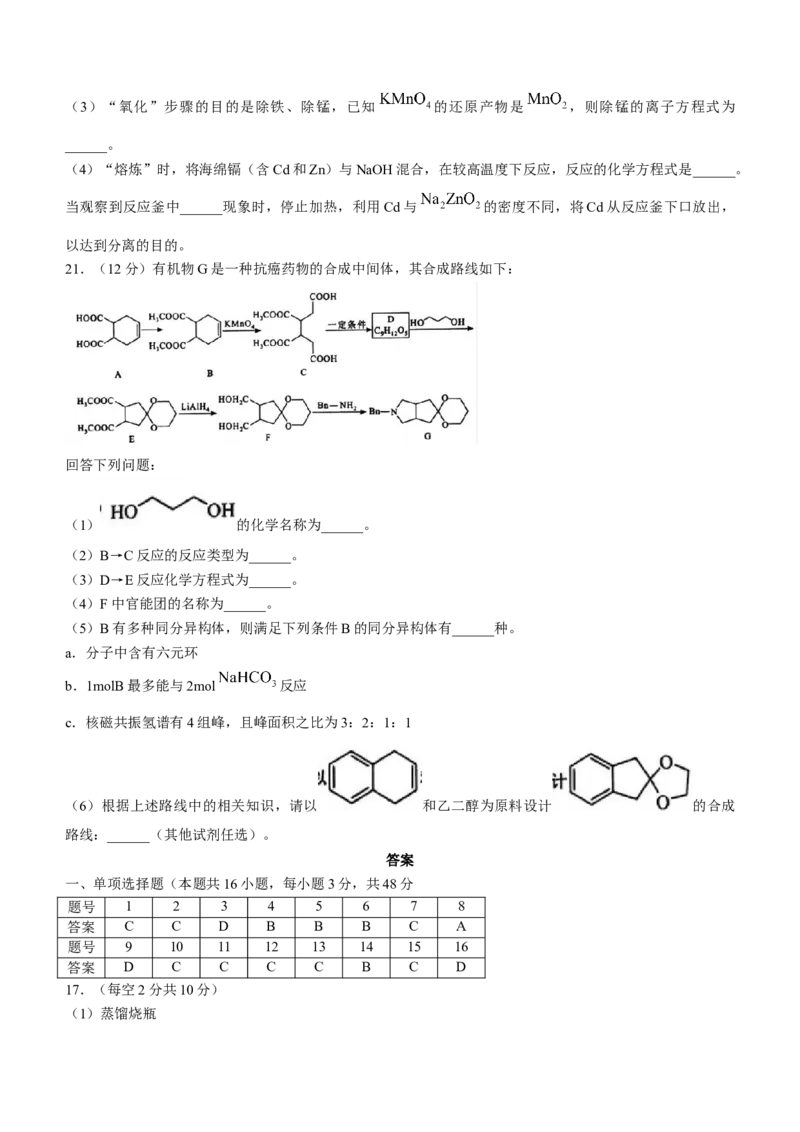
21.(12分)有机物G是一种抗癌药物的合成中间体,其合成路线如下:
回答下列问题:
(1) 的化学名称为______。
(2)B→C反应的反应类型为______。
(3)D→E反应化学方程式为______。
(4)F中官能团的名称为______。
(5)B有多种同分异构体,则满足下列条件B的同分异构体有______种。
a.分子中含有六元环
b.1molB最多能与2mol 反应
c.核磁共振氢谱有4组峰,且峰面积之比为3:2:1:1
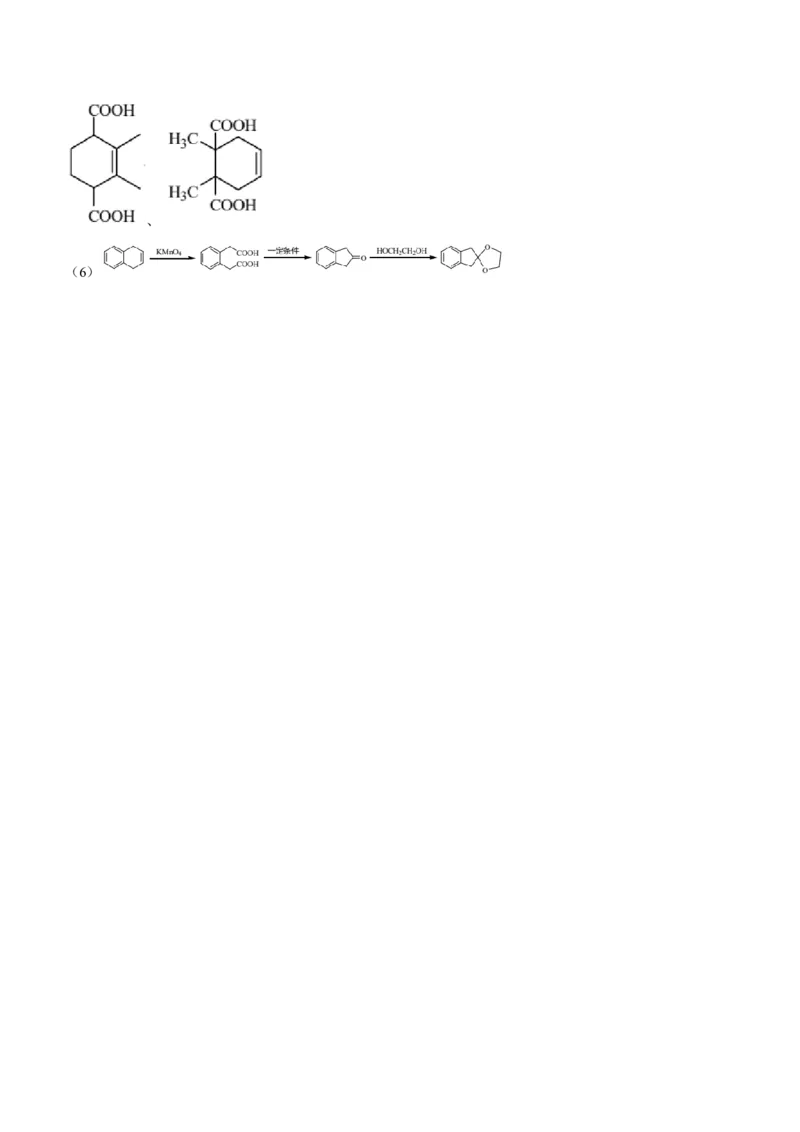
(6)根据上述路线中的相关知识,请以 和乙二醇为原料设计 的合成
路线:______(其他试剂任选)。
答案
一、单项选择题(本题共16小题,每小题3分,共48分
题号 1 2 3 4 5 6 7 8
答案 C C D B B B C A
题号 9 10 11 12 13 14 15 16
答案 D C C C C B C D
17.(每空2分共10分)
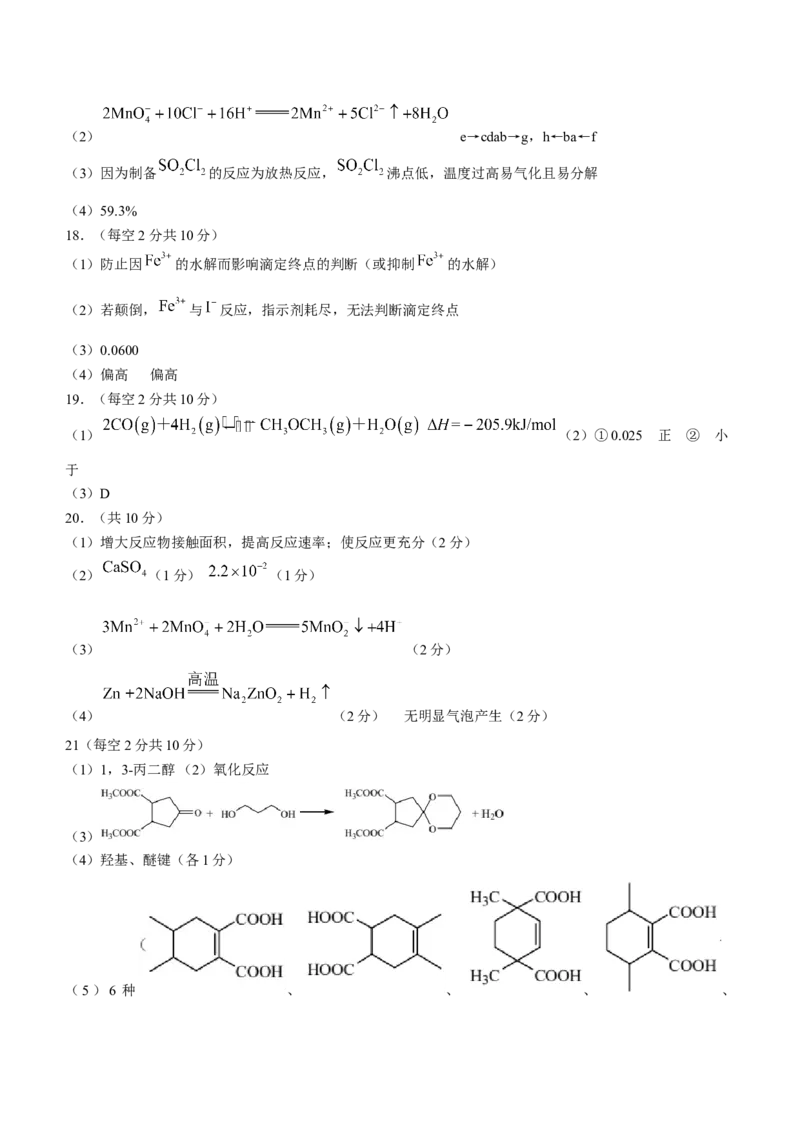
(1)蒸馏烧瓶(2) e→cdab→g,h←ba←f
(3)因为制备 的反应为放热反应, 沸点低,温度过高易气化且易分解
(4)59.3%
18.(每空2分共10分)
(1)防止因 的水解而影响滴定终点的判断(或抑制 的水解)
(2)若颠倒, 与 反应,指示剂耗尽,无法判断滴定终点
(3)0.0600
(4)偏高 偏高
19.(每空2分共10分)
(1) (2)①0.025 正 ② 小
于
(3)D
20.(共10分)
(1)增大反应物接触面积,提高反应速率;使反应更充分(2分)
(2) (1分) (1分)
(3) (2分)
(4) (2分) 无明显气泡产生(2分)
21(每空2分共10分)
(1)1,3-丙二醇(2)氧化反应
(3)
(4)羟基、醚键(各1分)
(5)6 种 、 、 、 、、
(6)