文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(江苏专用)
黄金卷01
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 下列做法能有效促进“碳中和”的是
A.火力发电 B.燃煤脱硫 C. 合成淀粉 D.可燃冰开采
2.反应 可用于制备还原剂肼(N H)。下列说法正确的是
2 4
A.HO为极性分子 B.NH 的空间构型为平面三角形
2 3
C.NaClO的电子式为 D.NH 中只含极性键
2 4
3. 利用废蚀刻液(含FeCl 、CuCl 及FeCl )制备碱性蚀刻液[Cu(NH )Cl 溶液]和FeCl •6H O步骤:用HO
2 2 3 3 4 2 3 2 2 2
氧化废蚀刻液、制备氨气、制备碱性蚀刻液[CuCl +4NH=Cu(NH)Cl]、固液分离、用盐酸溶解沉淀并制
2 3 3 4 2
备FeCl •6H O。下列有关实验的说法不正确的是
3 2
A.用装置甲制备氨气
B.用装置乙可以制备Cu(NH )Cl 溶液并沉铁
3 4 2
C.用装置丙可以分离Cu(NH )Cl 溶液和Fe(OH)
3 4 2 3
D.用装置丁蒸干FeCl 溶液可以直接制备FeCl •6H O
3 3 2
4.硼碳氮(BCN)材料可用作耐磨涂层。下列说法正确的是A.原子半径: B.第一电离能:
C.酸性强弱: D.硼、石墨、固态氮的晶体类型相同
阅读下列材料,回答5~7题:
海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠和氯元素。化学家常用廉价氯化钠
为原料制备纯碱,也可用于电解方法获得金属钠、氯气、氢气等,并进一步将其转化为生产、生活和科学
实验中用途更为广泛的新物质,如 、 、 等。
5.下列物质性质与用途具有对应关系的是
A. 溶液显碱性,可用作除油污剂B. 受热易分解,可用作抗酸药物
C. 具有还原性,可用作供氧剂 D. 具有强氧化性,可用作混凝剂
6.在指定条件下,下列选项所示的物质间转化能实现的是
A. B.
C. D.
7.下列说法正确的是
A.键角:
B.酸性:
C.侯氏制碱的反应:
D.电解饱和食盐水时,若两极共产生气体 (标准状况下),转移电子数为
8.硫及其化合物的转化具有重要应用。下列说法不正确的是
A.废水中的 可以被 还原后除去
B.大气中的 遇雨水最终形成 进入地面或海洋
C.工业排放尾气中的 可与 和 反应生成D.水垢中的 可与饱和 溶液反应生成
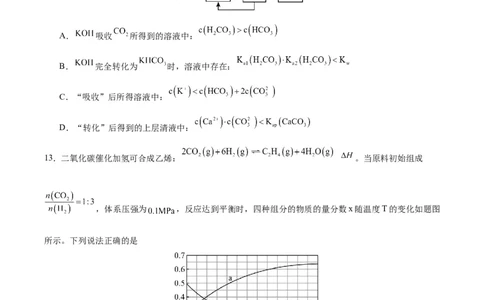
9.一种2-甲基色酮内酯(Y)可通过下列反应合成,下列说法正确的是
A.一定条件下,X可以发生加成、缩聚、消去、氧化反应
B.X、Y分子中所有碳原子处于同一平面
C.1molX最多能与含3molBr 的浓溴水发生反应
2
D.Y与H 完全加成,每个产物分子中含有5个手性碳原子
2
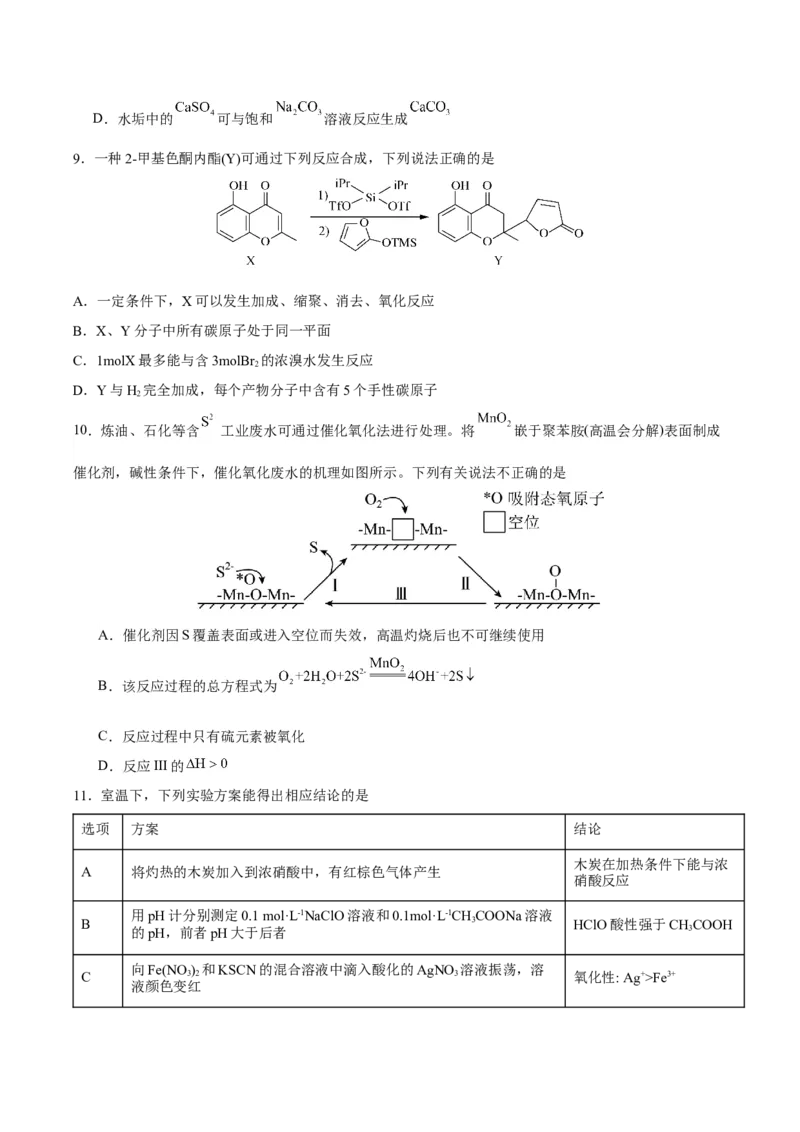
10.炼油、石化等含 工业废水可通过催化氧化法进行处理。将 嵌于聚苯胺(高温会分解)表面制成
催化剂,碱性条件下,催化氧化废水的机理如图所示。下列有关说法不正确的是
A.催化剂因S覆盖表面或进入空位而失效,高温灼烧后也不可继续使用
B.该反应过程的总方程式为
C.反应过程中只有硫元素被氧化
D.反应III的
11.室温下,下列实验方案能得出相应结论的是
选项 方案 结论
木炭在加热条件下能与浓
A 将灼热的木炭加入到浓硝酸中,有红棕色气体产生
硝酸反应
用pH计分别测定0.1 mol·L-1NaClO溶液和0.1mol·L-1CHCOONa溶液
B 3 HClO酸性强于CHCOOH
的pH,前者pH大于后者 3
向Fe(NO ) 和KSCN的混合溶液中滴入酸化的AgNO 溶液振荡,溶
C 3 2 3 氧化性: Ag+>Fe3+
液颜色变红向NaSO 溶液中滴入酚酞试液,溶液变红,再加入BaCl 溶液后产生 NaSO 溶液中存在水解平
D 2 3 2 2 3
白色沉淀且红色褪去 衡
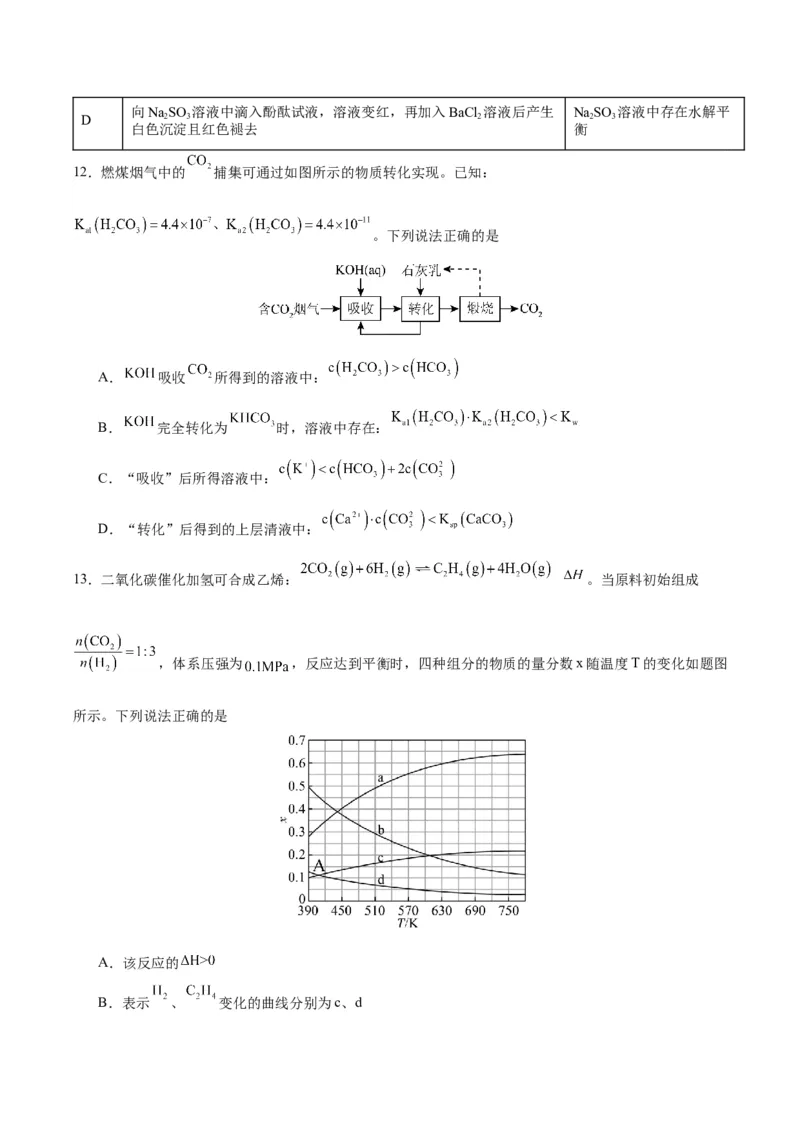
12.燃煤烟气中的 捕集可通过如图所示的物质转化实现。已知:
。下列说法正确的是
A. 吸收 所得到的溶液中:
B. 完全转化为 时,溶液中存在:
C.“吸收”后所得溶液中:
D.“转化”后得到的上层清液中:
13.二氧化碳催化加氢可合成乙烯: 。当原料初始组成
,体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图
所示。下列说法正确的是
A.该反应的
B.表示 、 变化的曲线分别为c、dC.A点对应温度为 ,此时 的转化率为66.7%
D.选择合适的催化剂可提高反应速率和乙烯的平衡产率
第Ⅱ卷
二、非选择题:共4题,共61分。
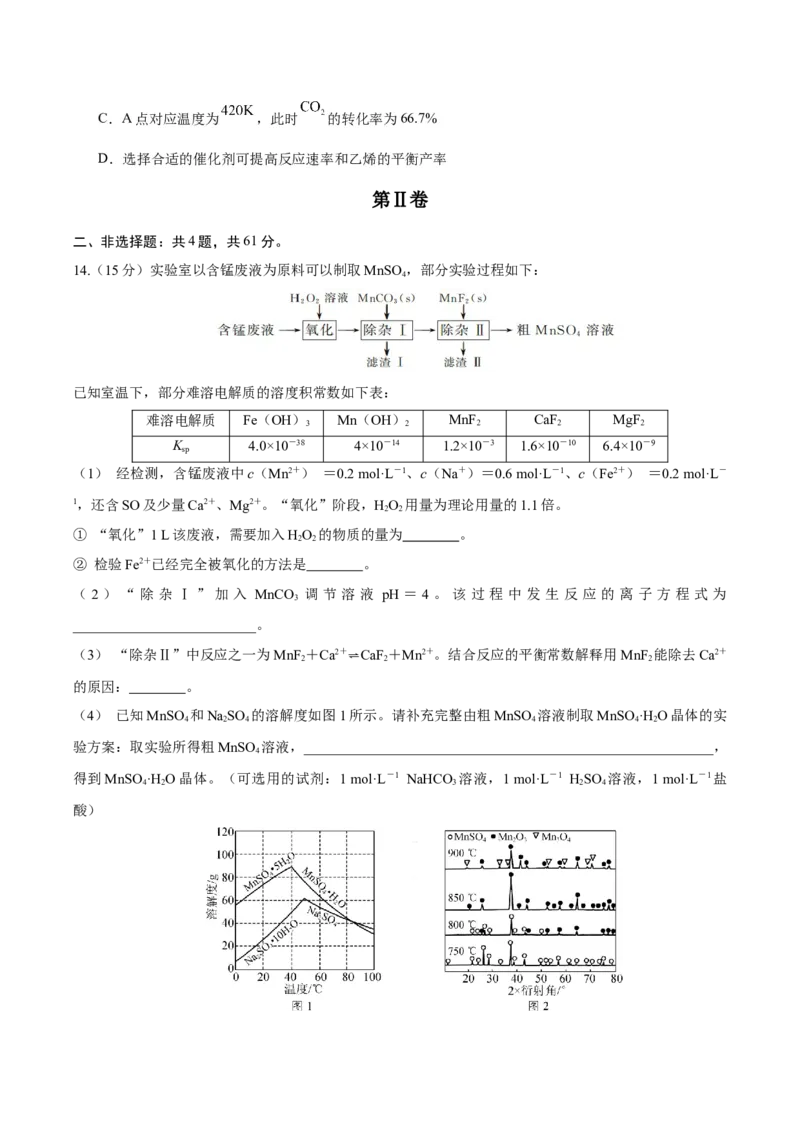
14.(15分)实验室以含锰废液为原料可以制取MnSO ,部分实验过程如下:
4
已知室温下,部分难溶电解质的溶度积常数如下表:
难溶电解质 Fe(OH) Mn(OH) MnF CaF MgF
3 2 2 2 2
K 4.0×10-38 4×10-14 1.2×10-3 1.6×10-10 6.4×10-9
sp
(1) 经检测,含锰废液中c(Mn2+) =0.2 mol·L-1、c(Na+)=0.6 mol·L-1、c(Fe2+) =0.2 mol·L-
1,还含SO及少量Ca2+、Mg2+。“氧化”阶段,HO 用量为理论用量的1.1倍。
2 2
① “氧化”1 L该废液,需要加入HO 的物质的量为 。
2 2
② 检验Fe2+已经完全被氧化的方法是 。
( 2 ) “ 除 杂 Ⅰ ” 加 入 MnCO 调 节 溶 液 pH = 4 。 该 过 程 中 发 生 反 应 的 离 子 方 程 式 为
3
__________________________。
(3) “除杂Ⅱ”中反应之一为MnF
2
+Ca2+ ⇌CaF
2
+Mn2+。结合反应的平衡常数解释用MnF
2
能除去Ca2+
的原因: 。
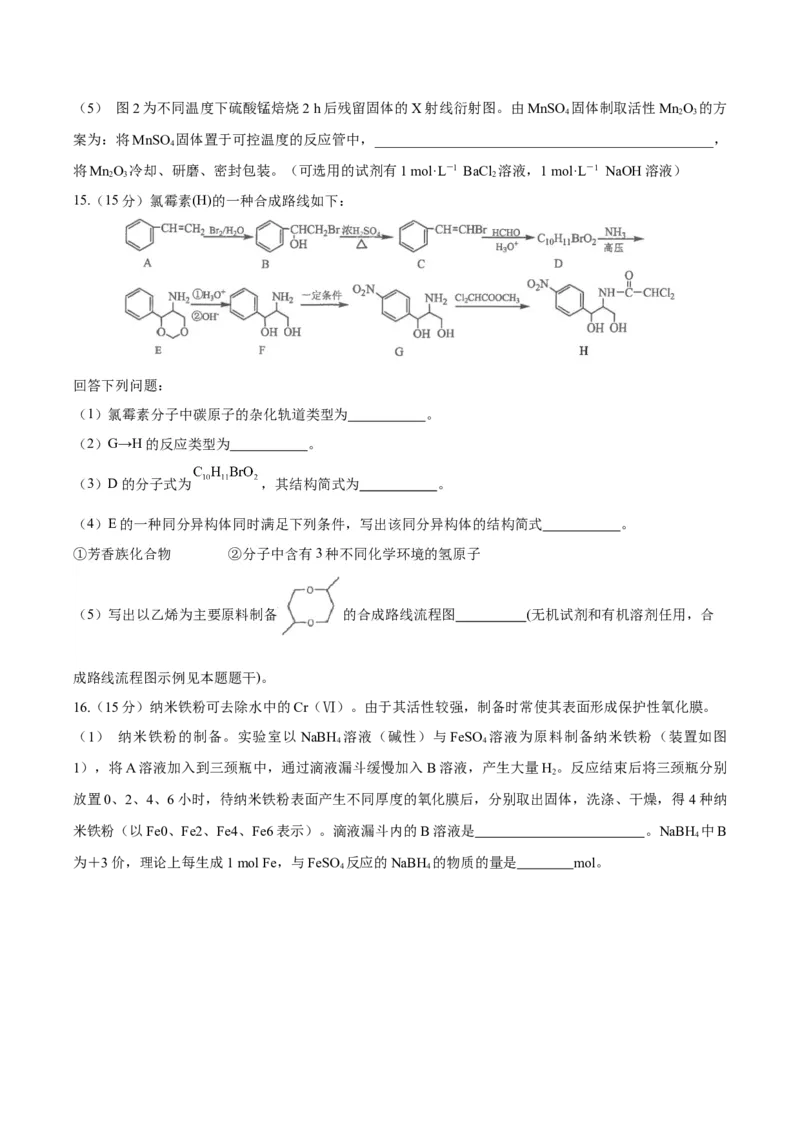
(4) 已知MnSO 和NaSO 的溶解度如图1所示。请补充完整由粗MnSO 溶液制取MnSO ·H O晶体的实
4 2 4 4 4 2
验方案:取实验所得粗MnSO 溶液,__________________________________________________________,
4
得到MnSO ·H O晶体。(可选用的试剂:1 mol·L-1 NaHCO 溶液,1 mol·L-1 HSO 溶液,1 mol·L-1盐
4 2 3 2 4
酸)(5) 图2为不同温度下硫酸锰焙烧2 h后残留固体的X射线衍射图。由MnSO 固体制取活性MnO 的方
4 2 3
案为:将MnSO 固体置于可控温度的反应管中,________________________________________________,
4
将MnO 冷却、研磨、密封包装。(可选用的试剂有1 mol·L-l BaCl 溶液,1 mol·L-1 NaOH溶液)
2 3 2
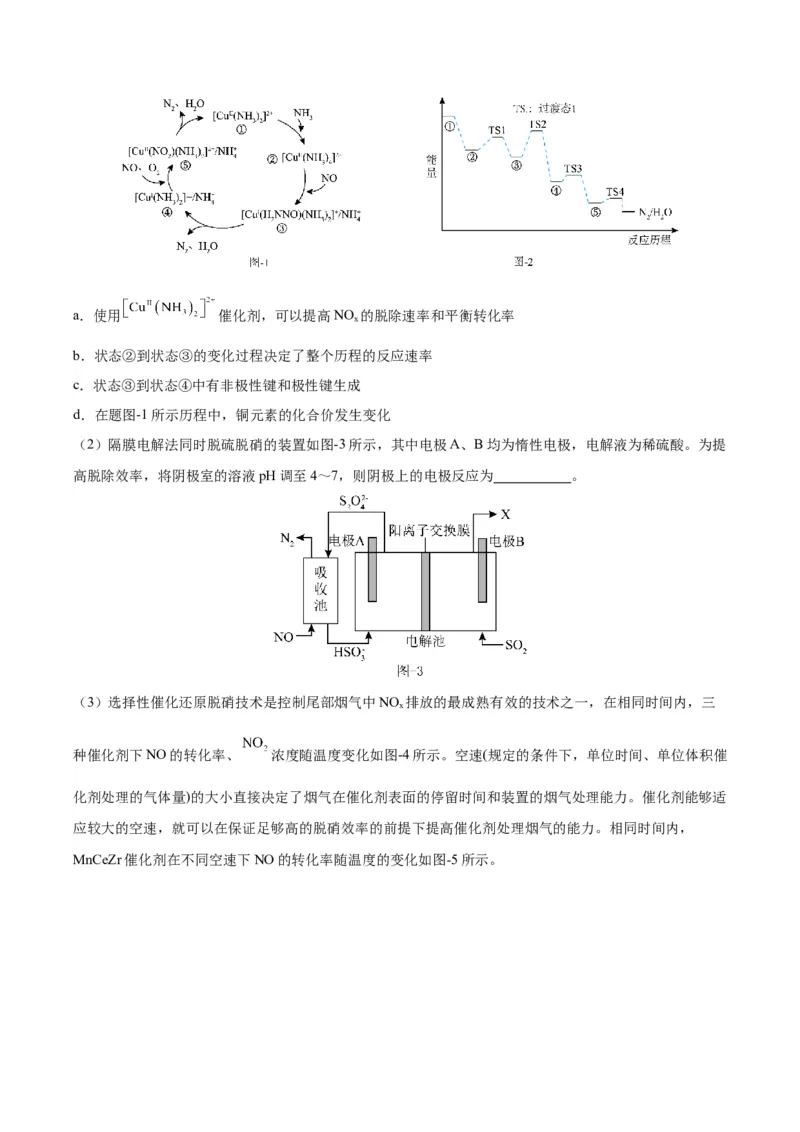
15.(15分)氯霉素(H)的一种合成路线如下:
回答下列问题:
(1)氯霉素分子中碳原子的杂化轨道类型为 。
(2)G→H的反应类型为 。
(3)D的分子式为 ,其结构简式为 。
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 。
①芳香族化合物 ②分子中含有3种不同化学环境的氢原子
(5)写出以乙烯为主要原料制备 的合成路线流程图 (无机试剂和有机溶剂任用,合
成路线流程图示例见本题题干)。
16.(15分)纳米铁粉可去除水中的Cr(Ⅵ)。由于其活性较强,制备时常使其表面形成保护性氧化膜。
(1) 纳米铁粉的制备。实验室以 NaBH 溶液(碱性)与FeSO 溶液为原料制备纳米铁粉(装置如图
4 4
1),将A溶液加入到三颈瓶中,通过滴液漏斗缓慢加入B溶液,产生大量H 。反应结束后将三颈瓶分别
2
放置0、2、4、6小时,待纳米铁粉表面产生不同厚度的氧化膜后,分别取出固体,洗涤、干燥,得4种纳
米铁粉(以Fe0、Fe2、Fe4、Fe6表示)。滴液漏斗内的B溶液是 。NaBH 中B
4
为+3价,理论上每生成1 mol Fe,与FeSO 反应的NaBH 的物质的量是 mol。
4 4(2) 研究放置时间对纳米铁粉性能的影响。实验一:室温下,取相同质量的4种纳米铁粉分别投入相同
体积、含Cr(Ⅵ)浓度相同的污水中,一段时间后测量Cr(Ⅵ)去除率;
实验二:取4份相同体积的蒸馏水分别置于三颈瓶中,再各加入相同质量的 4种纳米铁粉,搅拌,相同时
间后测量溶液中c(Fe2+),结果如图2所示。请对纳米铁粉制备时放置时间、使用时溶出的少量Fe2+与
Cr(Ⅵ)去除率之间的关系作出猜想:_______________________________________________。
(3) 研究影响纳米铁粉溶出c(Fe2+)的因素。取一定量蒸馏水,用HCl调节pH约为6。将其分为相同
体积的两份并分别置于三颈瓶中,向其中一支通入 N;再各加入相同质量的纳米铁粉,搅拌,一段时间后
2
测得未通N 的三颈瓶内溶液中c(Fe2+)大于通入N 的。
2 2
① 该条件下纳米铁粉溶出Fe2+的原因是 。
② 实验时不将蒸馏水调节至较低pH,理由是 。
(4) 纳米铁粉去除Cr(Ⅵ)主要是经过“吸附→反应→共沉淀”的过程。pH<8.6,纳米铁粉颗粒表面带
正电荷;pH=8.6,纳米铁粉颗粒表面不带电;pH>8.6,纳米铁粉颗粒表面带负电荷。在水溶液中 Cr
(Ⅵ)主要存在微粒平衡浓度占Cr(Ⅵ)总浓度的百分数与pH的关系如图3。以实验室制得的纳米铁粉
去除 pH=4 的水样中的 Cr(Ⅵ),请补充完整实验方案:将一定量水样置于烧杯中,
____________________________,反应一段时间,测量溶液中 c[Cr(Ⅵ)],待c[Cr(Ⅵ)]小于1×10-3
mol·L-1,分离出固体。(还可使用的试剂:0.1 mol·L-1 NaOH溶液,0.1 mol·L-1 HCl)
17.(16分)不同催化剂作用下 还原 的机理与效果是研究烟气(含 、 、 等)脱硝的热点。
(1)二价铜微粒 可用作汽车尾气脱硝的催化剂,其可能的催化机理如图-1所示,反应过程
中不同态物质体系所含的能量如图-2所示。下列说法正确的是。a.使用 催化剂,可以提高NO 的脱除速率和平衡转化率
x
b.状态②到状态③的变化过程决定了整个历程的反应速率
c.状态③到状态④中有非极性键和极性键生成
d.在题图-1所示历程中,铜元素的化合价发生变化
(2)隔膜电解法同时脱硫脱硝的装置如图-3所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为提
高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应为 。
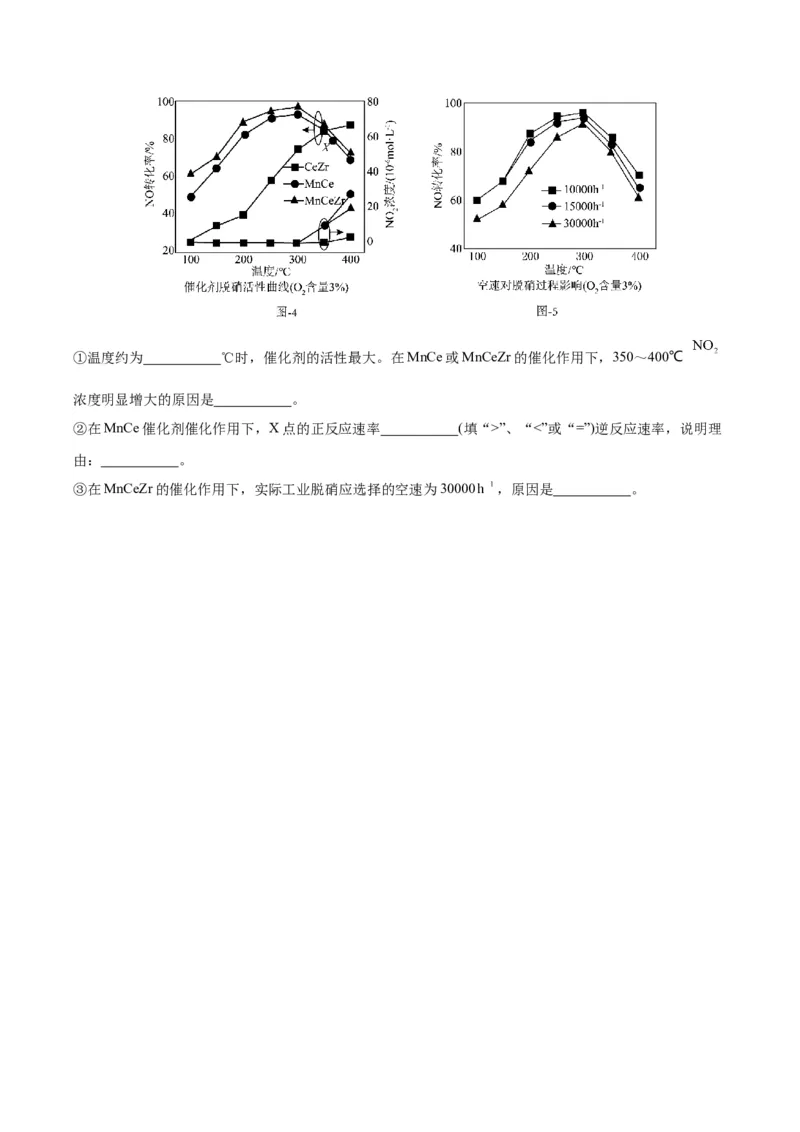
(3)选择性催化还原脱硝技术是控制尾部烟气中NO 排放的最成熟有效的技术之一,在相同时间内,三
x
种催化剂下NO的转化率、 浓度随温度变化如图-4所示。空速(规定的条件下,单位时间、单位体积催
化剂处理的气体量)的大小直接决定了烟气在催化剂表面的停留时间和装置的烟气处理能力。催化剂能够适
应较大的空速,就可以在保证足够高的脱硝效率的前提下提高催化剂处理烟气的能力。相同时间内,
MnCeZr催化剂在不同空速下NO的转化率随温度的变化如图-5所示。①温度约为 ℃时,催化剂的活性最大。在MnCe或MnCeZr的催化作用下,350~400℃
浓度明显增大的原因是 。
②在MnCe催化剂催化作用下,X点的正反应速率 (填“>”、“<”或“=”)逆反应速率,说明理
由: 。
③在MnCeZr的催化作用下,实际工业脱硝应选择的空速为30000 ,原因是 。