文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖南专用)
黄金卷01
(考试时间:75分钟;试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Ni-59
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学是现代生产、生活与科技的中心学科之一,下列与化学有关的说法正确的是
A. “神州十一号”飞船使用的半导体材料GaAs可用SiO 代替
2
B.羊毛织品水洗后会变形与氢键有关
C.制造医用口罩和防护服的主要原材料是聚丙烯(PP),聚丙烯与聚乙烯互为同系物
D.超分子内部分子之间通过共价键结合
2.古医典富载化学知识,下述之物见其氧化性者为
A.金(Au):“虽被火亦未熟"
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳( ):“色黄,以苦酒(醋)洗刷则白”
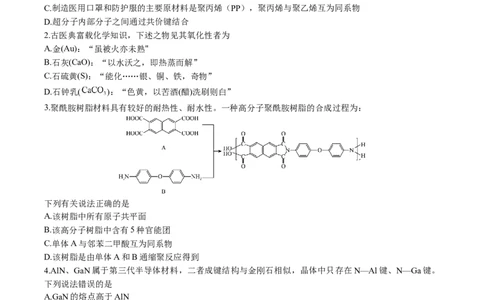
3.聚酰胺树脂材料具有较好的耐热性、耐水性。一种高分子聚酰胺树脂的合成过程为:
下列有关说法正确的是
A.该树脂中所有原子共平面
B.该高分子树脂中含有5种官能团
C.单体A与邻苯二甲酸互为同系物
D.该树脂是由单体A和B通缩聚反应得到
4.AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在N—Al键、N—Ga键。
下列说法错误的是
A.GaN的熔点高于AlN
B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化
D.晶体中所有原子的配位数均相同
5.“宏观辨识与微观探析”是学科核心素养之一,下列离子方程式正确且符合题意的是
A.在过量银氨溶液中滴加甲醛溶液并加热:
B.用铜片作电极,电解饱和食盐水:C.下水道堵塞用铝粉和烧碱溶液疏通:
D.向过量的 溶液中滴加少量“84”消毒液:
6.下列实验能达到实验目的的是
A B C D
测定HC O 溶液的浓度 证明苯环使羟基活 制作简单的燃料电池 检验溴乙烷的水解产物
2 2 4
化
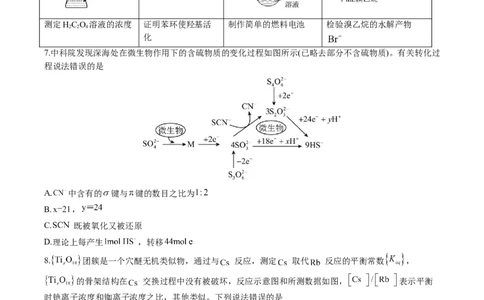
7.中科院发现深海处在微生物作用下的含硫物质的变化过程如图所示(已略去部分不含硫物质)。有关转化过
程说法错误的是
A. 中含有的 键与 键的数目之比为
B. ,
C. 既被氧化又被还原
D.理论上每产生 ,转移
8. 团簇是一个穴醚无机类似物,通过与 反应,测定 取代 反应的平衡常数 ,
的骨架结构在 交换过程中没有被破坏,反应示意图和所测数据如图, 表示平衡
时铯离子浓度和铷离子浓度之比,其他类似。下列说法错误的是
A. 团簇中 B.
C.增大 可使平衡时 增大 D. 团簇对于 具有比 大的亲和力9.二草酸合铜(II)酸钾晶体 是一种重要的化工原料,微溶于冷水、酒精,可溶于热
水,干燥时较为稳定,加热时易分解。制备产品二草酸合铜酸钾晶体可采用如下步骤,下列说法错误的是
已知:25℃草酸和碳酸的电离平衡常数数值如下表。
电离平衡常
数
A.过程①微热的目的是加快草酸溶解,但会使草酸分解
B.过程②中加入的碳酸钾物质的量与草酸物质的量相等时,得到草酸氢钾溶液
C.操作③为趁热过滤,操作④为降温结晶、过滤洗涤、干燥
D.得到的产品用热水洗涤优于冷水洗涤
10.热激活电池是一种需要达到启动温度才开始工作的电池。一种热激活电池的结构如图1所示,其放电后
的产物为LiSi 和LiMn O。
7 3 2 4
已知:LiCl和KCl混合物的熔点与KCl的物质的量分数的关系如图2所示。
下列说法不正确的是
A.放电时,Li+向b极区移动
B.放电时,a极的电极反应是3Li Si -11e-=4Li Si +11Li+
13 4 7 3
C.该电池中火药燃烧产生的热能转化为电能
D.调节混合物中KCl的物质的量分数可以改变电池的启动温度
11.探究乙醛的银镜反应,实验如下(水浴加热装置己略去,水浴温度均相同)。
已知:i.银氨溶液用2%AgNO 溶液和稀氨水配制
3
ii.
序号 ** 错误的表达式 ② ③ ④
**
装置
现象 一直无明显现象 8min有银镜产生 3min有银镜产生 d中较长时间无银镜产生,
e中有银镜产生下列说法错误的是
A. a与b中现象不同的原因是[Ag(NH)]+能氧化乙醛而Ag+不能
3 2
B. c中发生的氧化反应为CHCHO+3OH--2e--=CH COO-+2H O
3 3 2
C.其他条件不变时,增大pH能增强乙醛的还原性
D.由③和④可知,c与d现象不同的原因是c(Ag+)不同
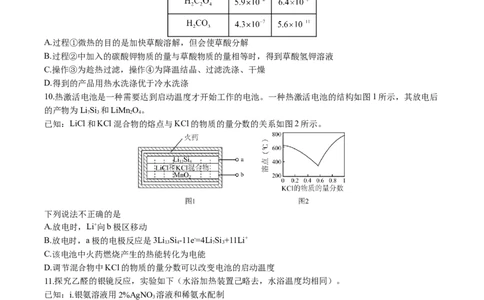
12.在一个体积恒为1L的恒温密闭容器中充入 和 ,发生反应①
和反应②
,混合气体中氨气的体积分数及气体总浓度随时间的变化如图所示。下列说法正确的是
A.混合气体的密度不变不能说明反应达到平衡状态
B.升高温度,反应①的平衡常数减小
C.A点正反应速率与B点逆反应速率大小关系是
D.在B点时氨气的转化率为50%
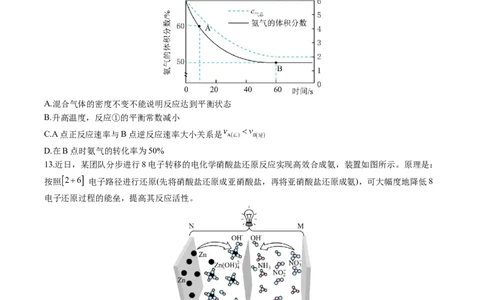
13.近日,某团队分步进行8电子转移的电化学硝酸盐还原反应实现高效合成氨,装置如图所示。原理是:
按照 电子路径进行还原(先将硝酸盐还原成亚硝酸盐,再将亚硝酸盐还原成氨),可大幅度地降低8
电子还原过程的能垒,提高其反应活性。
下列叙述正确的是
A.N极为负极,发生了还原反应
B. 、 的VSEPR模型名称分别为三角锥形、直线形
C.生成 的电极反应式为
D.由 生成34g 时至少转移12mol电子
14.某研究小组利用电位滴定法研究盐酸滴加亚磷酸钠 溶液过程中的化学变化,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法不正确的是
[已知:①电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,指示电极电位也发生了突跃,
进而确定滴定终点。②亚磷酸 是二元弱酸,其电离常数分别是 , ]
A.a点对应溶液的溶质为 和 ,
B.第二次电极电位突跃发生的化学反应为:
C.c点对应的溶液中可能存在:
D.水的电离程度:a>b
二、非选择题:本题共4小题,共58分。
15.(15分)某学生对 的还原性进行实验探究,根据所学知识,回答下列问题:
实验一: 与漂粉精(已在空气中露置了一小段时间)反应的实验探究
步骤①:取4g漂粉精固体,加入100 mL水,固体有少量不溶解,溶液略有颜色,过滤,pH计测得漂粉精
溶液的pH约为12。
步骤②:将 验持续通入漂粉精溶液中,液面上方出现白雾,稍后出现浑浊,溶液变为黄绿色,最后产
生大量白色沉淀,黄绿色褪去。
(1) 的VSEPR模型为 。
(2)若向水中持续通入 ,未观察到白雾。推测步骤②中的白雾是由HCl小液滴形成的,进行如下实
验:
a.用湿润的淀粉碘化钾试纸检验白雾,无变化;
b.用酸化的 溶液检验白雾,产生白色沉淀A。
I.实验a的目的是 。
II.白色沉淀A可能为 (填化学式)。
(3)步骤②中溶液变为黄绿色的可能原因:随着溶液酸性的增强,漂粉精的有效成分和 发生反应。通
过进一步实验确认了这种可能性,设计的实验操作为 。
(4)向步骤①中过滤后得到的固体中加入稀盐酸,可能观察到的实验现象为 。
实验二: 与 溶液反应的实验探究
实验步骤:将一定量的 通入 溶液中,有白色沉淀生成。
经分析, 与 溶液反应可能有两种情况:
c.若通入少量 ,则反应为
d.若通入过量 ,则反应为
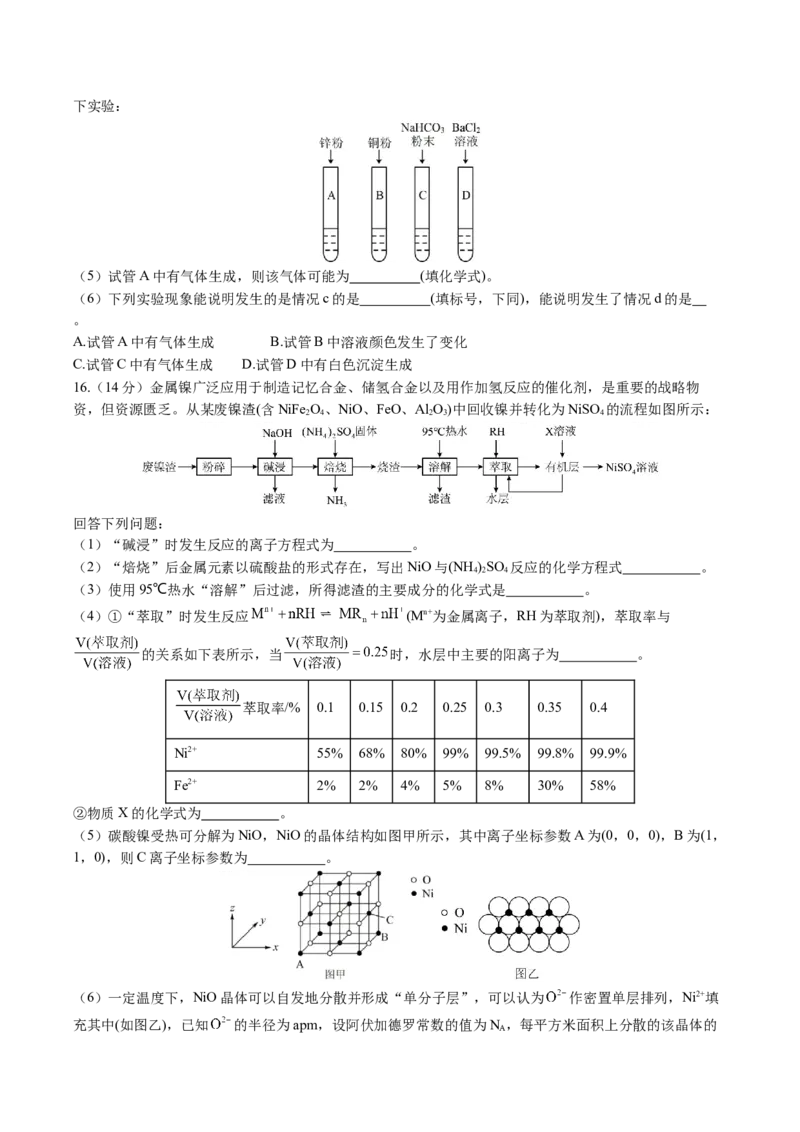
为了探究发生了哪一种情况,取上述反应后过滤所得的溶液,分别装入A、B、C、D四支试管中,进行如下实验:
(5)试管A中有气体生成,则该气体可能为 (填化学式)。
(6)下列实验现象能说明发生的是情况c的是 (填标号,下同),能说明发生了情况d的是
。
A.试管A中有气体生成 B.试管B中溶液颜色发生了变化
C.试管C中有气体生成 D.试管D中有白色沉淀生成
16.(14分)金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物
资,但资源匮乏。从某废镍渣(含NiFe O、NiO、FeO、Al O)中回收镍并转化为NiSO 的流程如图所示:
2 4 2 3 4
回答下列问题:
(1)“碱浸”时发生反应的离子方程式为 。
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与(NH )SO 反应的化学方程式 。
4 2 4
(3)使用95℃热水“溶解”后过滤,所得滤渣的主要成分的化学式是 。
(4)①“萃取”时发生反应 (Mn+为金属离子,RH为萃取剂),萃取率与
的关系如下表所示,当 时,水层中主要的阳离子为 。
萃取率/% 0.1 0.15 0.2 0.25 0.3 0.35 0.4
Ni2+ 55% 68% 80% 99% 99.5% 99.8% 99.9%
Fe2+ 2% 2% 4% 5% 8% 30% 58%
②物质X的化学式为 。
(5)碳酸镍受热可分解为NiO,NiO的晶体结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,
1,0),则C离子坐标参数为 。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,Ni2+填
充其中(如图乙),已知 的半径为apm,设阿伏加德罗常数的值为N ,每平方米面积上分散的该晶体的
A质量为
g(用含a、N 的代数式表示)。
A
17.(14分)I. 以CO 为原料加氢合成二甲醚、甲醇有利于促进实现“碳中和”。在二氧化碳加氢制取二
2
甲醚的合成塔中发生以下3个反应:
i.CO(g)+3H(g) CHOH(g)+H O(g) △H= - 49.01kJ·mol-1
2 2 3 2
ii.2CHOH(g) CHOCH (g)+HO(g) △H= -24.52kJ·mol-1
3 3 3 2
iii.CO(g)+H(g) CO(g)+HO(g) △H= + 41.17kJ·mol-1
2 2 2
(1)2CO(g)+6H(g) CHOCH (g)+3HO(g)的△H= kJ·mol-1。
2 2 3 3 2
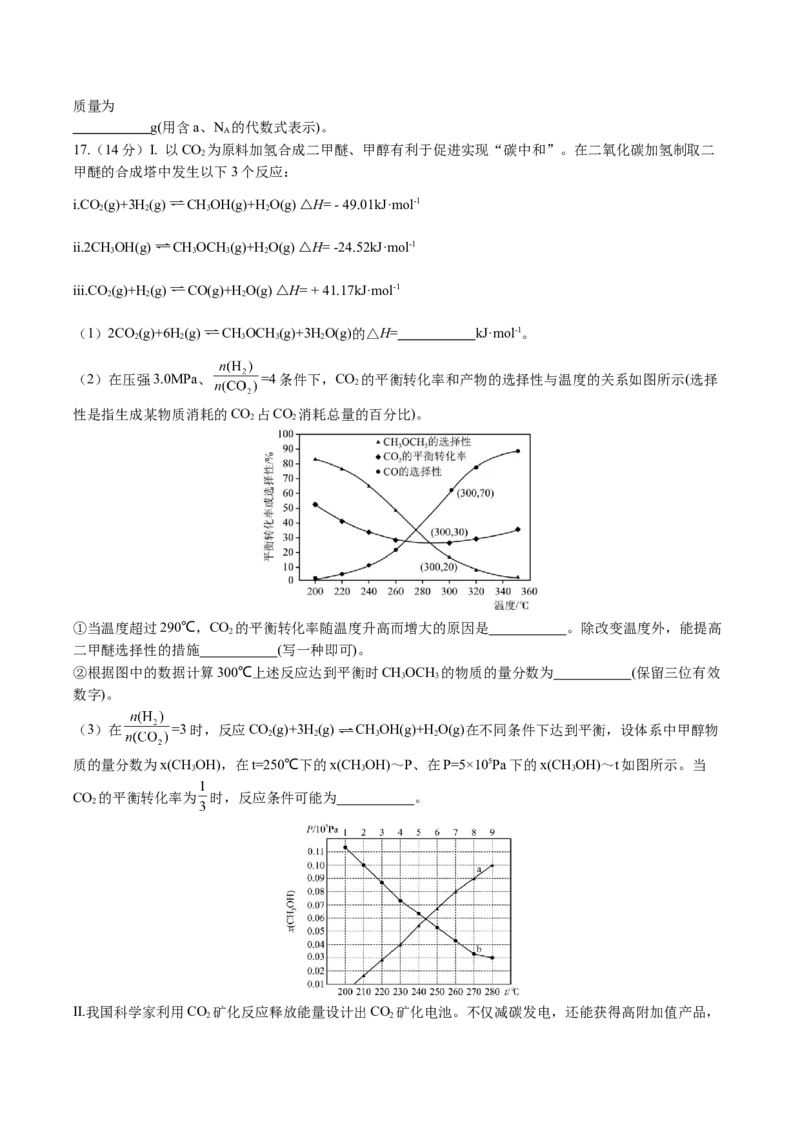
(2)在压强3.0MPa、 =4条件下,CO 的平衡转化率和产物的选择性与温度的关系如图所示(选择
2
性是指生成某物质消耗的CO 占CO 消耗总量的百分比)。
2 2
①当温度超过290℃,CO 的平衡转化率随温度升高而增大的原因是 。除改变温度外,能提高
2
二甲醚选择性的措施 (写一种即可)。
②根据图中的数据计算300℃上述反应达到平衡时CHOCH 的物质的量分数为 (保留三位有效
3 3
数字)。
(3)在 =3时,反应CO(g)+3H(g) CHOH(g)+H O(g)在不同条件下达到平衡,设体系中甲醇物
2 2 3 2
质的量分数为x(CHOH),在t=250℃下的x(CHOH)~P、在P=5×105Pa下的x(CHOH)~t如图所示。当
3 3 3
CO 的平衡转化率为 时,反应条件可能为 。
2
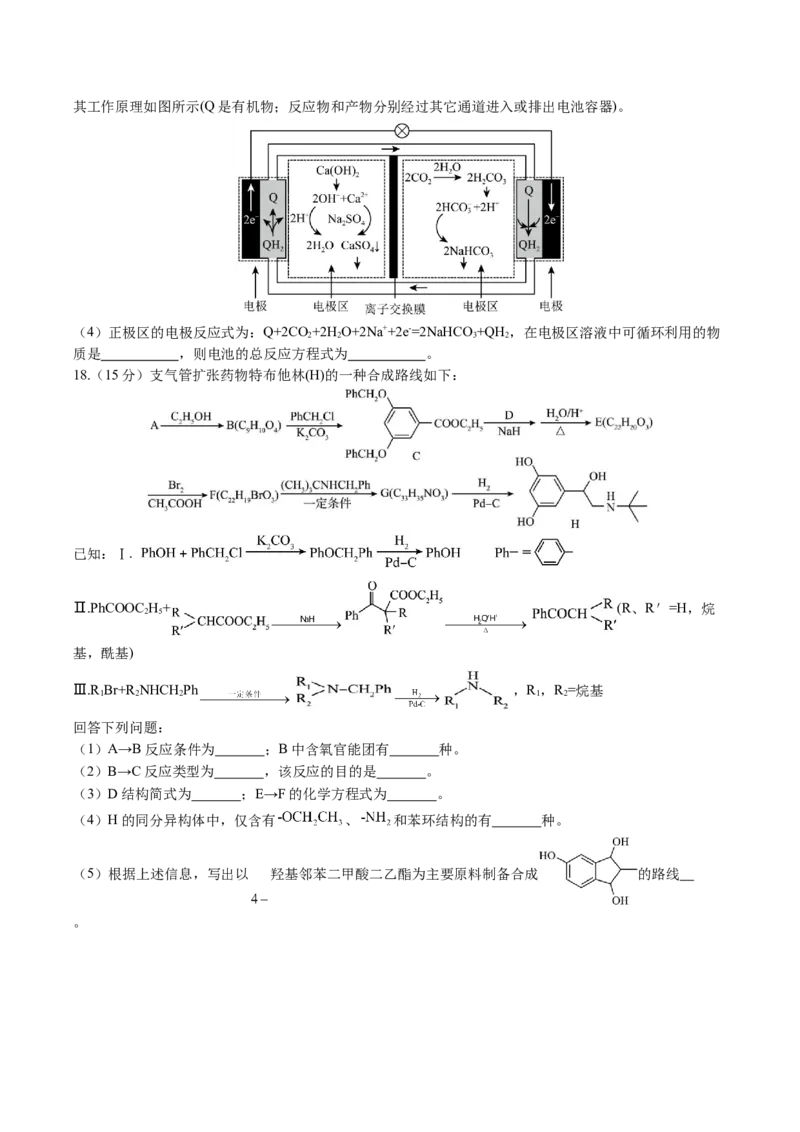
II.我国科学家利用CO 矿化反应释放能量设计出CO 矿化电池。不仅减碳发电,还能获得高附加值产品,
2 2其工作原理如图所示(Q是有机物;反应物和产物分别经过其它通道进入或排出电池容器)。
(4)正极区的电极反应式为:Q+2CO+2H O+2Na++2e-=2NaHCO+QH,在电极区溶液中可循环利用的物
2 2 3 2
质是 ,则电池的总反应方程式为 。
18.(15分)支气管扩张药物特布他林(H)的一种合成路线如下:
已知:Ⅰ.
Ⅱ.PhCOOC H+ (R、R'=H,烷
2 5
基,酰基)
Ⅲ.R Br+R NHCH Ph ,R ,R =烷基
1 2 2 1 2
回答下列问题:
(1)A→B反应条件为 ;B中含氧官能团有 种。
(2)B→C反应类型为 ,该反应的目的是 。
(3)D结构简式为 ;E→F的化学方程式为 。
(4)H的同分异构体中,仅含有 、 和苯环结构的有 种。
(5)根据上述信息,写出以 羟基邻苯二甲酸二乙酯为主要原料制备合成 的路线
。