文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(江苏专用)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 我国在联合国大会上提出“2030年前实现碳达峰,2060年前实现碳中和”,下列有关低碳生活的说法
正确的是
A.开发太阳能等新能源是践行低碳生活的有效途径
B.在一定条件下,选择合适的催化剂将CO 氧化为甲酸
2
C.推广使用煤液化,可减少CO 的排放
2
D.禁止煤炭等化石燃料的使用
2.NCl 可发生水解反应 ,下列说法正确的是
3
A. 中N原子杂化类型为 杂化 B. 为非极性分子
C. 分子空间构型为平面三角形 D. 的电子式为
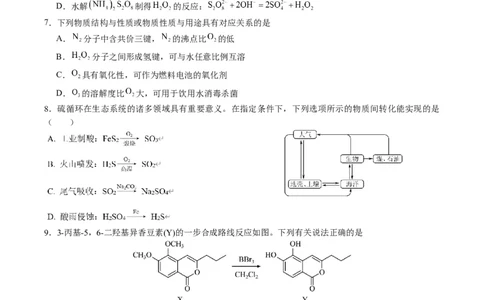
3. 实验室制取SO 并回收CuSO 的实验原理及装置不能达到实验目的是
2 4
A B C D
制取SO 干燥SO 吸收尾气中的SO 将硫酸铜溶液蒸发浓缩
2 2 2
4.元素P、As、Sb分别位于周期表中三、四、五周期VA族。下列说法不正确的是
A.原子半径:
B.第一电离能:
C.P的简单气态氢化物的热稳定性比As的强
D.VA族元素单质的晶体类型相同
阅读下列材料,回答5~7题:
氧及其化合物具有广泛用途。 是常用的氧化剂, 的燃烧热为 ,氧炔焰产生的高温可
用于焊接金属。 可用于水处理,pH约为8时, 可与 反应生成 、 和 。 可用
于研究酯化反应的机理。CaO可用于烟气(含 、 、 、 等)脱硫。 是一种绿色氧化剂,电
解 饱和溶液产生的 经水解可制得 。
5.下列说法正确的是
A. 是由极性键构成的极性分子B. 与 互为同素异形体
C. 和 的中心原子杂化轨道类型均为
D.CaO晶体中 与 的相互作用具有饱和性和方向性
6.下列化学反应表示正确的是
A.乙炔的燃烧:
B.CaO吸收 的反应:
C. 处理含 废水的反应:
D.水解 制得 的反应:
7.下列物质结构与性质或物质性质与用途具有对应关系的是
A. 分子中含共价三键, 的沸点比 的低
B. 分子之间形成氢键,可与水任意比例互溶
C. 具有氧化性,可作为燃料电池的氧化剂
D. 的溶解度比 大,可用于饮用水消毒杀菌
8.硫循环在生态系统的诸多领域具有重要意义。在指定条件下,下列选项所示的物质间转化能实现的是
( )
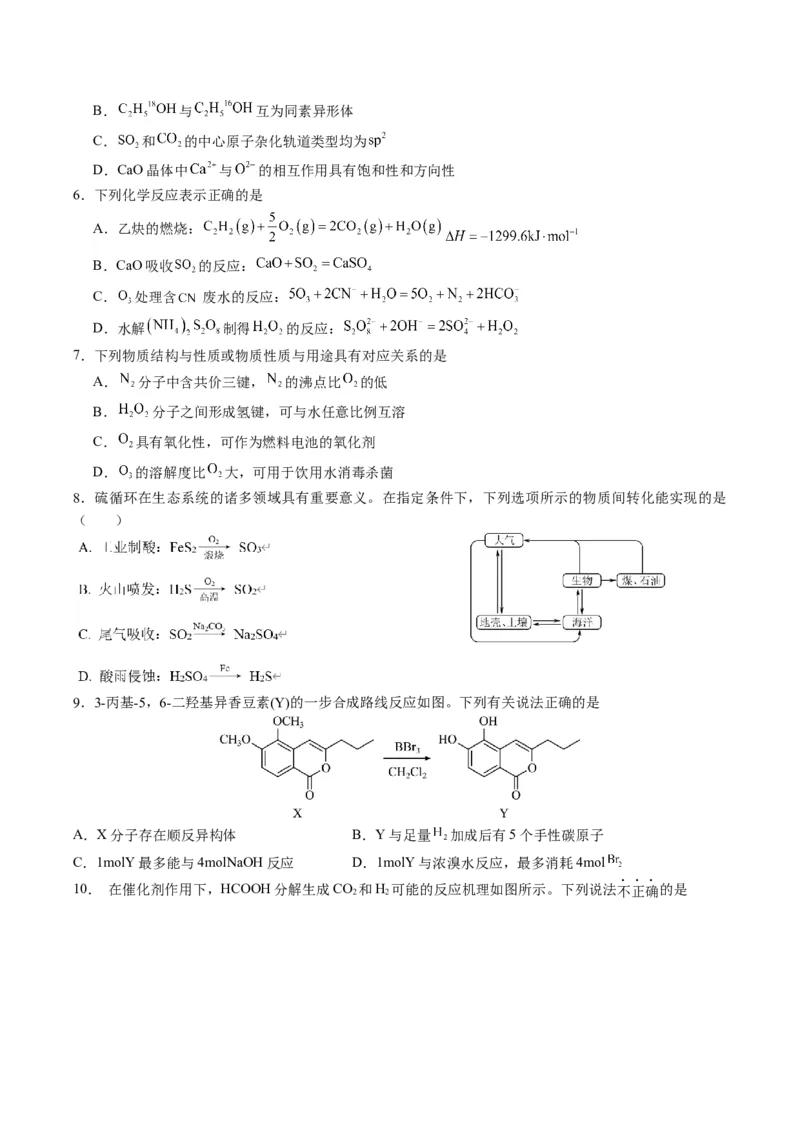
9.3-丙基-5,6-二羟基异香豆素(Y)的一步合成路线反应如图。下列有关说法正确的是
A.X分子存在顺反异构体 B.Y与足量 加成后有5个手性碳原子
C.1molY最多能与4molNaOH反应 D.1molY与浓溴水反应,最多消耗4mol
10. 在催化剂作用下,HCOOH分解生成CO 和H 可能的反应机理如图所示。下列说法不正确的是
2 2A.若用HCOOD催化释氢,反应除生成CO 外,还生成HD
2
B.第一步转化N与H间形成配位键
C.若用HCOOK溶液代替HCOOH释氢的速率加快
D.若用HCOOK溶液代替HCOOH最终所得气体中H 的纯度会降低
2
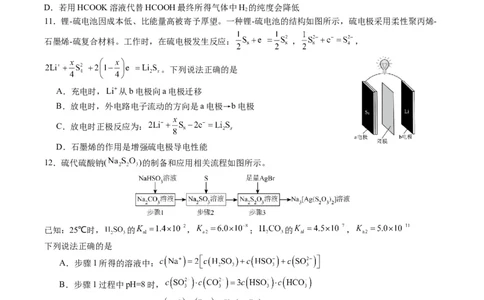
11.锂-硫电池因成本低、比能量高被寄予厚望。一种锂-硫电池的结构如图所示,硫电极采用柔性聚丙烯-
石墨烯-硫复合材料。工作时,在硫电极发生反应: , ,
。下列说法正确的是
A.充电时, 从b电极向a电极迁移
B.放电时,外电路电子流动的方向是a电极→b电极
C.放电时正极反应为:
D.石墨烯的作用是增强硫电极导电性能
12.硫代硫酸钠( )的制备和应用相关流程如图所示。
已知:25℃时, 的 , ; 的 ,
下列说法正确的是
A.步骤1所得的溶液中:
B.步骤1过程中pH=8时,
C.步骤3所得的清液中:
D.步骤3的离子方程式为:
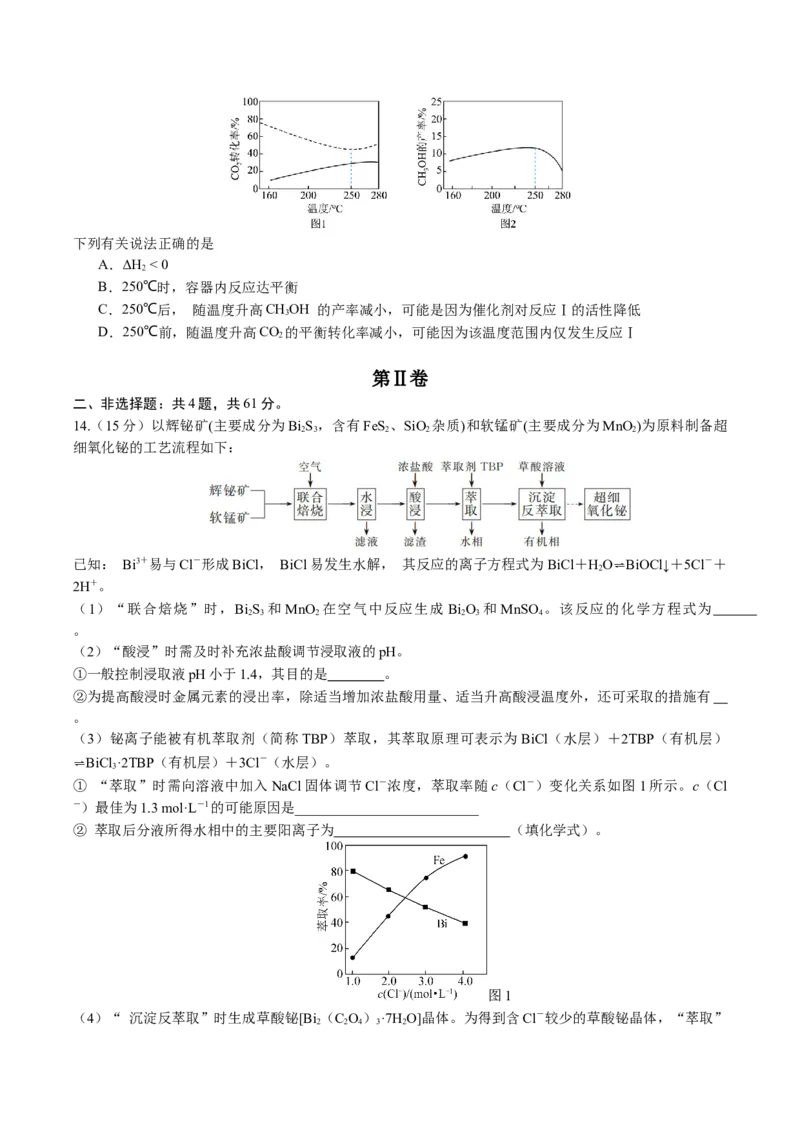
13.将一定量的CO 与H 通入某密闭容器中合成甲醇,在催化剂作用下发生下述反应:
2 2
Ⅰ. CO(g)+3H(g) CHOH(g)+H O(g) ΔH<0
2 2 3 2 1
Ⅱ. CO(g)+H(g) HO(g)+CO(g) ΔH
2 2 2 2
催化反应相同时间,测得不同温度下CO 的转化率如图1所示(图中虚线表示相同条件下CO 的平衡转化率
2 2
随温度的变化),CHOH 的产率如图2所示。
3下列有关说法正确的是
A.ΔH < 0
2
B.250℃时,容器内反应达平衡
C.250℃后, 随温度升高CHOH 的产率减小,可能是因为催化剂对反应Ⅰ的活性降低
3
D.250℃前,随温度升高CO 的平衡转化率减小,可能因为该温度范围内仅发生反应Ⅰ
2
第Ⅱ卷
二、非选择题:共4题,共61分。
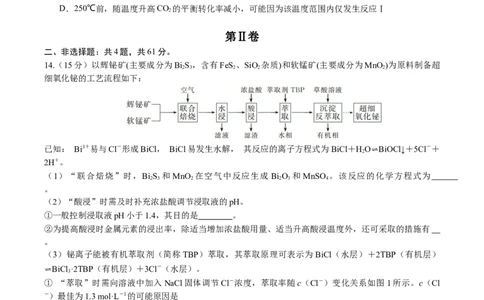
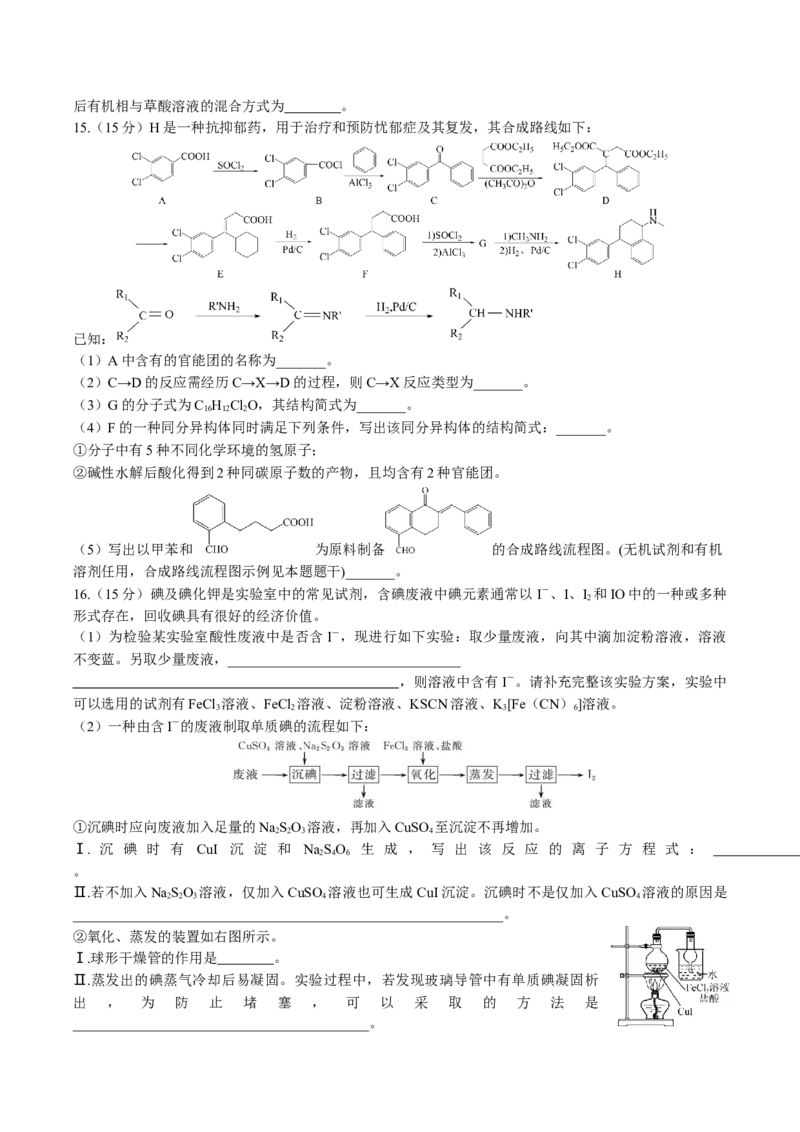
14.(15分)以辉铋矿(主要成分为BiS ,含有FeS 、SiO 杂质)和软锰矿(主要成分为MnO )为原料制备超
2 3 2 2 2
细氧化铋的工艺流程如下:
已知: Bi3+易与Cl-形成BiCl, BiCl易发生水解, 其反应的离子方程式为BiCl+H
2
O⇌BiOCl↓+5Cl-+
2H+。
(1)“联合焙烧”时,BiS 和 MnO 在空气中反应生成 BiO 和 MnSO 。该反应的化学方程式为
2 3 2 2 3 4
。
(2)“酸浸”时需及时补充浓盐酸调节浸取液的pH。
①一般控制浸取液pH小于1.4,其目的是 。
②为提高酸浸时金属元素的浸出率,除适当增加浓盐酸用量、适当升高酸浸温度外,还可采取的措施有
。
(3)铋离子能被有机萃取剂(简称TBP)萃取,其萃取原理可表示为BiCl(水层)+2TBP(有机层)
⇌BiCl
3
·2TBP(有机层)+3Cl-(水层)。
① “萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图1所示。c(Cl
-)最佳为1.3 mol·L-1的可能原因是__________________________
② 萃取后分液所得水相中的主要阳离子为 (填化学式)。
图1
(4)“ 沉淀反萃取”时生成草酸铋[Bi (C O)·7H O]晶体。为得到含Cl-较少的草酸铋晶体,“萃取”
2 2 4 3 2后有机相与草酸溶液的混合方式为 。
15.(15分)H是一种抗抑郁药,用于治疗和预防忧郁症及其复发,其合成路线如下:
已知:
(1)A中含有的官能团的名称为_______。
(2)C→D的反应需经历C→X→D的过程,则C→X反应类型为_______。
(3)G的分子式为C H ClO,其结构简式为_______。
16 12 2
(4)F的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。
①分子中有5种不同化学环境的氢原子;
②碱性水解后酸化得到2种同碳原子数的产物,且均含有2种官能团。
(5)写出以甲苯和 为原料制备 的合成路线流程图。(无机试剂和有机
溶剂任用,合成路线流程图示例见本题题干)_______。
16.(15分)碘及碘化钾是实验室中的常见试剂,含碘废液中碘元素通常以I-、I、I 和IO中的一种或多种
2
形式存在,回收碘具有很好的经济价值。
(1)为检验某实验室酸性废液中是否含I-,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液
不变蓝。另取少量废液,_________________________________
,则溶液中含有I-。请补充完整该实验方案,实验中
可以选用的试剂有FeCl 溶液、FeCl 溶液、淀粉溶液、KSCN溶液、K[Fe(CN)]溶液。
3 2 3 6
(2)一种由含I-的废液制取单质碘的流程如下:
①沉碘时应向废液加入足量的NaSO 溶液,再加入CuSO 至沉淀不再增加。
2 2 3 4
Ⅰ. 沉 碘 时 有 CuI 沉 淀 和 NaSO 生 成 , 写 出 该 反 应 的 离 子 方 程 式 :
2 4 6
。
Ⅱ.若不加入NaSO 溶液,仅加入CuSO 溶液也可生成CuI沉淀。沉碘时不是仅加入CuSO 溶液的原因是
2 2 3 4 4
_____________________________________________________________。
②氧化、蒸发的装置如右图所示。
Ⅰ.球形干燥管的作用是 。
Ⅱ.蒸发出的碘蒸气冷却后易凝固。实验过程中,若发现玻璃导管中有单质碘凝固析
出 , 为 防 止 堵 塞 , 可 以 采 取 的 方 法 是
__________________________________________。(3)若废液中含有I ,可以用CCl 进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后
2 4
所得水层中的溶质为KIO 和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所
3
得水层,_________________________________________。
(已知KI易溶于水;氧化性:KIO >S。实验中可以选用的试剂有HS 气体、NaOH 溶液、稀硫酸)
3 2
(4)某含碘废液中,碘元素以IO形式存在,为测定IO的浓度,现进行如下实验:准确量取20.00 mL废
液,加水稀释配成100.00 mL溶液,取20.00 mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,
用0.100 0 mol·L-1 Na SO 溶液滴定I 至恰好完全反应,消耗NaSO 溶液24.00 mL。已知测定过程中发生
2 2 3 2 2 2 3
的反应为IO+I-+H+——I +HO(未配平);I +SO——I-+SO(未配平)。计算废液中IO的物质的
2 2 2 2 4
量浓度,并写出计算过程。
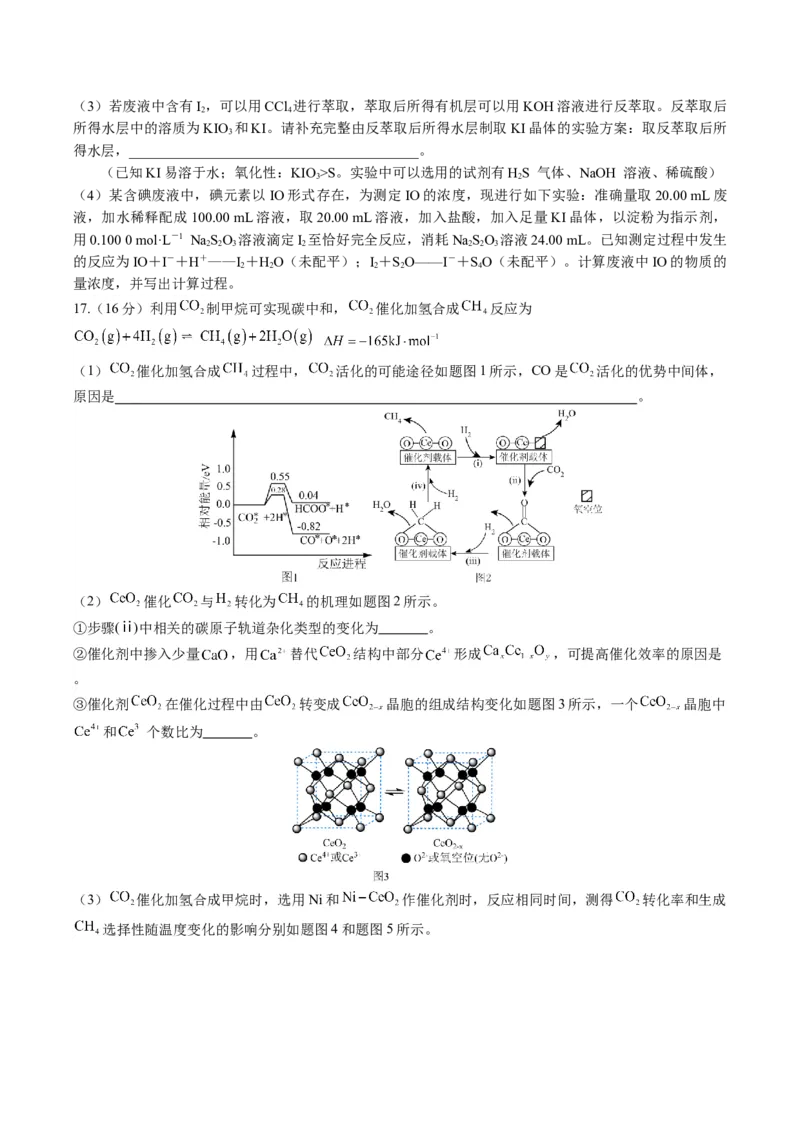
17.(16分)利用 制甲烷可实现碳中和, 催化加氢合成 反应为
(1) 催化加氢合成 过程中, 活化的可能途径如题图1所示,CO是 活化的优势中间体,
原因是 。
(2) 催化 与 转化为 的机理如题图2所示。
①步骤(ⅱ)中相关的碳原子轨道杂化类型的变化为 。
②催化剂中掺入少量 ,用 替代 结构中部分 形成 ,可提高催化效率的原因是
。
③催化剂 在催化过程中由 转变成 晶胞的组成结构变化如题图3所示,一个 晶胞中
和 个数比为 。
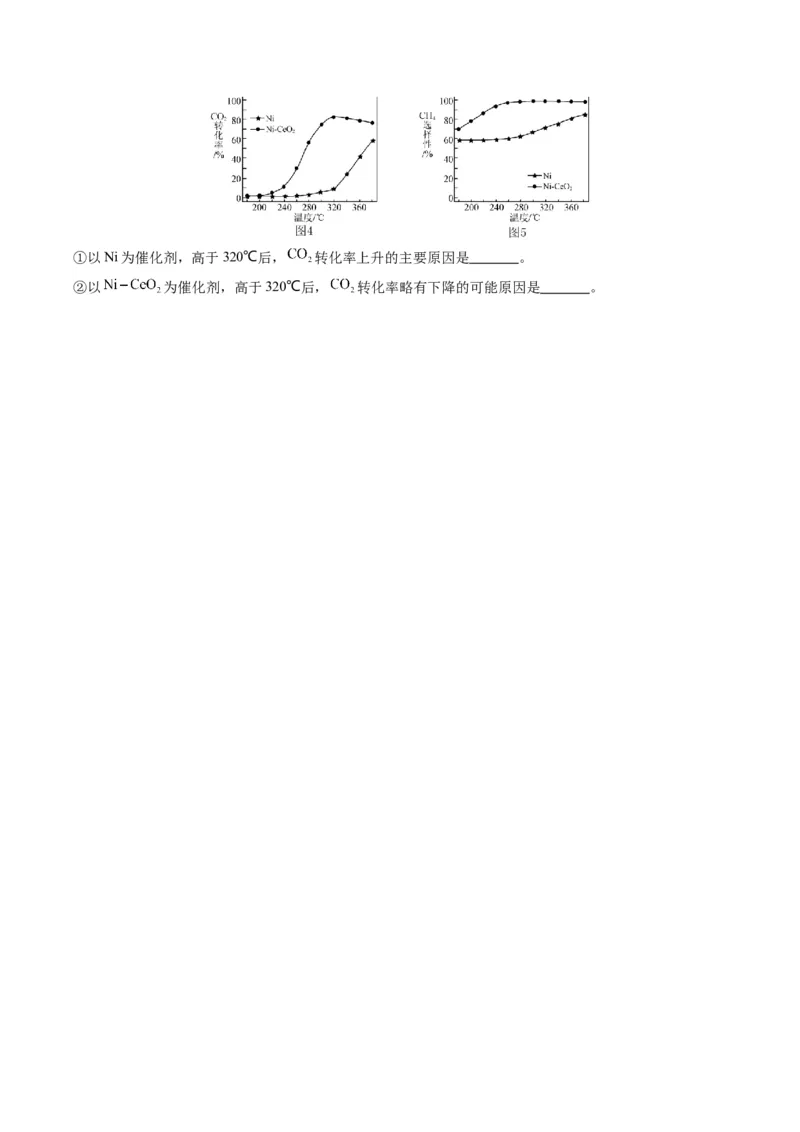
(3) 催化加氢合成甲烷时,选用Ni和 作催化剂时,反应相同时间,测得 转化率和生成
选择性随温度变化的影响分别如题图4和题图5所示。①以Ni为催化剂,高于320℃后, 转化率上升的主要原因是 。
②以 为催化剂,高于320℃后, 转化率略有下降的可能原因是 。