文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷新教材)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1. “泥人张”是中国传统案上雕塑的代表,“泥人”的制作过程中除用到上等泥外,辅助材料还有木材、
竹藤、纸张等,塑造好的作品自然风干后入窑烘烧,出窑后经打磨、整理即可着色。下列有关说法错
误的是
A.“泥人”属于陶瓷作品,属于传统的硅酸盐材料
B.“泥人”制作过程中发生复杂的物理和化学变化
C.“泥人”制作过程中使用的木材、竹藤、纸张的主要成分均是纤维素
D.出窑后着色时的黑色颜料可用氧化铁
2.为检验下列久置于空气中的物质是否变质,所选检验试剂(括号内)能达到目的的是
A.新制氯水(AgNO 溶液)
3
B.FeCl 溶液(KSCN溶液)
2
C.漂白粉(Na CO 溶液)
2 3
D.NaSO 溶液(BaCl 溶液)
2 3 2
3.下列离子反应方程式书写正确的是
A.向 溶液中滴加少量NaOH溶液:
B.小苏打溶液与明矾溶液混合:
C. 溶液中滴加KSCN溶液:
D.向 溶液中滴加少量 溶液:
4.植物对氮元素的吸收过程如下,下列说法正确的是
A.高温有利于加快过程①
B.浇水和松土有利于过程②
C.过程③中 被还原
D.过程④叫做氮的固定
5.甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反应制得。N 为阿伏加德罗常数的值。
A
下列有关说法正确的是
A.pH=3的甲酸溶液中氢离子数目为1×10-3N
A
B.0.5 mol甲酸甲酯中含有sp3杂化的原子数目为N
A
C.50g质量分数为64%的甲醇水溶液中含有σ键数目为5N
A
D.甲醇燃料电池中,每消耗22.4L(标准状况)甲醇,转移电子数目为6N
A
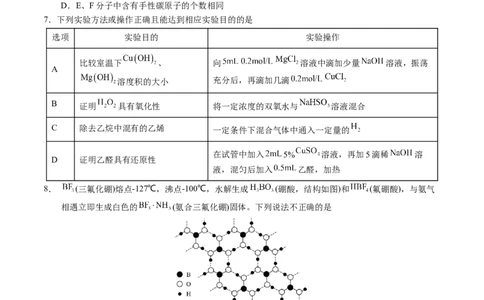
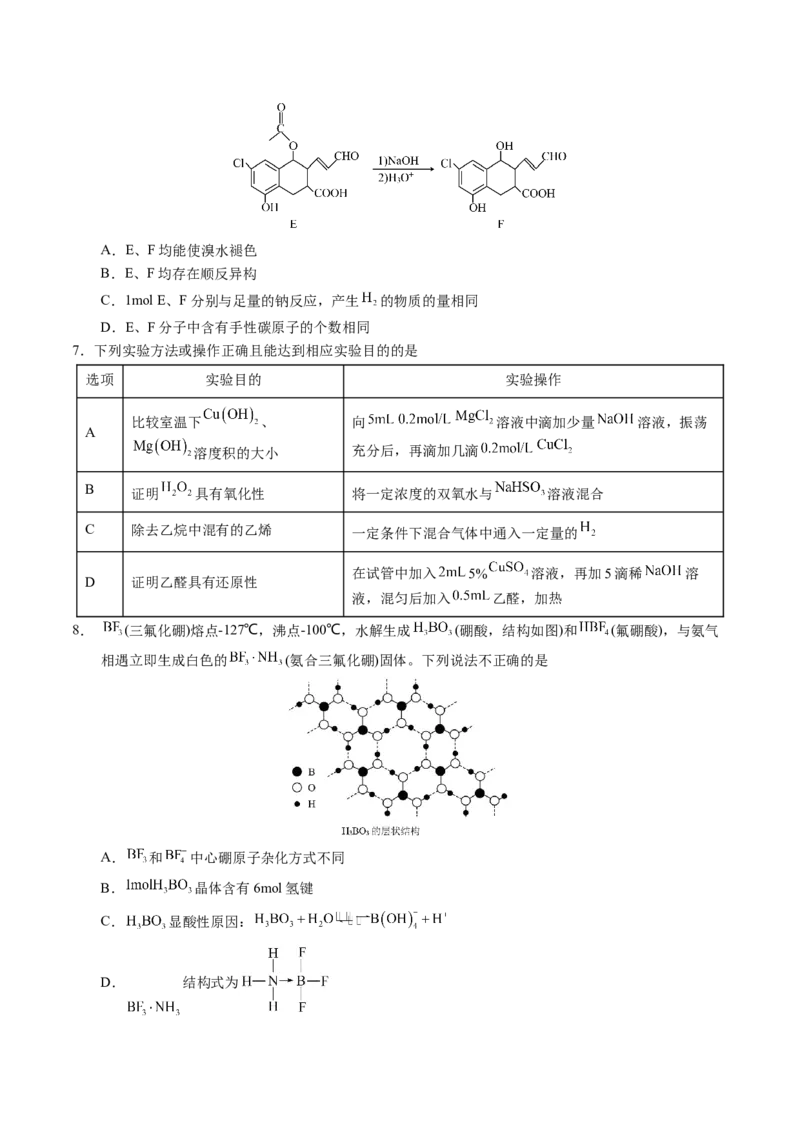
6.有机化合物F是合成一种治疗癌症新药的中间体,由化合物E转化成F的过程如图所示。下列有关说法
不正确的是A.E、F均能使溴水褪色
B.E、F均存在顺反异构
C.1mol E、F分别与足量的钠反应,产生 的物质的量相同
D.E、F分子中含有手性碳原子的个数相同
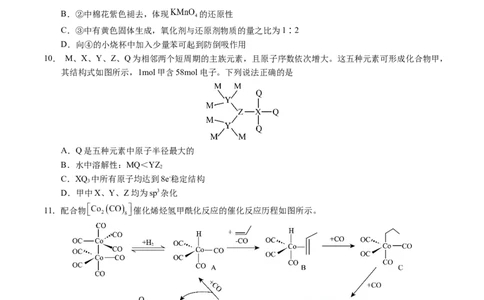
7.下列实验方法或操作正确且能达到相应实验目的的是
选项 实验目的 实验操作
比较室温下 、 向 溶液中滴加少量 溶液,振荡
A
溶度积的大小 充分后,再滴加几滴
B 证明 具有氧化性 将一定浓度的双氧水与 溶液混合
C 除去乙烷中混有的乙烯 一定条件下混合气体中通入一定量的
在试管中加入 5% 溶液,再加5滴稀 溶
D 证明乙醛具有还原性
液,混匀后加入 乙醛,加热
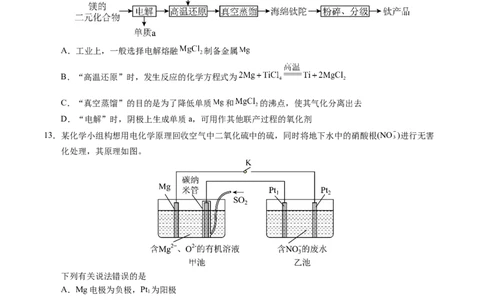
8. (三氟化硼)熔点-127℃,沸点-100℃,水解生成 (硼酸,结构如图)和 (氟硼酸),与氨气
相遇立即生成白色的 (氨合三氟化硼)固体。下列说法不正确的是
A. 和 中心硼原子杂化方式不同
B. 晶体含有6mol氢键
C. 显酸性原因:
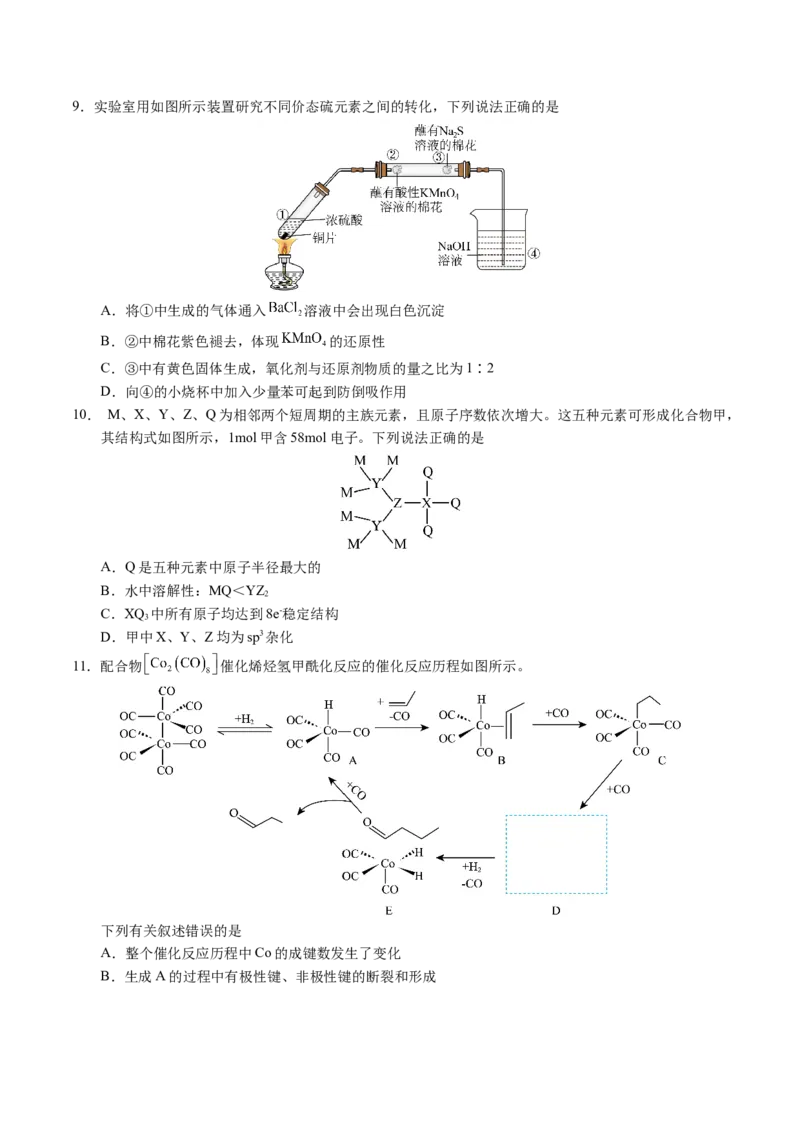
D. 结构式为9.实验室用如图所示装置研究不同价态硫元素之间的转化,下列说法正确的是
A.将①中生成的气体通入 溶液中会出现白色沉淀
B.②中棉花紫色褪去,体现 的还原性
C.③中有黄色固体生成,氧化剂与还原剂物质的量之比为1∶2
D.向④的小烧杯中加入少量苯可起到防倒吸作用
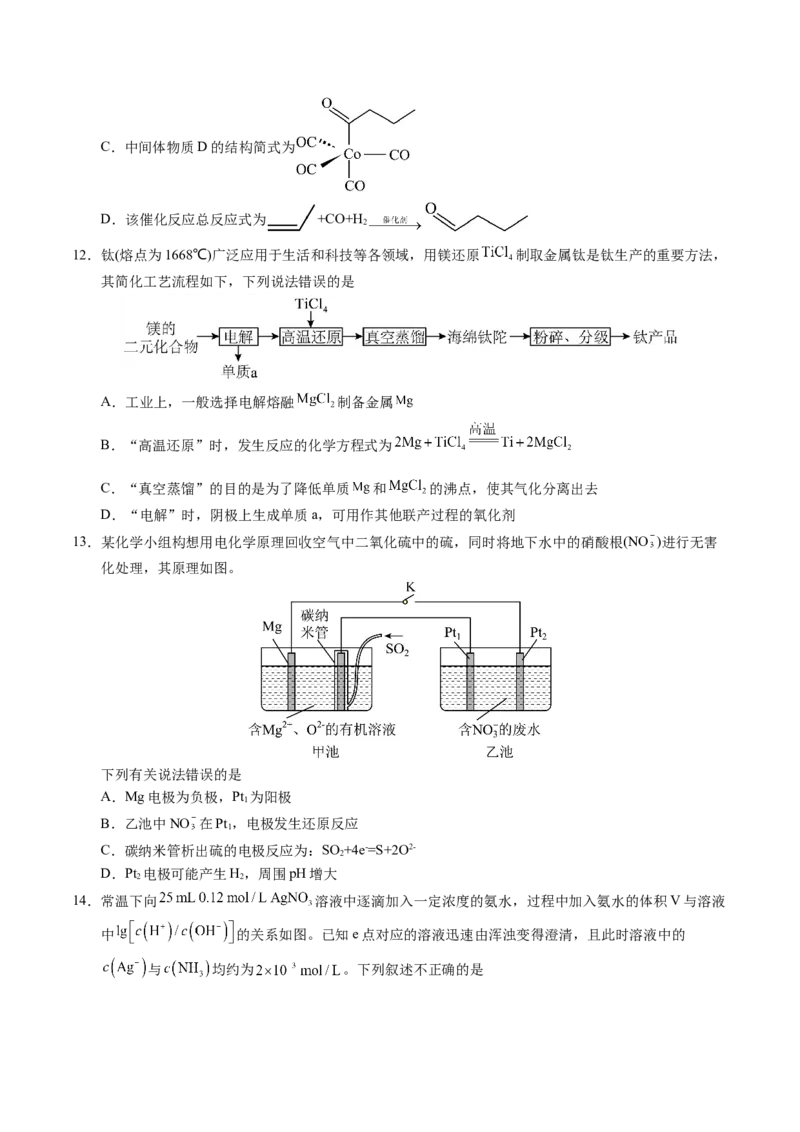
10. M、X、Y、Z、Q为相邻两个短周期的主族元素,且原子序数依次增大。这五种元素可形成化合物甲,
其结构式如图所示,1mol甲含58mol电子。下列说法正确的是
A.Q是五种元素中原子半径最大的
B.水中溶解性:MQ<YZ
2
C.XQ 中所有原子均达到8e-稳定结构
3
D.甲中X、Y、Z均为sp3杂化
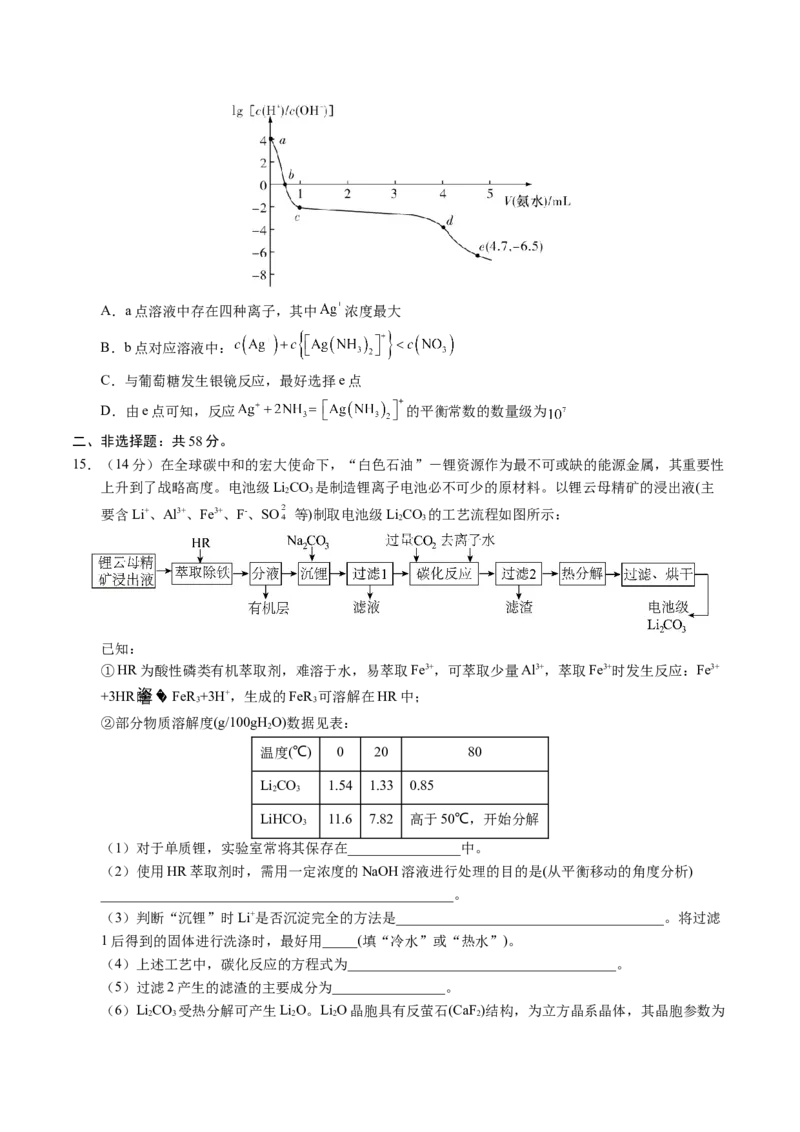
11.配合物 催化烯烃氢甲酰化反应的催化反应历程如图所示。
下列有关叙述错误的是
A.整个催化反应历程中Co的成键数发生了变化
B.生成A的过程中有极性键、非极性键的断裂和形成C.中间体物质D的结构简式为
D.该催化反应总反应式为 +CO+H
2
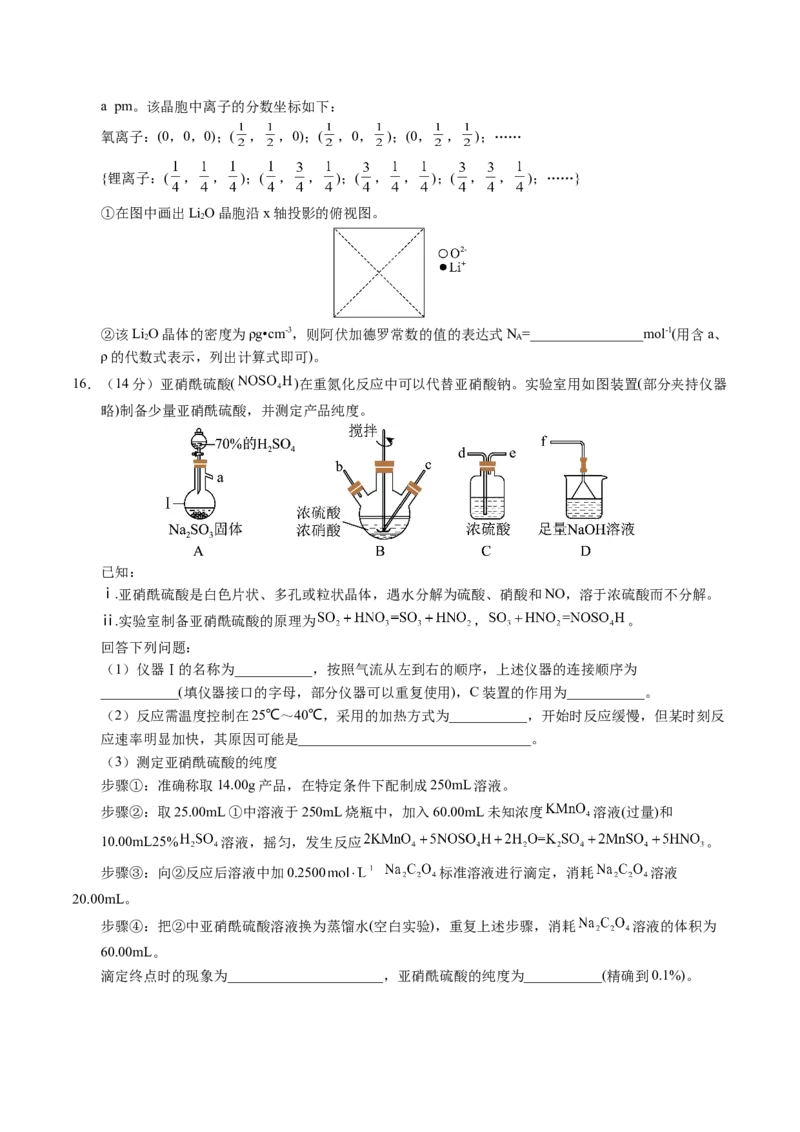
12.钛(熔点为1668℃)广泛应用于生活和科技等各领域,用镁还原 制取金属钛是钛生产的重要方法,
其简化工艺流程如下,下列说法错误的是
A.工业上,一般选择电解熔融 制备金属
B.“高温还原”时,发生反应的化学方程式为
C.“真空蒸馏”的目的是为了降低单质 和 的沸点,使其气化分离出去
D.“电解”时,阴极上生成单质a,可用作其他联产过程的氧化剂
13.某化学小组构想用电化学原理回收空气中二氧化硫中的硫,同时将地下水中的硝酸根(NO )进行无害
化处理,其原理如图。
下列有关说法错误的是
A.Mg电极为负极,Pt 为阳极
1
B.乙池中NO 在Pt ,电极发生还原反应
1
C.碳纳米管析出硫的电极反应为:SO +4e-=S+2O2-
2
D.Pt 电极可能产生H,周围pH增大
2 2
14.常温下向 溶液中逐滴加入一定浓度的氨水,过程中加入氨水的体积V与溶液
中 的关系如图。已知e点对应的溶液迅速由浑浊变得澄清,且此时溶液中的
与 均约为 。下列叙述不正确的是A.a点溶液中存在四种离子,其中 浓度最大
B.b点对应溶液中:
C.与葡萄糖发生银镜反应,最好选择e点
D.由e点可知,反应 的平衡常数的数量级为
二、非选择题:共58分。
15.(14分)在全球碳中和的宏大使命下,“白色石油”-锂资源作为最不可或缺的能源金属,其重要性
上升到了战略高度。电池级LiCO 是制造锂离子电池必不可少的原材料。以锂云母精矿的浸出液(主
2 3
要含Li+、Al3+、Fe3+、F-、SO 等)制取电池级LiCO 的工艺流程如图所示:
2 3
已知:
①HR为酸性磷类有机萃取剂,难溶于水,易萃取Fe3+,可萃取少量Al3+,萃取Fe3+时发生反应:Fe3+
+3HR FeR +3H+,生成的FeR 可溶解在HR中;
3 3
②部分物质溶解度(g/100gHO)数据见表:
2
温度(℃) 0 20 80
LiCO 1.54 1.33 0.85
2 3
LiHCO 11.6 7.82 高于50℃,开始分解
3
(1)对于单质锂,实验室常将其保存在________________中。
(2)使用HR萃取剂时,需用一定浓度的NaOH溶液进行处理的目的是(从平衡移动的角度分析)
__________________________________________________。
(3)判断“沉锂”时Li+是否沉淀完全的方法是______________________________________。将过滤
1后得到的固体进行洗涤时,最好用_____(填“冷水”或“热水”)。
(4)上述工艺中,碳化反应的方程式为______________________________________。
(5)过滤2产生的滤渣的主要成分为________________。
(6)LiCO 受热分解可产生LiO。LiO晶胞具有反萤石(CaF )结构,为立方晶系晶体,其晶胞参数为
2 3 2 2 2a pm。该晶胞中离子的分数坐标如下:
氧离子:(0,0,0);( , ,0);( ,0, );(0, , );……
{锂离子:( , , );( , , );( , , );( , , );……}
①在图中画出LiO晶胞沿x轴投影的俯视图。
2
②该LiO晶体的密度为ρg•cm-3,则阿伏加德罗常数的值的表达式N =________________mol-1(用含a、
2 A
ρ的代数式表示,列出计算式即可)。
16.(14分)亚硝酰硫酸( )在重氮化反应中可以代替亚硝酸钠。实验室用如图装置(部分夹持仪器
略)制备少量亚硝酰硫酸,并测定产品纯度。
已知:
ⅰ.亚硝酰硫酸是白色片状、多孔或粒状晶体,遇水分解为硫酸、硝酸和NO,溶于浓硫酸而不分解。
ⅱ.实验室制备亚硝酰硫酸的原理为 , 。
回答下列问题:
(1)仪器Ⅰ的名称为___________,按照气流从左到右的顺序,上述仪器的连接顺序为
___________(填仪器接口的字母,部分仪器可以重复使用),C装置的作用为___________。
(2)反应需温度控制在25℃~40℃,采用的加热方式为___________,开始时反应缓慢,但某时刻反
应速率明显加快,其原因可能是_________________________________。
(3)测定亚硝酰硫酸的纯度
步骤①:准确称取14.00g产品,在特定条件下配制成250mL溶液。
步骤②:取25.00mL①中溶液于250mL烧瓶中,加入60.00mL未知浓度 溶液(过量)和
10.00mL25% 溶液,摇匀,发生反应 。
步骤③:向②反应后溶液中加0.2500 标准溶液进行滴定,消耗 溶液
20.00mL。
步骤④:把②中亚硝酰硫酸溶液换为蒸馏水(空白实验),重复上述步骤,消耗 溶液的体积为
60.00mL。
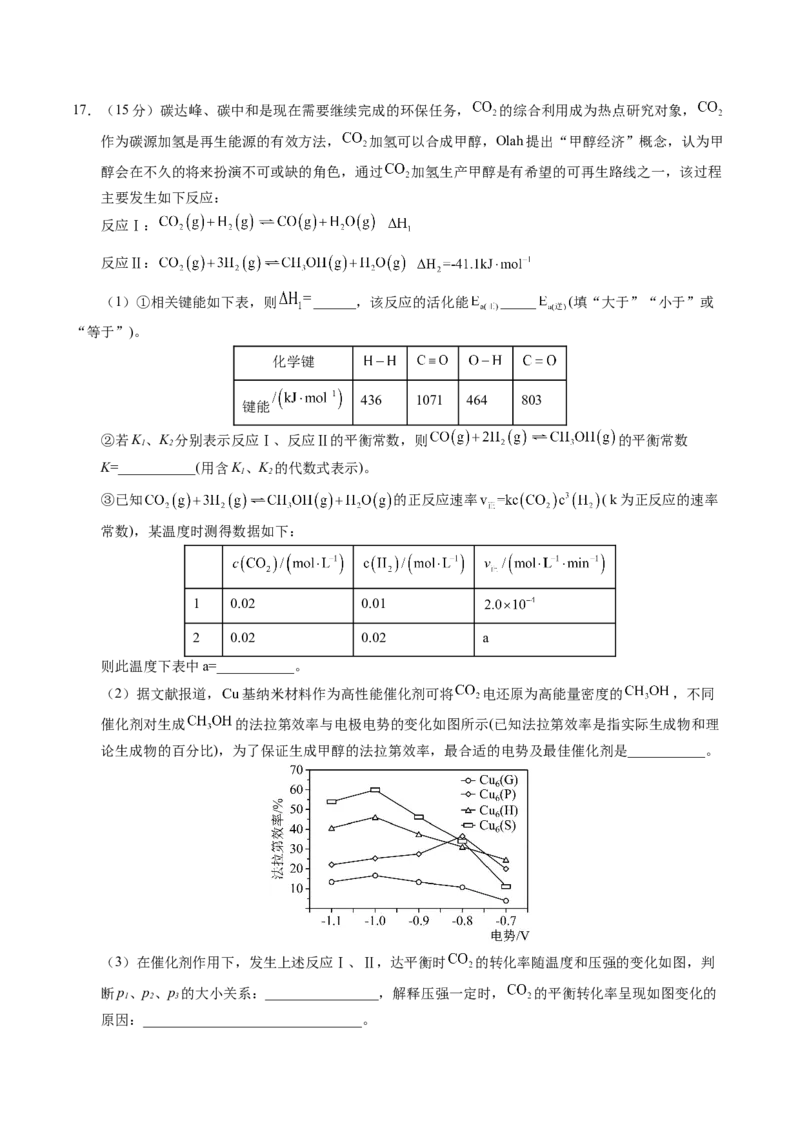
滴定终点时的现象为______________________,亚硝酰硫酸的纯度为___________(精确到0.1%)。17.(15分)碳达峰、碳中和是现在需要继续完成的环保任务, 的综合利用成为热点研究对象,
作为碳源加氢是再生能源的有效方法, 加氢可以合成甲醇,Olah提出“甲醇经济”概念,认为甲
醇会在不久的将来扮演不可或缺的角色,通过 加氢生产甲醇是有希望的可再生路线之一,该过程
主要发生如下反应:
反应Ⅰ:
反应Ⅱ:
(1)①相关键能如下表,则 ______,该反应的活化能 _____ (填“大于”“小于”或
“等于”)。
化学键
436 1071 464 803
键能
②若K 、K 分别表示反应Ⅰ、反应Ⅱ的平衡常数,则 的平衡常数
1 2
K=___________(用含K 、K 的代数式表示)。
1 2
③已知 的正反应速率 ( k为正反应的速率
常数),某温度时测得数据如下:
1 0.02 0.01
2 0.02 0.02 a
则此温度下表中a=___________。
(2)据文献报道, 基纳米材料作为高性能催化剂可将 电还原为高能量密度的 ,不同
催化剂对生成 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理
论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是___________。
(3)在催化剂作用下,发生上述反应Ⅰ、Ⅱ,达平衡时 的转化率随温度和压强的变化如图,判
断p、p、p 的大小关系:________________,解释压强一定时, 的平衡转化率呈现如图变化的
1 2 3
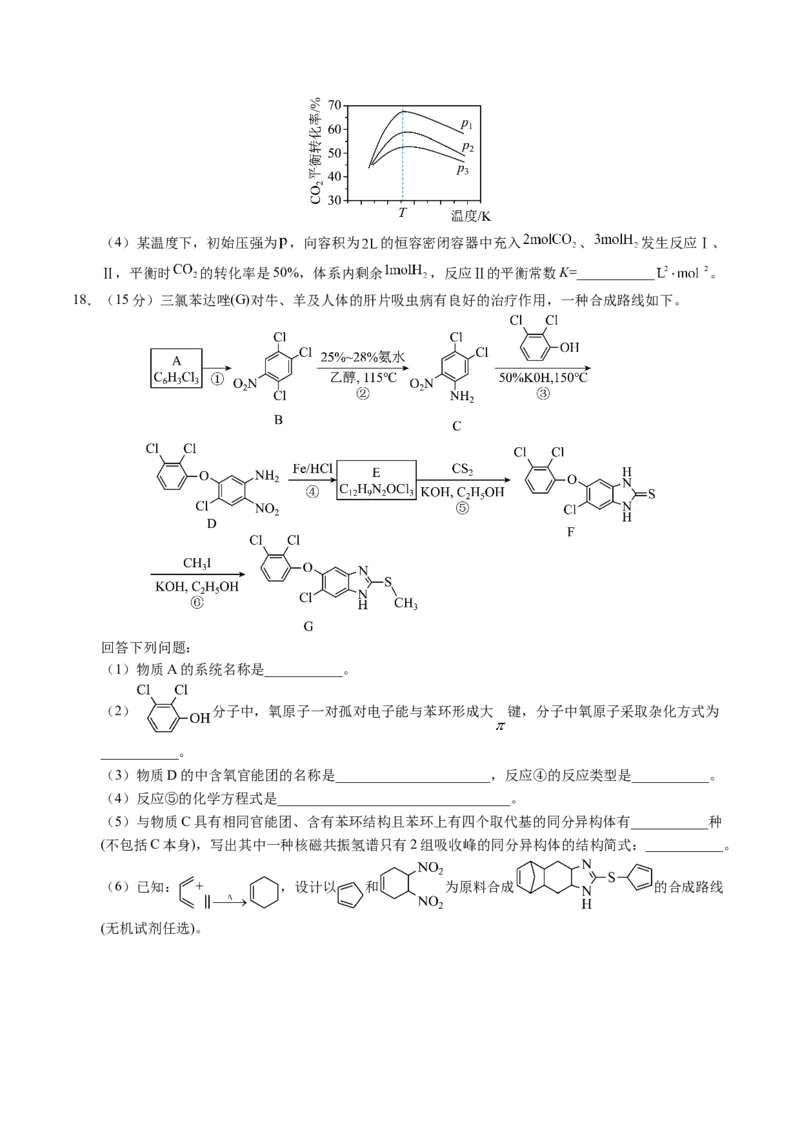
原因:_______________________________。(4)某温度下,初始压强为 ,向容积为 的恒容密闭容器中充入 、 发生反应Ⅰ、
Ⅱ,平衡时 的转化率是50%,体系内剩余 ,反应Ⅱ的平衡常数K=___________ 。
18.(15分)三氯苯达唑(G)对牛、羊及人体的肝片吸虫病有良好的治疗作用,一种合成路线如下。
回答下列问题:
(1)物质A的系统名称是___________。
(2) 分子中,氧原子一对孤对电子能与苯环形成大 键,分子中氧原子采取杂化方式为
___________。
(3)物质D的中含氧官能团的名称是______________________,反应④的反应类型是___________。
(4)反应⑤的化学方程式是_________________________________。
(5)与物质C具有相同官能团、含有苯环结构且苯环上有四个取代基的同分异构体有___________种
(不包括C本身),写出其中一种核磁共振氢谱只有2组吸收峰的同分异构体的结构简式:___________。
(6)已知: + ,设计以 和 为原料合成 的合成路线
(无机试剂任选)。