文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(广东专用)
黄金卷07
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第Ⅰ卷
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1.服饰文化是中华传统文化中的重要一脉。下列制作服饰所用原料的主要成分为纤维素的是
A.蚕丝 B.棉花
C.皮革 D.羊毛
【答案】B
【详解】A.蚕丝的主要成分为蛋白质,A错误;
B.棉花的主要成分为纤维素,B正确;
C.皮革的主要成分为蛋白质,C错误;
D.羊毛的主要成分为蛋白质,D错误;
故选B。
2.肼(N H)是发射航天飞船常用的高能燃料,可通过反应2NH +NaClO=N H+NaCl+HO制备。下列有关
2 4 3 2 4 2
微粒的描述错误的是
A.NH 的电子式为
3
B.NH 的结构式为
2 4
C.NH 的空间构型是三角锥形
3
D.质子数为17、中子数为18的氯原子可表示为 Cl
【答案】A
【详解】A.氨气分子中N原子最外层有8个电子,电子式应为 ,A错误;
B.NH 分子中两个N原子共用一对电子,每个N原子和两个H原子分别共用一对电子,结构式为
2 4,B正确;
C.NH 的空间构型是三角锥形,C正确;
3
D.质子数为17、中子数为18的氯原子质量数为17+18=35,可以表示为 Cl,D正确;
综上所述答案为A。
3.作为广东文化的代表之一,岭南文化历史悠久。下列岭南文化内容中蕴含的化学知识描述不正确的是
选
文化类别 文化内容 化学知识
项
A 饮食文化 早茶文化中的叉烧包 叉烧包中富含糖类、油脂、蛋白质等营养物质
B 劳动文化 热的纯碱溶液洗涤餐具 油脂在碱性条件下发生水解
C 服饰文化 “丝中贵族”香云纱 鉴别丝和棉花可以用灼烧的方法
D 节日文化 烟花舞龙 烟花利用了“焰色试验”原理,该原理属于化学变化
【答案】D
【详解】A.叉烧包中的叉烧含有肉、油脂、淀粉等,所以富含糖类、油脂、蛋白质等营养物质,A正确;
B. 水解使溶液显碱性,油脂在碱性条件下发生水解,所以可用纯碱去油污,B正确;
C.丝为蛋白质,灼烧时有烧焦羽毛的气味,棉花为纤维素,所以可以用灼烧的方法鉴别丝和棉花,C正
确;
D.烟花利用了“焰色试验”原理,焰色试验属于物理变化,D错误;
故选D。
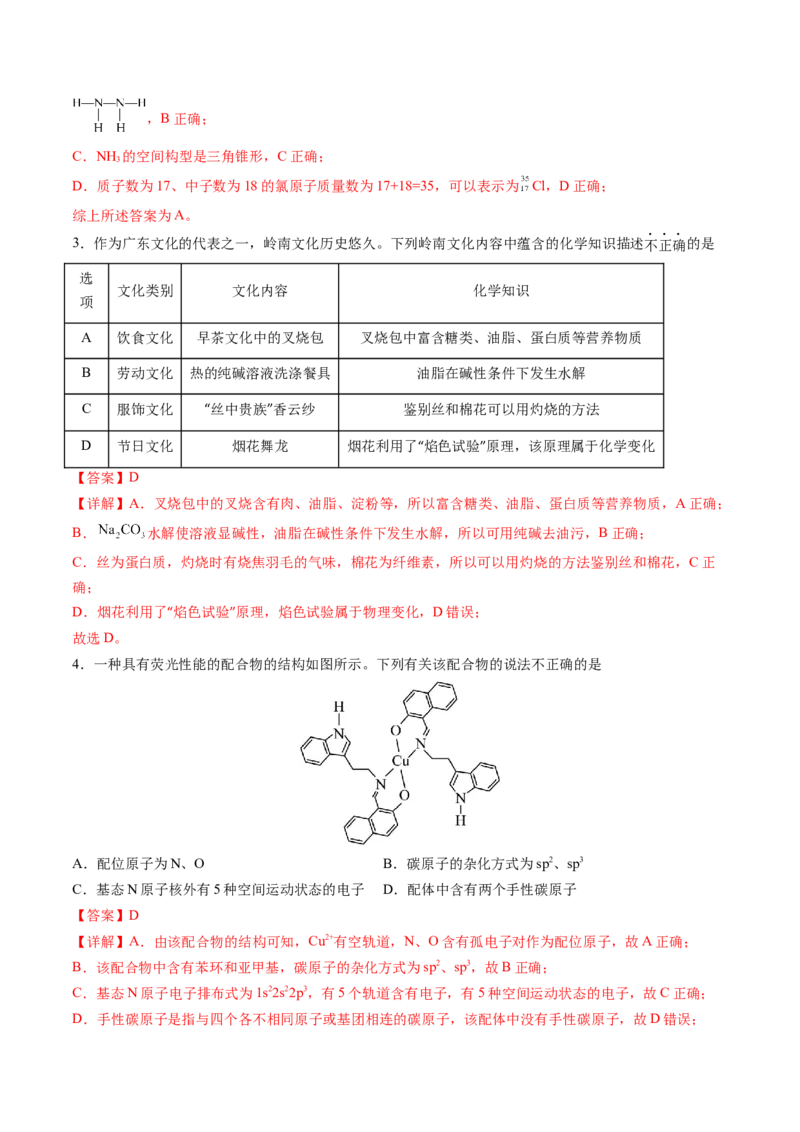
4.一种具有荧光性能的配合物的结构如图所示。下列有关该配合物的说法不正确的是
A.配位原子为N、O B.碳原子的杂化方式为sp2、sp3
C.基态N原子核外有5种空间运动状态的电子 D.配体中含有两个手性碳原子
【答案】D
【详解】A.由该配合物的结构可知,Cu2+有空轨道,N、O含有孤电子对作为配位原子,故A正确;
B.该配合物中含有苯环和亚甲基,碳原子的杂化方式为sp2、sp3,故B正确;
C.基态N原子电子排布式为1s22s22p3,有5个轨道含有电子,有5种空间运动状态的电子,故C正确;
D.手性碳原子是指与四个各不相同原子或基团相连的碳原子,该配体中没有手性碳原子,故D错误;故选D。
5.下列关于物质的性质和应用的说法正确的是
A.绿矾的化学式为 FeSO ·7H O,可用作补血剂
4 2
B.从铝土矿中获得氧化铝再制得氯化铝固体,电解熔融的氯化铝得到铝
C.泡沫灭火器中常使用的原料是碳酸钠和硫酸铝
D.用 NaS 作还原剂,除去水中的 Cu2+和 Hg2+
2
【答案】A
【详解】A.绿矾的化学式为FeSO ·7H O,FeSO 常用作补血剂,故A正确;
4 2 4
B.从铝土矿中获得氧化铝,电解熔融的氧化铝得到铝,故B错误;
C.泡沫灭火器中常使用的原料是碳酸氢钠和硫酸铝,两者发生双水解反应生成氢氧化铝和二氧化碳,故
C错误;
D.除去水中的 Cu2+和 Hg2+常用 NaS,将Cu2+和 Hg2+转化为CuS和HgS沉淀,NaS不是作还原剂,故
2 2
D错误。
综上所述,答案为A。
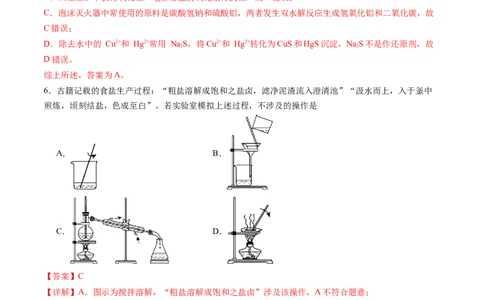
6.古籍记载的食盐生产过程:“粗盐溶解成饱和之盐卤,滤净泥渣流入澄清池”“汲水而上,入于釜中
煎炼,顷刻结盐,色成至白”。若实验室模拟上述过程,不涉及的操作是
A. B.
C. D.
【答案】C
【详解】A.图示为搅拌溶解,“粗盐溶解成饱和之盐卤”涉及该操作,A不符合题意;
B.图示为过滤,“滤净泥渣流入澄清池”涉及该操作,B不符合题意;
C.图示为蒸馏,没有涉及,C符合题意;
D.图示为蒸发结晶,“入于釜中煎炼,顷刻结盐”涉及该操作,D不符合题意;
综上所述答案为C。
7.铝空气电池因成本低廉、安全性高,有广阔的开发应用前景。一种铝空气电池放电过程示意如图,下
列说法正确的是A.a为正极,放电时发生氧化反应
B.放电时OH-往b极迁移
C.电路中每转移4 mol电子,消耗22.4 L氧气
D.该电池负极电极反应为:
【答案】D
【详解】A.根据图示可知:在a电极Al失去电子被氧化为 ,所以a电极为负极,放电时失去电子发
生氧化反应,A错误;
B.放电时OH-往负极区移动,对于该电池来说,移向a电极,与Al失去电子产生的Al3+反应产生 ,
B错误;
C.题干未指明气体所处的外界条件,故不能根据转移电子数目确定消耗的氧气的体积,C错误;
D.根据图示可知:在a电极Al失去电子产生Al3+,Al3+与溶液中的OH-反应产生为 ,则负极的电极
反应式为: ,D正确;
故合理选项是D。
8.理解与辨析是化学学科的关键能力,下列离子在溶液中能共存的是
A.S2-、Na+、H+、 B.Fe2+、 、H+、
C. 、 、OH-、Mg2+ D. 、Al3+、Cl-、Ca2+
【答案】D
【详解】A.氢离子和硫离子结合生成弱电解质硫化氢,不能大量共存,A错误;
B.氢离子和硅酸根离子结合生成硅酸沉淀,不能大量共存,B错误;
C.镁离子和氢氧根离子结合生成氢氧化镁沉淀,铵根离子和氢氧根离子结合生成一水合氨,不能大量共
存,C错误;
D.四种离子之间均不反应,可大量共存,D正确;
答案选D。
9.汽车尾气是造成雾霾天气的主要原因,研究其无害化处理具有现实意义。已知:2NO(g)+2CO(g)
2CO(g)+N(g)∆H<0,下列措施能提高该反应速率和NO转化率的是
2 2
A.改用高效催化剂 B.缩小容器的体积
C.降低温度 D.增加NO的浓度【答案】B
【详解】A. 改用高效催化剂,只改变反应速率,故A不选;
B. 缩小容器的体积,浓度增大,平衡向体积减小的方向即正向移动,能提高该反应速率和NO转化率,
故B选;
C. 降低温度反应速率降低,故C不选;
D. 增加NO的浓度,反应速率增大,但NO转化率降低,故D不选;
故选B。
10.载人航天器中的物质和能量资源都十分宝贵,我国科学家进行了如图所示的氧循环研究,实现了空间
站中氧气的再生。下列说法不正确的是
A.用于循环的氢原子利用率为100%
B.太阳能可作为反应①和②的能量来源
C.反应①为
D.等物质的量的 和 含有的电子数相同
【答案】A
【详解】A.反应①为 ,反应②2HO 2H +O ,氢原子部分进入甲
2 2 2
烷,用于循环的氢原子利用率达不到100%,A错误;
B.太阳能可作为反应①和②的能量来源,B正确;
C.根据得失电子守恒配平方程,反应①为 ,C正确;
D.水和甲烷都是常见的10电子微粒,等物质的量的 和 含有的电子数相同,D正确;
故选A。
11.铁及其化合物在生活中应用广泛,下列有关离子方程式书写正确的是
A.将铁片投入到稀硝酸中:
B.向 溶液中通入少量 :C.用铁氰化钾溶液检验 :
D.往 溶液中加入过量 粉:
【答案】B
【详解】A.铁片与稀硝酸反应生成一氧化氮,不生成氢气,故A错误;
B. 具有较强的氧化性,可将 还原为硫单质,离子方程式为 ;故B正
确;
C.铁氰化钾溶于水可拆为离子的形式,离子方程式为 ,故C错
误;
D.过量 将 还原为铁单质,离子方程式为 ;故D错误;
故答案选B。
12.用如下装置模拟汽车尾气系统中CO与NO的反应。下列有关该实验的说法错误的是
A.反应前需排尽装置中的空气
B.NO和CO在装置a中进行了预混合
C.可观察到装置d中澄清石灰水变浑浊
D.实验中的有害尾气均可用碱石灰吸收
【答案】D
【详解】A.NO与空气中氧气反应生成NO ,所以反应前需排尽装置中的空气,故A正确;
2
B.如图所示,NO和CO同时通入装置a,在装置a中进行了预混合,故B正确;
C.NO和CO在催化剂、加热条件下反应生成二氧化碳和氮气,二氧化碳通过澄清石灰水时,可观察到装
置d中澄清石灰水变浑浊,故C正确;
D.实验中的有害尾气包括未反应的NO和CO,不能用碱石灰吸收,故D错误。
故选D。
13.铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:下列说法不正确的是
A.该过程的总反应为HCOOH CO↑+H ↑
2 2
B.H+浓度过大或者过小,均导致反应速率降低
C.该历程中反应速率最慢的一步:
D.该催化循环中Fe元素的化合价发生了变化
【答案】D
【详解】A.根据反应进程图象可知,甲酸在催化剂的作用下,分解成CO 和H,即该过程中的总反应为
2 2
HCOOH CO↑+H ↑,故A说法正确;
2 2
B.根据反应机理图可知,甲酸电离产生H+和HCOO-,HCOO-参与反应,与催化剂结合放出二氧化碳,若
H+浓度过大,抑制甲酸的电离,使c(HCOO-)降低,反应速率减慢,若H+浓度降低,反应Ⅲ→Ⅳ速率减慢,
故B说法正确;
C.活化能越大,反应速率越慢,根据反应进程图象可知, ,
活化能最大,反应速率最慢,故C说法正确;
D.虽然铁连接的原子数和种类发生了改变,但是配离子的电荷数没变,因此Fe元素化合价不变,故D说
法错误;
答案为D。
14.短周期元素X、Y、Z、W是同周期主族元素,W元素形成的某种单质具有强氧化性,可用于杀菌消
毒。四种元素与锂组成的盐是一种新型的锂离子电池的电解质,结构如图所示(“→”表示配位键,指共价键
中共用的电子对是由其中一原子独自供应)。下列说法正确的是
A.原子半径:X>Y>Z>WB.Y的最高价氧化物的水化物 为强酸
C.单质氧化性:
D.阴离子中四种元素均满足8电子稳定结构
【答案】D
【分析】短周期元素X、Y、Z、W是同周期主族元素,W元素形成的某种单质具有强氧化性,可用于杀
菌消毒,W能形成2个共价键,W是O元素;Z能形成4个共价键,Z是C元素;X形成1个共价键,X
是F元素;Y能形成3个共价键和1个配位键,Y是B元素。
【详解】A.同周期元素从左到右,半径依次减小,原子半径:B>C>O>F,故A错误;
B.B的最高价氧化物的水化物为HBO,HBO 是弱酸,故B错误;
3 3 3 3
C.单质氧化性: ,故C错误;
D.根据阴离子结构图,阴离子中B、Si、O、F四种元素均满足8电子稳定结构,故D正确;
选D。
15.二氧化碳催化加氢合成乙烯是综合利用 CO 的热点研究领域,对节能减排有重要意义。已知反应:
2
6H(g)+2CO(g) CH=CH (g)+4HO(g),温度对 CO 的平衡转化率和催化剂催化效率的影
2 2 2 2 2 2
响如图所示,下列说法不正确的是
A.正反应为放热反应
B.化学平衡常数:K >K
M N
C.当温度高于 250 ℃时,催化剂的催化效率降低是因为平衡逆向移动引起的
D.若初始投料比 n(H )∶n(CO)=3∶1,则图中 M 点的乙烯体积分数约为 7.7%
2 2
【答案】C
【详解】A.由图示知,随着温度的升高,CO 平衡转化率下降,说明温度升高,平衡逆向移动,故逆向
2
为吸热反应,正向为放热反应,A正确;
B.升高温度,平衡逆向移动,平衡常数K减小,故K >K ,B正确;
M N
C.温度高于250℃时,催化剂催化效率下降,是因为温度升高使催化剂活性下降,而不是平衡移动的原因,
C错误;
D.由图示知,点M的CO 平衡转化率为50%,设H 起始为3 mol,CO 为1 mol,列三段式如下:
2 2 2,则平衡时乙烯的体积分数=
,D正确;
故答案选C。
16.次磷酸钴 广泛应用丁化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解
法制备次磷酸钴的装置如图所示。下列说法正确的是
A.Co电极连接电源负极
B.C采用阴离子交换膜
C.石墨电极的电极反应式为
D.工作时,原料室中 的浓度不变
【答案】C
【详解】A.此电解池用金属钴和次磷酸钠制备次磷酸钴,因此Co电极失去电子作阳极,与电源的正极相
连,A项错误;
B.电解池中,阳离子向阴极移动,阴离子向阳极移动。产品室中得到次磷酸钴,阳极区生成的 和原
料室中的 都移向产品室,为了确保产品的纯度和原料室电荷守恒,原料室中的 移向阴极区,因
此A、B、C分别采用阳离子交换膜、阴离子交换膜、阳离子交换膜,B项错误;
C.石墨电极作阴极,因此电极反应式为 ,C项正确;
D.产品室中得到次磷酸钴,阳极区生成的 和原料室中的 都移向产品室,原料室中的 移向
阴极区,所以工作时原料室中 的浓度减小,D项错误;
选C。
第Ⅱ卷
二、非选择题:本题共4个小题,共56分。
17.(14分)醋酸钠 是一种常用的防腐剂和缓冲剂。
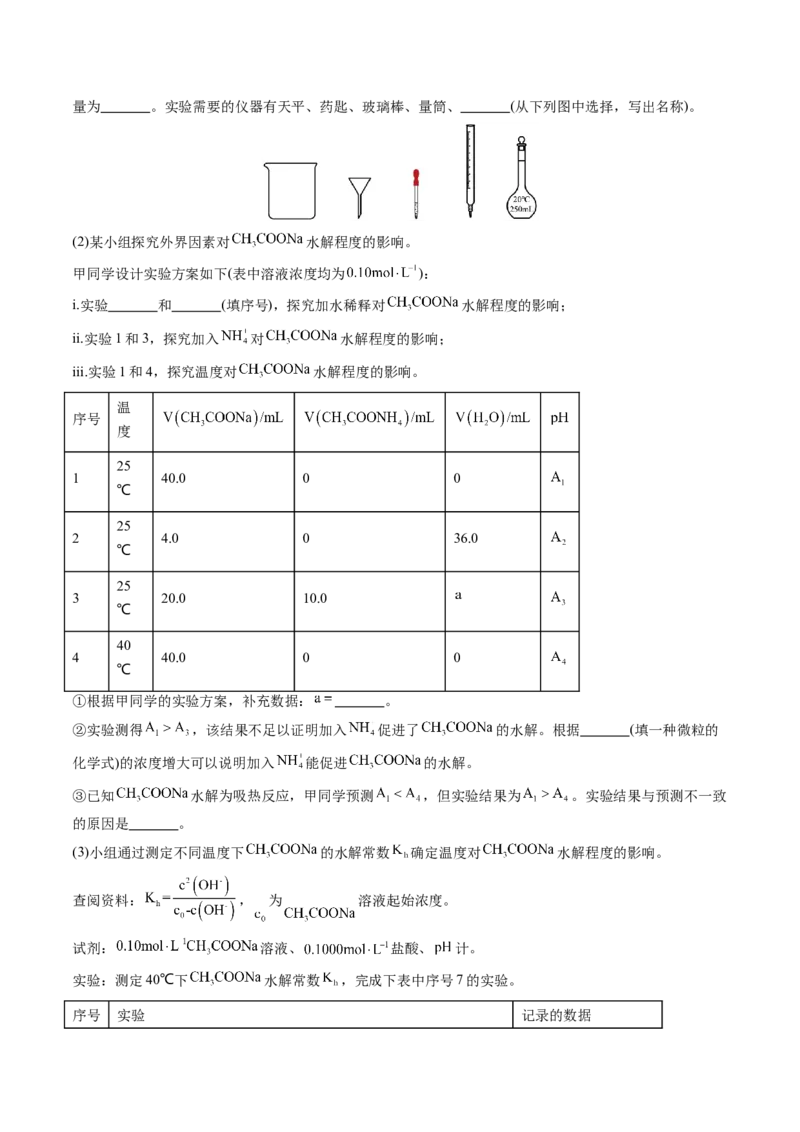
(1)配制 溶液,需要称量醋酸钠晶体( , )的质量为 。实验需要的仪器有天平、药匙、玻璃棒、量筒、 (从下列图中选择,写出名称)。
(2)某小组探究外界因素对 水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为 ):
i.实验 和 (填序号),探究加水稀释对 水解程度的影响;
ii.实验1和3,探究加入 对 水解程度的影响;
iii.实验1和4,探究温度对 水解程度的影响。
温
序号
度
25
1 40.0 0 0
℃
25
2 4.0 0 36.0
℃
25
3 20.0 10.0
℃
40
4 40.0 0 0
℃
①根据甲同学的实验方案,补充数据: 。
②实验测得 ,该结果不足以证明加入 促进了 的水解。根据 (填一种微粒的
化学式)的浓度增大可以说明加入 能促进 的水解。
③已知 水解为吸热反应,甲同学预测 ,但实验结果为 。实验结果与预测不一致
的原因是 。
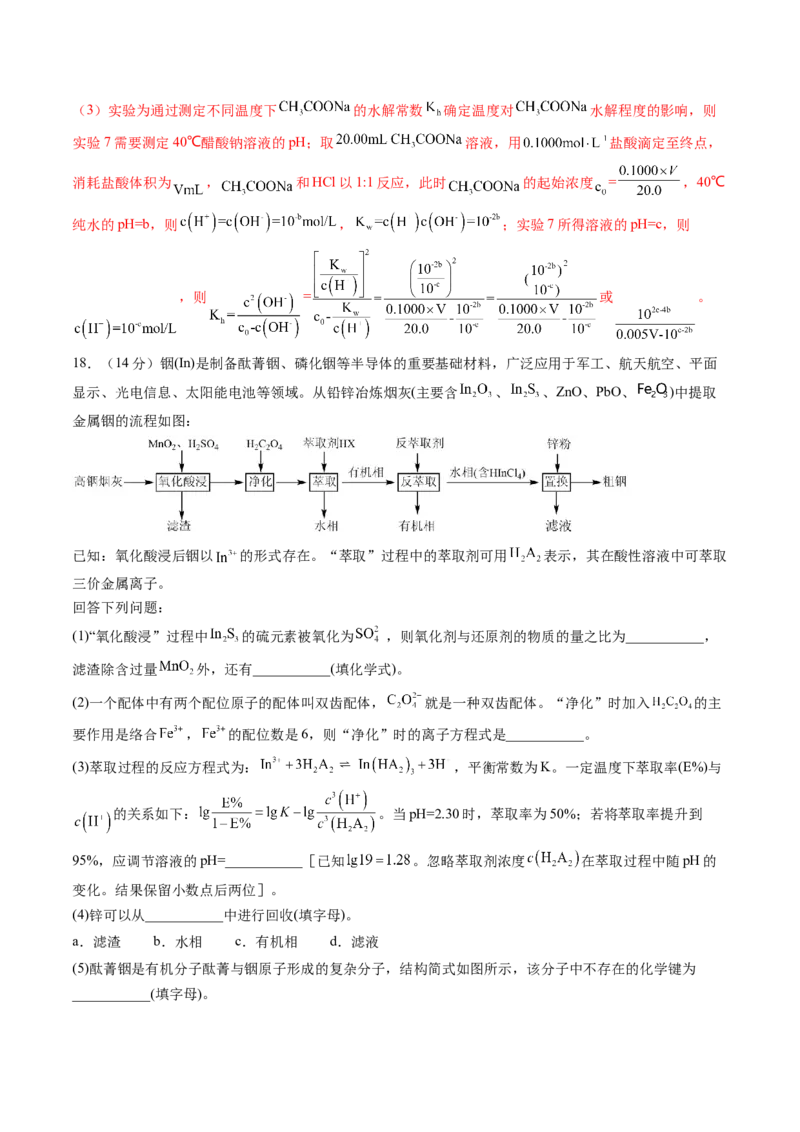
(3)小组通过测定不同温度下 的水解常数 确定温度对 水解程度的影响。
查阅资料: , 为 溶液起始浓度。
试剂: 溶液、 盐酸、 计。
实验:测定40℃下 水解常数 ,完成下表中序号7的实验。
序号 实验 记录的数据取 溶液,用 盐酸滴定至终
5 消耗盐酸体积为
点
6 测40℃纯水的
7
在50℃和60℃下重复上述实验。
数据处理:40℃, (用含 、 、 的计算式表示)
实验结论: ,温度升高,促进 水解。
【答案】(1) 3.4g 烧杯、胶头滴管、250mL容量瓶
(2) 1 2 0 升高温度促进水的电离导致溶液中氢离子浓度增大
(3) 测定40℃醋酸钠溶液的pH
或
【分析】配制一定物质的量浓度的溶液,所需的步骤有计算、称量、溶解(冷却)、转移、洗涤、定容、
摇匀、装瓶贴签;
滴定实验的步骤是:滴定前的准备:滴定管:查漏→洗涤→润洗→装液→调液面→记录,锥形瓶:注液体
→记体积→加指示剂;滴定:眼睛注视锥形瓶溶液颜色变化;终点判断:记录数据;数据处理:通过数据
进行计算;
【详解】(1)配制 溶液,需要称量醋酸钠晶体的质量为
。实验需要的仪器有天平、药匙、玻璃棒、量筒、烧杯、胶头滴管、
250mL容量瓶;
(2)探究加水稀释对 水解程度的影响,则实验中变量为醋酸钠的浓度,故实验1和2,探究
加水稀释对 水解程度的影响;
①实验1和3,探究加入 对 水解程度的影响;不能改变醋酸根的浓度,故 0;
②醋酸水解方程式为: ,铵根离子水解方程式为:
;铵根离子水解会导致溶液中酸性增强,实验测得 ,该结果不足以
证明加入 促进了 的水解,实验中可以根据 的浓度增大可以说明加入 能促
进 的水解;
③已知 水解为吸热反应,甲同学预测 ,但实验结果为 。实验结果与预测不一致
的原因是水的电离也为吸热过程,升高温度促进水的电离导致溶液中氢离子浓度增大;(3)实验为通过测定不同温度下 的水解常数 确定温度对 水解程度的影响,则
实验7需要测定40℃醋酸钠溶液的pH;取 溶液,用 盐酸滴定至终点,
消耗盐酸体积为 , 和HCl以1:1反应,此时 的起始浓度 = ,40℃
纯水的pH=b,则 , ;实验7所得溶液的pH=c,则
,则 = 或 。
18.(14分)铟(In)是制备酞菁铟、磷化铟等半导体的重要基础材料,广泛应用于军工、航天航空、平面
显示、光电信息、太阳能电池等领域。从铅锌冶炼烟灰(主要含 、 、ZnO、PbO、 )中提取
金属铟的流程如图:
已知:氧化酸浸后铟以 的形式存在。“萃取”过程中的萃取剂可用 表示,其在酸性溶液中可萃取
三价金属离子。
回答下列问题:
(1)“氧化酸浸”过程中 的硫元素被氧化为 ,则氧化剂与还原剂的物质的量之比为___________,
滤渣除含过量 外,还有___________(填化学式)。
(2)一个配体中有两个配位原子的配体叫双齿配体, 就是一种双齿配体。“净化”时加入 的主
要作用是络合 , 的配位数是6,则“净化”时的离子方程式是___________。
(3)萃取过程的反应方程式为: ,平衡常数为K。一定温度下萃取率(E%)与
的关系如下: 。当pH=2.30时,萃取率为50%;若将萃取率提升到
95%,应调节溶液的pH=___________[已知 。忽略萃取剂浓度 在萃取过程中随pH的
变化。结果保留小数点后两位]。
(4)锌可以从___________中进行回收(填字母)。
a.滤渣 b.水相 c.有机相 d.滤液
(5)酞菁铟是有机分子酞菁与铟原子形成的复杂分子,结构简式如图所示,该分子中不存在的化学键为
___________(填字母)。a.σ键 b.π键 c.离子键 d.配位键
(6)磷化铟的晶胞结构如图所示,晶胞参数为a nm,In的配位数为___________;与In原子间距离为
的In原子有___________个。
【答案】(1) 12:1 PbSO
4
(2)
(3)2.73
(4)b
(5)c
(6) 4 12
【分析】高铟烟灰(主要含ZnO、PbO、Fe O、 InO、 InS),在高铟烟灰加入硫酸、二氧化锰进行酸浸
2 3 2 3 2 3
氧化,将InS 氧化为硫酸根离子和In3+, ZnO、PbO、Fe O 分别和硫酸反应转化为ZnSO、PbSO 沉淀和
2 3 2 3 4 4
Fe ( SO) ,InO 和硫酸反应变为In3+,则滤渣为硫酸铅;过滤,向滤液中加入草酸,还原铁离子,防止
2 4 3 2 3
加入萃取剂时,铁离子进入有机相;加入萃取剂萃取In3+,则Zn2+、Fe2+均进入水相,经一系列操作得到粗
铟,据此分析。
【详解】(1)氧化酸浸过程中MnO 只将InS 中的硫元素氧化为硫酸根离子,S的化合价由-2价变为+6
2 2 3
价,共失去24个电子, Mn的化合价由+4价变为+2价,得到2个电子,根据得失电子总数相等,则氧化
剂与还原剂的物质的量之比为24 : 2,滤渣除了过量的二氧化锰外还有硫酸铅。
(2)草酸根离子为双齿配体,铁离子的配位数为6,故形成的配位离子为 ,该净化的离子方
程式为:
(3) 。当pH=2.30时,萃取率为50%;则 ,得
,若将萃取率提升到95%,则 ,将lgK代入,则有,lgc(H+)=-2.73,则应调节溶液的
pH=2.73。
(4)Zn2+、Fe2+均进入水相,故锌可以从水相中进行回收。
(5)In3+和氮原子之间存在配位键、共价键,单键为键,双键为一个σ键和一个π键,所以不含c。
(6)磷周围有4个In原子形成正四面体结构,磷的配位数为4,晶胞中In为 ,磷原子数为
4,磷原子和In个数相等,故In的配位数也为4,晶胞参数为a nm,与In原子间距离为 anm的In原子
在晶胞面对角线上,每个顶点为8个晶胞共用,每个面为2个晶胞共用,则与In原子间距离为 anm的
In原子数为 。
19.(14分)乙烯是重要的基础化工原料,工业上利用乙烷脱氢制乙烯的相关反应如下:
反应Ⅰ:
反应Ⅱ:
(1)反应 的 _______ 。
(2)以 和 的混合气体为起始投料( 不参与反应),保持混合气体总物质的量不变,在恒容的容器中
对反应Ⅰ进行研究。下列说法正确的是_______。
A.升高温度,正、逆反应速率同时增大
B. 和 的物质的量相等时,反应达到平衡状态
C.增加起始投料时 的体积分数,单位体积的活化分子数增加
D.增加起始投料时 的体积分数, 平衡转化率增大
(3)科研人员研究催化剂对乙烷无氧脱氢的影响
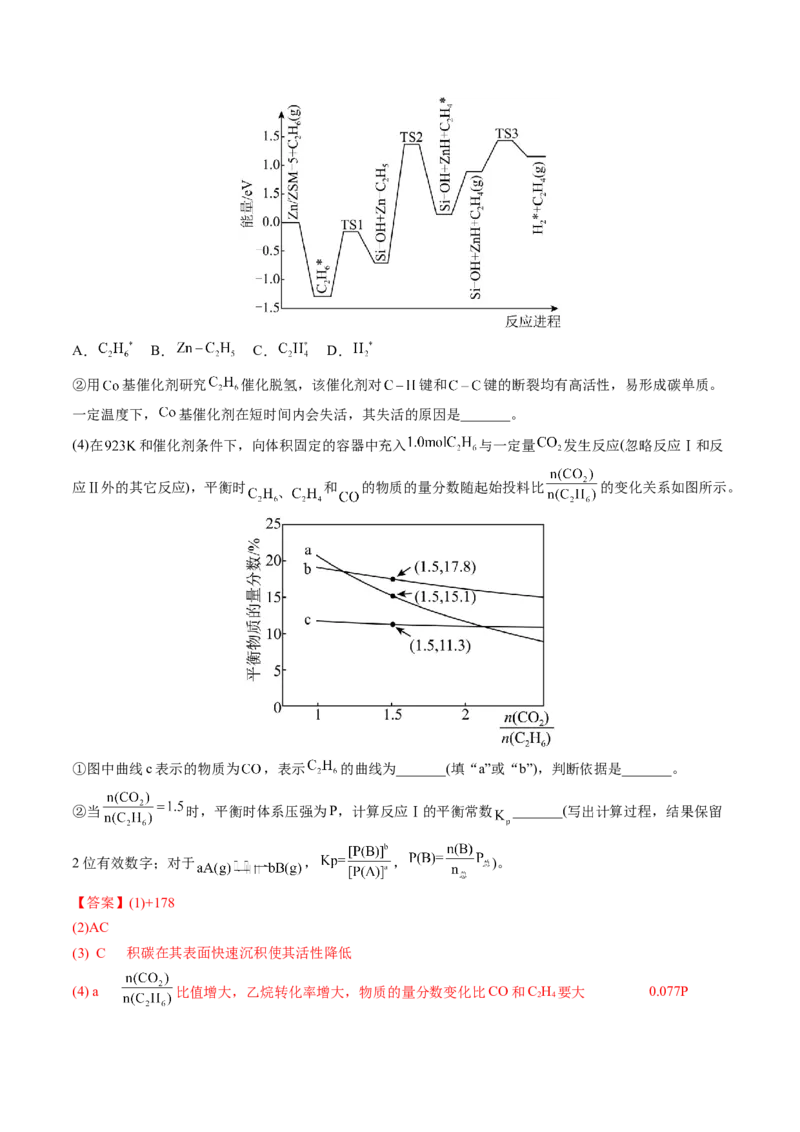
①在一定条件下, 催化乙烷脱氢转化为乙烯的反应历程如图所示,该历程的各步反应中,生
成下列物质速率最慢的是_______。A. B. C. D.
②用 基催化剂研究 催化脱氢,该催化剂对 键和 键的断裂均有高活性,易形成碳单质。
一定温度下, 基催化剂在短时间内会失活,其失活的原因是_______。
(4)在 和催化剂条件下,向体积固定的容器中充入 与一定量 发生反应(忽略反应Ⅰ和反
应Ⅱ外的其它反应),平衡时 和 的物质的量分数随起始投料比 的变化关系如图所示。
①图中曲线c表示的物质为 ,表示 的曲线为_______(填“a”或“b”),判断依据是_______。
②当 时,平衡时体系压强为P,计算反应Ⅰ的平衡常数 _______(写出计算过程,结果保留
2位有效数字;对于 , , )。
【答案】(1)+178
(2)AC
(3) C 积碳在其表面快速沉积使其活性降低
(4) a 比值增大,乙烷转化率增大,物质的量分数变化比CO和C H 要大 0.077P
2 4【详解】(1)将反应Ⅰ加上反应Ⅱ得到反应 的
;故答案为:+178。
(2)A.升高温度,活化分子数目增多,活化分子百分数增多,碰撞几率增大,因此正、逆反应速率同时
增大,故A正确;
B. 和 的物质的量不再改变时,反应达到平衡状态,不能是物质的量相等,故B错误;
C.增加起始投料时 的体积分数,单位体积的活化分子数增加,碰撞几率增大,反应速率加快,故C
正确;D.增加起始投料时 的体积分数,可以理解为再另外一个容器中加入后再加压,由于反应是体
积增大的反应,因此加压后平衡逆向移动, 平衡转化率减小,故D错误;
综上所述,答案为:AC。
(3)①在一定条件下, 催化乙烷脱氢转化为乙烯的反应历程如图所示,该历程的各步反应中,
生成下列物质速率最慢的是活化能最大的即第二步(TS2);故答案为:C。
②用 基催化剂研究 催化脱氢,该催化剂对 键和 键的断裂均有高活性,易形成碳单质。
一定温度下, 基催化剂在短时间内会失活,说明碳单质沉积在Co上,Co没有与乙烷接触从而使其活性
失活;故答案为:积碳在其表面快速沉积使其活性降低;故答案为:积碳在其表面快速沉积使其活性降低。
(4)①图中曲线c表示的物质为 , 比值增大,致使反应Ⅱ正向移动,乙烯浓度降低,致使反
应Ⅰ也正向移动,乙烷的转化率增大,因此乙烷的改变量比乙烯变化量大,因此表示 的曲线为a,判
断依据是 比值增大,乙烷转化率增大,物质的量分数变化比CO和C H 要大;故答案为:a;
2 4
比值增大,乙烷转化率增大,物质的量分数变化比CO和C H 要大。
2 4
②当 时,平衡时体系压强为P,建立三段式 ,
,则反应Ⅰ的平衡常数
;故答案为:0.077P。
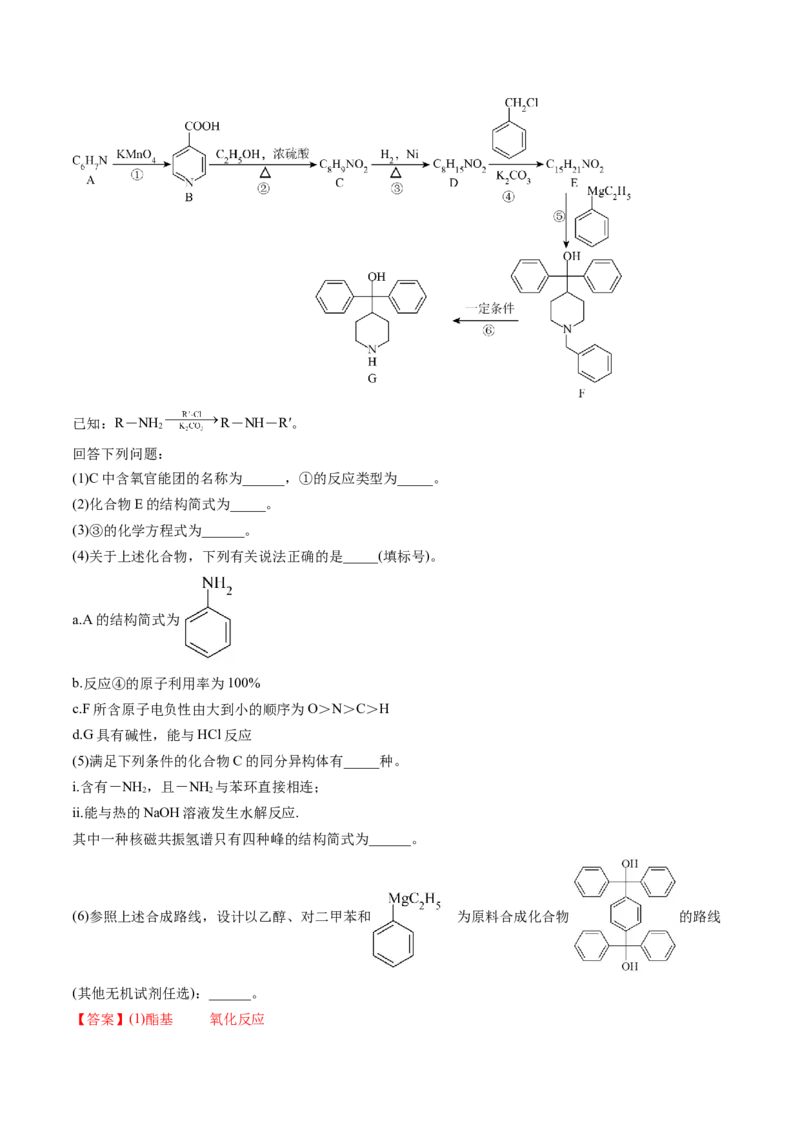
20.(14分)化合物G是某药物中间体,其一种合成路线如图。已知:R-NH R-NH-R′。
2
回答下列问题:
(1)C中含氧官能团的名称为______,①的反应类型为_____。
(2)化合物E的结构简式为_____。
(3)③的化学方程式为______。
(4)关于上述化合物,下列有关说法正确的是_____(填标号)。
a.A的结构简式为
b.反应④的原子利用率为100%
c.F所含原子电负性由大到小的顺序为O>N>C>H
d.G具有碱性,能与HCl反应
(5)满足下列条件的化合物C的同分异构体有_____种。
i.含有-NH ,且-NH 与苯环直接相连;
2 2
ii.能与热的NaOH溶液发生水解反应.
其中一种核磁共振氢谱只有四种峰的结构简式为______。
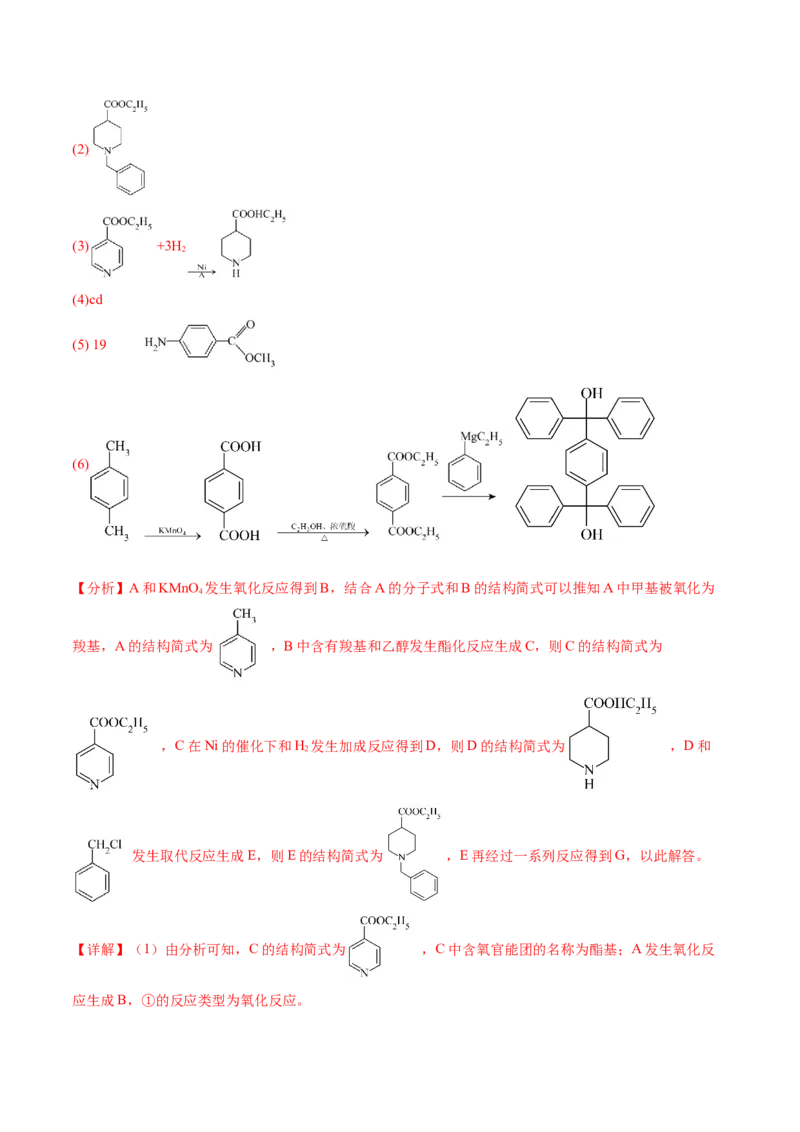
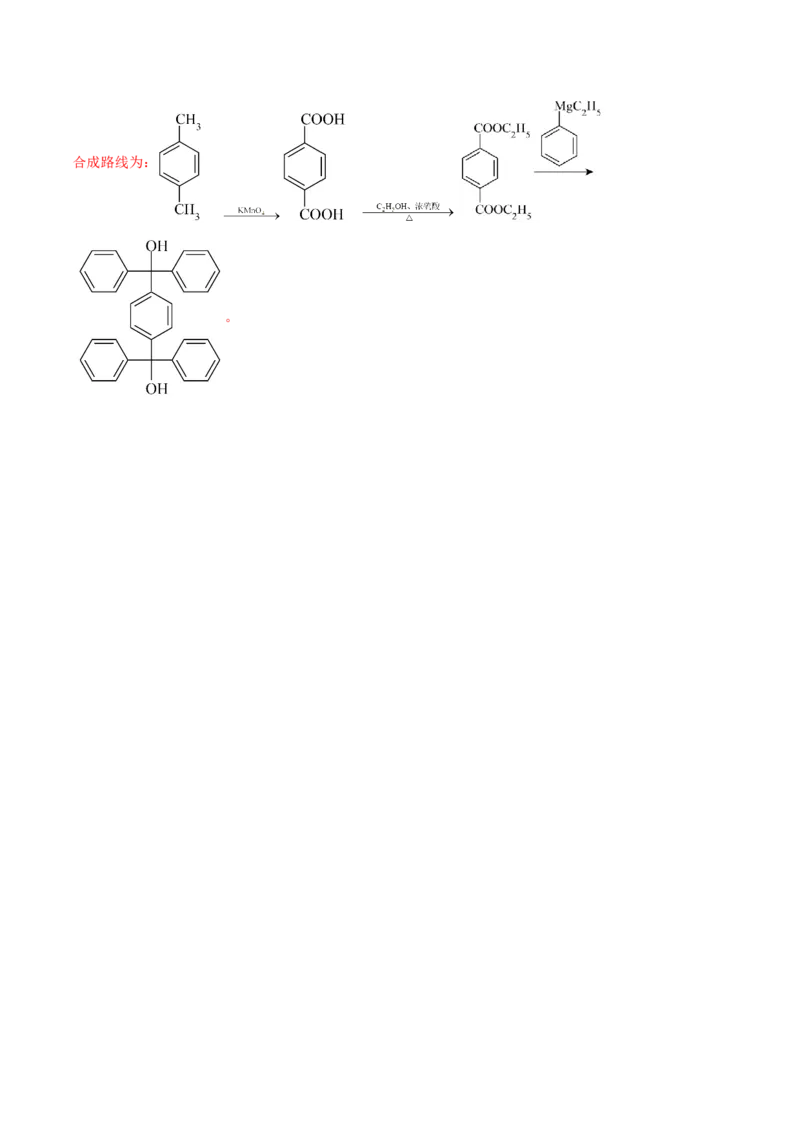
(6)参照上述合成路线,设计以乙醇、对二甲苯和 为原料合成化合物 的路线
(其他无机试剂任选):______。
【答案】(1)酯基 氧化反应(2)
(3) +3H
2
(4)cd
(5) 19
(6)
【分析】A和KMnO 发生氧化反应得到B,结合A的分子式和B的结构简式可以推知A中甲基被氧化为
4
羧基,A的结构简式为 ,B中含有羧基和乙醇发生酯化反应生成C,则C的结构简式为
,C在Ni的催化下和H 发生加成反应得到D,则D的结构简式为 ,D和
2
发生取代反应生成E,则E的结构简式为 ,E再经过一系列反应得到G,以此解答。
【详解】(1)由分析可知,C的结构简式为 ,C中含氧官能团的名称为酯基;A发生氧化反
应生成B,①的反应类型为氧化反应。(2)由分析可知,化合物E的结构简式为 。
(3)C发生加成反应得到D,③的化学方程式为 +3H 。
2
(4)a.由分析可知,A的结构简式为 ,故a错误;
b.D发生取代反应生成E,该过程中还有小分子HCl生成,反应④的原子利用率小于100%,故b错误;
c.F中含有C、H、O、N,电负性由大到小的顺序为O>N>C>H,故c正确;
d.G中含有亚氨基,具有碱性,能与HCl反应,故d正确;
故选cd。
(5)化合物C的同分异构体满足i.含有-NH ,且-NH 与苯环直接相连;ii.能与热的NaOH溶液发生水
2 2
解反应,说明其中含有酯基;若苯环上有两个取代基可能为:-NH 、-COOCH 或-NH 、-OOCCH 或-
2 3 2 3
NH 、-CHOOCH,每一种情况都有邻、间、对三种位置关系,共有9种,若苯环上有三个取代基为:-
2 2
NH 、-CH、-OOCH,共有10种位置关系,则满足条件的同分异构体共有10种,其中一种核磁共振氢谱
2 3 3
只有四种峰的结构简式为 。
(6)由E生成F的反应原理可知, 可由 和 反应得到,
可由 和乙醇发生酯化反应得到, 可由 和KMnO 反应得到,
4合成路线为:
。