文档内容
哈师大附中 12021 级高二上学期开学考试
化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mn 55 Cu 64 Zn 65
一、选择题(本题包括 20小题,每小题2分,共40分;每小题只有一个选项符合题
意。)
1、下列物品的俗名、有效成分和用途都正确的是
A.漂白粉,有效成分 ,做消毒剂
B.小苏打, ,做发酵粉
C.碱石灰, ,做干燥剂
D.铝热剂, 和Fe,冶炼金属
2、下列离子方程式书写正确的是
A.向 溶液中滴加少量新制氯水:
B.向 溶液中加入少量钠:
C.向NaOH溶液中加入足量的铝粉:
D. 溶于稀硫酸中:
3、下列物质各3g氧气中完全燃烧,150℃时将产物通过足量的 固体后固体增重大
于3g的是
A.HCOOH B. C. D.
4、下述对焰色反应实验操作注意事项的说明,正确的是
①钾的火焰颜色要透过蓝色钴玻璃观察
②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质
③每次实验后,要将铂丝用盐酸洗净
④实验时最好选择本身颜色较浅的火焰
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确 C.仅有⑤不正确 D.全正确
5、下列离子方程式中书写正确的是
A.水玻璃中通入过量的二氧化碳:
B.二氧化硅放入澄清石灰水中:
C.二氧化硅与氢氟酸反应:
D.单质硅溶于烧碱溶液中:
6、64g铜与 的浓硝酸1L充分反应,铜完全溶解,生成含 、NO的混合气体
33.6L(标况下)。若反应前后硝酸溶液的体积没有变化,下列说法错误的是
A.起氧化作用的硝酸有1.5mol
B.不起氧化作用但参与反应的硝酸有2mol
C.反应后溶液中 的浓度为5
D.混合气体中NO 与NO的体积比为5:1
27、已知 与足量的 硫酸溶液混合微热,产生下列现象:①有红色固
体生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
A. 完全反应转移0.5mol电子
B. 中硫元素被氧化
C.反应中硫酸作氧化剂
D.刺激性气味的气体是氨气
8、含有 的溶液中,通入 。下列各项为通入Cl 过程中,溶液内发生反
2
应的离子方程式,其中不正确的是
A. ,
B. ,
C. ,
D. ,
9、下列关于硅酸盐工业的叙述正确的是
A.普通玻璃的主要成分可以表示为 ,说明玻璃为纯净物
B.陶瓷、玻璃、水泥都属于硅酸盐产品
C.制玻璃、水泥时都用到了石灰石和黏土
D.制玻璃的过程中发生了反应: ,说明酸性:
H
10、下列有关元素周期表的说法正确的是
A.第ⅣA族元素在第14列
B.元素周期表中共有7个周期、16列、16个族
C.第ⅠA族所含元素种类最多
D.过渡元素就是副族元素,不包含Ⅷ族元素
11、下列关于离子化合物的判断正确的是
A.盐酸中含有H+和Cl-,故HCl为离子化合物
B.含有离子键的化合物一定是离子化合物
C.在化合物CaCl 中,两个Cl-之间存在离子键
2
D.仅由非金属元素组成的化合物一定不是离子化合物
12、下列各分子中,所有原子最外层都满足8电子稳定结构的是
A.HClO B.BF C.PCl D.SF
3 3 6
13、下列比较不正确的是
A.酸性: B.碱性:
C.稳定性: D.离子半径:
14、碱性锌锰电池以KOH糊作电解液,电池总反应式为
,下列说法错误的是
A.电池工作时,锌失去电子,发生还原反应
B.电池正极的电极反应式为C.电池工作时,电解液中 向负极移动
D.外电路中每通过0.4mol电子,理论上负极质量增加6.8g
15、下列说法正确的是
A. 完全燃烧生成液态水,放热285.8kJ,则表示氢气燃烧热的热化学方程式为
B .
C. ,比较白磷、红磷的燃烧热:∆H
(白磷)<∆H(红磷)
D. ,理论上可利用该反应设计成原电池
16、某有机物的结构简式为 ,下列关于该有机物的叙述错
误的是
A.能与乙酸在一定条件下发生酯化反应
B.在一定条件下能发生还原反应、氧化反应
C.不能使溴的四氯化碳溶液褪色
D.含有两种官能团
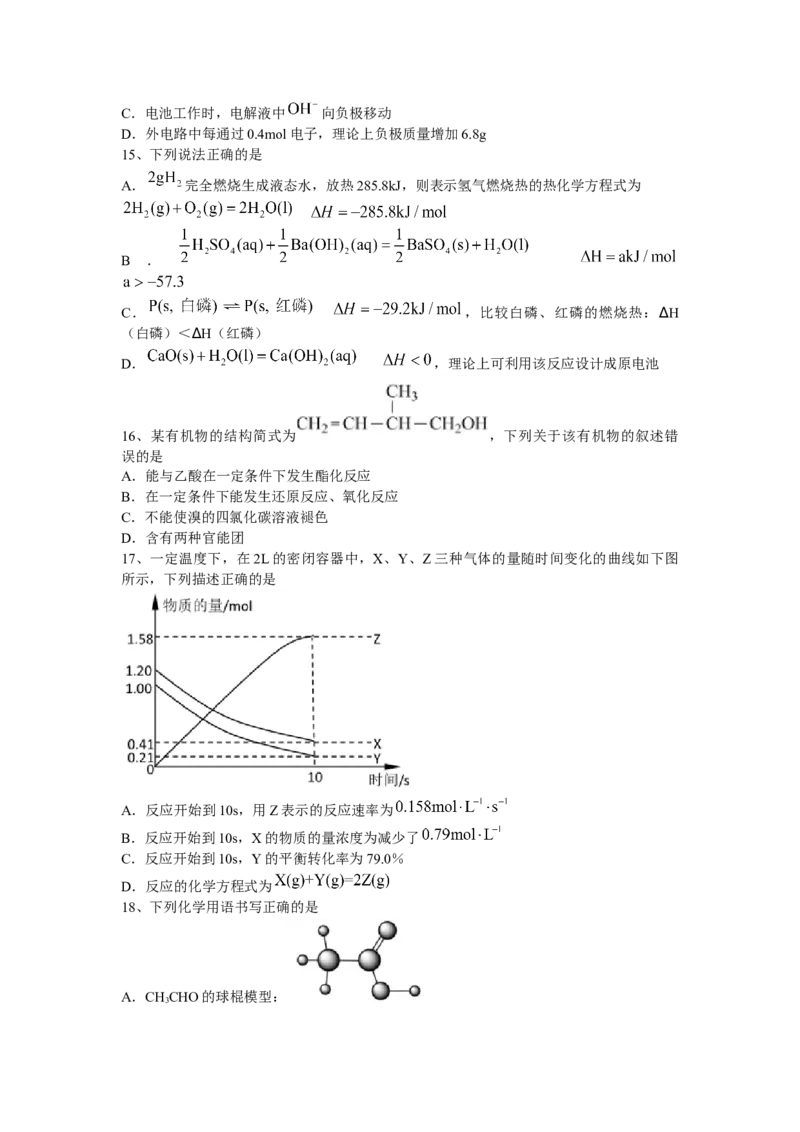
17、一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如下图
所示,下列描述正确的是
A.反应开始到10s,用Z表示的反应速率为
B.反应开始到10s,X的物质的量浓度为减少了
C.反应开始到10s,Y的平衡转化率为79.0%
D.反应的化学方程式为
18、下列化学用语书写正确的是
A.CHCHO的球棍模型:
3B. 按照系统命名法的名称:2-乙基丙烷
C.过氧化氢的空间填充模型:
D.-NH 的电子式:
2
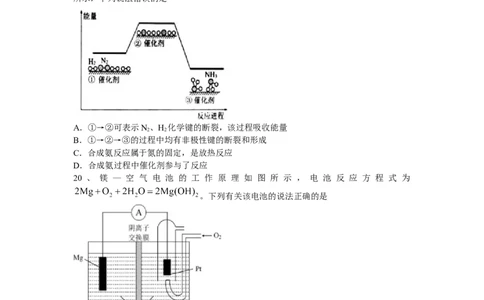
19、工业上合成氨 ,在催化剂表面的微观历程及能量变化如图
所示,下列说法错误的是
A.①→②可表示N、H 化学键的断裂,该过程吸收能量
2 2
B.①→②→③的过程中均有非极性键的断裂和形成
C.合成氨反应属于氮的固定,是放热反应
D.合成氨过程中催化剂参与了反应
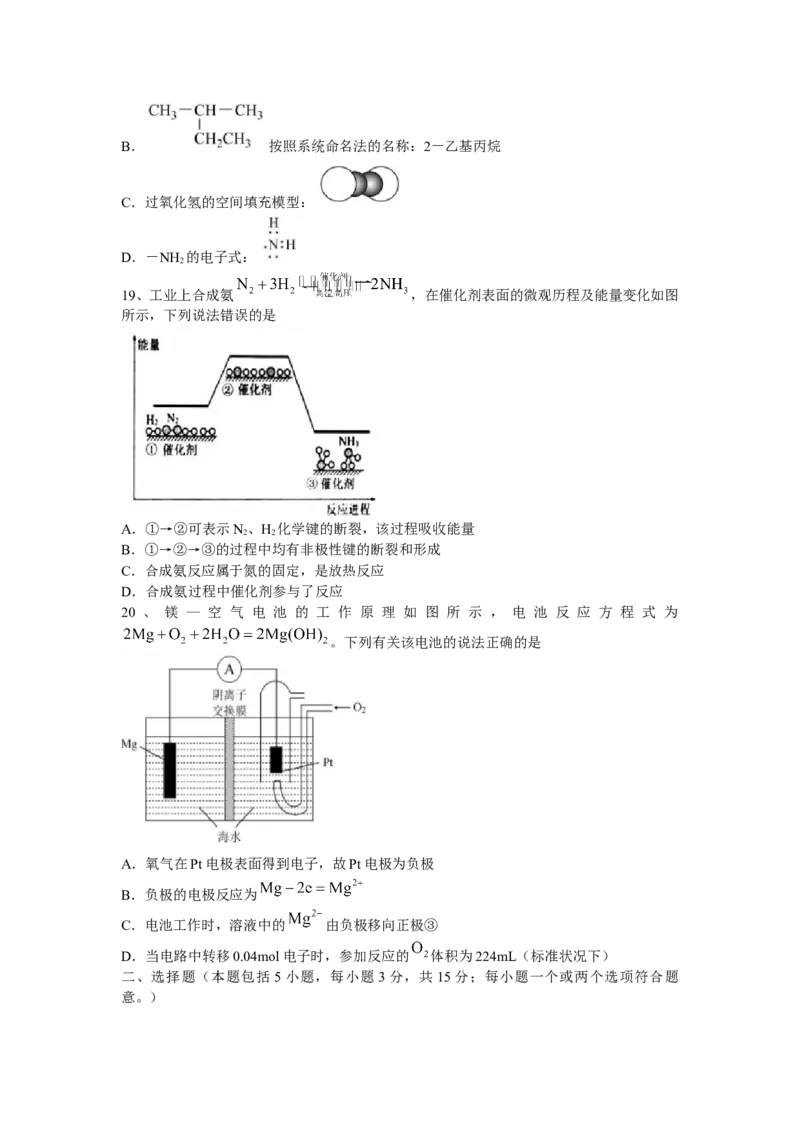
20 、 镁 — 空 气 电 池 的 工 作 原 理 如 图 所 示 , 电 池 反 应 方 程 式 为
。下列有关该电池的说法正确的是
A.氧气在Pt电极表面得到电子,故Pt电极为负极
B.负极的电极反应为
C.电池工作时,溶液中的 由负极移向正极③
D.当电路中转移0.04mol电子时,参加反应的 体积为224mL(标准状况下)
二、选择题(本题包括 5小题,每小题3分,共15分;每小题一个或两个选项符合题
意。)21、已知某物质X能发生如下转化: ,在上述转化关系中
关于物质及其反应的叙述错误的是
A.若X为N 或NH ,则A为硝酸
2 3
B.若X为S或HS,则A一定为硫酸
2
C.若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
22 、 一 定 条 件 下 硝 酸 铵 受 热 分 解 的 化 学 方 程 式 ( 未 配 平 ) 为
,下列说法正确的是
A.配平后HO的系数为9
2
B.氧化产物和还原产物的物质的量之比为1∶2
C.N 只是还原产物
2
D.被氧化与被还原的氮原子数之比为5∶3
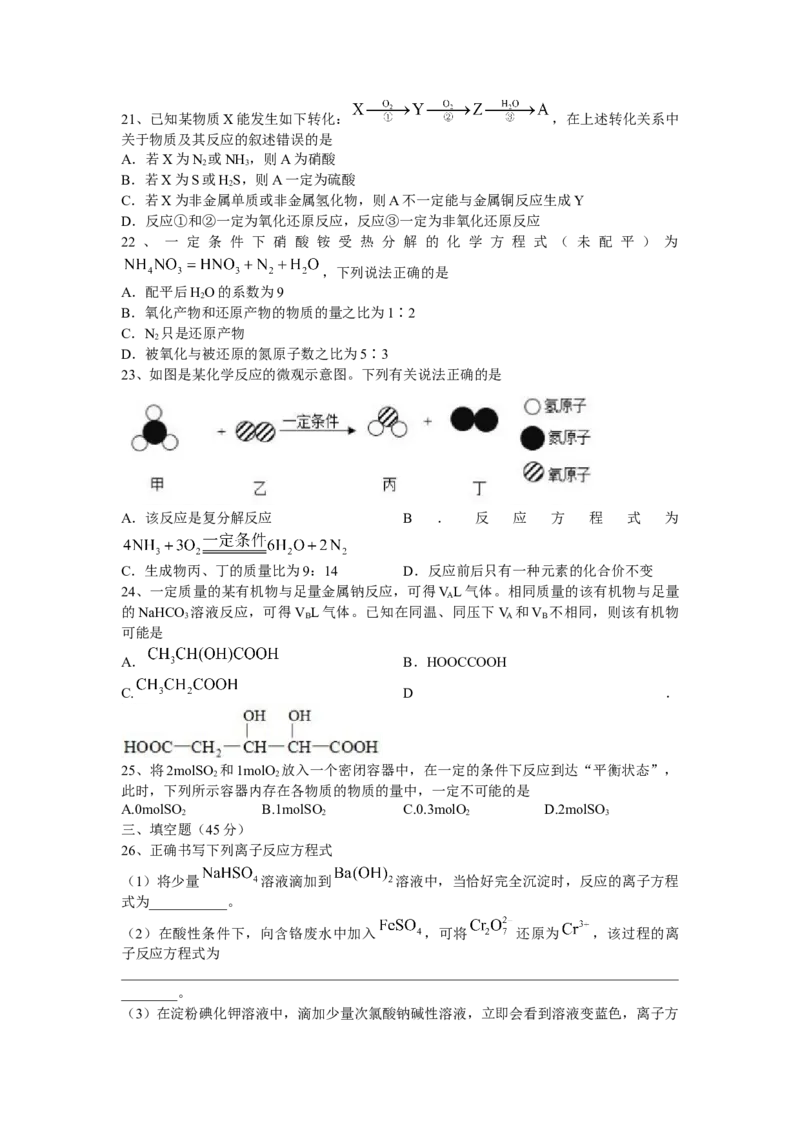
23、如图是某化学反应的微观示意图。下列有关说法正确的是
A.该反应是复分解反应 B . 反 应 方 程 式 为
C.生成物丙、丁的质量比为9:14 D.反应前后只有一种元素的化合价不变
24、一定质量的某有机物与足量金属钠反应,可得VL气体。相同质量的该有机物与足量
A
的NaHCO 溶液反应,可得V L气体。已知在同温、同压下V 和V 不相同,则该有机物
3 B A B
可能是
A. B.HOOCCOOH
C. D .
25、将2molSO 和1molO 放入一个密闭容器中,在一定的条件下反应到达“平衡状态”,
2 2
此时,下列所示容器内存在各物质的物质的量中,一定不可能的是
A.0molSO B.1molSO C.0.3molO D.2molSO
2 2 2 3
三、填空题(45分)
26、正确书写下列离子反应方程式
(1)将少量 溶液滴加到 溶液中,当恰好完全沉淀时,反应的离子方程
式为___________。
(2)在酸性条件下,向含铬废水中加入 ,可将 还原为 ,该过程的离
子反应方程式为
_______________________________________________________________________________
________。
(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为
_______________________________________________________________________________
________。
( 4 ) MnO 与 浓 盐 酸 制 备 氯 气 的 离 子 方 程 式 :
2
______________________________________________。
(5)已知酸性环境下, 可将 氧化成 ,自身被还原成 ,该过程的离
子反应方程式为
______________________________。
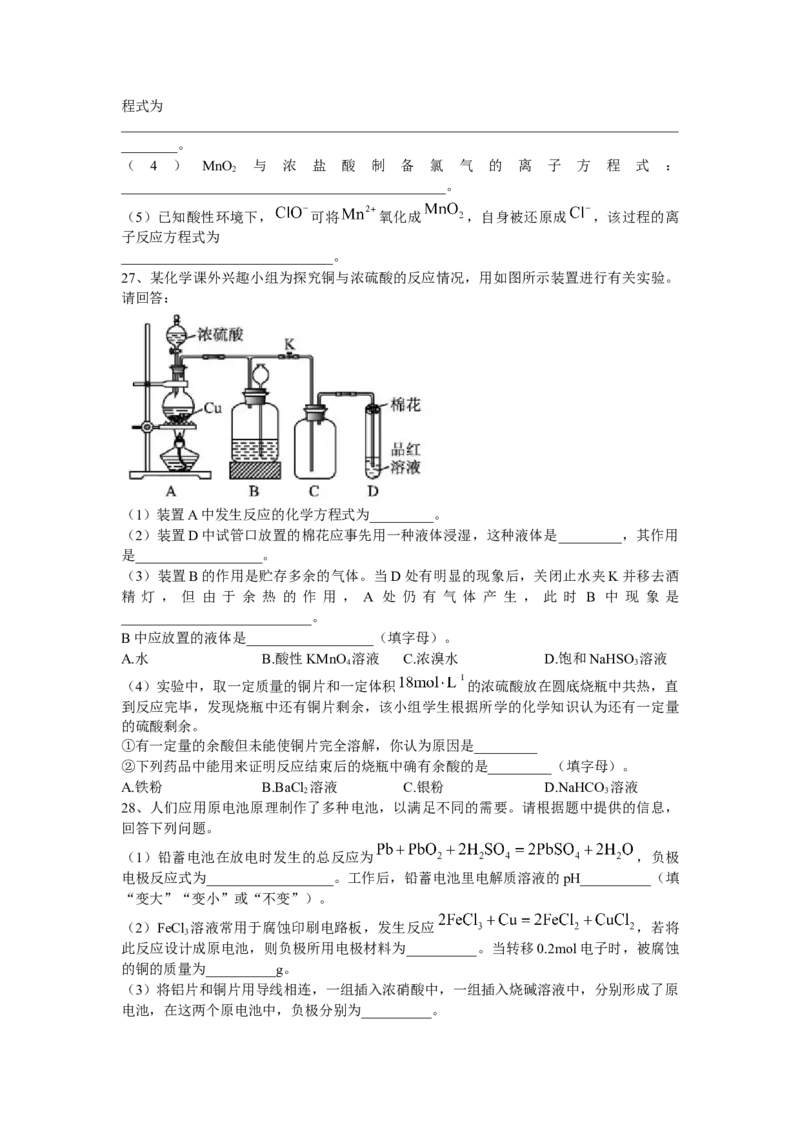
27、某化学课外兴趣小组为探究铜与浓硫酸的反应情况,用如图所示装置进行有关实验。
请回答:
(1)装置A中发生反应的化学方程式为_________。
(2)装置D中试管口放置的棉花应事先用一种液体浸湿,这种液体是_________,其作用
是__________________。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭止水夹K并移去酒
精 灯 , 但 由 于 余 热 的 作 用 , A 处 仍 有 气 体 产 生 , 此 时 B 中 现 象 是
___________________________。
B中应放置的液体是__________________(填字母)。
A.水 B.酸性KMnO 溶液 C.浓溴水 D.饱和NaHSO 溶液
4 3
(4)实验中,取一定质量的铜片和一定体积 的浓硫酸放在圆底烧瓶中共热,直
到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量
的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是_________
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是_________(填字母)。
A.铁粉 B.BaCl 溶液 C.银粉 D.NaHCO 溶液
2 3
28、人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,
回答下列问题。
(1)铅蓄电池在放电时发生的总反应为 ,负极
电极反应式为__________________。工作后,铅蓄电池里电解质溶液的pH__________(填
“变大”“变小”或“不变”)。
(2)FeCl 溶液常用于腐蚀印刷电路板,发生反应 ,若将
3
此反应设计成原电池,则负极所用电极材料为__________。当转移0.2mol电子时,被腐蚀
的铜的质量为__________g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原
电池,在这两个原电池中,负极分别为__________。A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置。
①如图是电解质溶液为稀硫酸的氢氧燃料电池原理示意图:
氢氧燃料电池的总反应方程式是______________________。
②将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则
通 入 甲 烷 气 体 的 一 极 是 原 电 池 的 __________ 极 , 该 极 的 电 极 反 应 式 是
______________________________________。
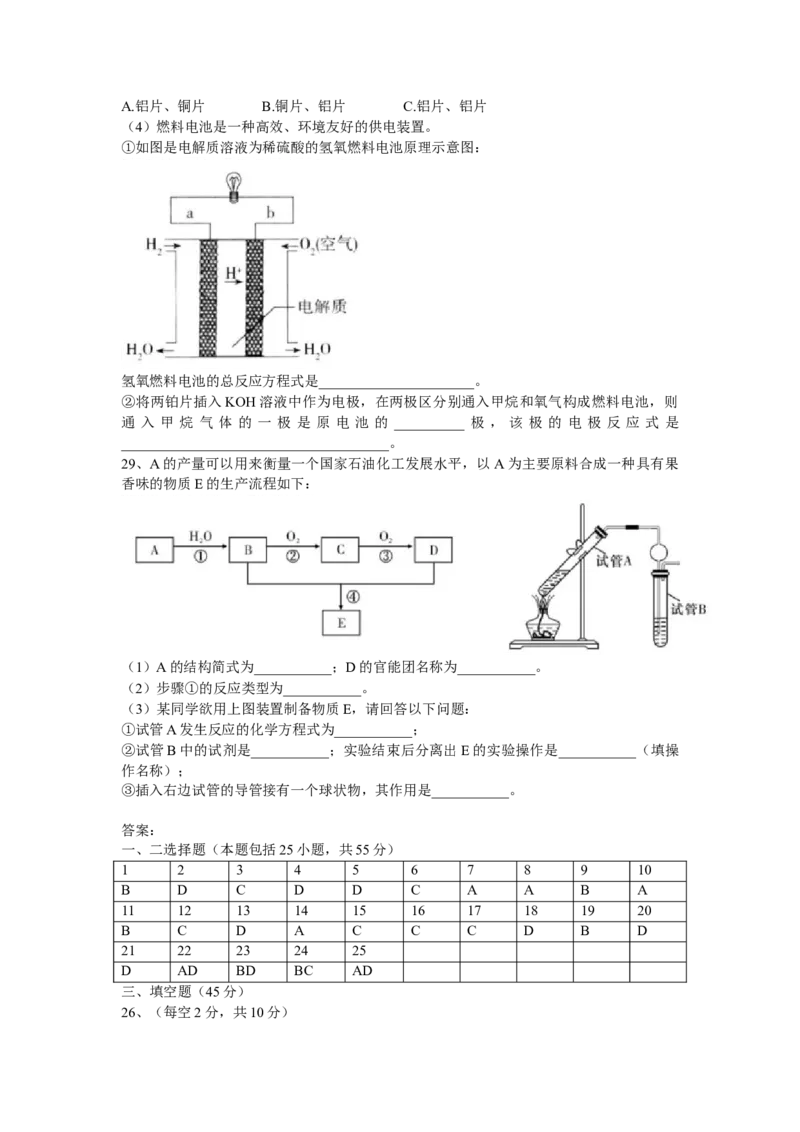
29、A的产量可以用来衡量一个国家石油化工发展水平,以 A为主要原料合成一种具有果
香味的物质E的生产流程如下:
(1)A的结构简式为___________;D的官能团名称为___________。
(2)步骤①的反应类型为___________。
(3)某同学欲用上图装置制备物质E,请回答以下问题:
①试管A发生反应的化学方程式为___________;
②试管B中的试剂是___________;实验结束后分离出E的实验操作是___________(填操
作名称);
③插入右边试管的导管接有一个球状物,其作用是___________。
答案:
一、二选择题(本题包括25小题,共55分)
1 2 3 4 5 6 7 8 9 10
B D C D D C A A B A
11 12 13 14 15 16 17 18 19 20
B C D A C C C D B D
21 22 23 24 25
D AD BD BC AD
三、填空题(45分)
26、(每空2分,共10分)(1)
(2)
(3)
(4)
(5)
27、(每空2分,共14分)
(1)
(2)NaOH溶液(其他合理答案均可)吸收多余的二氧化硫,防止污染空气
(3)瓶中液面下降,而长颈漏斗中液面上升 D
(4)①反应过程中硫酸被消耗,浓硫酸逐渐变稀,而铜不和稀硫酸反应
②AD
28、(共13分)
(1) (2分);变大(1分)
(2)Cu(1分);6.4(2分)
(3)B(2分)
( 4 ) ① ( 2 分 ) ② 负 ( 1 分 )
(2分)
29、(共8分)
(1)CH=CH (1分) 羧基(1分)
2 2
(2)加成反应(1分)
(3)① (2分)
②.饱和碳酸钠溶液(1分) 分液(1分) ③防倒吸(1分)