文档内容
主观题突破二
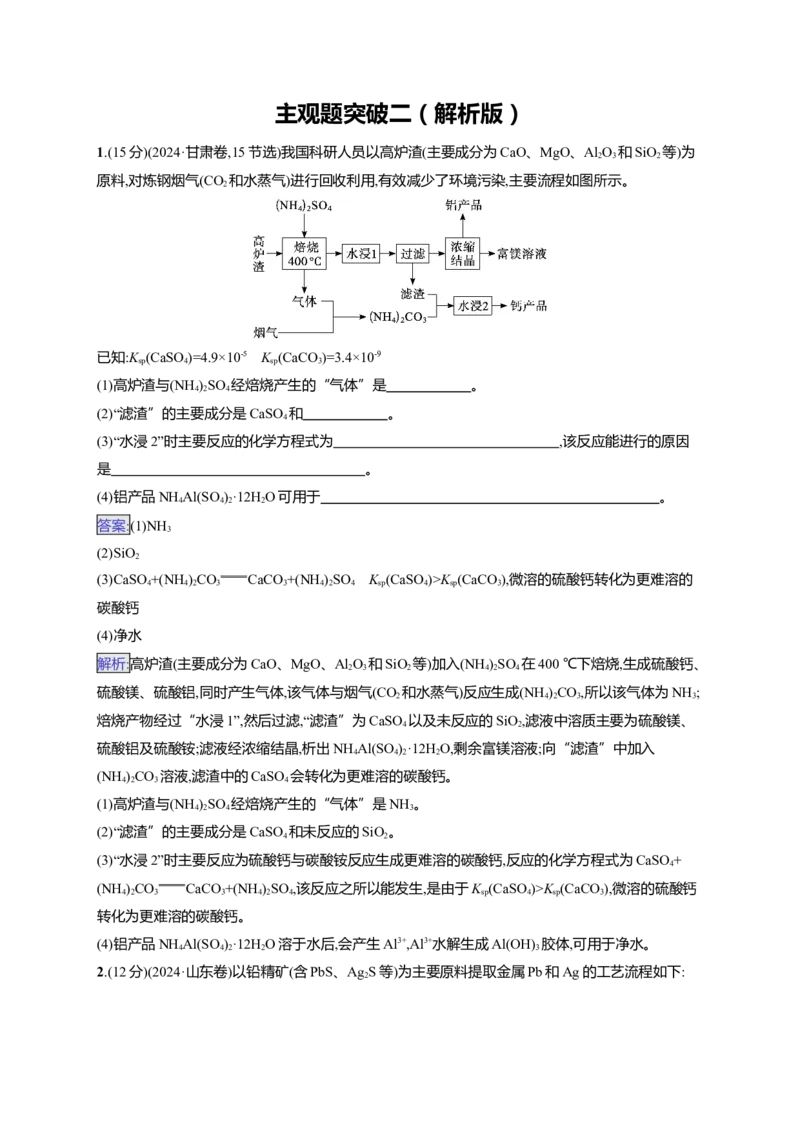
1.(15分)(2024·甘肃卷,15节选)我国科研人员以高炉渣(主要成分为CaO、MgO、Al O 和SiO 等)为
2 3 2
原料,对炼钢烟气(CO 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示。
2
已知:K (CaSO)=4.9×10-5 K (CaCO)=3.4×10-9
sp 4 sp 3
(1)高炉渣与(NH )SO 经焙烧产生的“气体”是 。
4 2 4
(2)“滤渣”的主要成分是CaSO 和 。
4
(3)“水浸2”时主要反应的化学方程式为 ,该反应能进行的原因
是 。
(4)铝产品NH Al(SO )·12H O可用于 。
4 4 2 2
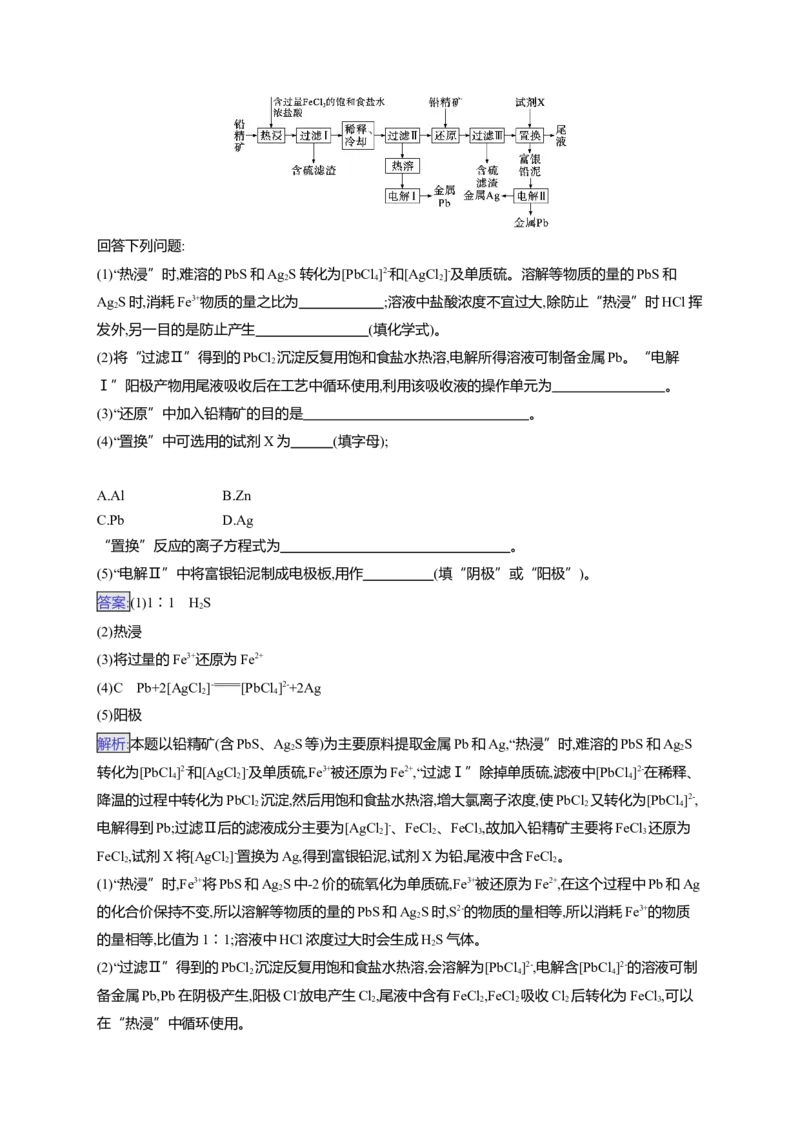
2.(12分)(2024·山东卷)以铅精矿(含PbS、Ag S等)为主要原料提取金属Pb和Ag的工艺流程如下:
2
回答下列问题:
(1)“热浸”时,难溶的PbS和Ag S转化为[PbCl ]2-和[AgCl ]-及单质硫。溶解等物质的量的PbS和
2 4 2
Ag S时,消耗Fe3+物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时HCl挥
2
发外,另一目的是防止产生 (填化学式)。
(2)将“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属Pb。“电解
2
Ⅰ”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为 。
(3)“还原”中加入铅精矿的目的是 。
(4)“置换”中可选用的试剂X为 (填字母);
A.Al B.Zn
C.Pb D.Ag
“置换”反应的离子方程式为 。
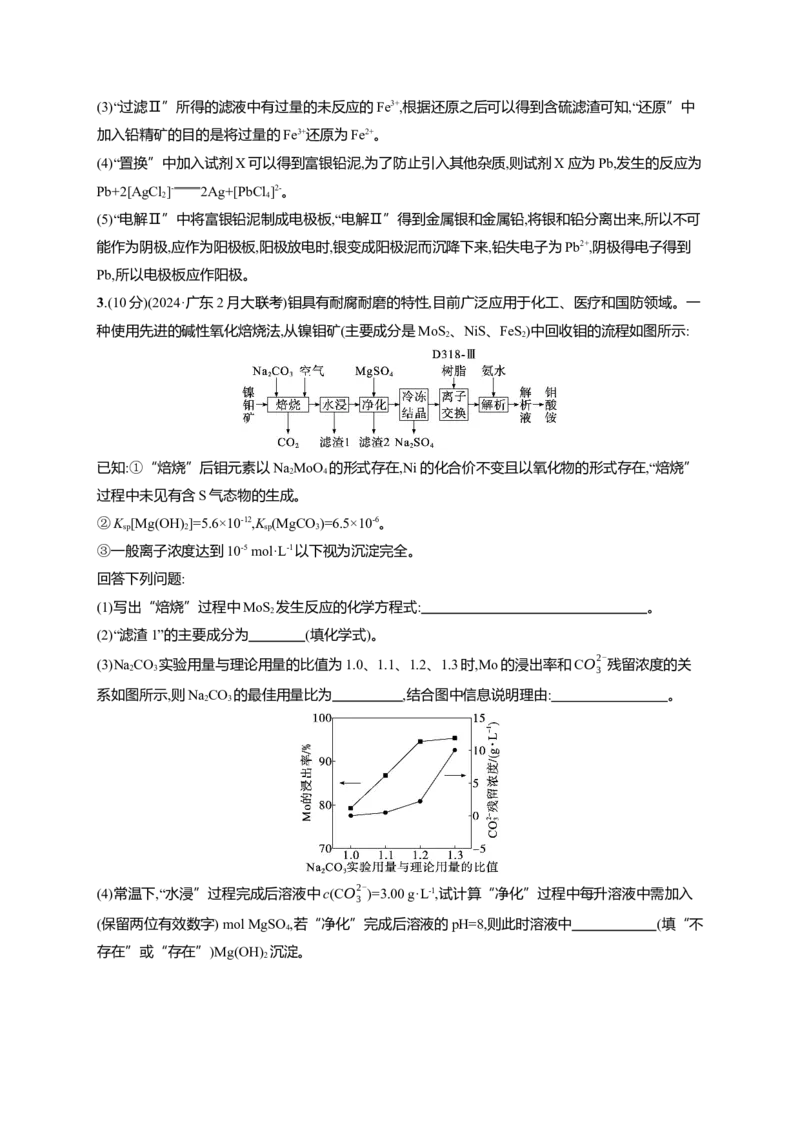
(5)“电解Ⅱ”中将富银铅泥制成电极板,用作 (填“阴极”或“阳极”)。3.(10分)(2024·广东2月大联考)钼具有耐腐耐磨的特性,目前广泛应用于化工、医疗和国防领域。一
种使用先进的碱性氧化焙烧法,从镍钼矿(主要成分是MoS 、NiS、FeS)中回收钼的流程如图所示:
2 2
已知:①“焙烧”后钼元素以NaMoO 的形式存在,Ni的化合价不变且以氧化物的形式存在,“焙烧”
2 4
过程中未见有含S气态物的生成。
②K [Mg(OH) ]=5.6×10-12,K (MgCO )=6.5×10-6。
sp 2 sp 3
③一般离子浓度达到10-5 mol·L-1以下视为沉淀完全。
回答下列问题:
(1)写出“焙烧”过程中MoS 发生反应的化学方程式: 。
2
(2)“滤渣1”的主要成分为 (填化学式)。
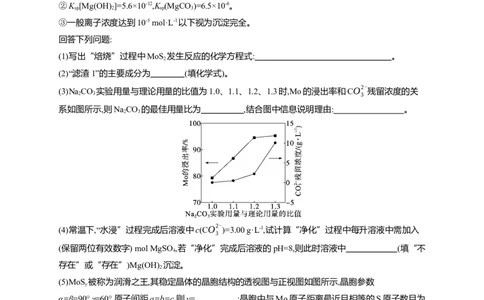
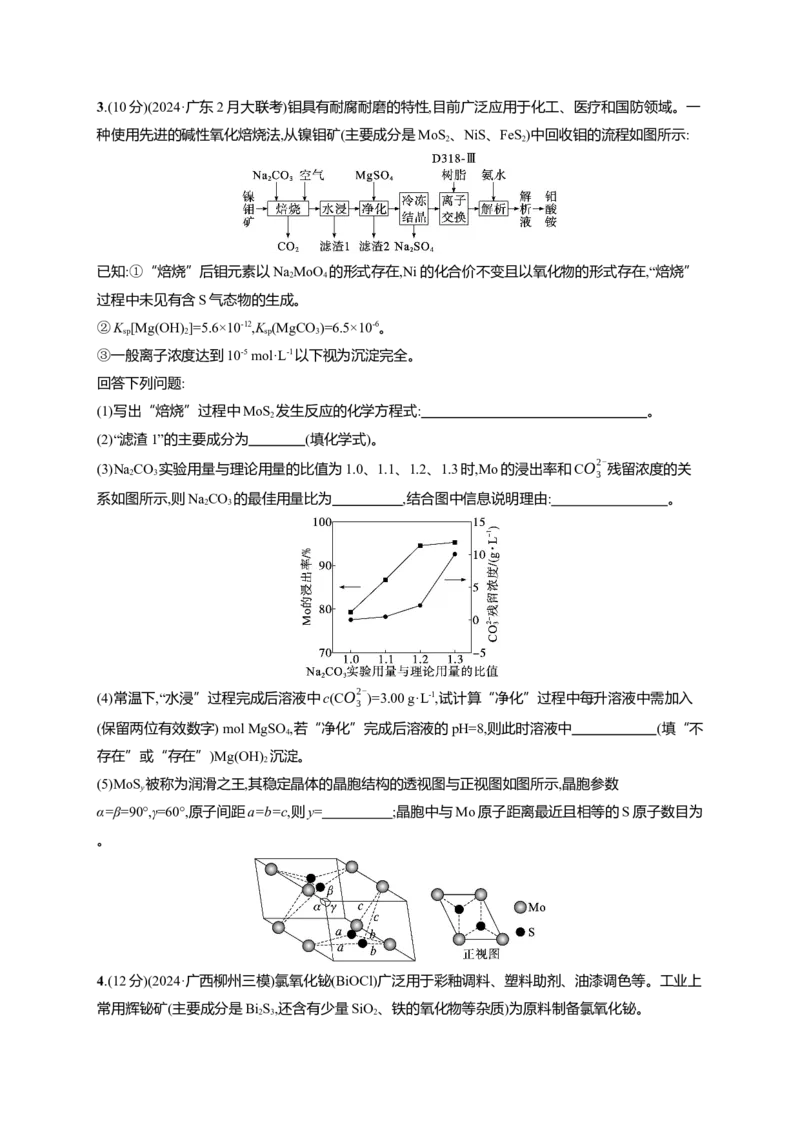
(3)Na CO
实验用量与理论用量的比值为1.0、1.1、1.2、1.3时,Mo的浸出率和CO2-
残留浓度的关
2 3 3
系如图所示,则NaCO 的最佳用量比为 ,结合图中信息说明理由: 。
2 3
(4)常温下,“水浸”过程完成后溶液中c(CO2-
)=3.00 g·L-1,试计算“净化”过程中每升溶液中需加入
3
(保留两位有效数字) mol MgSO ,若“净化”完成后溶液的pH=8,则此时溶液中 (填“不
4
存在”或“存在”)Mg(OH) 沉淀。
2
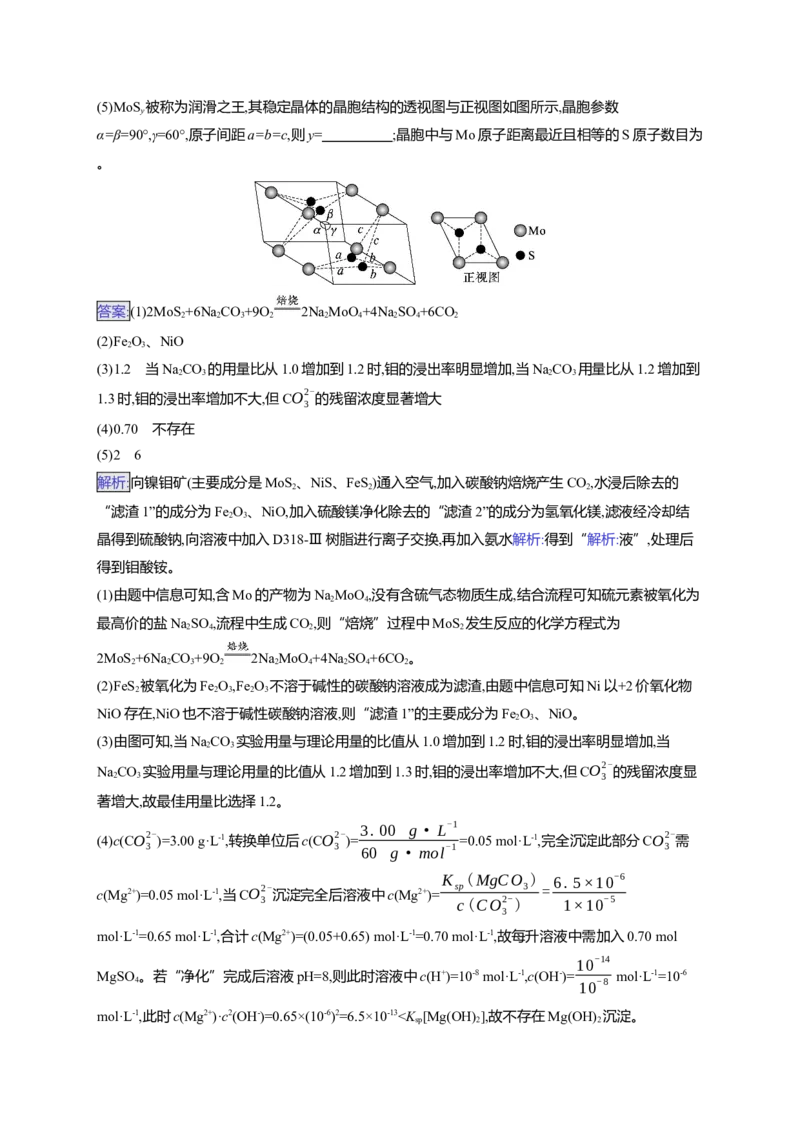
(5)MoS 被称为润滑之王,其稳定晶体的晶胞结构的透视图与正视图如图所示,晶胞参数
y
α=β=90°,γ=60°,原子间距a=b=c,则y= ;晶胞中与Mo原子距离最近且相等的S原子数目为
。
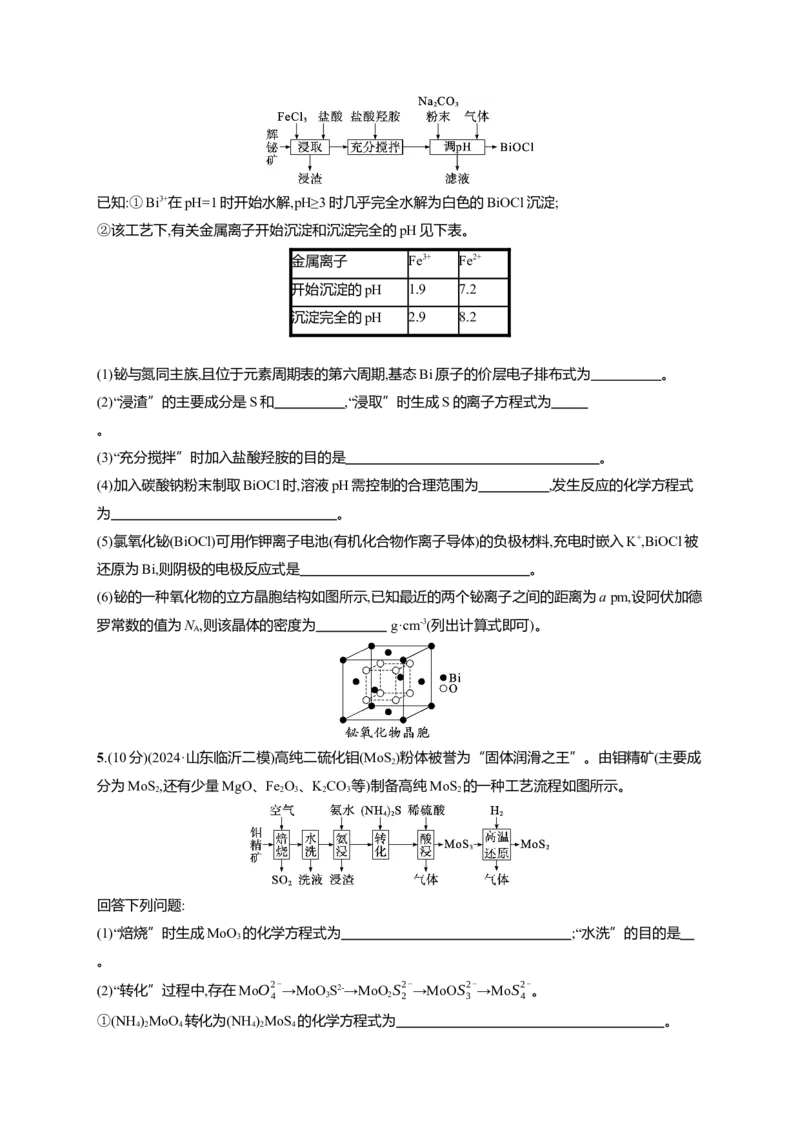
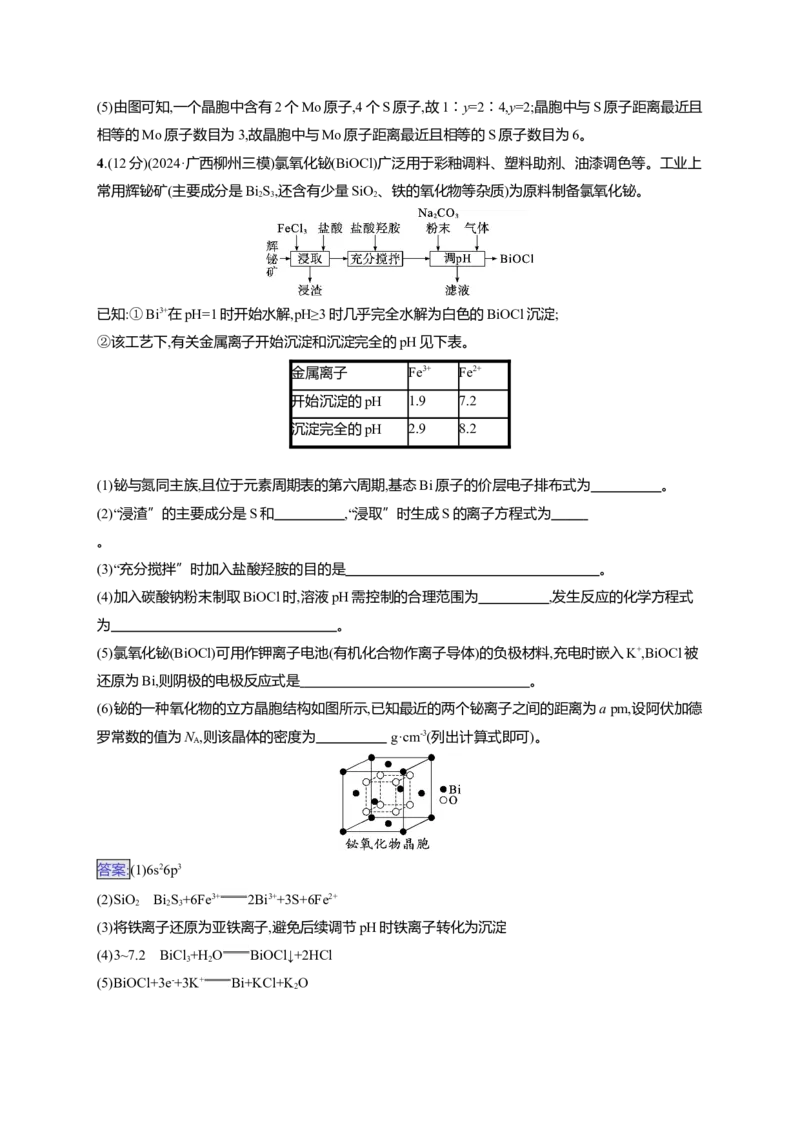
4.(12分)(2024·广西柳州三模)氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色等。工业上
常用辉铋矿(主要成分是BiS,还含有少量SiO、铁的氧化物等杂质)为原料制备氯氧化铋。
2 3 2已知:①Bi3+在pH=1时开始水解,pH≥3时几乎完全水解为白色的BiOCl沉淀;
②该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表。
金属离子 Fe3+ Fe2+
开始沉淀的pH 1.9 7.2
沉淀完全的pH 2.9 8.2
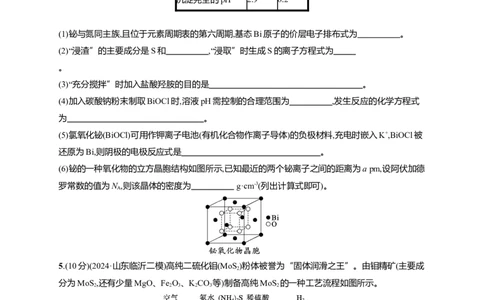
(1)铋与氮同主族,且位于元素周期表的第六周期,基态Bi原子的价层电子排布式为 。
(2)“浸渣”的主要成分是S和 ,“浸取”时生成S的离子方程式为
。
(3)“充分搅拌”时加入盐酸羟胺的目的是 。
(4)加入碳酸钠粉末制取BiOCl时,溶液pH需控制的合理范围为 ,发生反应的化学方程式
为 。
(5)氯氧化铋(BiOCl)可用作钾离子电池(有机化合物作离子导体)的负极材料,充电时嵌入K+,BiOCl被
还原为Bi,则阴极的电极反应式是 。
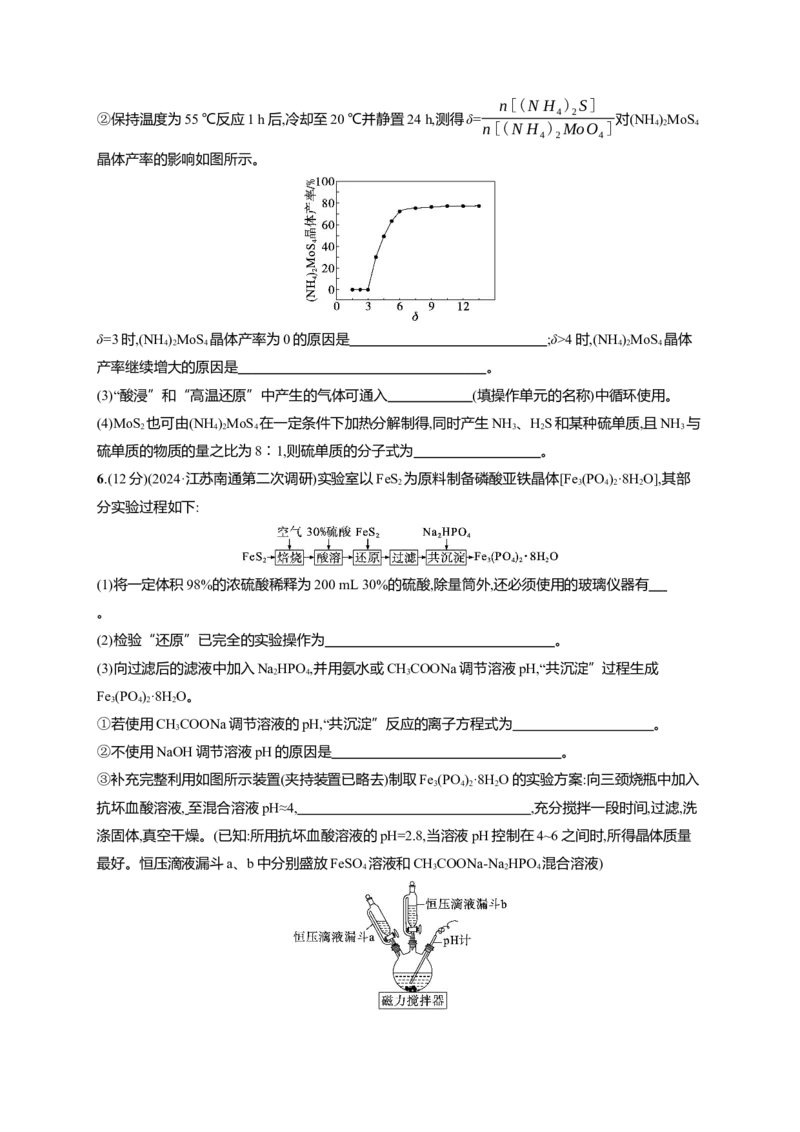
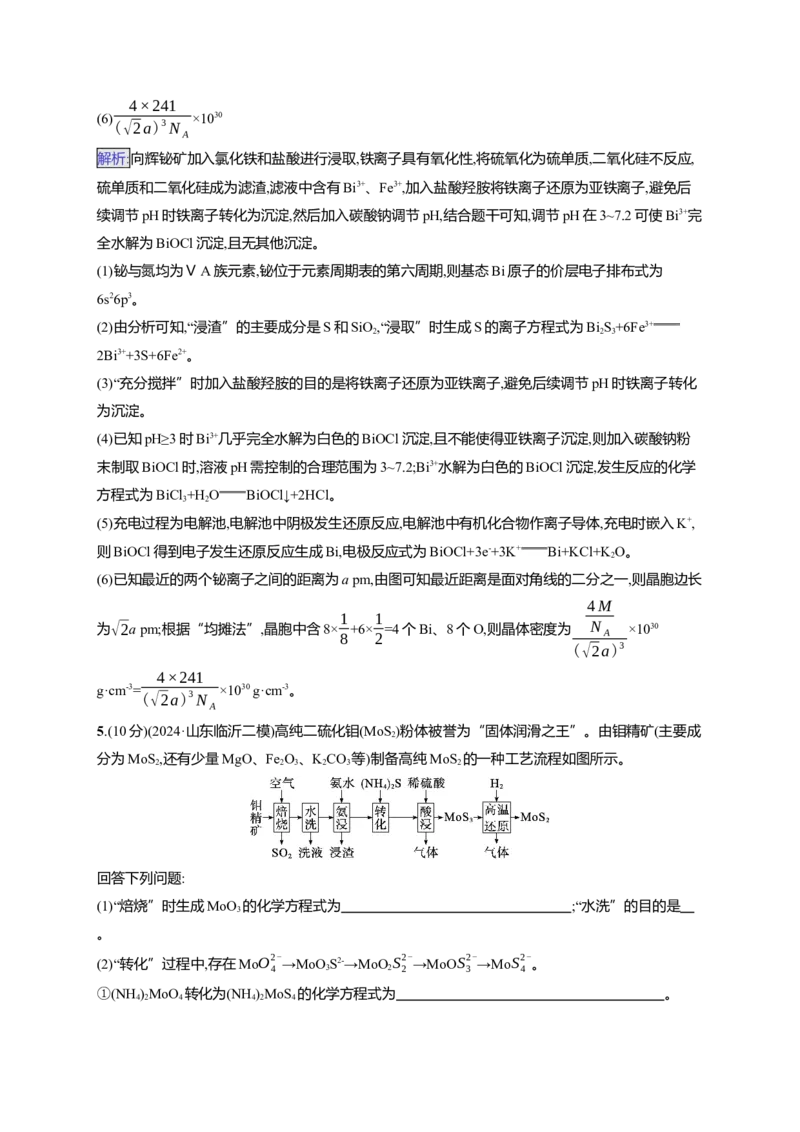
(6)铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为a pm,设阿伏加德
罗常数的值为N ,则该晶体的密度为 g·cm-3(列出计算式即可)。
A
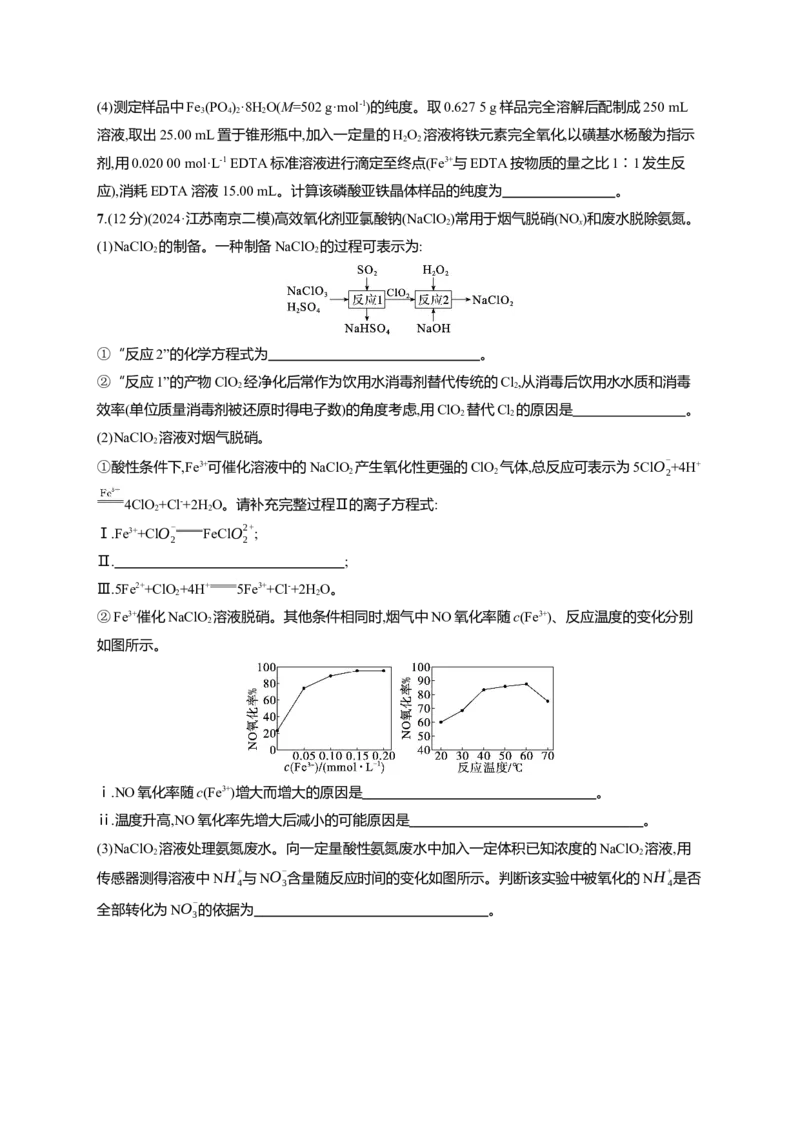
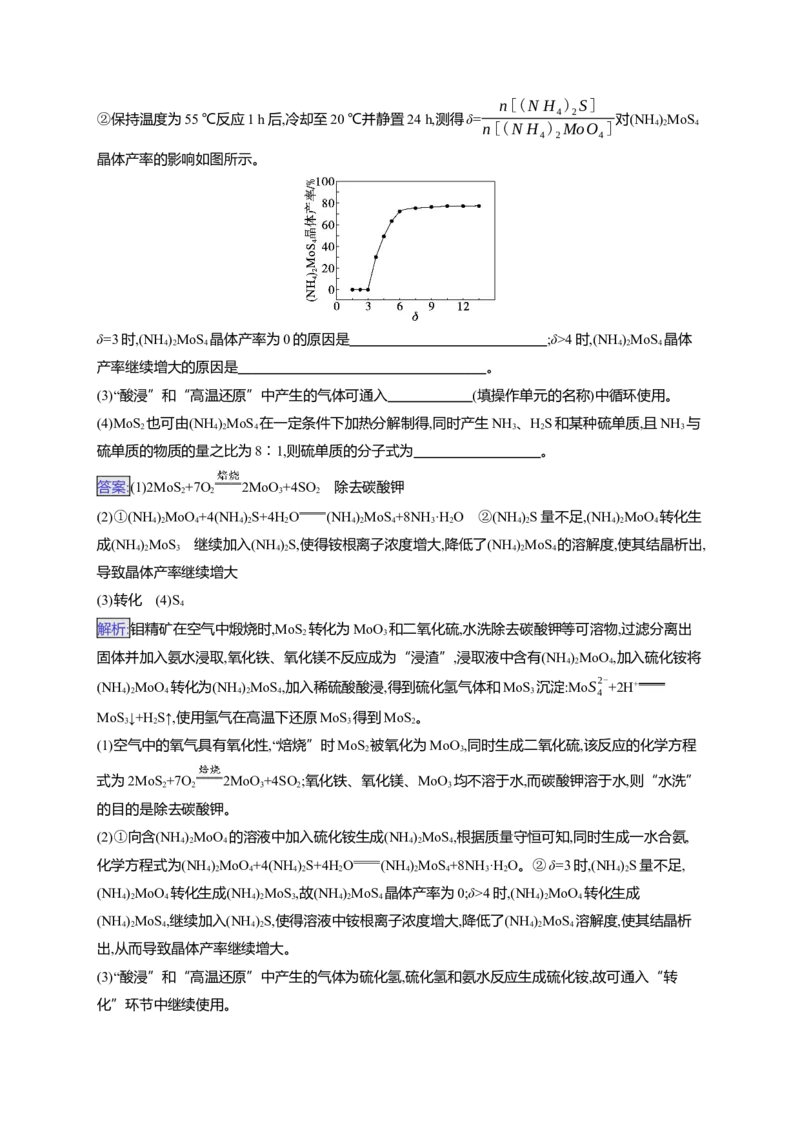
5.(10分)(2024·山东临沂二模)高纯二硫化钼(MoS )粉体被誉为“固体润滑之王”。由钼精矿(主要成
2
分为MoS ,还有少量MgO、Fe O、KCO 等)制备高纯MoS 的一种工艺流程如图所示。
2 2 3 2 3 2
回答下列问题:
(1)“焙烧”时生成MoO 的化学方程式为 ;“水洗”的目的是
3
。
(2)“转化”过程中,存在MoO2-
→MoO S2-→MoO
S2- →MoOS2- →MoS2-
。
4 3 2 2 3 4
①(NH )MoO 转化为(NH )MoS 的化学方程式为 。
4 2 4 4 2 4n[(N H ) S]
4 2
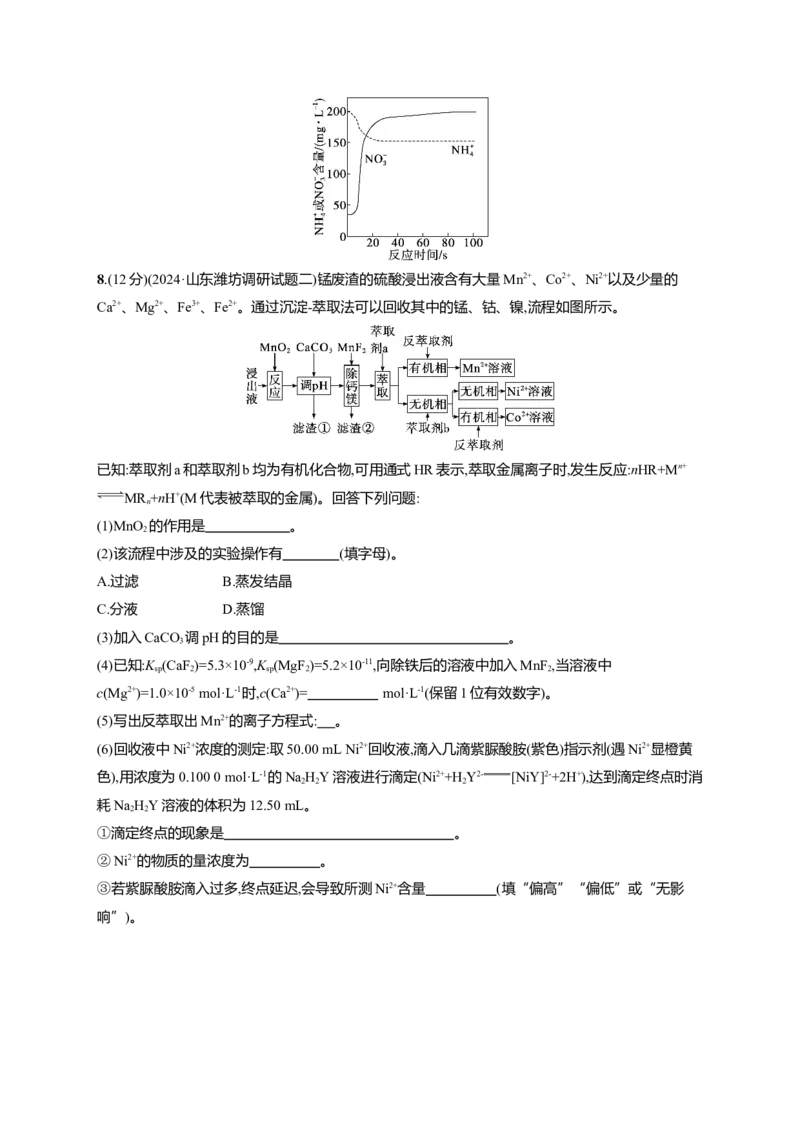
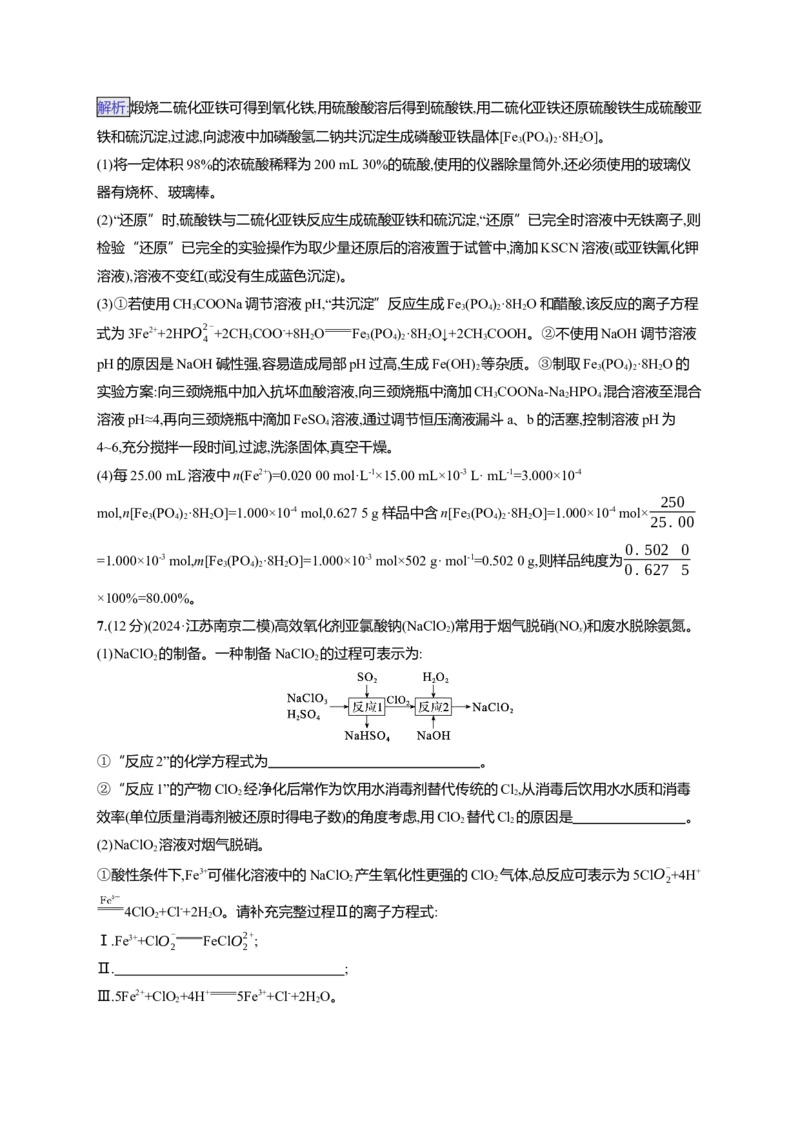
②保持温度为55 ℃反应1 h后,冷却至20 ℃并静置24 h,测得δ= 对(NH )MoS
n[(N H ) MoO ] 4 2 4
4 2 4
晶体产率的影响如图所示。
δ=3时,(NH)MoS 晶体产率为0的原因是 ;δ>4时,(NH)MoS 晶体
4 2 4 4 2 4
产率继续增大的原因是 。
(3)“酸浸”和“高温还原”中产生的气体可通入 (填操作单元的名称)中循环使用。
(4)MoS 也可由(NH )MoS 在一定条件下加热分解制得,同时产生NH 、HS和某种硫单质,且NH 与
2 4 2 4 3 2 3
硫单质的物质的量之比为8∶1,则硫单质的分子式为 。
6.(12分)(2024·江苏南通第二次调研)实验室以FeS 为原料制备磷酸亚铁晶体[Fe (PO )·8H O],其部
2 3 4 2 2
分实验过程如下:
(1)将一定体积98%的浓硫酸稀释为200 mL 30%的硫酸,除量筒外,还必须使用的玻璃仪器有
。
(2)检验“还原”已完全的实验操作为 。
(3)向过滤后的滤液中加入NaHPO ,并用氨水或CHCOONa调节溶液pH,“共沉淀”过程生成
2 4 3
Fe (PO )·8H O。
3 4 2 2
①若使用CHCOONa调节溶液的pH,“共沉淀”反应的离子方程式为 。
3
②不使用NaOH调节溶液pH的原因是 。
③补充完整利用如图所示装置(夹持装置已略去)制取Fe (PO )·8H O的实验方案:向三颈烧瓶中加入
3 4 2 2
抗坏血酸溶液, 至混合溶液pH≈4, ,充分搅拌一段时间,过滤,洗
涤固体,真空干燥。(已知:所用抗坏血酸溶液的pH=2.8,当溶液pH控制在4~6之间时,所得晶体质量
最好。恒压滴液漏斗a、b中分别盛放FeSO 溶液和CHCOONa-Na HPO 混合溶液)
4 3 2 4(4)测定样品中Fe (PO )·8H O(M=502 g·mol-1)的纯度。取0.627 5 g样品完全溶解后配制成250 mL
3 4 2 2
溶液,取出25.00 mL置于锥形瓶中,加入一定量的HO 溶液将铁元素完全氧化,以磺基水杨酸为指示
2 2
剂,用0.020 00 mol·L-1 EDTA标准溶液进行滴定至终点(Fe3+与EDTA按物质的量之比1∶1发生反
应),消耗EDTA溶液15.00 mL。计算该磷酸亚铁晶体样品的纯度为 。
7.(12分)(2024·江苏南京二模)高效氧化剂亚氯酸钠(NaClO)常用于烟气脱硝(NO)和废水脱除氨氮。
2 x
(1)NaClO 的制备。一种制备NaClO 的过程可表示为:
2 2
①“反应2”的化学方程式为 。
②“反应1”的产物ClO 经净化后常作为饮用水消毒剂替代传统的Cl,从消毒后饮用水水质和消毒
2 2
效率(单位质量消毒剂被还原时得电子数)的角度考虑,用ClO 替代Cl 的原因是 。
2 2
(2)NaClO 溶液对烟气脱硝。
2
①酸性条件下,Fe3+可催化溶液中的NaClO 产生氧化性更强的ClO
气体,总反应可表示为5ClO-
+4H+
2 2 2
4ClO +Cl-+2H O。请补充完整过程Ⅱ的离子方程式:
2 2
Ⅰ.Fe3++ClO- FeClO2+
;
2 2
Ⅱ. ;
Ⅲ.5Fe2++ClO +4H+ 5Fe3++Cl-+2H O。
2 2
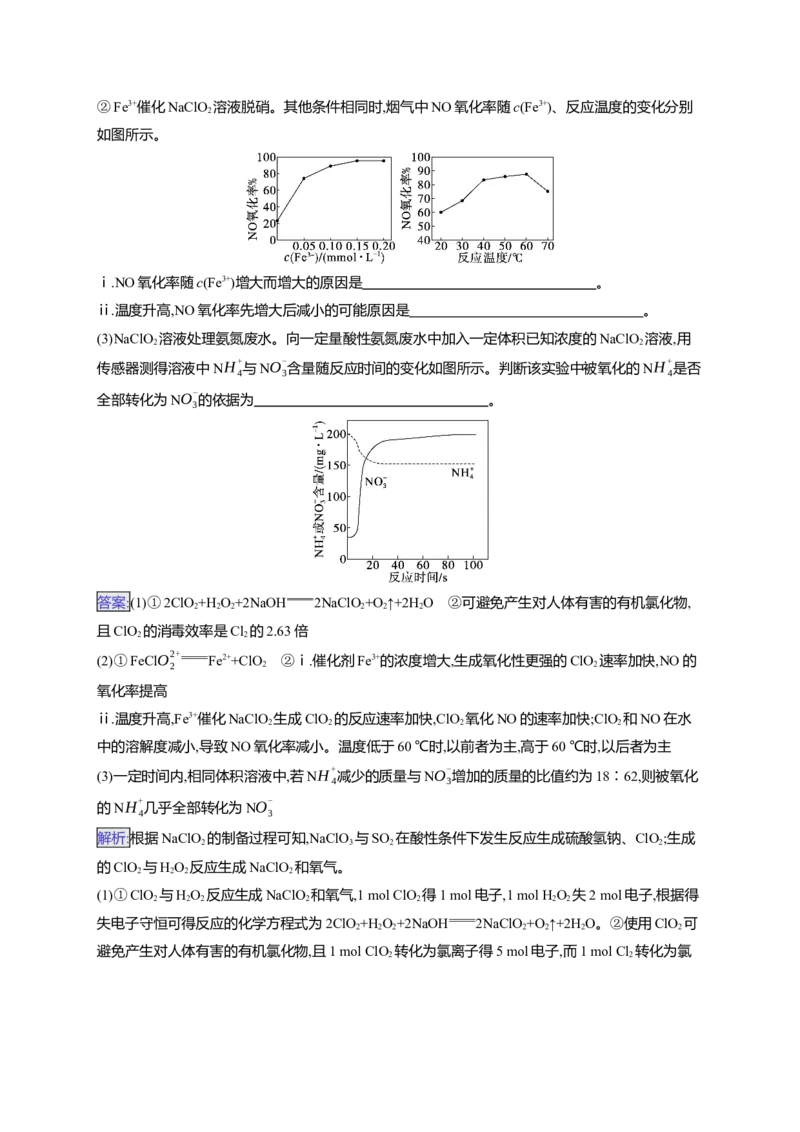
②Fe3+催化NaClO 溶液脱硝。其他条件相同时,烟气中NO氧化率随c(Fe3+)、反应温度的变化分别
2
如图所示。
ⅰ.NO氧化率随c(Fe3+)增大而增大的原因是 。
ⅱ.温度升高,NO氧化率先增大后减小的可能原因是 。
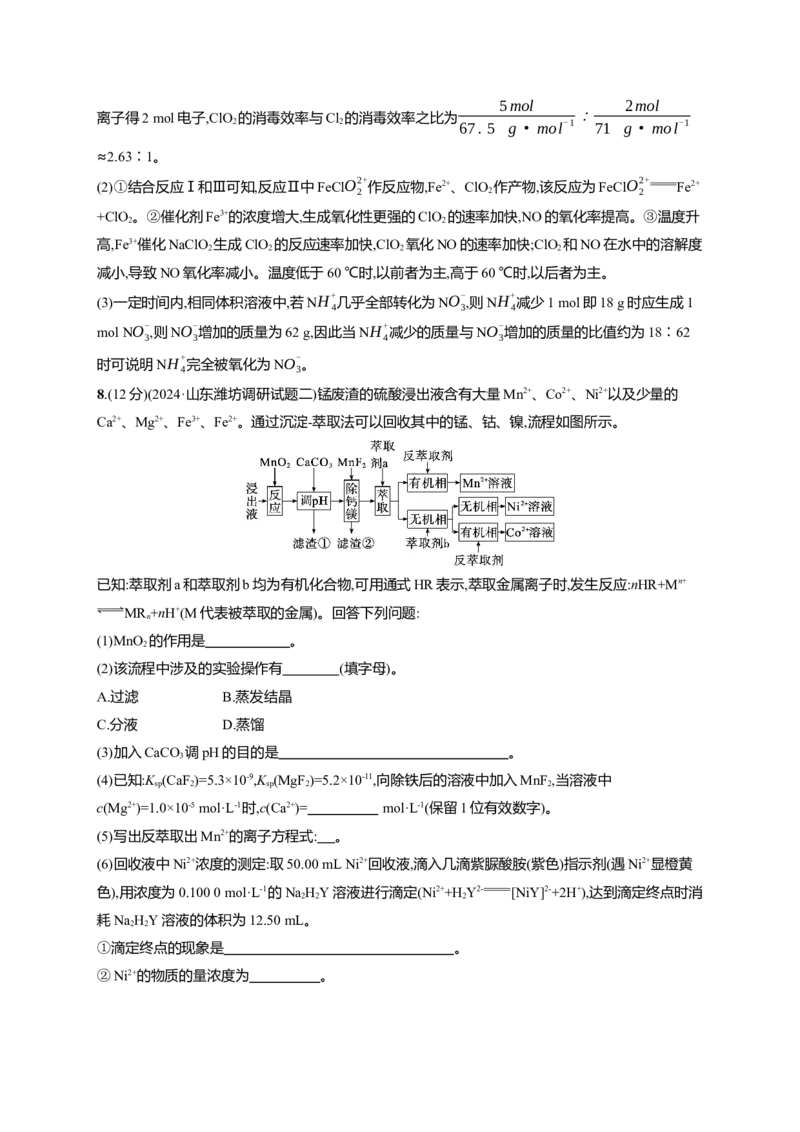
(3)NaClO 溶液处理氨氮废水。向一定量酸性氨氮废水中加入一定体积已知浓度的NaClO 溶液,用
2 2
传感器测得溶液中NH+ 与NO- 含量随反应时间的变化如图所示。判断该实验中被氧化的NH+
是否
4 3 4
全部转化为NO-
的依据为 。
38.(12分)(2024·山东潍坊调研试题二)锰废渣的硫酸浸出液含有大量Mn2+、Co2+、Ni2+以及少量的
Ca2+、Mg2+、Fe3+、Fe2+。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
已知:萃取剂a和萃取剂b均为有机化合物,可用通式HR表示,萃取金属离子时,发生反应:nHR+Mn+
MR +nH+(M代表被萃取的金属)。回答下列问题:
n
(1)MnO 的作用是 。
2
(2)该流程中涉及的实验操作有 (填字母)。
A.过滤 B.蒸发结晶
C.分液 D.蒸馏
(3)加入CaCO 调pH的目的是 。
3
(4)已知:K (CaF )=5.3×10-9,K (MgF )=5.2×10-11,向除铁后的溶液中加入MnF ,当溶液中
sp 2 sp 2 2
c(Mg2+)=1.0×10-5 mol·L-1时,c(Ca2+)= mol·L-1(保留1位有效数字)。
(5)写出反萃取出Mn2+的离子方程式: 。
(6)回收液中Ni2+浓度的测定:取50.00 mL Ni2+回收液,滴入几滴紫脲酸胺(紫色)指示剂(遇Ni2+显橙黄
色),用浓度为0.100 0 mol·L-1的NaHY溶液进行滴定(Ni2++H Y2- [NiY]2-+2H+),达到滴定终点时消
2 2 2
耗NaHY溶液的体积为12.50 mL。
2 2
①滴定终点的现象是 。
②Ni2+的物质的量浓度为 。
③若紫脲酸胺滴入过多,终点延迟,会导致所测Ni2+含量 (填“偏高”“偏低”或“无影
响”)。主观题突破二(解析版)
1.(15分)(2024·甘肃卷,15节选)我国科研人员以高炉渣(主要成分为CaO、MgO、Al O 和SiO 等)为
2 3 2
原料,对炼钢烟气(CO 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示。
2
已知:K (CaSO)=4.9×10-5 K (CaCO)=3.4×10-9
sp 4 sp 3
(1)高炉渣与(NH )SO 经焙烧产生的“气体”是 。
4 2 4
(2)“滤渣”的主要成分是CaSO 和 。
4
(3)“水浸2”时主要反应的化学方程式为 ,该反应能进行的原因
是 。
(4)铝产品NH Al(SO )·12H O可用于 。
4 4 2 2
答案:(1)NH
3
(2)SiO
2
(3)CaSO +(NH)CO CaCO +(NH)SO K (CaSO)>K (CaCO),微溶的硫酸钙转化为更难溶的
4 4 2 3 3 4 2 4 sp 4 sp 3
碳酸钙
(4)净水
解析:高炉渣(主要成分为CaO、MgO、Al O 和SiO 等)加入(NH )SO 在400 ℃下焙烧,生成硫酸钙、
2 3 2 4 2 4
硫酸镁、硫酸铝,同时产生气体,该气体与烟气(CO 和水蒸气)反应生成(NH )CO,所以该气体为NH ;
2 4 2 3 3
焙烧产物经过“水浸1”,然后过滤,“滤渣”为CaSO 以及未反应的SiO,滤液中溶质主要为硫酸镁、
4 2
硫酸铝及硫酸铵;滤液经浓缩结晶,析出NH Al(SO )·12H O,剩余富镁溶液;向“滤渣”中加入
4 4 2 2
(NH )CO 溶液,滤渣中的CaSO 会转化为更难溶的碳酸钙。
4 2 3 4
(1)高炉渣与(NH )SO 经焙烧产生的“气体”是NH 。
4 2 4 3
(2)“滤渣”的主要成分是CaSO 和未反应的SiO。
4 2
(3)“水浸2”时主要反应为硫酸钙与碳酸铵反应生成更难溶的碳酸钙,反应的化学方程式为CaSO+
4
(NH )CO CaCO +(NH)SO ,该反应之所以能发生,是由于K (CaSO)>K (CaCO),微溶的硫酸钙
4 2 3 3 4 2 4 sp 4 sp 3
转化为更难溶的碳酸钙。
(4)铝产品NH Al(SO )·12H O溶于水后,会产生Al3+,Al3+水解生成Al(OH) 胶体,可用于净水。
4 4 2 2 3
2.(12分)(2024·山东卷)以铅精矿(含PbS、Ag S等)为主要原料提取金属Pb和Ag的工艺流程如下:
2回答下列问题:
(1)“热浸”时,难溶的PbS和Ag S转化为[PbCl ]2-和[AgCl ]-及单质硫。溶解等物质的量的PbS和
2 4 2
Ag S时,消耗Fe3+物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时HCl挥
2
发外,另一目的是防止产生 (填化学式)。
(2)将“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属Pb。“电解
2
Ⅰ”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为 。
(3)“还原”中加入铅精矿的目的是 。
(4)“置换”中可选用的试剂X为 (填字母);
A.Al B.Zn
C.Pb D.Ag
“置换”反应的离子方程式为 。
(5)“电解Ⅱ”中将富银铅泥制成电极板,用作 (填“阴极”或“阳极”)。
答案:(1)1∶1 HS
2
(2)热浸
(3)将过量的Fe3+还原为Fe2+
(4)C Pb+2[AgCl ]- [PbCl ]2-+2Ag
2 4
(5)阳极
解析:本题以铅精矿(含PbS、Ag S等)为主要原料提取金属Pb和Ag,“热浸”时,难溶的PbS和Ag S
2 2
转化为[PbCl ]2-和[AgCl ]-及单质硫,Fe3+被还原为Fe2+,“过滤Ⅰ”除掉单质硫,滤液中[PbCl ]2-在稀释、
4 2 4
降温的过程中转化为PbCl 沉淀,然后用饱和食盐水热溶,增大氯离子浓度,使PbCl 又转化为[PbCl ]2-,
2 2 4
电解得到Pb;过滤Ⅱ后的滤液成分主要为[AgCl ]-、FeCl 、FeCl ,故加入铅精矿主要将FeCl 还原为
2 2 3 3
FeCl ,试剂X将[AgCl ]-置换为Ag,得到富银铅泥,试剂X为铅,尾液中含FeCl 。
2 2 2
(1)“热浸”时,Fe3+将PbS和Ag S中-2价的硫氧化为单质硫,Fe3+被还原为Fe2+,在这个过程中Pb和Ag
2
的化合价保持不变,所以溶解等物质的量的PbS和Ag S时,S2-的物质的量相等,所以消耗Fe3+的物质
2
的量相等,比值为1∶1;溶液中HCl浓度过大时会生成HS气体。
2
(2)“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水热溶,会溶解为[PbCl ]2-,电解含[PbCl ]2-的溶液可制
2 4 4
备金属Pb,Pb在阴极产生,阳极Cl-放电产生Cl,尾液中含有FeCl ,FeCl 吸收Cl 后转化为FeCl ,可以
2 2 2 2 3
在“热浸”中循环使用。(3)“过滤Ⅱ”所得的滤液中有过量的未反应的Fe3+,根据还原之后可以得到含硫滤渣可知,“还原”中
加入铅精矿的目的是将过量的Fe3+还原为Fe2+。
(4)“置换”中加入试剂X可以得到富银铅泥,为了防止引入其他杂质,则试剂X应为Pb,发生的反应为
Pb+2[AgCl ]- 2Ag+[PbCl ]2-。
2 4
(5)“电解Ⅱ”中将富银铅泥制成电极板,“电解Ⅱ”得到金属银和金属铅,将银和铅分离出来,所以不可
能作为阴极,应作为阳极板,阳极放电时,银变成阳极泥而沉降下来,铅失电子为Pb2+,阴极得电子得到
Pb,所以电极板应作阳极。
3.(10分)(2024·广东2月大联考)钼具有耐腐耐磨的特性,目前广泛应用于化工、医疗和国防领域。一
种使用先进的碱性氧化焙烧法,从镍钼矿(主要成分是MoS 、NiS、FeS)中回收钼的流程如图所示:
2 2
已知:①“焙烧”后钼元素以NaMoO 的形式存在,Ni的化合价不变且以氧化物的形式存在,“焙烧”
2 4
过程中未见有含S气态物的生成。
②K [Mg(OH) ]=5.6×10-12,K (MgCO )=6.5×10-6。
sp 2 sp 3
③一般离子浓度达到10-5 mol·L-1以下视为沉淀完全。
回答下列问题:
(1)写出“焙烧”过程中MoS 发生反应的化学方程式: 。
2
(2)“滤渣1”的主要成分为 (填化学式)。
(3)Na CO
实验用量与理论用量的比值为1.0、1.1、1.2、1.3时,Mo的浸出率和CO2-
残留浓度的关
2 3 3
系如图所示,则NaCO 的最佳用量比为 ,结合图中信息说明理由: 。
2 3
(4)常温下,“水浸”过程完成后溶液中c(CO2-
)=3.00 g·L-1,试计算“净化”过程中每升溶液中需加入
3
(保留两位有效数字) mol MgSO ,若“净化”完成后溶液的pH=8,则此时溶液中 (填“不
4
存在”或“存在”)Mg(OH) 沉淀。
2(5)MoS 被称为润滑之王,其稳定晶体的晶胞结构的透视图与正视图如图所示,晶胞参数
y
α=β=90°,γ=60°,原子间距a=b=c,则y= ;晶胞中与Mo原子距离最近且相等的S原子数目为
。
答案:(1)2MoS +6Na CO+9O 2NaMoO +4Na SO +6CO
2 2 3 2 2 4 2 4 2
(2)Fe O、NiO
2 3
(3)1.2 当NaCO 的用量比从1.0增加到1.2时,钼的浸出率明显增加,当NaCO 用量比从1.2增加到
2 3 2 3
1.3时,钼的浸出率增加不大,但CO2-
的残留浓度显著增大
3
(4)0.70 不存在
(5)2 6
解析:向镍钼矿(主要成分是MoS 、NiS、FeS)通入空气,加入碳酸钠焙烧产生CO,水浸后除去的
2 2 2
“滤渣1”的成分为Fe O、NiO,加入硫酸镁净化除去的“滤渣2”的成分为氢氧化镁,滤液经冷却结
2 3
晶得到硫酸钠,向溶液中加入D318-Ⅲ树脂进行离子交换,再加入氨水解析:得到“解析:液”,处理后
得到钼酸铵。
(1)由题中信息可知,含Mo的产物为NaMoO ,没有含硫气态物质生成,结合流程可知硫元素被氧化为
2 4
最高价的盐NaSO ,流程中生成CO,则“焙烧”过程中MoS 发生反应的化学方程式为
2 4 2 2
2MoS +6Na CO+9O 2NaMoO +4Na SO +6CO 。
2 2 3 2 2 4 2 4 2
(2)FeS 被氧化为Fe O,Fe O 不溶于碱性的碳酸钠溶液成为滤渣,由题中信息可知Ni以+2价氧化物
2 2 3 2 3
NiO存在,NiO也不溶于碱性碳酸钠溶液,则“滤渣1”的主要成分为Fe O、NiO。
2 3
(3)由图可知,当NaCO 实验用量与理论用量的比值从1.0增加到1.2时,钼的浸出率明显增加,当
2 3
NaCO
实验用量与理论用量的比值从1.2增加到1.3时,钼的浸出率增加不大,但CO2-
的残留浓度显
2 3 3
著增大,故最佳用量比选择1.2。
3.00 g·L-1
(4)c(CO2-
)=3.00
g·L-1,转换单位后c(CO2-
)= =0.05
mol·L-1,完全沉淀此部分CO2-
需
3 3 60 g·mol-1 3
K (MgCO ) 6.5×10-6
c(Mg2+)=0.05
mol·L-1,当CO2-
沉淀完全后溶液中c(Mg2+)=
sp 3 =
3 c(CO2-) 1×10-5
3
mol·L-1=0.65 mol·L-1,合计c(Mg2+)=(0.05+0.65) mol·L-1=0.70 mol·L-1,故每升溶液中需加入0.70 mol
10-14
MgSO 。若“净化”完成后溶液pH=8,则此时溶液中c(H+)=10-8 mol·L-1,c(OH-)= mol·L-1=10-6
4 10-8
mol·L-1,此时c(Mg2+)·c2(OH-)=0.65×(10-6)2=6.5×10-134时,(NH)MoS 晶体
4 2 4 4 2 4
产率继续增大的原因是 。
(3)“酸浸”和“高温还原”中产生的气体可通入 (填操作单元的名称)中循环使用。
(4)MoS 也可由(NH )MoS 在一定条件下加热分解制得,同时产生NH 、HS和某种硫单质,且NH 与
2 4 2 4 3 2 3
硫单质的物质的量之比为8∶1,则硫单质的分子式为 。
答案:(1)2MoS +7O 2MoO +4SO 除去碳酸钾
2 2 3 2
(2)①(NH )MoO +4(NH)S+4HO (NH )MoS +8NH·H O ②(NH )S量不足,(NH)MoO 转化生
4 2 4 4 2 2 4 2 4 3 2 4 2 4 2 4
成(NH )MoS 继续加入(NH )S,使得铵根离子浓度增大,降低了(NH )MoS 的溶解度,使其结晶析出,
4 2 3 4 2 4 2 4
导致晶体产率继续增大
(3)转化 (4)S
4
解析:钼精矿在空气中煅烧时,MoS 转化为MoO 和二氧化硫,水洗除去碳酸钾等可溶物,过滤分离出
2 3
固体并加入氨水浸取,氧化铁、氧化镁不反应成为“浸渣”,浸取液中含有(NH )MoO ,加入硫化铵将
4 2 4
(NH )MoO 转化为(NH )MoS ,加入稀硫酸酸浸,得到硫化氢气体和MoS
沉淀:MoS2-
+2H+
4 2 4 4 2 4 3 4
MoS ↓+H S↑,使用氢气在高温下还原MoS 得到MoS 。
3 2 3 2
(1)空气中的氧气具有氧化性,“焙烧”时MoS 被氧化为MoO ,同时生成二氧化硫,该反应的化学方程
2 3
式为2MoS +7O 2MoO +4SO;氧化铁、氧化镁、MoO 均不溶于水,而碳酸钾溶于水,则“水洗”
2 2 3 2 3
的目的是除去碳酸钾。
(2)①向含(NH )MoO 的溶液中加入硫化铵生成(NH )MoS ,根据质量守恒可知,同时生成一水合氨,
4 2 4 4 2 4
化学方程式为(NH )MoO +4(NH)S+4HO (NH )MoS +8NH·H O。②δ=3时,(NH)S量不足,
4 2 4 4 2 2 4 2 4 3 2 4 2
(NH )MoO 转化生成(NH )MoS ,故(NH )MoS 晶体产率为0;δ>4时,(NH)MoO 转化生成
4 2 4 4 2 3 4 2 4 4 2 4
(NH )MoS ,继续加入(NH )S,使得溶液中铵根离子浓度增大,降低了(NH )MoS 溶解度,使其结晶析
4 2 4 4 2 4 2 4
出,从而导致晶体产率继续增大。
(3)“酸浸”和“高温还原”中产生的气体为硫化氢,硫化氢和氨水反应生成硫化铵,故可通入“转
化”环节中继续使用。(4)NH 与硫单质的物质的量之比为8∶1,假设生成8分子氨气、1分子硫单质,根据质量守恒可知,有
3
4分子(NH )MoS 参与反应,则生成4分子MoS ,Mo化合价由+6价变为+4价,转移4×2=8个电子,生
4 2 4 2
成硫单质的硫化合价由-2价变为0价,根据得失电子守恒可知,生成硫单质中硫原子数目为8÷2=4,故
硫单质化学式为S。
4
6.(12分)(2024·江苏南通第二次调研)实验室以FeS 为原料制备磷酸亚铁晶体[Fe (PO )·8H O],其部
2 3 4 2 2
分实验过程如下:
(1)将一定体积98%的浓硫酸稀释为200 mL 30%的硫酸,除量筒外,还必须使用的玻璃仪器有
。
(2)检验“还原”已完全的实验操作为 。
(3)向过滤后的滤液中加入NaHPO ,并用氨水或CHCOONa调节溶液pH,“共沉淀”过程生成
2 4 3
Fe (PO )·8H O。
3 4 2 2
①若使用CHCOONa调节溶液的pH,“共沉淀”反应的离子方程式为 。
3
②不使用NaOH调节溶液pH的原因是 。
③补充完整利用如图所示装置(夹持装置已略去)制取Fe (PO )·8H O的实验方案:向三颈烧瓶中加入
3 4 2 2
抗坏血酸溶液, 至混合溶液pH≈4, ,充分搅拌一段时间,过滤,洗
涤固体,真空干燥。(已知:所用抗坏血酸溶液的pH=2.8,当溶液pH控制在4~6之间时,所得晶体质量
最好。恒压滴液漏斗a、b中分别盛放FeSO 溶液和CHCOONa-Na HPO 混合溶液)
4 3 2 4
(4)测定样品中Fe (PO )·8H O(M=502 g·mol-1)的纯度。取0.627 5 g样品完全溶解后配制成250 mL
3 4 2 2
溶液,取出25.00 mL置于锥形瓶中,加入一定量的HO 溶液将铁元素完全氧化,以磺基水杨酸为指示
2 2
剂,用0.020 00 mol·L-1 EDTA标准溶液进行滴定至终点(Fe3+与EDTA按物质的量之比1∶1发生反
应),消耗EDTA溶液15.00 mL。计算该磷酸亚铁晶体样品的纯度为 。
答案:(1)烧杯、玻璃棒
(2)取少量还原后的溶液置于试管中,滴加KSCN溶液(或亚铁氰化钾溶液)
(3)①3Fe2++2HPO2-
+2CH COO-+8H O Fe (PO )·8H O↓+2CHCOOH ②NaOH碱性强,容易造成
4 3 2 3 4 2 2 3
局部pH过高,生成Fe(OH) 等杂质 ③向三颈烧瓶中滴加CHCOONa-Na HPO 混合溶液 再向三颈
2 3 2 4
烧瓶中滴加FeSO 溶液,通过调节恒压滴液漏斗a、b的活塞,控制溶液pH为4~6
4
(4)80.00%解析:煅烧二硫化亚铁可得到氧化铁,用硫酸酸溶后得到硫酸铁,用二硫化亚铁还原硫酸铁生成硫酸亚
铁和硫沉淀,过滤,向滤液中加磷酸氢二钠共沉淀生成磷酸亚铁晶体[Fe (PO )·8H O]。
3 4 2 2
(1)将一定体积98%的浓硫酸稀释为200 mL 30%的硫酸,使用的仪器除量筒外,还必须使用的玻璃仪
器有烧杯、玻璃棒。
(2)“还原”时,硫酸铁与二硫化亚铁反应生成硫酸亚铁和硫沉淀,“还原”已完全时溶液中无铁离子,则
检验“还原”已完全的实验操作为取少量还原后的溶液置于试管中,滴加KSCN溶液(或亚铁氰化钾
溶液),溶液不变红(或没有生成蓝色沉淀)。
(3)①若使用CHCOONa调节溶液pH,“共沉淀”反应生成Fe (PO )·8H O和醋酸,该反应的离子方程
3 3 4 2 2
式为3Fe2++2HPO2-
+2CH COO-+8H O Fe (PO )·8H O↓+2CHCOOH。②不使用NaOH调节溶液
4 3 2 3 4 2 2 3
pH的原因是NaOH碱性强,容易造成局部pH过高,生成Fe(OH) 等杂质。③制取Fe (PO )·8H O的
2 3 4 2 2
实验方案:向三颈烧瓶中加入抗坏血酸溶液,向三颈烧瓶中滴加CHCOONa-Na HPO 混合溶液至混合
3 2 4
溶液pH≈4,再向三颈烧瓶中滴加FeSO 溶液,通过调节恒压滴液漏斗a、b的活塞,控制溶液pH为
4
4~6,充分搅拌一段时间,过滤,洗涤固体,真空干燥。
(4)每25.00 mL溶液中n(Fe2+)=0.020 00 mol·L-1×15.00 mL×10-3 L· mL-1=3.000×10-4
250
mol,n[Fe (PO )·8H O]=1.000×10-4 mol,0.627 5 g样品中含n[Fe (PO )·8H O]=1.000×10-4 mol×
3 4 2 2 3 4 2 2 25.00
0.502 0
=1.000×10-3 mol,m[Fe (PO )·8H O]=1.000×10-3 mol×502 g· mol-1=0.502 0 g,则样品纯度为
3 4 2 2 0.627 5
×100%=80.00%。
7.(12分)(2024·江苏南京二模)高效氧化剂亚氯酸钠(NaClO)常用于烟气脱硝(NO)和废水脱除氨氮。
2 x
(1)NaClO 的制备。一种制备NaClO 的过程可表示为:
2 2
①“反应2”的化学方程式为 。
②“反应1”的产物ClO 经净化后常作为饮用水消毒剂替代传统的Cl,从消毒后饮用水水质和消毒
2 2
效率(单位质量消毒剂被还原时得电子数)的角度考虑,用ClO 替代Cl 的原因是 。
2 2
(2)NaClO 溶液对烟气脱硝。
2
①酸性条件下,Fe3+可催化溶液中的NaClO 产生氧化性更强的ClO
气体,总反应可表示为5ClO-
+4H+
2 2 2
4ClO +Cl-+2H O。请补充完整过程Ⅱ的离子方程式:
2 2
Ⅰ.Fe3++ClO- FeClO2+
;
2 2
Ⅱ. ;
Ⅲ.5Fe2++ClO +4H+ 5Fe3++Cl-+2H O。
2 2②Fe3+催化NaClO 溶液脱硝。其他条件相同时,烟气中NO氧化率随c(Fe3+)、反应温度的变化分别
2
如图所示。
ⅰ.NO氧化率随c(Fe3+)增大而增大的原因是 。
ⅱ.温度升高,NO氧化率先增大后减小的可能原因是 。
(3)NaClO 溶液处理氨氮废水。向一定量酸性氨氮废水中加入一定体积已知浓度的NaClO 溶液,用
2 2
传感器测得溶液中NH+ 与NO- 含量随反应时间的变化如图所示。判断该实验中被氧化的NH+
是否
4 3 4
全部转化为NO-
的依据为 。
3
答案:(1)①2ClO +H O+2NaOH 2NaClO+O ↑+2H O ②可避免产生对人体有害的有机氯化物,
2 2 2 2 2 2
且ClO 的消毒效率是Cl 的2.63倍
2 2
(2)①FeClO2+
Fe2++ClO ②ⅰ.催化剂Fe3+的浓度增大,生成氧化性更强的ClO 速率加快,NO的
2 2 2
氧化率提高
ⅱ.温度升高,Fe3+催化NaClO 生成ClO 的反应速率加快,ClO 氧化NO的速率加快;ClO 和NO在水
2 2 2 2
中的溶解度减小,导致NO氧化率减小。温度低于60 ℃时,以前者为主,高于60 ℃时,以后者为主
(3)一定时间内,相同体积溶液中,若NH+ 减少的质量与NO-
增加的质量的比值约为18∶62,则被氧化
4 3
的NH+ 几乎全部转化为NO-
4 3
解析:根据NaClO 的制备过程可知,NaClO 与SO 在酸性条件下发生反应生成硫酸氢钠、ClO ;生成
2 3 2 2
的ClO 与HO 反应生成NaClO 和氧气。
2 2 2 2
(1)①ClO 与HO 反应生成NaClO 和氧气,1 mol ClO 得1 mol电子,1 mol HO 失2 mol电子,根据得
2 2 2 2 2 2 2
失电子守恒可得反应的化学方程式为2ClO +H O+2NaOH 2NaClO+O ↑+2H O。②使用ClO 可
2 2 2 2 2 2 2
避免产生对人体有害的有机氯化物,且1 mol ClO 转化为氯离子得5 mol电子,而1 mol Cl 转化为氯
2 25mol 2mol
离子得2 mol电子,ClO 的消毒效率与Cl 的消毒效率之比为 ∶
2 2 67.5 g·mol-1 71 g·mol-1
≈2.63∶1。
(2)①结合反应Ⅰ和Ⅲ可知,反应Ⅱ中FeClO2+
作反应物,Fe2+、ClO
作产物,该反应为FeClO2+
Fe2+
2 2 2
+ClO 。②催化剂Fe3+的浓度增大,生成氧化性更强的ClO 的速率加快,NO的氧化率提高。③温度升
2 2
高,Fe3+催化NaClO 生成ClO 的反应速率加快,ClO 氧化NO的速率加快;ClO 和NO在水中的溶解度
2 2 2 2
减小,导致NO氧化率减小。温度低于60 ℃时,以前者为主,高于60 ℃时,以后者为主。
(3)一定时间内,相同体积溶液中,若NH+ 几乎全部转化为NO- ,则NH+
减少1 mol即18 g时应生成1
4 3 4
mol NO- ,则NO- 增加的质量为62 g,因此当NH+ 减少的质量与NO- 增加的质量的比值约为18∶62
3 3 4 3
时可说明NH+ 完全被氧化为NO-
。
4 3
8.(12分)(2024·山东潍坊调研试题二)锰废渣的硫酸浸出液含有大量Mn2+、Co2+、Ni2+以及少量的
Ca2+、Mg2+、Fe3+、Fe2+。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
已知:萃取剂a和萃取剂b均为有机化合物,可用通式HR表示,萃取金属离子时,发生反应:nHR+Mn+
MR +nH+(M代表被萃取的金属)。回答下列问题:
n
(1)MnO 的作用是 。
2
(2)该流程中涉及的实验操作有 (填字母)。
A.过滤 B.蒸发结晶
C.分液 D.蒸馏
(3)加入CaCO 调pH的目的是 。
3
(4)已知:K (CaF )=5.3×10-9,K (MgF )=5.2×10-11,向除铁后的溶液中加入MnF ,当溶液中
sp 2 sp 2 2
c(Mg2+)=1.0×10-5 mol·L-1时,c(Ca2+)= mol·L-1(保留1位有效数字)。
(5)写出反萃取出Mn2+的离子方程式: 。
(6)回收液中Ni2+浓度的测定:取50.00 mL Ni2+回收液,滴入几滴紫脲酸胺(紫色)指示剂(遇Ni2+显橙黄
色),用浓度为0.100 0 mol·L-1的NaHY溶液进行滴定(Ni2++H Y2- [NiY]2-+2H+),达到滴定终点时消
2 2 2
耗NaHY溶液的体积为12.50 mL。
2 2
①滴定终点的现象是 。
②Ni2+的物质的量浓度为 。③若紫脲酸胺滴入过多,终点延迟,会导致所测Ni2+含量 (填“偏高”“偏低”或“无影
响”)。
答案:(1)氧化Fe2+
(2)AC
(3)使Fe3+转化成Fe(OH) 沉淀除去
3
(4)0.001
(5)MnR +2H+ 2HR+Mn2+
2
(6)①当滴入最后半滴NaHY标准溶液后,溶液由橙黄色变为紫色,且半分钟内不恢复橙黄色
2 2
②0.025 0 mol·L-1 ③偏高
解析:锰废渣的硫酸浸出液含有大量Mn2+、Co2+、Ni2+以及少量的Ca2+、Mg2+、Fe3+、Fe2+,往其中加
二氧化锰将二价铁氧化为三价铁,加碳酸钙调溶液pH,使铁离子转化为氢氧化铁沉淀,往滤液中加
MnF 沉淀钙离子和镁离子,过滤,往滤液中加萃取剂a萃取锰离子,向所得有机相中加入反萃取剂得到
2
含Mn2+的溶液;无机相用萃取剂b萃取Co2+,所得无机相为含Ni2+的溶液,向有机相中加入反萃取剂得
到含Co2+的溶液。
(1)“浸出液”中含二价铁,MnO 的作用是将二价铁氧化为三价铁。
2
(2)流程中得滤渣①和滤渣②的操作为过滤,萃取之后得有机相和无机相的操作为分液,故答案:为
AC。
(3)用二氧化锰将二价铁氧化为三价铁后,加入CaCO 调pH可以使Fe3+转化为氢氧化铁沉淀,即加入
3
CaCO 调pH的目的是使Fe3+转化成氢氧化铁沉淀除去。
3
(4)已知:K (CaF )=5.3×10-9,K (MgF )=5.2×10-11,向除铁后的溶液中加入MnF ,当溶液中
sp 2 sp 2 2
√K (MgF ) √5.2×10-11
c(Mg2+)=1.0×10-5 mol·L-1时,c(F-)= sp 2 = mol·L-1=√5.2×10-6 mol·L-1,则
c(M g2+) 1.0×10-5
K (CaF ) 5.3×10-9
c(Ca2+)= sp 2 = mol·L-1≈0.001 mol·L-1。
c2(F-) 5.2×10-6
(5)根据信息可知,反萃取剂为酸,即反萃取出Mn2+时加入适量的酸将Mn2+反萃取出来,相应的离子方
程式为MnR +2H+ 2HR+Mn2+。
2
(6)①在Ni2+与NaHY溶液恰好完全反应之前,溶液呈橙黄色,恰好完全反应后,溶液中无Ni2+,此时再
2 2
加半滴NaHY溶液,溶液将会呈紫色,且半分钟内不恢复橙黄色,所以滴定终点的现象是当滴入最后
2 2
半滴NaHY标准溶液后,溶液由橙黄色变为紫色,且半分钟内不恢复橙黄色。②反应时Ni2+与
2 2
0.100 0mol·L-1×0.012 5 L
NaHY按物质的量1∶1反应,所以Ni2+物质的量浓度为
2 2 0.05 L
=0.025 0 mol·L-1。③若紫脲酸胺滴入过多,终点延迟,会导致NaHY偏多,则所测Ni2+含量偏高。
2 2