文档内容
课堂检测·素养达标
1.(2019·三明高一检测)用物质的量浓度来表示溶液的组成对生产和科学研究
都有重要的意义。下表是某人体检表上的部分信息,其中是用物质的量浓度来
表示的是 ( )
A.谷丙转氨酶 B.球蛋白
C.乳酸脱氢酶 D.葡萄糖
2.(2019·三明高一检测)下列溶液中,跟100 mL 0.5 mol·L-1 NaCl溶液中所
含的Cl-物质的量浓度相同的是( )
A.100 mL 0.5 mol·L-1 MgCl 溶液
2
B.200 mL 0.25 mol·L-1 AlCl 溶液
3
C.50 mL 1 mol·L-1 NaCl溶液
D.25 mL 0.5 mol·L-1 HCl溶液
【补偿训练】(2019·济南高一检测)与100 mL 0.2 mol·L-1 CaCl 溶液中Cl-浓度相同的是
2
( )
A.50 mL 0.1 mol·L-1 FeCl 溶液
3
B.200 mL 0.4 mol·L-1 NaCl溶液
C.200 mL 0.1 mol·L-1 MgCl 溶液
2
D.200 mL 0.2 mol·L-1 KCl溶液
3.(2019·长春高一检测)关于容量瓶的四种叙述:①是配制一定物质的量浓度
溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。
这些叙述中正确的是 ( )
A.①②③④ B.②③
C.①②④ D.②③④
【补偿训练】
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是 ( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
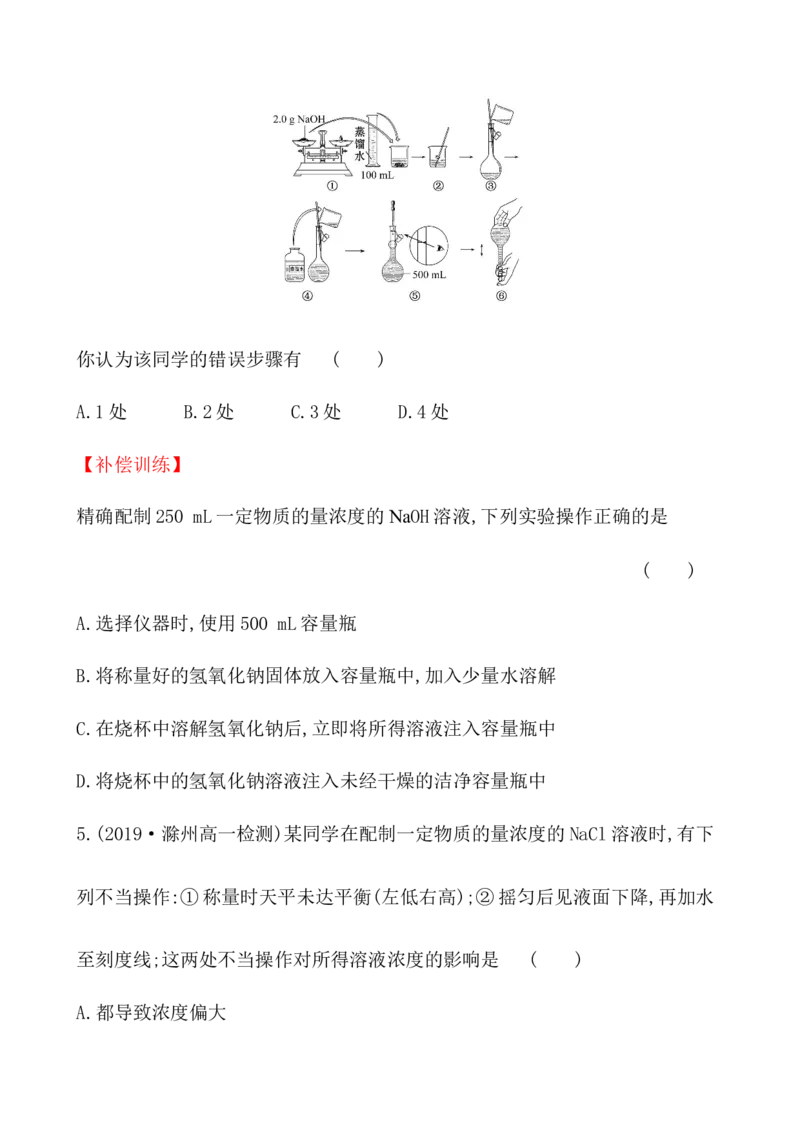
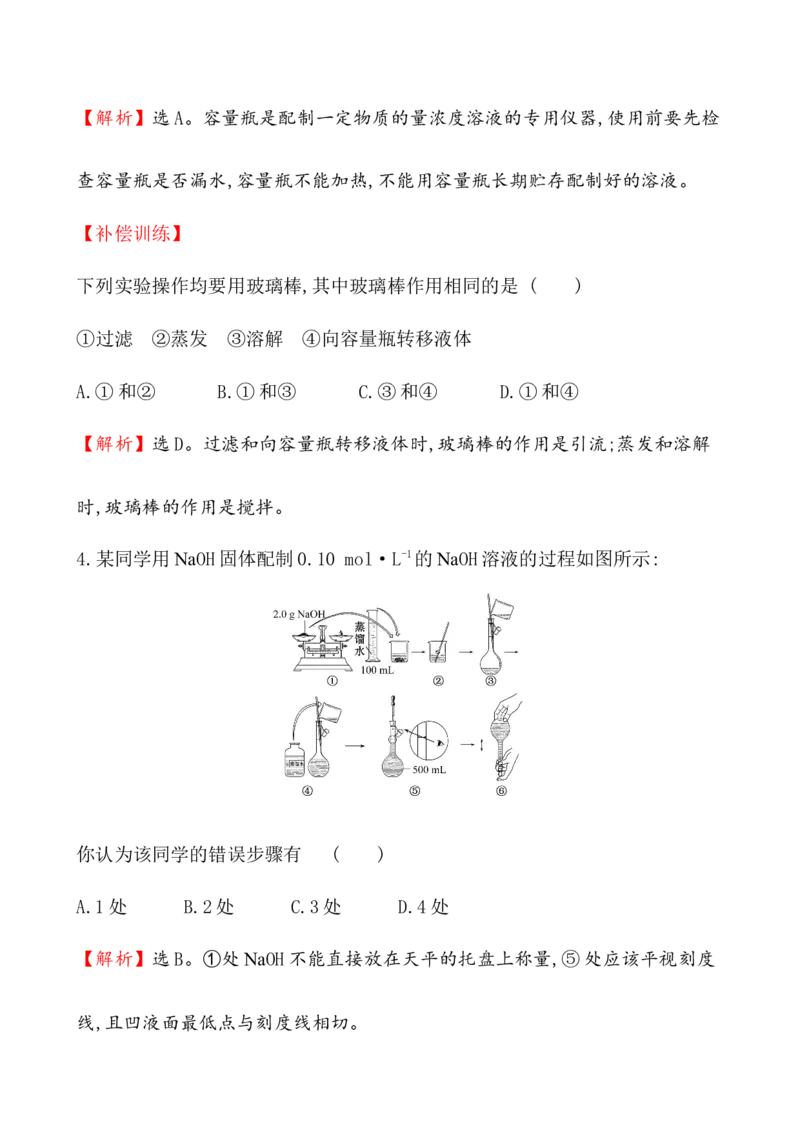
4.某同学用NaOH固体配制0.10 mol·L-1的NaOH溶液的过程如图所示:你认为该同学的错误步骤有 ( )
A.1处 B.2处 C.3处 D.4处
【补偿训练】
精确配制250 mL一定物质的量浓度的NaOH溶液,下列实验操作正确的是
( )
A.选择仪器时,使用500 mL容量瓶
B.将称量好的氢氧化钠固体放入容量瓶中,加入少量水溶解
C.在烧杯中溶解氢氧化钠后,立即将所得溶液注入容量瓶中
D.将烧杯中的氢氧化钠溶液注入未经干燥的洁净容量瓶中
5.(2019·滁州高一检测)某同学在配制一定物质的量浓度的NaCl溶液时,有下
列不当操作:①称量时天平未达平衡(左低右高);②摇匀后见液面下降,再加水
至刻度线;这两处不当操作对所得溶液浓度的影响是 ( )
A.都导致浓度偏大B.①导致浓度偏小,②导致浓度偏大
C.都导致浓度偏小
D.①导致浓度偏大,②导致浓度偏小
6.(2019·东城区高一检测)取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的
硫酸注入500 mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度
是 ( )
A.0.21 mol·L-1 B.0.42 mol·L-1
C.0.56 mol·L-1 D.0.26 mol·L-1
【补偿训练】
1.(2019·襄阳高一检测)将10 mL 5 mol·L-1的盐酸稀释到200 mL,再从中取
出5 mL,这5 mL盐酸的物质的量浓度为 ( )
A.0.5 mol·L-1 B.0.25 mol·L-1
C.0.1 mol·L-1 D.1 mol·L-1
2.表示溶液组成的常用方法有两种:①溶质的质量分数;②物质的量浓度。如图
所示为实验室浓硫酸的试剂瓶上的标签。请思考:
(1)在图示的浓硫酸试剂瓶标签上,描述浓硫酸组成的物理量是哪个物理量?
(2)若取1 L这种浓硫酸,其中含有溶质的质量是多少?物质的量是多少?
(3)根据物质的量浓度的定义计算该浓硫酸的物质的量浓度。
7.(新思维·新考向)鲜花是美丽的,但是美丽的鲜花的保鲜期却很短,在花瓶中
加入“鲜花保鲜剂”却可以延长鲜花的寿命。
下表是1 L“鲜花保鲜剂”的成分(其中阿司匹林不含K+,其存在也不会干扰成
分中其他离子的检验),回答下列问题
:
成分 蔗糖 硫酸钾阿司匹林高锰酸钾
质量/g 50.00 0.50 0.35 0.50
摩尔质量
342 174 180 158
/
(g·mol-1)
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是 ______________________ _(填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为 __________mol·L-1。(只要求写
表达式,不用化简,不需计算)
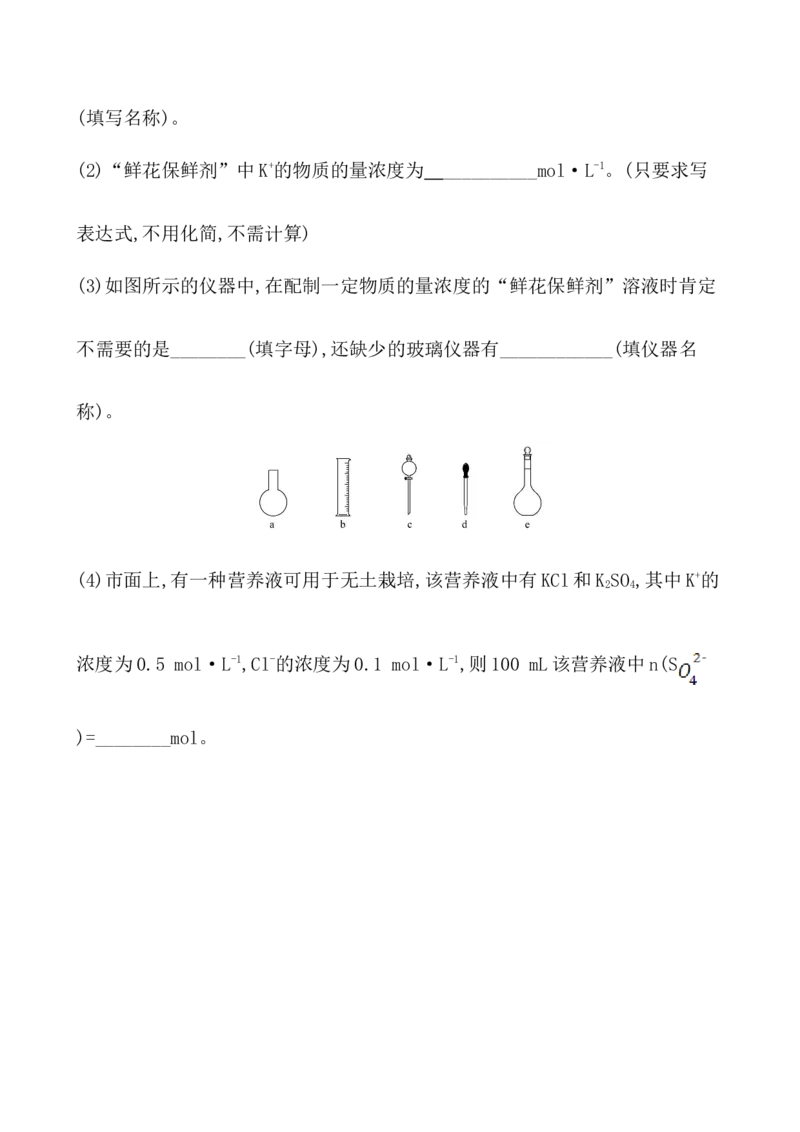
(3)如图所示的仪器中,在配制一定物质的量浓度的“鲜花保鲜剂”溶液时肯定
不需要的是________(填字母),还缺少的玻璃仪器有____________(填仪器名
称)。
(4)市面上,有一种营养液可用于无土栽培,该营养液中有KCl和K SO ,其中K+的
2 4
浓度为0.5 mol·L-1,Cl-的浓度为0.1 mol·L-1,则100 mL该营养液中n(S
)=________mol。课堂检测·素养达标
1.(2019·三明高一检测)用物质的量浓度来表示溶液的组成对生产和科学研究
都有重要的意义。下表是某人体检表上的部分信息,其中是用物质的量浓度来
表示的是 ( )
A.谷丙转氨酶 B.球蛋白
C.乳酸脱氢酶 D.葡萄糖
【解析】选D。看清物理量的单位即可,物质的量浓度的单位通常为mol·L-1,
此处为mmol·L-1。
2.(2019·三明高一检测)下列溶液中,跟100 mL 0.5 mol·L-1 NaCl溶液中所
含的Cl-物质的量浓度相同的是( )
A.100 mL 0.5 mol·L-1 MgCl 溶液
2
B.200 mL 0.25 mol·L-1 AlCl 溶液
3
C.50 mL 1 mol·L-1 NaCl溶液D.25 mL 0.5 mol·L-1 HCl溶液
【解析】选D。物质的量浓度与溶液的体积无关,100 mL 0.5 mol·L-1 NaCl溶
液中c(Cl-)=0.5 mol·L-1,而A、B、C、D项中,c(Cl-)分别为1 mol·L-1、0.75
mol·L-1、1 mol·L-1、0.5 mol·L-1,D项正确。
【补偿训练】
(2019·济南高一检测)与100 mL 0.2 mol·L-1 CaCl 溶液中Cl-浓度相同的是
2
( )
A.50 mL 0.1 mol·L-1 FeCl 溶液
3
B.200 mL 0.4 mol·L-1 NaCl溶液
C.200 mL 0.1 mol·L-1 MgCl 溶液
2
D.200 mL 0.2 mol·L-1 KCl溶液
【解析】选B。溶液中离子浓度不随所取用的体积的多少而改变。
3.(2019·长春高一检测)关于容量瓶的四种叙述:①是配制一定物质的量浓度
溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。
这些叙述中正确的是 ( )
A.①②③④ B.②③
C.①②④ D.②③④【解析】选A。容量瓶是配制一定物质的量浓度溶液的专用仪器,使用前要先检
查容量瓶是否漏水,容量瓶不能加热,不能用容量瓶长期贮存配制好的溶液。
【补偿训练】
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是 ( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
【解析】选D。过滤和向容量瓶转移液体时,玻璃棒的作用是引流;蒸发和溶解
时,玻璃棒的作用是搅拌。
4.某同学用NaOH固体配制0.10 mol·L-1的NaOH溶液的过程如图所示:
你认为该同学的错误步骤有 ( )
A.1处 B.2处 C.3处 D.4处
【解析】选B。①处NaOH不能直接放在天平的托盘上称量,⑤处应该平视刻度
线,且凹液面最低点与刻度线相切。【补偿训练】
精确配制250 mL一定物质的量浓度的NaOH溶液,下列实验操作正确的是
( )
A.选择仪器时,使用500 mL容量瓶
B.将称量好的氢氧化钠固体放入容量瓶中,加入少量水溶解
C.在烧杯中溶解氢氧化钠后,立即将所得溶液注入容量瓶中
D.将烧杯中的氢氧化钠溶液注入未经干燥的洁净容量瓶中
【解析】选D。A项,应选用250 mL容量瓶。B项,容量瓶不能用作溶解的仪器,
应在烧杯中溶解。C项,应将溶解NaOH后的溶液恢复到室温后再向容量瓶中转
移。D项容量瓶未干燥对所配溶液浓度无影响,正确。
5.(2019·滁州高一检测)某同学在配制一定物质的量浓度的NaCl溶液时,有下
列不当操作:①称量时天平未达平衡(左低右高);②摇匀后见液面下降,再加水
至刻度线;这两处不当操作对所得溶液浓度的影响是 ( )
A.都导致浓度偏大
B.①导致浓度偏小,②导致浓度偏大
C.都导致浓度偏小
D.①导致浓度偏大,②导致浓度偏小【解析】选D。根据c= = ,①天平称量时“左物右码”,左低右高,说明药品
多,因此所配溶液浓度偏大;②摇匀后见液面下降,再加水至刻度线,溶液体积偏
大,因此所配溶液浓度偏小。
6.(2019·东城区高一检测)取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的
硫酸注入500 mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度
是 ( )
A.0.21 mol·L-1 B.0.42 mol·L-1
C.0.56 mol·L-1 D.0.26 mol·L-1
【解析】选B。容量瓶中H SO 溶液的H+的物质的量为n(H+)=(0.1 L×
2 4
0.3 mol·L-1+0.3 L×0.25 mol·L-1)×2=0.21 mol,所以c(H+)= =
0.42 mol·L-1。
【补偿训练】
1.(2019·襄阳高一检测)将10 mL 5 mol·L-1的盐酸稀释到200 mL,再从中取
出5 mL,这5 mL盐酸的物质的量浓度为 ( )
A.0.5 mol·L-1 B.0.25 mol·L-1
C.0.1 mol·L-1 D.1 mol·L-1【解析】选B。10 mL 5 mol·L-1的盐酸稀释到200 mL,浓度为0.25 mol·L-1,
从中取出5 mL,浓度仍为0.25 mol·L-1。
2.表示溶液组成的常用方法有两种:①溶质的质量分数;②物质的量浓度。如图
所示为实验室浓硫酸的试剂瓶上的标签。
请思考:
(1)在图示的浓硫酸试剂瓶标签上,描述浓硫酸组成的物理量是哪个物理量?
提示:质量分数是描述溶液组成的物理量。
(2)若取1 L这种浓硫酸,其中含有溶质的质量是多少?物质的量是多少?
提示:1 L这种浓硫酸中所含硫酸溶质的质量:
1 000 mL×1.84 g·cm-3×98%=18.4×98 g=
1 803.2 g。物质的量: =18.4 mol。
(3)根据物质的量浓度的定义计算该浓硫酸的物质的量浓度。
提示:该浓硫酸的物质的量浓度为 =18.4 mol·L-1。
7.(新思维·新考向)鲜花是美丽的,但是美丽的鲜花的保鲜期却很短,在花瓶中
加入“鲜花保鲜剂”却可以延长鲜花的寿命。
下表是1 L“鲜花保鲜剂”的成分(其中阿司匹林不含K+,其存在也不会干扰成
分中其他离子的检验),回答下列问题
:
成分 蔗糖 硫酸钾阿司匹林高锰酸钾
质量/g 50.00 0.50 0.35 0.50
摩尔质量
342 174 180 158
/
(g·mol-1)
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是 ______________________ _
(填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为 __________mol·L-1。(只要求写
表达式,不用化简,不需计算)
(3)如图所示的仪器中,在配制一定物质的量浓度的“鲜花保鲜剂”溶液时肯定
不需要的是________(填字母),还缺少的玻璃仪器有____________(填仪器名
称)。(4)市面上,有一种营养液可用于无土栽培,该营养液中有KCl和K SO ,其中K+的
2 4
浓度为0.5 mol·L-1,Cl-的浓度为0.1 mol·L-1,则100 mL该营养液中n(S
)=________mol。
【解析】(1)c(蔗糖)= mol·L-1,c(硫酸钾)= mol·L-1,c(阿司匹林)=
mol·L-1,c(高锰酸
钾)= mol·L-1,所以“鲜花保鲜剂”中物质的量浓度最大的成分是蔗糖。
(2)c(K+)=2c(硫酸钾)+c(高锰酸钾)=( + )mol·L-1。
(3)配制一定物质的量浓度的溶液所需要的仪器包括:托盘天平、量筒、烧杯、
玻璃棒、容量瓶、胶头滴管,不需要使用烧瓶和分液漏斗。
(4)根据电荷守恒c(K+)=c(Cl-)+2c(S ),c(S )=0.2 mol·L-1,n(S )=
0.2 mol·L-1×0.1 L=0.02 mol。
答案:(1)蔗糖 (2)( + ) (3)ac 玻璃棒、烧杯 (4)0.02