文档内容
气体摩尔体积
(30分钟 50分)
一、选择题(本题包括4小题,每小题5分,共20分)
1.(2019·宁夏育才中学高一检测)下列关于决定物质体积的因素的说法,不正
确的是 ( )
A.物质的体积取决于粒子数目、粒子大小和粒子间距
B.相同条件下,粒子数相同的任何气体都具有相同体积
C.同温同压下,1 mol任何物质所占有的体积均相同
D.等质量的H ,压强越小、温度越高,气体所占体积越大
2
2.在标准状况下,0.4 mol HCl气体的体积是 ( )
A.22.4 L B.8.96 L
C.4.48 L D.11.2 L
3.以下说法中,正确的是 ( )
A.在标准状况下1 mol N 的体积是22.4 L·mol-1
2
B.在标准状况下SO 的摩尔体积约是22.4 L·mol-1
3
C.同温同压下的两种气体,只要所含微粒数目相同,则所占体积一定相同
D.一定状况下,N 的摩尔体积可能恰好为22.4 L·mol-1
2【补偿训练】
用N 表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A
A.含有N 个氦原子的氦气在标准状况下的体积约为11.2 L
A
B.25 ℃,1.01×105 Pa,32 g O 和O 的混合气体所含原子数为2.5N
2 3 A
C.标准状况下,11.2 L H O含有的原子数为1.5N
2 A
D.常温常压下,44 g CO 含有的原子数为3N
2 A
4.两份质量相同的CH 和NH 比较,下列结论错误的是 ( )
4 3
A.分子个数比为17∶16
B.同温同压下两种气体的体积之比是17∶16
C.氢原子个数比为17∶12
D.原子个数比为17∶16
【补偿训练】
如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )
A.所含原子数相等 B.气体密度相等
C.气体质量相等 D.摩尔质量相等
二、非选择题(本题包括1小题,共10分)5.(Ⅰ)设N 代表阿伏加德罗常数的值,完成下列填空:
A
(1)1 mol CH 含原子个数为______________;34 g H O 所含分子数目和原子数
4 2 2
目分别为________________________。
(2)标准状况下,0.5N 个CO分子所占有的体积为________L。
A
(3)标准状况下,33.6 L H 和CH 的混合气体所含的分子数目为________。
2 4
(Ⅱ)某双原子分子构成的气体,其摩尔质量为M g·mol-1,该气体的质量为m g,
阿伏加德罗常数为N ,则:
A
(1)该气体在标准状况下的体积为________L。
(2)该气体在标准状况下的密度为__g·L-1。
(3)该气体所含的原子总数为________个。
(4)该气体的一个分子的质量为________g。
一、选择题(本题包括2小题,每小题5分,共10分)
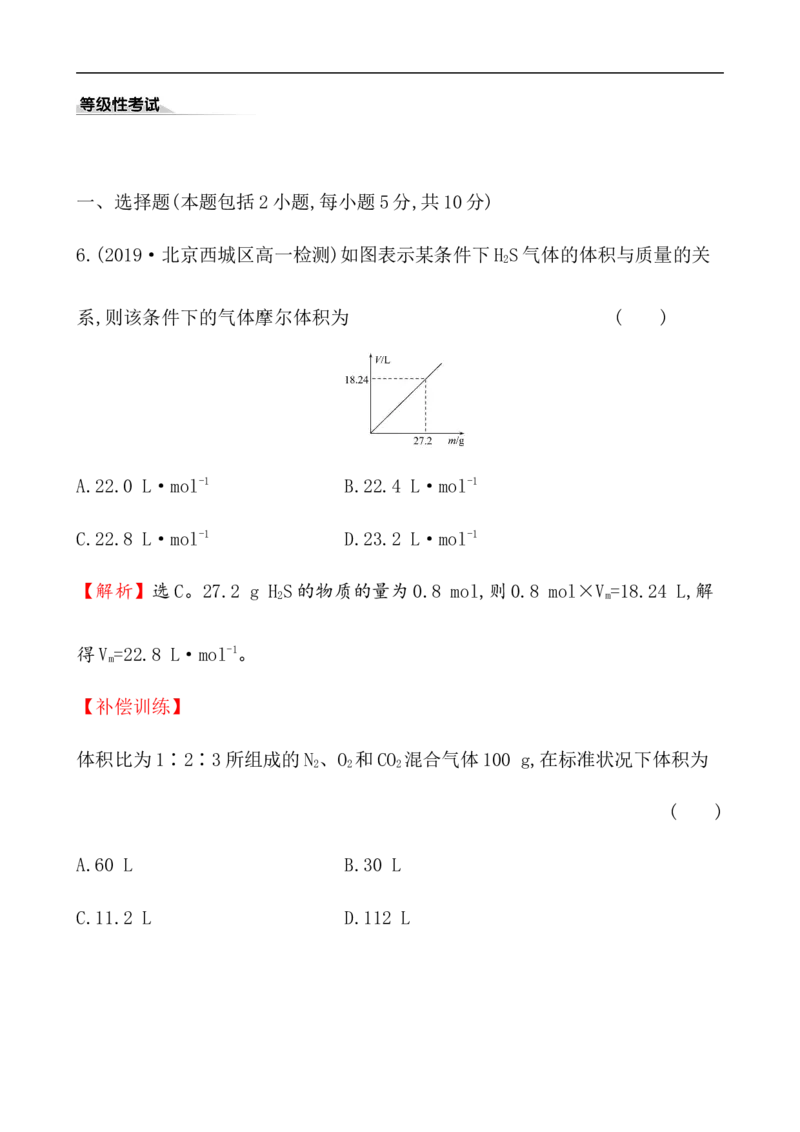
6.(2019·北京西城区高一检测)如图表示某条件下H S气体的体积与质量的关
2
系,则该条件下的气体摩尔体积为 ( )A.22.0 L·mol-1 B.22.4 L·mol-1
C.22.8 L·mol-1 D.23.2 L·mol-1
【补偿训练】
体积比为1∶2∶3所组成的N 、O 和CO 混合气体100 g,在标准状况下体积为
2 2 2
( )
A.60 L B.30 L
C.11.2 L D.112 L
7.(2019·朝阳高一检测)只给出表中甲和乙对应的量,不能用来求物质的量的
是
( )
甲 乙
A 物质的微粒数 阿伏加德罗常数
B 标准状况下气体摩尔体积 标准状况下气体体积
C 固体体积 固体密度
D 非标准状况下物质的质量 物质的摩尔质量
二、非选择题(本题包括1小题,共10分)8.(2019·济南高一检测)现有14.4 g CO和CO 的混合气体,在标准状况下其体
2
积为8.96 L。回答下列问题:
(1)混合气体中碳原子的个数为________(用N 表示阿伏加德罗常数的值)。
A
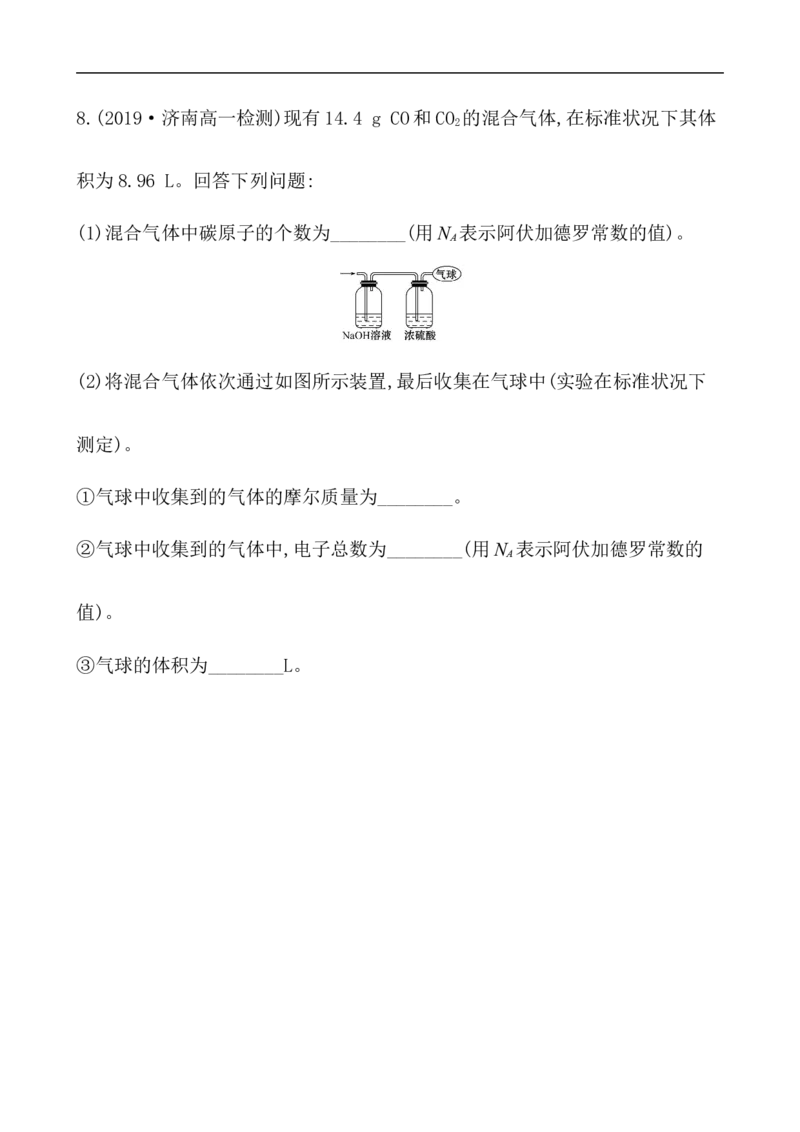
(2)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下
测定)。
①气球中收集到的气体的摩尔质量为________。
②气球中收集到的气体中,电子总数为________(用N 表示阿伏加德罗常数的
A
值)。
③气球的体积为________L。气体摩尔体积
(30分钟 50分)
一、选择题(本题包括4小题,每小题5分,共20分)
1.(2019·宁夏育才中学高一检测)下列关于决定物质体积的因素的说法,不正
确的是 ( )
A.物质的体积取决于粒子数目、粒子大小和粒子间距
B.相同条件下,粒子数相同的任何气体都具有相同体积
C.同温同压下,1 mol任何物质所占有的体积均相同
D.等质量的H ,压强越小、温度越高,气体所占体积越大
2
【解析】选C。从微观角度来说,物质的体积由粒子数目、粒子大小和粒子间距
决定, A正确;粒子数相同的气体的物质的量相同,相同条件下体积也相同, B正
确;C项结论只适用于气态物质, C错误;等质量的H ,压强越小、温度越高,气体
2
体积越大, D正确。
2.在标准状况下,0.4 mol HCl气体的体积是 ( )
A.22.4 L B.8.96 L
C.4.48 L D.11.2 L【解析】选B。V=0.4 mol×22.4 L·mol-1=8.96 L。
3.以下说法中,正确的是 ( )
A.在标准状况下1 mol N 的体积是22.4 L·mol-1
2
B.在标准状况下SO 的摩尔体积约是22.4 L·mol-1
3
C.同温同压下的两种气体,只要所含微粒数目相同,则所占体积一定相同
D.一定状况下,N 的摩尔体积可能恰好为22.4 L·mol-1
2
【解析】选D。标准状况下,1 mol N 的体积是22.4 L,A错误。标准状况下,SO
2 3
是固态,摩尔体积远小于22.4 L·mol-1,B错误。同温同压下,分子数相等则体
积相等,而微粒包括分子、原子、质子、电子等,C错误。在非标准状况下,可能
存在V =22.4 L·mol-1,D正确。
m
【补偿训练】
用N 表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A
A.含有N 个氦原子的氦气在标准状况下的体积约为11.2 L
A
B.25 ℃,1.01×105 Pa,32 g O 和O 的混合气体所含原子数为2.5N
2 3 A
C.标准状况下,11.2 L H O含有的原子数为1.5N
2 A
D.常温常压下,44 g CO 含有的原子数为3N
2 A【解析】选D。A项,氦为单原子分子,N 个氦原子在标准状况下的体积为22.4
A
L;B项,所含的氧原子数为2N ;C项,在标准状况下,水为液体。4.两份质量相同
A
的CH 和NH 比较,下列结论错误的是 ( )
4 3
A.分子个数比为17∶16
B.同温同压下两种气体的体积之比是17∶16
C.氢原子个数比为17∶12
D.原子个数比为17∶16
【解析】选D。设质量相同的CH 和NH 的物质的量分别是 、 ;分子个数比为
4 3
∶ =17∶16,故A正确;同温同压下两种气体的体积之比是 ∶ =17∶16,故
B正确;氢原子个数比为 ×4∶ ×3=17∶12,故C正确;原子个数比为 ×5∶
×4=85∶64,故D错误。
【补偿训练】
如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )
A.所含原子数相等 B.气体密度相等C.气体质量相等 D.摩尔质量相等
【解析】选A。同温同压时,体积相等的两瓶气体,具有相同的分子数,因为都是
双原子分子,故所含原子数相等,由于N 和O 的比例不固定,故两瓶气体的质量
2 2
不一定相等,密度和摩尔质量也不一定相等。
二、非选择题(本题包括1小题,共10分)
5.(Ⅰ)设N 代表阿伏加德罗常数的值,完成下列填空:
A
(1)1 mol CH 含原子个数为______________;34 g H O 所含分子数目和原子数
4 2 2
目分别为________________________。
(2)标准状况下,0.5N 个CO分子所占有的体积为________L。
A
(3)标准状况下,33.6 L H 和CH 的混合气体所含的分子数目为________。
2 4
(Ⅱ)某双原子分子构成的气体,其摩尔质量为M g·mol-1,该气体的质量为m g,
阿伏加德罗常数为N ,则:
A
(1)该气体在标准状况下的体积为________L。
(2)该气体在标准状况下的密度为__g·L-1。
(3)该气体所含的原子总数为________个。
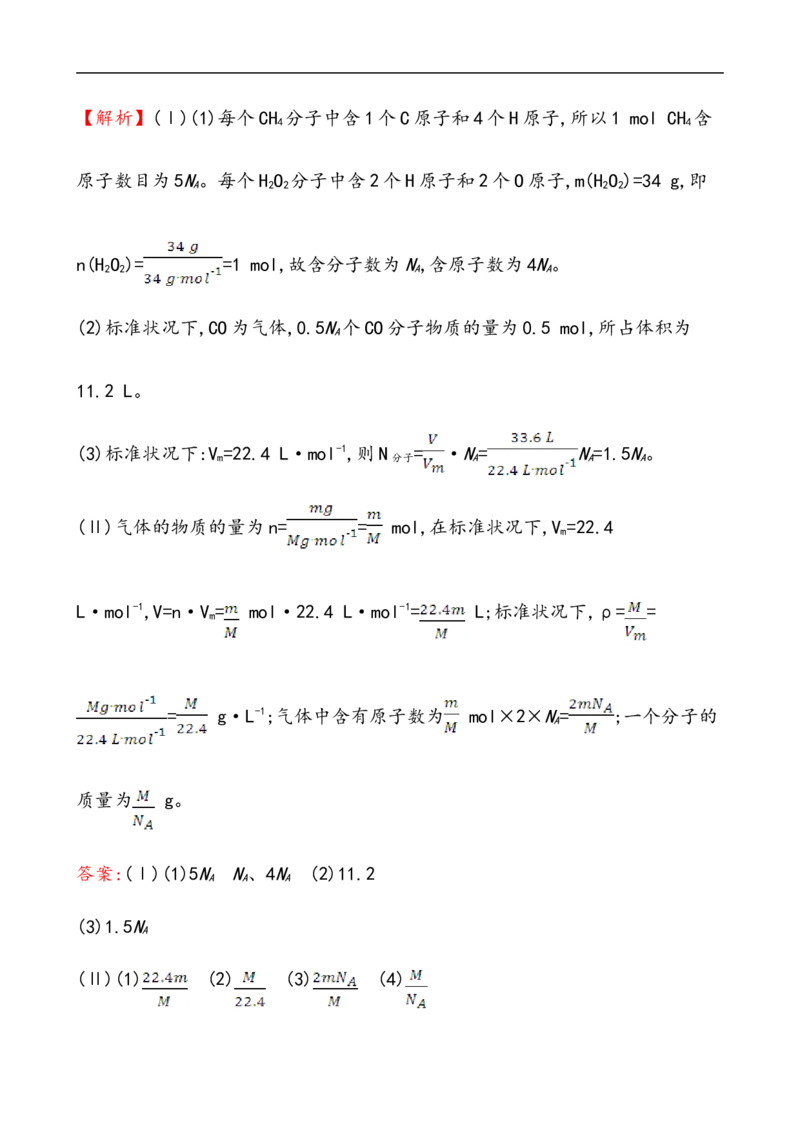
(4)该气体的一个分子的质量为________g。【解析】(Ⅰ)(1)每个CH 分子中含1个C原子和4个H原子,所以1 mol CH 含
4 4
原子数目为5N。每个H O 分子中含2个H原子和2个O原子,m(H O )=34 g,即
A 2 2 2 2
n(H O )= =1 mol,故含分子数为N,含原子数为4N。
2 2 A A
(2)标准状况下,CO为气体,0.5N个CO分子物质的量为0.5 mol,所占体积为
A
11.2 L。
(3)标准状况下:V =22.4 L·mol-1,则N = ·N= N=1.5N。
m 分子 A A A
(Ⅱ)气体的物质的量为n= = mol,在标准状况下,V =22.4
m
L·mol-1,V=n·V = mol·22.4 L·mol-1= L;标准状况下,ρ= =
m
= g·L-1;气体中含有原子数为 mol×2×N= ;一个分子的
A
质量为 g。
答案:(Ⅰ)(1)5N N、4N (2)11.2
A A A
(3)1.5N
A
(Ⅱ)(1) (2) (3) (4)一、选择题(本题包括2小题,每小题5分,共10分)
6.(2019·北京西城区高一检测)如图表示某条件下H S气体的体积与质量的关
2
系,则该条件下的气体摩尔体积为 ( )
A.22.0 L·mol-1 B.22.4 L·mol-1
C.22.8 L·mol-1 D.23.2 L·mol-1
【解析】选C。27.2 g H S的物质的量为0.8 mol,则0.8 mol×V =18.24 L,解
2 m
得V =22.8 L·mol-1。
m
【补偿训练】
体积比为1∶2∶3所组成的N 、O 和CO 混合气体100 g,在标准状况下体积为
2 2 2
( )
A.60 L B.30 L
C.11.2 L D.112 L【解析】选A。体积之比等于物质的量之比,令氮气的物质的量为x mol,则氧气、
二氧化碳的物质的量分别为2x mol、3x mol,所以:x mol×28 g·mol-1+2x
mol×
32 g·mol-1+3x mol×44 g·mol-1=100 g。解得,x= mol,所以标准状况下,
混合气体的体积为( mol+2× mol+3× mol)×22.4 L·mol-1=60 L。
7.(2019·朝阳高一检测)只给出表中甲和乙对应的量,不能用来求物质的量的
是
( )
甲 乙
A 物质的微粒数 阿伏加德罗常数
B 标准状况下气体摩尔体积 标准状况下气体体积
C 固体体积 固体密度
D 非标准状况下物质的质量 物质的摩尔质量
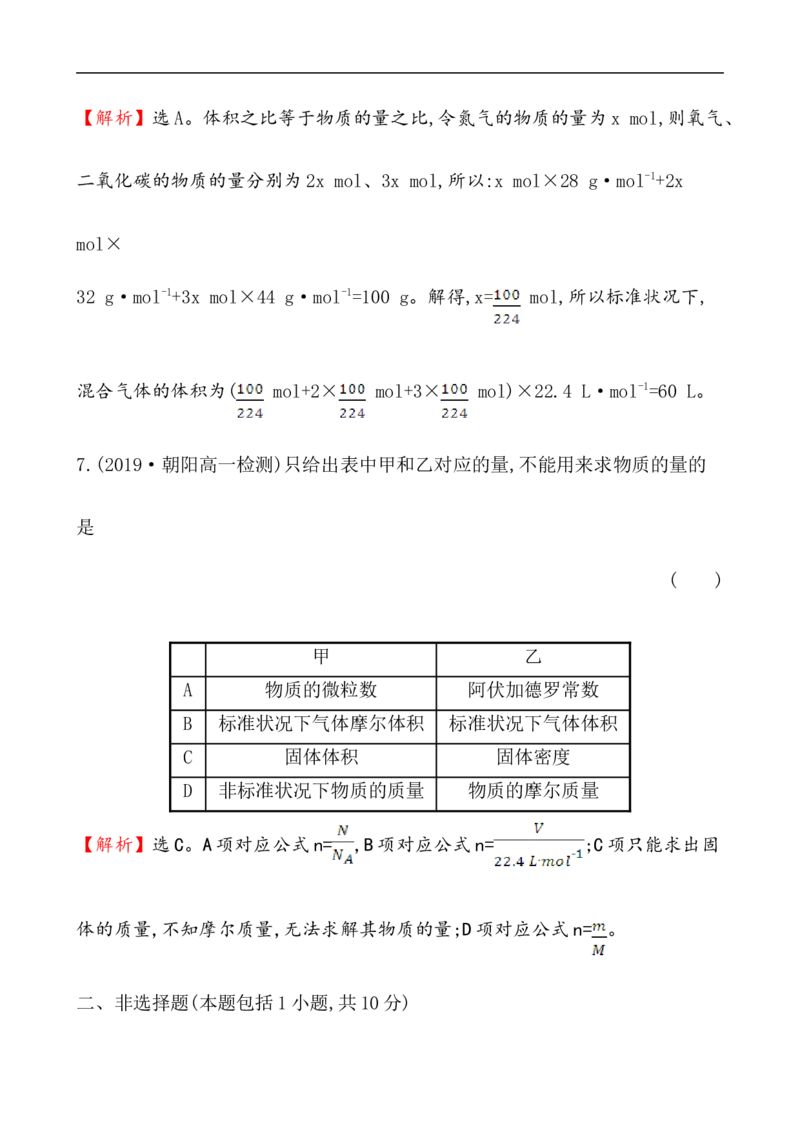
【解析】选C。A项对应公式n= ,B项对应公式n= ;C项只能求出固
体的质量,不知摩尔质量,无法求解其物质的量;D项对应公式n= 。
二、非选择题(本题包括1小题,共10分)8.(2019·济南高一检测)现有14.4 g CO和CO 的混合气体,在标准状况下其体
2
积为8.96 L。回答下列问题:
(1)混合气体中碳原子的个数为________(用N 表示阿伏加德罗常数的值)。
A
(2)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下
测定)。
①气球中收集到的气体的摩尔质量为________。
②气球中收集到的气体中,电子总数为________(用N 表示阿伏加德罗常数的
A
值)。
③气球的体积为________L。
【解析】(1) 0.4 mol CO和CO 的混合气体中,碳原子为0.4 mol,即0.4N。
2 A
(2)①将混合气体依次通过NaOH溶液和浓硫酸,则最后收集到的气体是CO。②
设原混合气体中CO的物质的量为n ,CO 的物质的量为n 。
1 2 2
则
解得因此气球中收集到0.2 mol CO,含有2.8 mol电子。③0.2 mol CO在标准状况
下的体积为4.48 L。
答案:(1) 0.4N
A
(2)①28 g·mol-1 ②2.8N ③4.48
A