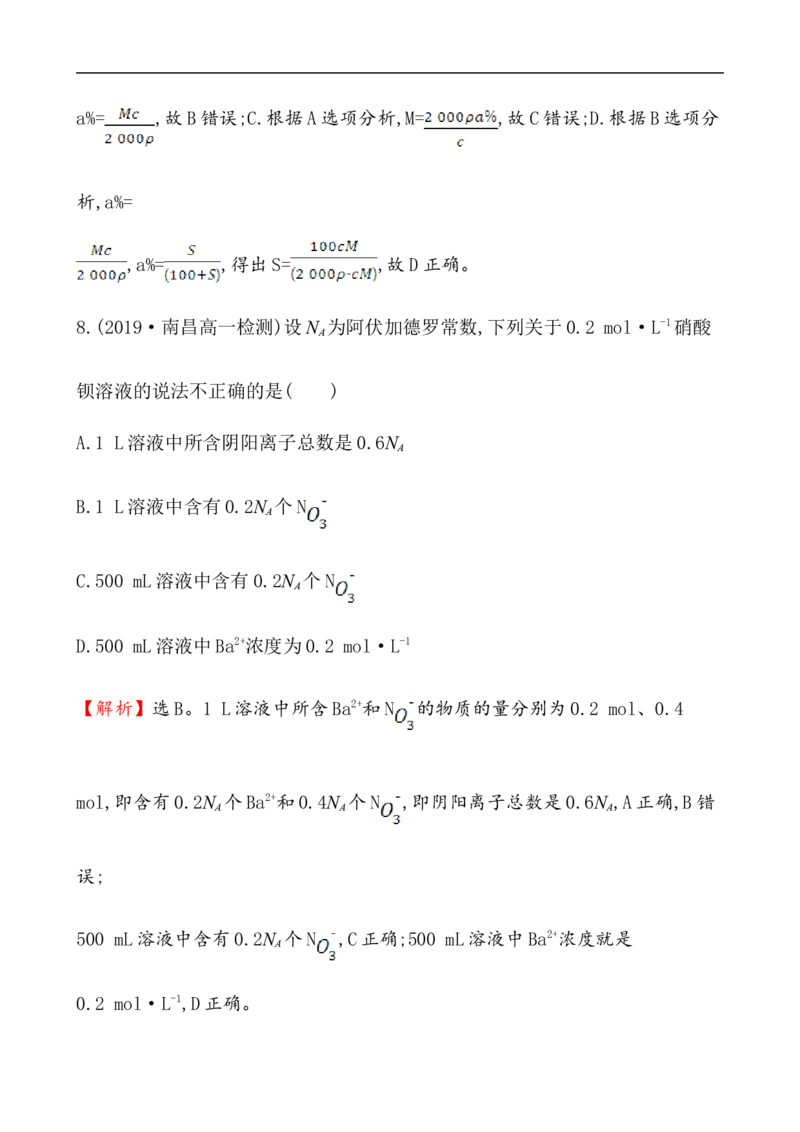文档内容
物质的量浓度
(30分钟 50分)
一、选择题(本题包括5小题,每小题4分,共20分)
1.容量瓶是配制一定物质的量浓度溶液的定量仪器。在容量瓶上标有的是
( )
①温度 ②浓度
③容量 ④压强
⑤刻度线
A.①③⑤ B.③⑤
C.①⑤ D.②③⑤
【补偿训练】
用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是 ( )
A.干燥的
B.瓶塞不漏水的
C.用欲配制的溶液润洗过的
D.以上三项均要求的
2.下列溶液中溶质的物质的量浓度为1 mol·L-1的是 ( )A.将40 g NaOH溶解在1 L水中
B.将1 L 10 mol·L-1的浓盐酸加入9 L水中
C.将22.4 L HCl气体溶于水配成1 L溶液
D.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL
【补偿训练】
下列有关实验用品的使用或操作的叙述中,正确的是 ( )
A.用托盘天平称出NaOH的质量16.00 g
B.容量瓶配制准确浓度的溶液,但不能作为反应容器使用
C.配制稀硫酸时,先向烧杯中注入浓硫酸,再加水稀释
D.称量NaOH固体时,将NaOH直接放在托盘上的纸上
3.(2019·石家庄高一检测)如图是实验室配制好的两瓶NaOH溶液的标签(14%
的NaOH溶液的密度为1.14 g·cm-3)。
14%的NaOH溶液的物质的量浓度及从瓶中取出20 mL该溶液中含有溶质的质量
分别是 ( )
A.4.0 mol·L-1 3.2 gB.2.0 mol·L-1 3.2 g
C.4.0 mol·L-1 6.4 g
D.2.0 mol·L-1 6.4 g
【补偿训练】
用10 mL 0.1 mol·L-1的BaCl 溶液恰好使相同体积的硫酸铁、硫酸锌和硫酸
2
钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质
的量浓度之比是 ( )
A.3∶2∶2 B.1∶2∶3
C.1∶3∶3 D.3∶1∶1
4.(2018·郑州高一检测)实验室需用480 mL 0.1 mol·L-1的硫酸铜溶液,以下
操作正确的是 ( )
A.称取7.68 g硫酸铜,加入480 mL水
B.称取12.5 g胆矾,配成480 mL溶液
C.称取8.0 g硫酸铜,加入500 mL水
D.称取12.5 g胆矾,配成500 mL溶液
5.物质的量浓度相同的NaCl、MgCl 、AlCl 三种溶液,当溶液的体积比为
2 3
3∶2∶1时,三种溶液中Cl-的物质的量之比为 ( )A.1∶1∶1 B.1∶2∶3
C.3∶2∶1 D.3∶4∶3
【补偿训练】
1.(2019·合肥高一检测)某MgCl 溶液的密度为1.6 g·cm-3,其中Mg2+的质量分
2
数为10%,300 mL该溶液中Cl-的物质的量约等于 ( )
A.4.0 mol B.3.0 mol
C.2.0 mol D.1.0 mol
2.(2019·北京四中高一检测)用98%的浓硫酸(密度为1.84 g·cm-3)配制100
mL l mol·L-1的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量
筒
②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻
璃棒,按使用仪器的先后顺序排列正确的是 ( )
A.④③⑦⑤⑥ B.②⑤⑦⑥
C.①③⑤⑥⑦ D.②⑥③⑦⑤⑥
二、非选择题(本题包括1小题,共10分)
6.(1)1 L K SO 和MgSO 的混合溶液中,含Mg2+ 2.4 g,S 的物质的量浓度为
2 4 41 mol·L-1,则MgSO 和K SO 的物质的量浓度分别是__________、
4 2 4
____________。
(2)常温下,10.0 mL 1.0 mol·L-1的H SO (aq),加水稀释到500 mL,所得
2 4
H SO (aq)的浓度为________mol·L-1;蒸发浓缩,使溶液的体积为2.40 mL,所得
2 4
H SO (aq)的浓度为____________________ mol·L-1。
2 4
【补偿训练】
1.将24.4 g氢氧化钠固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中氢氧化钠的物质的量浓度为_______________________。
(2)该溶液中氢氧化钠的质量分数为__________________。
(3)从该溶液中取出10 mL,含氢氧化钠的质量为____________,含氢氧化钠的物
质的量为____________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中氢氧化钠的物质的量
浓度为________。
2.(2019·山东潍坊高一检测)实验室欲用NaOH固体配制1.0 mol·L-1的NaOH
溶液240 mL,根据溶液的配制情况回答下列问题:(1)实验中除了用到托盘天平、药匙、量筒、烧杯外,还需用到的仪器有
____________________。
(2)通过计算可知,该实验需要称量NaOH________g;某同学欲称量NaOH的质量,
他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示,则烧杯的实际质
量为________g。
(3)使用容量瓶前必须进行的一步操作是________。
(4)在配制过程中,下列操作会使溶液浓度偏大的是________(填序号)。
A.转移溶液时不慎有少量洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
一、选择题(本题包括2小题,每小题4分,共8分)
7. 25 ℃时,将10 mL质量分数为50%(密度为1.4 g·cm-3)的硫酸稀释成100
mL。下列说法正确的是 ( )A.仰视容量瓶刻度线定容,所配溶液的浓度偏大
B.上述稀释过程所需要的蒸馏水为90 mL
C.质量分数为50%的硫酸溶液的物质的量浓度约为7.14 mol·L-1
D.上述10 mL稀硫酸中含溶质14 g
【补偿训练】
某温度下,物质X SO 的饱和溶液密度为ρ g·mL-1,c(X+)= c mol·L-1,溶质的
2 4
质量分数为a%,溶质的摩尔质量为M g·mol-1,溶解度为S g,下列表达式正确的
是
( )
A.c= B.a%=
C.M= D.S=
8.(2019·南昌高一检测)设N 为阿伏加德罗常数,下列关于0.2 mol·L-1硝酸
A
钡溶液的说法不正确的是( )
A.1 L溶液中所含阴阳离子总数是0.6N
A
B.1 L溶液中含有0.2N 个N
A
C.500 mL溶液中含有0.2N 个N
AD.500 mL溶液中Ba2+浓度为0.2 mol·L-1
二、非选择题(本题包括1小题,共12分)
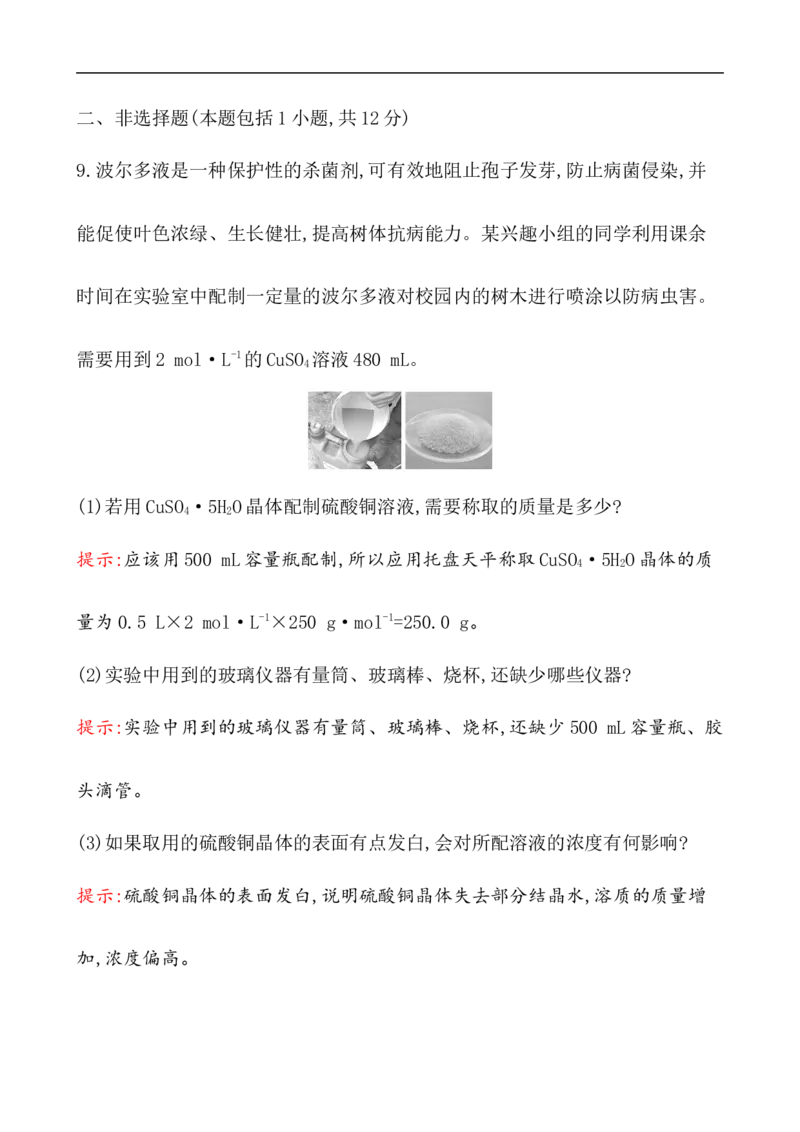
9.波尔多液是一种保护性的杀菌剂,可有效地阻止孢子发芽,防止病菌侵染,并
能促使叶色浓绿、生长健壮,提高树体抗病能力。某兴趣小组的同学利用课余
时间在实验室中配制一定量的波尔多液对校园内的树木进行喷涂以防病虫害。
需要用到2 mol·L-1的CuSO 溶液480 mL。
4
(1)若用CuSO ·5H O晶体配制硫酸铜溶液,需要称取的质量是多少?
4 2
(2)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少哪些仪器?
(3)如果取用的硫酸铜晶体的表面有点发白,会对所配溶液的浓度有何影响?
(4)若从所配溶液中取出20 mL溶液,加水稀释至50 mL,则所得溶液中S 的
浓度是多少?其中含有的溶质CuSO 的质量是多少?
4物质的量浓度
(30分钟 50分)
一、选择题(本题包括5小题,每小题4分,共20分)
1.容量瓶是配制一定物质的量浓度溶液的定量仪器。在容量瓶上标有的是
( )
①温度 ②浓度
③容量 ④压强
⑤刻度线
A.①③⑤ B.③⑤
C.①⑤ D.②③⑤
【解析】选A。容量瓶上标有:温度、容量、刻度线。
【补偿训练】
用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是 ( )
A.干燥的
B.瓶塞不漏水的
C.用欲配制的溶液润洗过的
D.以上三项均要求的【解析】选B。容量瓶使用前必须检漏,B正确;容量瓶是定容仪器,内含少量蒸
馏水不会产生误差,但不能用欲配溶液润洗。2.下列溶液中溶质的物质的量浓
度为1 mol·L-1的是 ( )
A.将40 g NaOH溶解在1 L水中
B.将1 L 10 mol·L-1的浓盐酸加入9 L水中
C.将22.4 L HCl气体溶于水配成1 L溶液
D.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL
【解析】选D。物质的量浓度是用单位体积的溶液中含有溶质的物质的量来表
示的溶液组成。A.1 L是溶剂的体积,不是溶液的体积,错误。B.物质的微粒间
有间隔,所以体积不能相加,1 L 10 mol·L-1的浓盐酸加入9 L水中得到的溶液
体积不是10 L,错误。C.气体的体积受温度的影响较大,不指明体积是在什么条
件下的没有意义,错误。D.c(NaOH)=( )/V=( )÷0.25 L=1 mol·L-1,
正确。
【补偿训练】
下列有关实验用品的使用或操作的叙述中,正确的是 ( )
A.用托盘天平称出NaOH的质量16.00 gB.容量瓶配制准确浓度的溶液,但不能作为反应容器使用
C.配制稀硫酸时,先向烧杯中注入浓硫酸,再加水稀释
D.称量NaOH固体时,将NaOH直接放在托盘上的纸上
【解析】选B。托盘天平称量物质的质量只能精确到0.1 g,A项错误;容量瓶只
能用于配制特定体积的溶液,不能作反应容器,B项正确;稀释浓硫酸应将浓硫酸
向水中加入,C项错误;NaOH具有吸水性和腐蚀性,称量时应在小烧杯中进行,D
项错误。
3.(2019·石家庄高一检测)如图是实验室配制好的两瓶NaOH溶液的标签(14%
的NaOH溶液的密度为1.14 g·cm-3)。
14%的NaOH溶液的物质的量浓度及从瓶中取出20 mL该溶液中含有溶质的质量
分别是 ( )
A.4.0 mol·L-1 3.2 g
B.2.0 mol·L-1 3.2 g
C.4.0 mol·L-1 6.4 g
D.2.0 mol·L-1 6.4 g【解析】选A。根据c= = mol·L-1≈4.0 mol·L-1,20 mL
该溶液中含有溶质的质量是0.02 L×4.0 mol·L-1×40 g·mol-1=3.2 g。
【补偿训练】
用10 mL 0.1 mol·L-1的BaCl 溶液恰好使相同体积的硫酸铁、硫酸锌和硫酸
2
钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质
的量浓度之比是 ( )
A.3∶2∶2 B.1∶2∶3
C.1∶3∶3 D.3∶1∶1
【解析】选C。根据质量守恒定律,三种溶液中S 的物质的量相同,结合化学
式:Fe (SO ) 、ZnSO 、K SO 可知三者的物质的量之比为1∶3∶3 ,溶液体积相
2 4 3 4 2 4
同,故浓度之比为1∶3∶3 。
4.(2018·郑州高一检测)实验室需用480 mL 0.1 mol·L-1的硫酸铜溶液,以下
操作正确的是 ( )
A.称取7.68 g硫酸铜,加入480 mL水
B.称取12.5 g胆矾,配成480 mL溶液
C.称取8.0 g硫酸铜,加入500 mL水D.称取12.5 g胆矾,配成500 mL溶液
【解析】选D。此题易错选A或C。首先明确实验室没有480 mL的容量瓶,因此
配制480 mL溶液只能选取500 mL的容量瓶,配完后再从中取出480 mL。其次
计算溶质的物质的量时不能用480 mL,而必须用500 mL来计算,因为实际配制
溶液的体积是500 mL。若直接称量硫酸铜,则溶质的质量是
m(CuSO )=n(CuSO )·
4 4
M(CuSO )=0.5 L×0.1 mol·L-1×160 g·mol-1=8.0 g;若直接称量胆矾,则溶质
4
的质量是m(CuSO ·5H O)=n(CuSO ·5H O)·M(CuSO ·5H O)=0.5 L×0.1
4 2 4 2 4 2
mol·L-1×
250 g·mol-1=12.5 g。最后容量瓶只有一条刻度线,当加水至凹液面与刻度线
相切时,此时溶液的体积恰好为500 mL,但所加水的体积并不是500 mL。
5.物质的量浓度相同的NaCl、MgCl 、AlCl 三种溶液,当溶液的体积比为
2 3
3∶2∶1时,三种溶液中Cl-的物质的量之比为 ( )
A.1∶1∶1 B.1∶2∶3
C.3∶2∶1 D.3∶4∶3【解析】选D。设物质的量浓度均为x,则三种溶液中Cl-物质的量分别为3x、
4x、3x。
【补偿训练】
1.(2019·合肥高一检测)某MgCl 溶液的密度为1.6 g·cm-3,其中Mg2+的质量分
2
数为10%,300 mL该溶液中Cl-的物质的量约等于 ( )
A.4.0 mol B.3.0 mol
C.2.0 mol D.1.0 mol
【解析】选A。方法一:由物质的量浓度和质量分数的换算关系式可知:
c(Mg2+)= = ≈6.67 mol·L-1,则
c(Cl-)=2c(Mg2+)≈13.34 mol·L-1,n(Cl-)=13.34 mol·L-1×0.3 L≈4.0 mol。
方法二:由Mg2+的质量分数10%可知,100 g溶液中含有10 g Mg2+,则c(Mg2+)=
≈6.67 mol·L-1,n(Mg2+)=6.67 mol·L-1×0.3 L≈2.0
mol,n(Cl-)=4.0 mol。
方法三:m(Mg2+)=300 mL×1.6 g·cm-3×10% =48 g,n(Mg2+)=48 g÷24
g·mol-1=2 mol,溶液中n(Cl-)=2n(Mg2+)=2 mol×2=4 mol。2.(2019·北京四中高一检测)用98%的浓硫酸(密度为1.84 g·cm-3)配制100
mL l mol·L-1的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量
筒
②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻
璃棒,按使用仪器的先后顺序排列正确的是 ( )
A.④③⑦⑤⑥ B.②⑤⑦⑥
C.①③⑤⑥⑦ D.②⑥③⑦⑤⑥
【解析】选D。98%的浓硫酸的物质的量浓度为c= =
mol·L-1=18.4 mol·L-1,配制1 mol·L-1的稀硫酸100 mL,需要
浓硫酸的体积为V= ≈0.0054 L,即5.4 mL,应选择10 mL量筒和胶
头滴管,实验时用10 mL量筒量取5.4 mL浓硫酸,因配制一定物质的量浓度的溶
液需要量取、溶解、移液、洗涤、定容、摇匀等操作,所以正确顺序为
②⑥③⑦⑤⑥。
二、非选择题(本题包括1小题,共10分)
6.(1)1 L K SO 和MgSO 的混合溶液中,含Mg2+ 2.4 g,S 的物质的量浓度为
2 4 41 mol·L-1,则MgSO 和K SO 的物质的量浓度分别是__________、
4 2 4
____________。
(2)常温下,10.0 mL 1.0 mol·L-1的H SO (aq),加水稀释到500 mL,所得
2 4
H SO (aq)的浓度为________mol·L-1;蒸发浓缩,使溶液的体积为2.40 mL,所得
2 4
H SO (aq)的浓度为____________________ mol·L-1。
2 4
【解析】(1)n(Mg2+)= =0.1 mol,
则c(MgSO )= =0.1 mol·L-1。
4
MgSO 提供的c(S )=0.1 mol·L-1,则K SO 提供的c(S )=1 mol·L-1-
4 2 4
0.1 mol·L-1=0.9 mol·L-1,所以c(K SO )=0.9 mol·L-1。
2 4
(2)根据溶液的稀释定律,溶液稀释或浓缩前后溶质的质量和物质的量不
变:c V =c V =c V 。稀释到500 mL时:c (H SO )= =
1 1 2 2 3 3 2 2 4
=0.02 mol·L-1;
浓缩到2.40 mL时:c (H SO )=
3 2 4
=≈4.2 mol·L-1。
答案:(1)0.1 mol·L-1 0.9 mol·L-1
(2)0.02 4.2
【补偿训练】
1.将24.4 g氢氧化钠固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中氢氧化钠的物质的量浓度为_______________________。
(2)该溶液中氢氧化钠的质量分数为__________________。
(3)从该溶液中取出10 mL,含氢氧化钠的质量为____________,含氢氧化钠的物
质的量为____________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中氢氧化钠的物质的量
浓度为________。
【解析】(1)24.4 g 氢氧化钠的物质的量为0.61 mol,c(NaOH)=0.61 mol÷
0.1 L=6.1 mol·L-1。
(2)100 mL氢氧化钠溶液的质量为100 mL×1.219 g·mL-1=121.9 g;氢氧化钠
的质量分数为 ×100%≈20%。(3)由于整个溶液都是均匀的,所以这10 mL溶液与原100 mL溶液相比,氢氧化
钠的质量分数和溶液的密度均相同,但氢氧化钠的质量和物质的量均为原来的
。
(4)这10 mL溶液中氢氧化钠的物质的量为0.061 mol,稀释到100 mL以后,氢
氧化钠的物质的量浓度为0.061 mol÷0.1 L=0.61 mol·L-1。
答案:(1)6.1 mol·L-1 (2)20%
(3)2.44 g 0.061 mol (4)0.61 mol·L-1
2.(2019·山东潍坊高一检测)实验室欲用NaOH固体配制1.0 mol·L-1的NaOH
溶液240 mL,根据溶液的配制情况回答下列问题:
(1)实验中除了用到托盘天平、药匙、量筒、烧杯外,还需用到的仪器有
____________________。
(2)通过计算可知,该实验需要称量NaOH________g;某同学欲称量NaOH的质量,
他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示,则烧杯的实际质
量为________g。(3)使用容量瓶前必须进行的一步操作是________。
(4)在配制过程中,下列操作会使溶液浓度偏大的是________(填序号)。
A.转移溶液时不慎有少量洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
【解析】(1)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀
等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到
250 mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2 cm时,改用
胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、量筒、烧杯、玻璃棒、
250 mL容量瓶、胶头滴管。
(2)因配制溶液的体积为240 mL,而容量瓶的规格没有240 mL,只能选用250
mL,NaOH的质量m=cVM=1.0 mol·L-1×0.25 L×40 g·mol-1=10.0 g,因天平的
称量原理为左盘物体的质量=右盘物体的质量+游码的读数,所以烧杯的实际质
量为27.4 g。(4)A错,转移溶液时不慎有少量洒到容量瓶外面,溶质的质量减少,浓度偏小;B
对,定容时俯视刻度线,溶液的体积偏小,浓度偏高;C对,未冷却到室温就将溶液
转移到容量瓶并定容,冷却下来溶液的体积偏小,浓度偏高;D错,定容后塞上瓶
塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,溶液的体积偏大,浓度
偏小。
答案:(1)玻璃棒、250 mL容量瓶、胶头滴管
(2)10.0 27.4 (3)检查容量瓶是否漏水 (4)BC
一、选择题(本题包括2小题,每小题4分,共8分)
7. 25 ℃时,将10 mL质量分数为50%(密度为1.4 g·cm-3)的硫酸稀释成100
mL。下列说法正确的是 ( )
A.仰视容量瓶刻度线定容,所配溶液的浓度偏大
B.上述稀释过程所需要的蒸馏水为90 mL
C.质量分数为50%的硫酸溶液的物质的量浓度约为7.14 mol·L-1
D.上述10 mL稀硫酸中含溶质14 g
【解析】选C。俯视容量瓶刻度线定容,导致溶液的体积偏小,所配溶液的浓度
偏大,故A项错误;上述稀释后溶液的密度不知,所以无法计算所需要的蒸馏水的体积或质量,故B项错误;根据c= = mol·L-1≈7.14
mol·L-1,所以质量分数为50%的硫酸溶液的物质的量浓度约为7.14 mol·L-1,
故C项正确;稀释过程中溶质的质量不变,所以上述10 mL稀硫酸中含溶质1.4
g·cm-3×
10 cm3×50%=7.0 g,故D项错误。
【补偿训练】
某温度下,物质X SO 的饱和溶液密度为ρ g·mL-1,c(X+)= c mol·L-1,溶质的
2 4
质量分数为a%,溶质的摩尔质量为M g·mol-1,溶解度为S g,下列表达式正确的
是
( )
A.c= B.a%=
C.M= D.S=
【解析】选D。A.X SO 的浓度为 mol·L-1,则X+浓度为
2 4
mol·L-1,或者为 mol·L-1,故A错误;B.根据A选项分析,溶质的质量分数a%= ,故B错误;C.根据A选项分析,M= ,故C错误;D.根据B选项分
析,a%=
,a%= ,得出S= ,故D正确。
8.(2019·南昌高一检测)设N 为阿伏加德罗常数,下列关于0.2 mol·L-1硝酸
A
钡溶液的说法不正确的是( )
A.1 L溶液中所含阴阳离子总数是0.6N
A
B.1 L溶液中含有0.2N 个N
A
C.500 mL溶液中含有0.2N 个N
A
D.500 mL溶液中Ba2+浓度为0.2 mol·L-1
【解析】选B。1 L溶液中所含Ba2+和N 的物质的量分别为0.2 mol、0.4
mol,即含有0.2N 个Ba2+和0.4N 个N ,即阴阳离子总数是0.6N ,A正确,B错
A A A
误;
500 mL溶液中含有0.2N 个N ,C正确;500 mL溶液中Ba2+浓度就是
A
0.2 mol·L-1,D正确。二、非选择题(本题包括1小题,共12分)
9.波尔多液是一种保护性的杀菌剂,可有效地阻止孢子发芽,防止病菌侵染,并
能促使叶色浓绿、生长健壮,提高树体抗病能力。某兴趣小组的同学利用课余
时间在实验室中配制一定量的波尔多液对校园内的树木进行喷涂以防病虫害。
需要用到2 mol·L-1的CuSO 溶液480 mL。
4
(1)若用CuSO ·5H O晶体配制硫酸铜溶液,需要称取的质量是多少?
4 2
提示:应该用500 mL容量瓶配制,所以应用托盘天平称取CuSO ·5H O晶体的质
4 2
量为0.5 L×2 mol·L-1×250 g·mol-1=250.0 g。
(2)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少哪些仪器?
提示:实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少500 mL容量瓶、胶
头滴管。
(3)如果取用的硫酸铜晶体的表面有点发白,会对所配溶液的浓度有何影响?
提示:硫酸铜晶体的表面发白,说明硫酸铜晶体失去部分结晶水,溶质的质量增
加,浓度偏高。(4)若从所配溶液中取出20 mL溶液,加水稀释至50 mL,则所得溶液中S 的浓
度是多少?其中含有的溶质CuSO 的质量是多少?
4
提示:20 mL溶液加水稀释至50 mL,即稀释了2.5倍,因此稀释后的浓度为原来
的 ,为2 mol·L-1× =0.8 mol·L-1。所含有的溶质CuSO 的质量为0.02
4
L×
2 mol·L-1×160 g·mol-1=6.4 g。