文档内容
氯及其化合物
第2课时
◆ 教学目标与核心素养
证据推理与模型认知:通过对实验室制取氯气的实验装置和实验过程的学习,建立实验室
制取气体的装置和流程的模型,掌握利用该模型分析其他气体的实验室制取的方法。
科学探究与创新意识:通过完成氯离子检验的相关实验,使学生了解实验探究的一般过程
与一般方法,培养初步的科学探究能力。
科学精神与社会责任:通过对于氯气制取过程中氯气的尾气处理和吸收,培养学生的环保
意识,理解化学家在环境保护中的社会责任。
◆ 教学重难点
氯气的实验室制法和氯离子检验。
◆ 教学过程
一、导入新课
【引入】在上节课的学习中同学们已经学习了氯气的主要物理性质和化学性质,也知道了
氯气的用途,氯气有什么用途呢?(自来水消毒剂、制氯化氢、制漂白液、制漂白粉),
氯气是一种重要的化工原料,那么氯气是如何得到的?
二、讲授新课
【板书】氯及其化合物
二、氯气的制取
【投影】氯及其化合物
二、氯气的制取
【讲解】上节课我们曾经提过,氯气的发现应该归功于瑞典化学家舍勒,舍勒发现氯气是
在1774年,当时他正在研究软锰矿(即二氧化锰),当他使软锰矿与浓盐酸混合并加热时,产
生了一种有强烈刺激性气味的黄绿色气体,这种气体就是氯气。其反应方程式为MnO +
2
4HCl(浓) MnCl + Cl ↑ + 2H O,现在这种方法仍然是实验室制取氯气的重要方法之一。
2 2 2
需要注意的是,这种方法这个使用的必须是浓盐酸,稀盐酸是无法与二氧化锰反应的。
【学生活动】同学之间互相交流根据初中学习过的气体实验室制法填写下表,找几位同学
来复述其填写的结果。
气体 制取原理(方程式) 反应物状态 反应条件 装置图【投影】
气体 制取原理(方程式) 反应物状态 反应条件 装置图
== 加 == 热 ===== 点 == 燃 === —— 高 — 温 —→ —— 高 — 温 —→ — 高 — 温 —— 、 — 高 — 压 → == M = n = O =2=
催化剂 O 催化 2 剂 KClO 3 △ 2KCl + 3O 2 ↑ 固体+固体 加热
2
2KMnO KMnO + MnO + O↑
4 2 4 2 2
O 2 2H 2 O 2 2H 2 O + O 2 ↑ 固体+液体 不加热
CO CaCO + 2HCl = CaCl + CO↑+HO 固体+液体 不加热
2 3 2 2 2
【讲解】通过上面的表格,同学们可以分析得到实验室制取气体的装置,应该根据反应物
的状态和反应条件来决定。固体+固体加热的反应会选取大试管、酒精灯加热(大试管管
口略向下倾斜),固体+液体不加热的反应会选取分液漏斗和锥形瓶(或者圆底烧瓶)的
装置。
【设疑】根据上述表格分类,指出实验室制取氯气的反应物状态和反应条件。(固体+液
体,加热)应该选用上面的哪个装置?(都不可以)
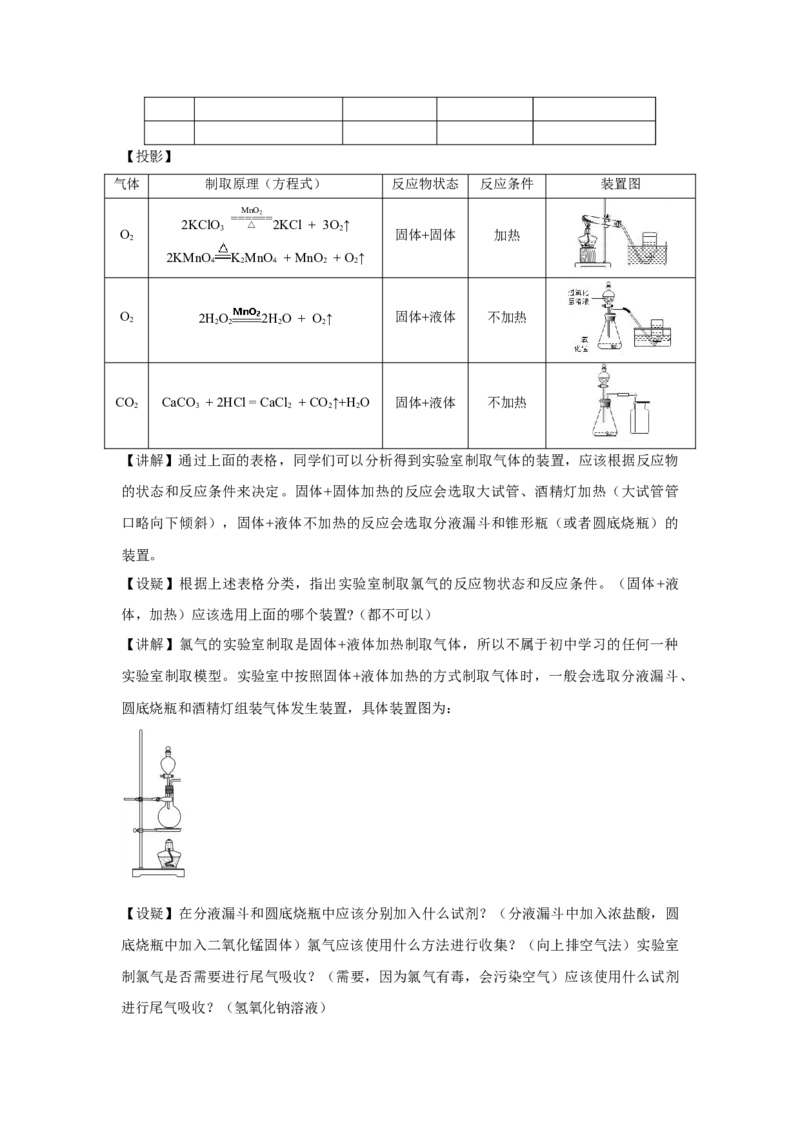
【讲解】氯气的实验室制取是固体+液体加热制取气体,所以不属于初中学习的任何一种
实验室制取模型。实验室中按照固体+液体加热的方式制取气体时,一般会选取分液漏斗、
圆底烧瓶和酒精灯组装气体发生装置,具体装置图为:
【设疑】在分液漏斗和圆底烧瓶中应该分别加入什么试剂?(分液漏斗中加入浓盐酸,圆
底烧瓶中加入二氧化锰固体)氯气应该使用什么方法进行收集?(向上排空气法)实验室
制氯气是否需要进行尾气吸收?(需要,因为氯气有毒,会污染空气)应该使用什么试剂
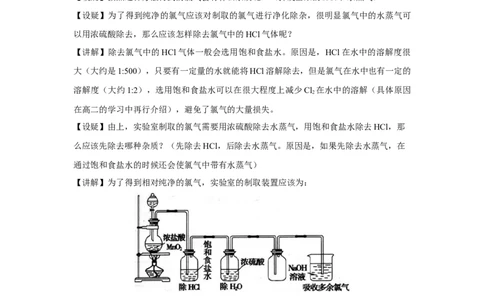
进行尾气吸收?(氢氧化钠溶液)【讲解】所以实验室制取氯气的装置应该是:
【设疑】按照这种方法得到的氯气会有什么杂质呢?(挥发出来的HCl和水蒸气)
【设疑】为了得到纯净的氯气应该对制取的氯气进行净化除杂,很明显氯气中的水蒸气可
以用浓硫酸除去,那么应该怎样除去氯气中的HCl气体呢?
【讲解】除去氯气中的HCl气体一般会选用饱和食盐水。原因是,HCl在水中的溶解度很
大(大约是1:500),只要有一定量的水就能将HCl溶解除去,但是氯气在水中也有一定的
溶解度(大约1:2),选用饱和食盐水可以在很大程度上减少Cl 在水中的溶解(具体原因
2
在高二的学习中再行介绍),避免了氯气的大量损失。
【设疑】由上,实验室制取的氯气需要用浓硫酸除去水蒸气,用饱和食盐水除去HCl,那
么应该先除去哪种杂质?(先除去HCl,后除去水蒸气。原因是,如果先除去水蒸气,在
通过饱和食盐水的时候还会使氯气中带有水蒸气)
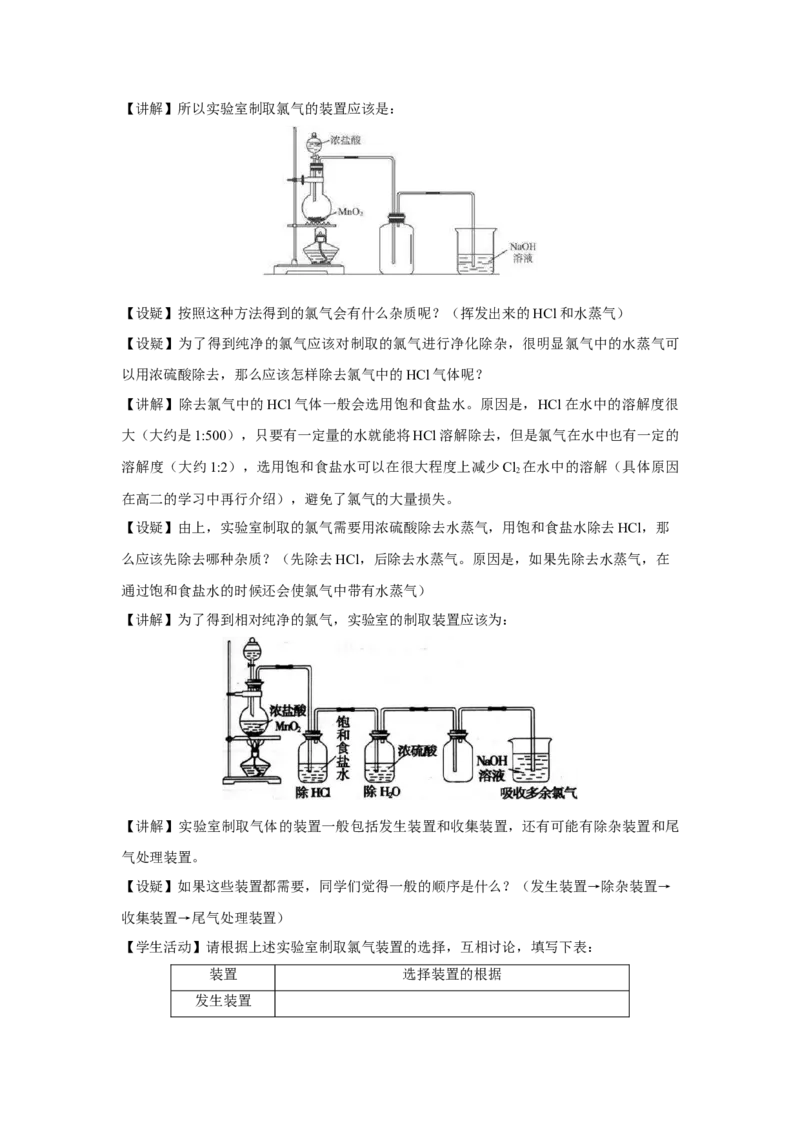
【讲解】为了得到相对纯净的氯气,实验室的制取装置应该为:
【讲解】实验室制取气体的装置一般包括发生装置和收集装置,还有可能有除杂装置和尾
气处理装置。
【设疑】如果这些装置都需要,同学们觉得一般的顺序是什么?(发生装置→除杂装置→
收集装置→尾气处理装置)
【学生活动】请根据上述实验室制取氯气装置的选择,互相讨论,填写下表:
装置 选择装置的根据
发生装置除杂装置
收集装置
尾气处理装置
【投影】
装置 选择装置的根据
发生装置 反应物状态及反应条件
除杂装置 气体和杂质的性质
收集装置 气体密度、气体在水中的溶解度、是否与水反应
尾气处理装置 气体性质
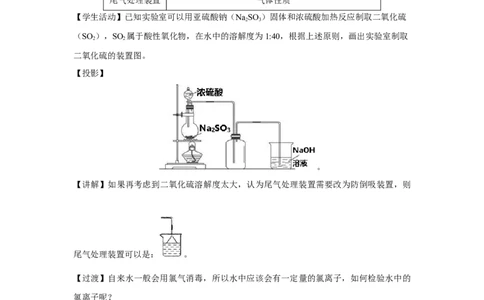
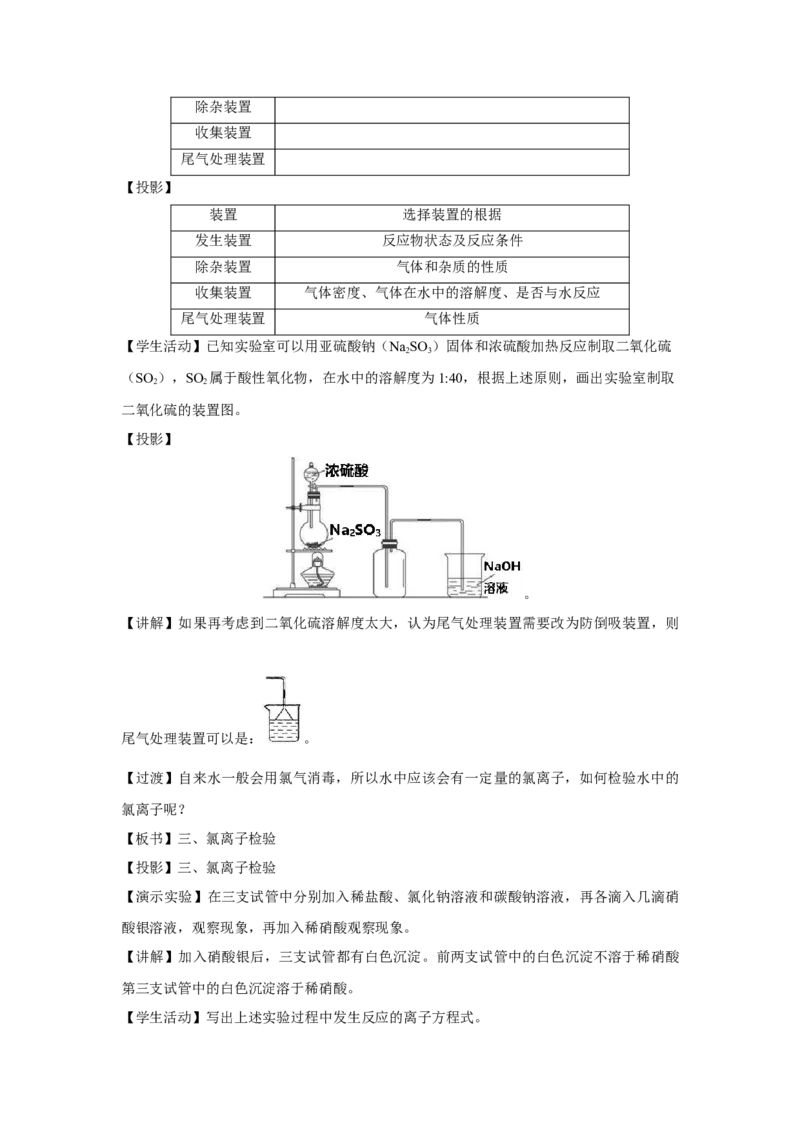
【学生活动】已知实验室可以用亚硫酸钠(NaSO )固体和浓硫酸加热反应制取二氧化硫
2 3
(SO ),SO 属于酸性氧化物,在水中的溶解度为1:40,根据上述原则,画出实验室制取
2 2
二氧化硫的装置图。
【投影】
。
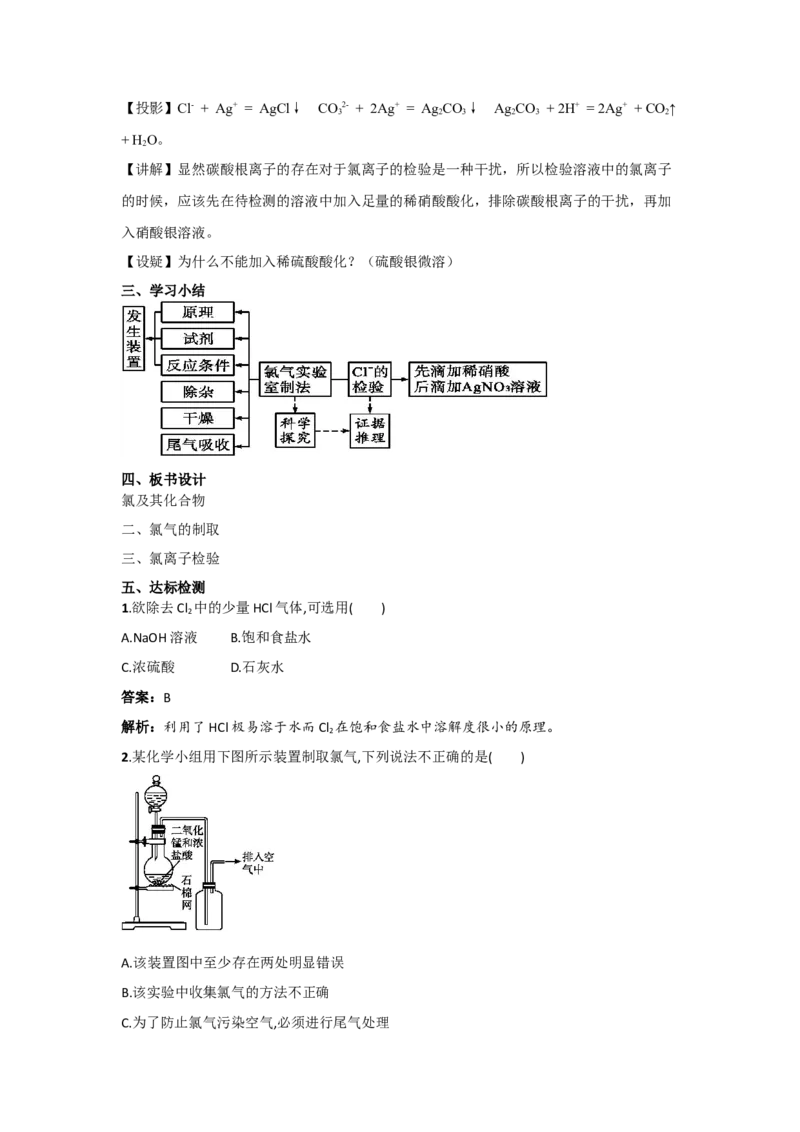
【讲解】如果再考虑到二氧化硫溶解度太大,认为尾气处理装置需要改为防倒吸装置,则
尾气处理装置可以是: 。
【过渡】自来水一般会用氯气消毒,所以水中应该会有一定量的氯离子,如何检验水中的
氯离子呢?
【板书】三、氯离子检验
【投影】三、氯离子检验
【演示实验】在三支试管中分别加入稀盐酸、氯化钠溶液和碳酸钠溶液,再各滴入几滴硝
酸银溶液,观察现象,再加入稀硝酸观察现象。
【讲解】加入硝酸银后,三支试管都有白色沉淀。前两支试管中的白色沉淀不溶于稀硝酸
第三支试管中的白色沉淀溶于稀硝酸。
【学生活动】写出上述实验过程中发生反应的离子方程式。【投影】Cl- + Ag+ = AgCl↓ CO2- + 2Ag+ = Ag CO↓ Ag CO + 2H+ = 2Ag+ + CO↑
3 2 3 2 3 2
+ H O。
2
【讲解】显然碳酸根离子的存在对于氯离子的检验是一种干扰,所以检验溶液中的氯离子
的时候,应该先在待检测的溶液中加入足量的稀硝酸酸化,排除碳酸根离子的干扰,再加
入硝酸银溶液。
【设疑】为什么不能加入稀硫酸酸化?(硫酸银微溶)
三、学习小结
四、板书设计
氯及其化合物
二、氯气的制取
三、氯离子检验
五、达标检测
1.欲除去Cl 中的少量HCl气体,可选用( )
2
A.NaOH溶液 B.饱和食盐水
C.浓硫酸 D.石灰水
答案:B
解析:利用了HCl极易溶于水而Cl 在饱和食盐水中溶解度很小的原理。
2
2.某化学小组用下图所示装置制取氯气,下列说法不正确的是( )
A.该装置图中至少存在两处明显错误
B.该实验中收集氯气的方法不正确
C.为了防止氯气污染空气,必须进行尾气处理D.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出
答案:B
3.在实验室中用浓盐酸与MnO 共热制取Cl 并进行相关实验。下列收集Cl 的正确装置是(
2 2 2
)
答案:C
解析:集气瓶用单孔橡胶塞塞紧,只能进气,不能排气,则瓶内压强增大到一定程度,可能将橡
胶塞弹出,A项错误;因为Cl 比空气的密度大,用B项装置收集时,Cl 应从短管进入,空气从长管
2 2
排出,B项错误;C项装置既能收集Cl ,又能进行尾气处理且防倒吸,C项正确;由于Cl 和NaOH
2 2
溶液反应,所以D项装置不能收集到Cl ,D项错误。
2
4.实验室用下列两种方法制氯气:①用含HCl 146 g的浓盐酸与足量的MnO 反应;②用87 g
2
MnO 与足量浓盐酸反应。所得的氯气( )
2
A.①比②多 B.②比①多 C.一样多 D.无法比较
答案:B
解析:由化学方程式MnO +4HCl(浓) MnCl +Cl ↑+2H O知,参加反应的MnO 与HCl的质
2 2 2 2 2
量比为87∶146,但是由于稀盐酸与MnO 不反应,所以含有146 g HCl的浓盐酸不能与MnO
2 2
完全反应,但87 g MnO 可与足量的浓盐酸完全反应,所以途径②产生的氯气多。
2
5.向盛有氯气的集气瓶中,注入约五分之一容器体积的下列液体并轻轻振荡,观察到的现象记
录如图所示。判断瓶中注入的液体是( )
A.AgNO 溶液 B.NaOH溶液
3
C.水 D.FeCl 溶液
2答案:C
解析:A项,Cl 作用于AgNO 溶液会产生AgCl白色沉淀;B项,Cl 与NaOH溶液反应会产生
2 3 2
NaCl、H O和NaClO,溶液呈无色;C项,Cl 溶于水,所得氯水呈浅黄绿色;D项,Cl 氧化FeCl 生成
2 2 2 2
FeCl ,溶液呈棕黄色。
3
6.检验某溶液中是否含有Cl-,正确的操作是( )
A.取样,滴加AgNO 溶液,看是否有白色沉淀生成
3
B.取样,先加盐酸酸化,再加入AgNO 溶液,看是否有白色沉淀生成
3
C.取样,先加稀硫酸酸化,再加入AgNO 溶液,看是否有白色沉淀生成
3
D.取样,加少量AgNO 溶液,有白色沉淀;再加稀硝酸,看白色沉淀是否消失
3
答案:D
解析:A项,没有排除C等离子的干扰;B项,加入盐酸,引入了Cl-;C项,先加稀硫酸酸化会产生
Ag SO 沉淀。
2 4
7.有一包白色固体,它可能是KCl、K CO 、KNO 中的一种或几种,进行下列实验:
2 3 3
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO 溶液,生成白色沉淀;
3
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是 ,可能含有的成分是 。
(2)请写出上述实验中有关反应的离子方程式: 。
答案:(1)KCl和K CO KNO
2 3 3
(2)Ag++Cl- AgCl↓,2Ag++C Ag CO ↓,Ag CO +2H+ 2Ag++H O+CO ↑
2 3 2 3 2 2
解析:由②中产生白色沉淀知,原白色固体可能含有K CO 和KCl中的一种或两种;由③中沉
2 3
淀量减少且有气泡生成知,一定含有K CO ;根据沉淀不完全消失可知,一定含有KCl。
2 3