文档内容
物质的聚集状态与晶体的常识同步练习
(答题时间:45分钟)
一、选择题
1. 普通玻璃和水晶的根本区别在于( )
A. 外形不一样
B. 普通玻璃的基本构成粒子无规律性地排列,水晶的基本构成粒子呈周期性有序排列
C. 水晶有固定的熔点,普通玻璃无固定的熔点
D. 水晶可用于能量转换,普通玻璃不能用于能量转换
2. 下列关于晶体性质的叙述中,不正确的是( )
A. 晶体的自范性指的是在适宜条件下晶体能够自发地呈现规则的多面体几何外形
B. 晶体的各向异性和对称性是矛盾的
C. 晶体的对称性是微观粒子按一定规律做周期性有序排列的必然结果
D. 晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
3. 下列过程得到的固体不是晶体的是( )
A. 将NaCl饱和溶液降温,所得到的固体
B. 气态HO冷却直接形成的固体
2
C. 熔融的KNO 冷却后所得到的固体
3
D. 将液态的玻璃冷却后所得到的固体
4. 某化学兴趣小组在学习分子晶体后,查阅了几种氯化物的熔、沸点,记录如下:
NaCl MgCl AlCl SiCl CaCl
2 3 4 2
熔点/℃ 801 712 190 -68 782
沸点/℃ 1 465 1 418 230 57 1 600
根据这些数据分析,他们认为属于分子晶体的是( )
A. NaCl、MgCl 、CaCl B. AlCl 、SiCl
2 2 3 4
C. NaCl、CaCl D. 全部
2
5. 下列有关冰和干冰的叙述不正确的是( )
A. 干冰和冰都是由分子密堆积形成的晶体
B. 冰晶体中每个水分子周围只有4个紧邻的水分子
C. 干冰比冰的熔点低得多,常压下易升华
D. 干冰中只存在范德华力不存在氢键,一个分子周围有12个紧邻的分子
6. 下列有关分子晶体的说法中一定正确的是( )
A. 分子内均存在共价键
B. 分子间一定存在范德华力
C. 分子间一定存在氢键
第1页D. 其结构一定为分子密堆积
7. HF分子晶体、NH 分子晶体与冰的结构极为相似,在HF分子晶体中,与F原子距离
3
最近的HF分子有( )
A. 3个 B. 4个 C. 5个 D. 12个
8. 下列物质按熔、沸点由高到低顺序排列,正确的一组是( )
A. HF、HCl、HBr、HI
B. F、Cl、Br 、I
2 2 2 2
C. HO、HS、HSe、HTe
2 2 2 2
D. CI 、CBr 、CCl 、CF
4 4 4 4
二、非选择题
9. 水分子间可通过一种叫“氢键”的作用(作用力介于化学键与范德华力大小之间)彼
此结合而形成(HO),在冰中n值为5。即每个水分子被其他4个水分子包围形成变形四
2 n
面体,如图所示为(HO) 单元,由无限个这样的四面体通过氢键构成一个庞大的分子晶
2 5
体,即冰。下列有关叙述正确的是( )
A. 1 mol冰中含有4 mol氢键
B. 1 mol冰中含有4×5 mol氢键
C. 平均每个水分子只含有2个氢键
5
4
D. 平均每个水分子只含有 个氢键
10. (1)比较下列化合物熔、沸点的高低(填“>”或“<”)。
①CO________SO ②NH ________PH ③O________O
2 2 3 3 3 2
④Ne________Ar ⑤CHCHOH________CH OH ⑥CO________N
3 2 3 2
(2)已知AlCl 的熔点为190 ℃(2.02×105 Pa),但它在180 ℃即开始升华。请回答:
3
①AlCl 固体是________晶体。
3
②设计一个可靠的实验,判断氯化铝是离子化合物还是共价化合物。你设计的实验是
__________________。
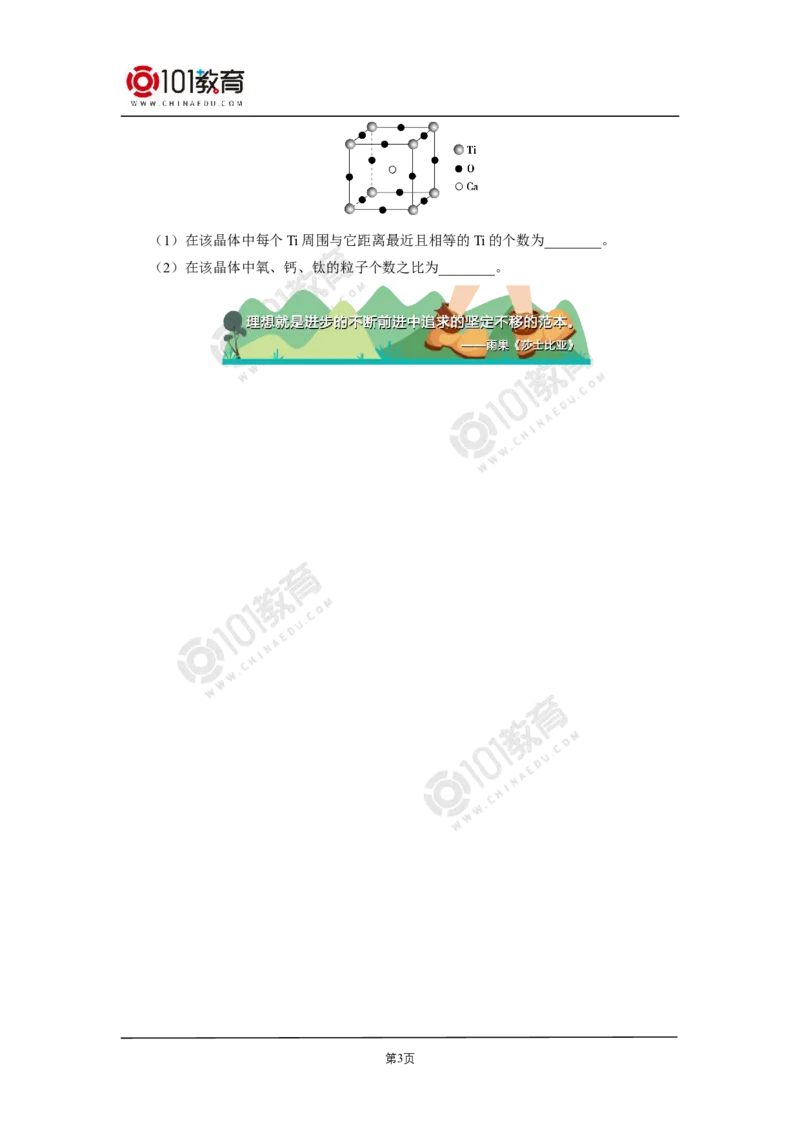
11. 在高温超导领域中,有一种化合物叫钙钛矿,其晶胞结构如图所示。试回答:
第2页(1)在该晶体中每个Ti周围与它距离最近且相等的Ti的个数为________。
(2)在该晶体中氧、钙、钛的粒子个数之比为________。
第3页物质的聚集状态与晶体的常识同步练习参考答案
1. B 解析:普通玻璃为非晶体,水晶为晶体,它们的根本区别在于内部粒子是否呈周
期性有序排列,B项正确。
2. B 解析:晶体在不同方向上粒子的排列情况不同,即为各向异性,晶体的对称性是
微观粒子按一定规律做周期性有序排列,两者没有矛盾,故B错误。
3. D 解析:得到晶体的三个途径是:①溶质从溶液中析出,②气态物质凝华,③熔融
态物质的凝固。A选项符合①,B选项符合②,C选项符合③。由于玻璃本来就属于非晶
体,熔融后再冷却所得固体仍为非晶体。
4. B 解析:由于由分子构成的晶体,分子与分子之间以分子间作用力相互作用,而分
子间作用力较小,克服分子间作用力所需能量较低,故分子晶体的熔沸点较低,表中的
MgCl 、NaCl、CaCl 熔、沸点很高,不属于分子晶体,AlCl 、SiCl 熔、沸点较低,应为
2 2 3 4
分子晶体,所以B项正确,A、C、D三项错误。
5. A 解析:干冰晶体中CO 分子间作用力只是范德华力,分子采取密堆积,一个分子
2
周围有12个紧邻的分子;冰晶体中水分子间除了范德华力之外还存在氢键,由于氢键具有
方向性和饱和性,故每个水分子周围只有4个紧邻的水分子,采取非密堆积的方式,空间
利用率小,因而密度小。干冰熔化只需克服范德华力,冰融化需要克服范德华力和氢键,
由于氢键作用力比范德华力大,所以干冰比冰的熔点低得多,而且常压下易升华。
6. B 解析:稀有气体元素组成的分子晶体中,不存在由多个原子组成的分子,而是原
子间通过范德华力结合成晶体,所以不存在任何化学键,A错误;分子间作用力包括范德
华力和氢键,范德华力存在于所有的分子晶体中,而氢键只存在于含有与电负性较强的
N、O、F原子结合的氢原子的分子之间或者分子之内,B正确,C错误;只存在范德华力
的分子晶体才采取分子密堆积的方式,D错误。
7. B 解析:根据HF分子晶体与冰结构相似可知,每个 HF分子周围有4个HF分子与
之最近,构成四面体,故B项正确。
8. D 解析:对结构和组成相似的分子晶体,其熔、沸点随着相对分子质量的增大而升
高,但HF、HO分子之间都存在氢键,熔、沸点反常。所以 A中应为HF>HI>HBr>HCl;
2
B中应为I>Br >Cl>F ;C中应为HO>HTe>HSe>H S;只有D正确。
2 2 2 2 2 2 2 2
9. C 解析:由图可知,每个水分子(处于四面体的中心)与 4个水分子(处于四面体
的四个顶点)形成四个氢键,因为每个氢键都是由2个水分子共同形成的,所以每个水分
1
2
子形成的氢键数为4× =2。
10.(1)①< ②> ③> ④< ⑤> ⑥>(2)①分子 ②在熔融状态下,试验其是否
导电,若不导电是共价化合物,若导电是离子化合物
第4页解析:(1)各组物质均为分子晶体,根据分子晶体熔、沸点的判断规律,分子间作用
力越大,相对分子质量越大,分子极性越大,则晶体的熔、沸点越高,较容易比较六组物
质熔、沸点的高低。
(2)由AlCl 的熔点低以及在180 ℃时开始升华判断AlCl 晶体为分子晶体。若验证
3 3
一种化合物是共价化合物还是离子化合物,可测其熔融状态下是否导电,若不导电是共价
化合物,导电则是离子化合物。
11.(1)6 (2)3∶1∶1
解析:(1)由晶胞结构可知,在每个Ti的上、下、左、右、前、后各有1个等距离
的Ti,与它距离最近且相等的Ti有6个。(2)Ca位于晶胞的体心,为一个晶胞独占;Ti
1
8
位于晶胞的顶点,则一个晶胞含有8× =1个Ti;O位于晶胞的棱上,则一个晶胞含有
1
4
12× =3个O。故氧、钙、钛的粒子个数之比为3∶1∶1。
第5页分子晶体与共价晶体同步练习
(答题时间:45分钟)
一、选择题
1. 下列物质中,属于共价晶体的化合物是( )
A. 无色水晶 B. 晶体硅
C. 金刚石 D. 干冰
2. 下列有关共价晶体的叙述错误的是( )
A. 共价晶体中,只存在共价键
B. 共价晶体具有空间网状结构
C. 共价晶体中不存在独立的分子
D. 共价晶体熔化时不破坏共价键
3. 氮化硼是一种新合成的结构材料,它是超硬、耐磨、耐高温的物质,下列各组物质熔
化时所克服的粒子间的作用力与氮化硼熔化时所克服的粒子间作用力相同的是( )
A. C 和金刚石 B. 晶体硅和水晶
60
C. 冰和干冰 D. 碘和金刚砂
4. 金刚石具有硬度大、熔点高等特点,大量用于制造钻头、金属切割刀具等。其结构如
图所示,下列判断正确的是( )
A. 金刚石中C—C的键角均为109°28′,所以金刚石和CH 的晶体类型相同
4
B. 金刚石的熔点高与C—C的键能无关
C. 金刚石中碳原子个数与C—C键数之比为1∶2
D. 金刚石的熔点高,所以在打孔过程中不需要进行浇水冷却
5. 最近科学家成功研制成了一种新型的碳氧化物,该化合物晶体与 SiO 的晶体的结构相
2
似,晶体中每个碳原子均以4个共价单键与氧原子结合,形成一种无限伸展的空间网状结
构。下列对该晶体的叙述错误的是( )
A. 该晶体是共价晶体
B. 该晶体中碳原子和氧原子的个数比为1∶2
第6页C. 该晶体中碳原子数与C—O键数之比为1∶2
D. 该晶体中最小的环由12个原子构成
6. 下表是某些共价晶体的熔点和硬度,分析表中的数据,判断下列叙述正确的是
( )
共价晶体 金刚石 氮化硼 碳化硅 石英 硅 锗
熔点/℃ 3 900 3 000 2 700 1 710 1 410 1 211
硬度 10 9.5 9.5 7 6.5 6.0
①构成共价晶体的原子种类越多,晶体的熔点越高
②构成共价晶体的原子间的共价键的键能越大,晶体的熔点越高
③构成共价晶体的原子半径越大,晶体的硬度越大
④构成共价晶体的原子半径越小,晶体的硬度越大
A. ①② B. ③④ C. ①③ D. ②④
二、非选择题
7. 现有两组物质的熔点数据如表所示:
A组 B组
金刚石:>3 500 ℃ HF:-83 ℃
晶体硅:1 410 ℃ HCl:-115 ℃
晶体硼:2 300 ℃ HBr:-89 ℃
二氧化硅:1 710 ℃ HI:-51 ℃
根据表中数据回答下列问题:
(1)A组属于________晶体,其熔化时克服的粒子间的作用力是________。
(2)B组中HF熔点反常是由于________。
(3)B组晶体不可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④液体状态能导电
第7页分子晶体与共价晶体同步练习参考答案
1. A 解析:A项,无色水晶是共价晶体,属于化合物;B项,晶体硅是单质;C项,金
刚石是单质;D项,干冰属于化合物,但它是分子晶体。
2. D 解析:A项,共价晶体中原子之间通过共价键相连;B项,共价晶体是相邻原子之
间通过共价键结合而成的空间网状结构;C项,共价晶体是由原子以共价键相结合形成的,
不存在独立的分子;D项,共价晶体中原子是通过共价键连接的,熔化时需要破坏共价键。
3. B 解析:氮化硼是由两种非金属元素形成的化合物,根据该化合物的性质可知其为
共价晶体,粒子间作用力为共价键。C 和金刚石熔化时分别克服的是分子间作用力和共价
60
键,A项错误;冰和干冰熔化时均克服的是分子间作用力,C项错误;碘和金刚砂熔化时
分别克服的是分子间作用力和共价键,D项错误。
4. C 解析:选项A,金刚石是共价晶体,CH 是分子晶体,二者的晶体类型不同;选项
4
B,金刚石熔化过程中C—C断裂,因C—C的键能大,断裂时需要的能量多,故金刚石的
熔点很高;选项C,金刚石中每个C都参与了4个C—C的形成,而每个C对每条键的贡
1
2
献只有一半,故碳原子个数与C—C键数之比为(4× )∶4=1∶2;选项D,金刚石的熔
点高,但在打孔过程中会产生很高的温度,如不浇水冷却钻头,会导致钻头熔化。
5. C 解析:该化合物晶体中每个碳原子均以4个共价单键与氧原子结合,形成一种无
限伸展的空间网状结构,则该化合物晶体中不存在分子,属于共价晶体,A项正确;晶体
中每个碳原子均以4个共价单键与氧原子结合,每个氧原子和2个碳原子以共价单键相结
合,所以碳、氧原子个数比为1∶2,B项正确;该晶体中每个碳原子形成4个C—O共价
键,所以C原子与C—O数目之比为1∶4,C项错误;该晶体中最小的环由6个碳原子和6
个氧原子构成,D项正确。
6. D 解析:共价晶体的熔、沸点和硬度等物理性质取决于晶体内的共价键,构成共价
晶体的原子半径越小,键长越短,键能越大,对应共价晶体的熔、沸点越高,硬度越大。
7. (1)共价 共价键 (2)HF分子间能形成氢键 (3)③④
解析:A组熔点很高,应是共价晶体,共价晶体熔化时破坏的是共价键;B组是分子
晶体,且结构相似,一般是相对分子质量越大,熔点越高;HF的相对分子质量最小但熔点
比HCl高,出现反常的原因是HF分子间存在氢键,HF熔化时除了破坏范德华力,还要破
坏氢键,所需能量更多,因而熔点更高。分子晶体在固态和熔化状态都不导电。
第8页