文档内容
晶体结构与性质同步练习
(答题时间:45分钟)
一、选择题
1. 下列说法正确的是( )
A. 晶体在受热熔化过程中一定存在化学键的断裂
B. 原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力
C. 区分晶体和非晶体最科学的方法是对固体进行X射线衍射实验
D. 非金属元素的原子间只形成共价键,金属元素的原子与非金属元素的原子间只形成
离子键
2. 共价键、金属键、离子键和分子间作用力都是构成物质微粒间的不同相互作用力,下
列含有上述两种相互作用力的晶体是( )
A. SiC晶体 B. Ar晶体 C. NaCl晶体 D. NaOH晶体
3. 仅由下列各组元素所组成的化合物的晶体,不可能属于离子晶体的是( )
A. H、O、S B. Na、H、O C. K、Cl、O D. Na、O、S
4. 下列叙述中正确的是( )
A. 原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
B. 同素异形体之间的转化都是物理变化
C. 原子晶体的熔点不一定比金属晶体的高,分子晶体的熔点不一定比金属晶体的低
D. 已知12 g金刚石中含有2N 个C—C键,则60 g SiO 中也含有2N 个Si—O键
A 2 A
5. 下列物质所属晶体类型分类正确的是( )
A B C D
原子晶体 石墨 生石灰 碳化硅 金刚石
分子晶体 冰 固态氨 氯化铯 干冰
离子晶体 氮化铝 食盐 明矾 芒硝
金属晶体 铜 汞 铝 铁
6. 用烧热的钢针去接触涂有薄薄一层石蜡的云母片的反面,熔化了的石蜡成椭圆形,这
是因为( )
A. 云母是热的不良导体,传热不均匀
B. 石蜡是热的不良导体,传热不均匀
C. 石蜡具有各向异性,不同方向导热性能不同
D. 云母具有各向异性,不同方向导热性能不同
7. 下列有关冰和干冰的叙述不正确的是( )
A. 干冰和冰都是由分子密堆积形成的晶体
B. 冰是由氢键形成的晶体,每个水分子周围有4个紧邻的水分子
第1页C. 干冰比冰的熔点低得多,常压下易升华
D. 干冰中只存在范德华力不存在氢键,一个分子周围有12个紧邻的分子
8. 下列叙述正确的是( )
A. 金属晶体的一个晶胞中所含的原子数:钾型=镁型<铜型
B. 在卤族元素(F、Cl、Br、I)的氢化物中,HF的沸点最低
C. CaH 、NaO 晶体的阴、阳离子个数比分别为2∶1、1∶1
2 2 2
D. 晶体熔点:金刚石>食盐>干冰>冰
9. 对于钠的卤化物(NaX)和硅的卤化物分子(SiX),下列叙述正确的是( )
4
A. SiX 呈空间网状结构,硬度大
4
B. NaX的熔点一般高于SiX
4
C. NaX易水解
D. SiX 由原子构成,熔化时破坏共价键
4
二、非选择题
10. 铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛
的应用。
(1)铜的熔点比钙的高,其原因是______________________________。
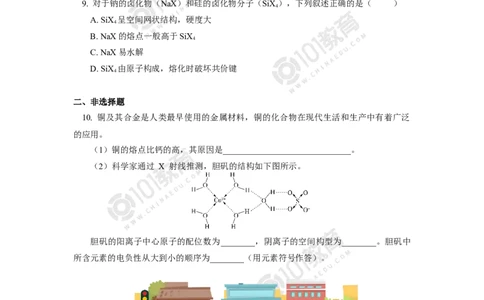
(2)科学家通过 X 射线推测,胆矾的结构如下图所示。
胆矾的阳离子中心原子的配位数为________,阴离子的空间构型为________。胆矾中
所含元素的电负性从大到小的顺序为________(用元素符号作答)。
第2页晶体结构与性质同步练习参考答案
1.【答案】C
【解析】A项,分子晶体受热熔化时破坏的是分子间作用力而不是化学键,错误;B
项,有的分子晶体中存在氢键,错误;D项,金属元素原子与非金属元素原子间也可形成
共价键,如AlCl 错误。
3
2.【答案】D
【解析】SiC晶体、Ar晶体、NaCl晶体中都只含有一种作用力,分别是共价键、范德
华力、离子键。
3.【答案】A
【解析】A 项不可能形成离子化合物,B、C、D 三项形成的离子化合物可能为
NaOH、KClO、NaSO 等。
3 2 3
4.【答案】C
【解析】稀有气体的晶体中不含有化学键,A项错;3O 2O 是化学变化,B项错;
2 3
晶体硅的熔点比金属钨的熔点低,蔗糖的熔点比汞高,C项正确;60 g SiO 中有4N 个Si
2 A
—O键,D项错。
5.【答案】D
【解析】石墨为混合型晶体,生石灰、氯化铯为离子晶体,氮化铝为 原子晶体。
6.【答案】D
【解析】云母是晶体,具有各向异性,在不同方向的导热性能不同,使得熔化的石蜡
成椭圆形。
7.【答案】A
【解析】干冰晶体中CO 分子间作用力只有范德华力,分子采用紧密堆积,一个分子
2
周围有12个紧邻的分子;冰晶体中水分子间除了范德华力还存在氢键,由于氢键具有方向
性,每个水分子周围有4个紧邻的水分子,采用非紧密堆积的方式,空间利用率小,因而
密度小。干冰融化只需克服范德华力,冰融化还需要克服氢键,由于氢键比范德华力大,
所以干冰比冰的熔点低得多,而且常压下易升华。
8.【答案】A
【解析】A项中1个晶胞内的原子数分别是2、2、4,正确;B项因HF分子间存在氢
2−
键,故HF沸点最高;D项熔点:冰>干冰;C项NaO 中阴离子(O2 )与阳离子(Na
2 2
+)个数比为1∶2。
9.【答案】B
【解析】硅的卤化物(SiX )属于分子晶体,不是空间网状结构,其硬度较小,A错
4
误;钠的卤化物(NaX)为离子化合物,属于离子晶体,硅的卤化物(SiX )为共价化合
4
第3页物,属于分子晶体,离子晶体的熔点大于分子晶体的熔点,即NaX的熔点一般高于SiX ,
4
故 B 正确;钠的强酸盐不水解,NaX(NaF 除外)不易水解,C 错误;硅的卤化物
(SiX)是由分子构成的,属于分子晶体,熔化时破坏分子间作用力,故D错误。
4
二、非选择题
10.【答案】(1)铜的金属键强度大于钙 (2)4 正四面体 O>S>H>Cu
【解析】(1)铜的原子半径比钙小,金属键比钙强,因此铜的熔点比钙的高;
(2)根据图示,胆矾晶体中铜离子周围有 4个水分子,配位数=4,阴离子为硫酸根
离子,S的价层电子对数=4,采用sp3杂化,空间构型为正四面体;元素的非金属性越强,
电负性数值越大,胆矾中所含元素 O、S、H、Cu 的电负性从大到小的顺序为
O>S>H>Cu;
第4页