文档内容
乙醇与乙酸
重难点 题型 分值
1. 掌握乙醇的分子结构和主要化学性质——
与钠的反应、氧化反应
2. 了解乙酸的分子式和结构式,理解羧基的
结构特点;
重点
3. 理解酯化反应的概念;掌握乙酸的酸性和
酯化反应等化学性质; 选择和填空 4-6分
4. 能够初步熟悉乙酸的酯化反应实验的有关
操作;
1. 乙醇的分子结构和主要化学性质
难点 2. 乙酸的酸性和酯化反应等化学性质;
3. 乙酸的酯化反应实验的有关操作;
核心知识点一:
一、乙醇
1. 物理性质
第1页【名师提醒】(1)乙醇(俗称酒精)沸点低,一挥发,应密封保存。
(2)检验乙醇中是否含有水通常加入无水硫酸铜固体,无水硫酸铜固体变蓝,则证明
其中含有水。
(3)工业上或实验室通过蒸馏法分离乙醇和水的混合物时,当乙醇的体积分数达到
95%左右时,乙醇和水会形成共沸物,即蒸发出的蒸气的组成与混合液的组成完全相同,
此时无法得到体积分数更大的乙醇溶液。要得到无水乙醇(乙醇的体积分数为99. 5%)应
在体积分数为95%的乙醇溶液中加入新制的生石灰再进行蒸馏(生石灰与水反应生成稳定
的氢氧化钙)即可。
2. 分子结构
乙醇可以看成是乙烷分子(CHCH )中的一个氢原子被-OH取代后的产物,也可以看
3 3
成是水分子(H-OH)中的一个氢原子被乙基(-CHCH )取代后的产物,故乙醇分子可看
3 2
作是由乙基和羟基组成的:CHCH-OH
3 2
【点拨提升】(1)烃的衍生物
烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。
如:乙醇可看成是乙烷分子的一个氢原子被羟基取代后的衍生物。
(2)官能团
决定有机化合物化学特性的原子或原子团。如—Cl(氯原子)、—OH(羟基)、
(碳碳双键)等。
羟基与氢氧根的比较
羟基 氢氧根
电子式
电子数 9 10
质子数 9 9
电性 不显电性 显电负性
第2页稳定程度 不稳定 较稳定
存在 不能独立存在,必须与其他基团结合 能独立存在
在一起
来源
失去H•的剩余部分 失去H+的剩余部分
相同点 组成元素相同
3. 化学性质
(1)乙醇的化学性质与化学键断裂的关系
分子结构 反应 断键位置 反应类型
与金属钠反应 ① 置换反应
催化氧化 ①③
与O 反应 氧化反应
2
燃烧 所有键
酯化反应(取代反
与乙酸反应 ①
应)
【注意】在有机反应中,有机分子中化学键的断裂与反应条件有着很大关系。如当反
应条件不同时,乙醇分子的断键方式也不同,乙醇发生的反应类型也不同,生成的产物也
各不相同。因此要注意反应条件和断键的关系,理清断键的过程和机理。
【名师提醒】有机反应中,有机物“去氢”或“得氧”的反应称为氧化反应;“加
氢”或“去氧”的反应称为还原反应。
(2)醇的催化氧化反应规律
醇在有催化剂(铜或银)存在的条件下,可以发生催化氧化反应生成醛,但并不是所
有的醇都能被氧化生成醛。
(1)凡是含有R—CHOH(R代表烃基)结构的醇,在一定条件下都能被氧化成醛;
2
2R—CHOH+O 2R—CHO+2HO。
2 2 2
第3页(2)凡是含有 结构的醇,在一定条件下也能被氧化,但生成物不是醛,
而是酮( )。
(3)凡是含有 结构的醇通常情况下不能被氧化。
【名师提醒】(1)催化氧化的断键方式:
在催化氧化反应中乙醇分子中的O-H键与羟基直接相连的碳原子上的C-H键断开,可
见乙醇与H、CO相似,具有还原性,能被氧化剂氧化。
2
(2)与羟基相连碳原子上有2个或3个氢原子的醇,可被氧化生成醛。
4. 用途
(1)用作酒精灯、火锅、内燃机等的燃料。
(2)用作化工原料和溶剂,用于生产医药、香料、化妆品、涂料等。
(3)用作消毒剂。医用酒精消毒剂是体积分数为75%的乙醇溶液,碘酒也是医疗上广
泛使用的消毒剂。医疗上常用体积分数为75%的乙醇溶液作消毒剂。
核心知识点二:
二、乙酸
1. 物理性质
俗名 颜色 状态 气味 溶解性 挥发性 熔点
16. 6 ℃
醋酸 无色 液体 强烈刺激性 易溶于水和乙醇 易挥发
食醋是有着悠久历史的调味品,其中含有3%-5%的乙酸,所以乙酸又被称为醋酸。
【注意】(1)当温度低于乙酸的熔点(16. 6℃)时,乙酸会凝结成类似冰一样的晶体,
故纯的乙酸又称为冰醋酸。冰醋酸是指纯净的乙酸,不一定是固态乙酸。
(2)“冰”是指固态的水,“干冰”是指固态的二氧化碳。“冰醋酸”是指纯净的乙
酸,不一定是固态乙酸。
2. 乙酸的分子结构
乙酸从结构上可以看成是甲基和羧基(-COOH)相连而成的化合物。乙酸的官能团是-
COOH。
第4页3. 乙酸的化学性质
(1)乙酸发生反应时的断键位置对比
乙酸的化学性质主要是由羧基决定,在化学反应中O-H键和C-O键断裂。
分子结构 化学性质 断键位置
体现酸的通性 ** 错误的表达式 **
酯化反应 ** 错误的表达式 **
(2)乙酸的弱酸性
①弱酸性:乙酸是一种重要的有机酸,其酸性强于碳酸,但仍属于弱酸。乙酸在水中
的电离方程式为CHCOOH CHCOO-+H+,是一元弱酸,具有酸的通性。
3 3
反应 现象或化学方程式
与酸碱指示剂反应 使紫色石蕊溶液变红
与活泼金属反应 2CHCOOH + Zn = (CHCOO)Zn + H ↑
3 3 2 2
与碱性氧化物反应 2CHCOOH + CuO = (CHCOO)Cu + H O
3 3 2 2
CHCOOH + NaOH = CH COONa + H O
3 3 2
与碱反应 2CHCOOH + Cu(OH) = (CHCOO) Cu + 2H O(蓝色固体溶
3 2 3 2 2
解得到蓝色溶液)
CHCOOH + NaHCO = CH COONa + CO ↑+ H O(此反应证明酸
3 3 3 2 2
与弱酸盐反应
性:醋酸>碳酸)
(3)乙酸的酯化反应
实验装置
第5页在一支试管中加入3 mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸
和2mL乙酸,再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将
实验步骤
产生的蒸气经导管通到饱和NaCO 溶液的液面上,观察现象。
2 3
实验现象 饱和NaCO 溶液的液面上有透明的油状液体生成,并可能闻到香味。
2 3
实验结论 在浓硫酸、加热的条件下,乙醇和乙酸发生反应,生成无色、透明、不
溶于水、有香味的油状液体。
化学方程式
CHCOOH+C HOH CHCOOC H+HO(酸去羟基醇去氢)
3 2 5 3 2 5 2
【注意事项】(1)试剂的加入顺序,先加入乙醇,然后沿器壁慢慢加入浓 HSO ,冷
2 4
却后再加入CHCOOH。
3
(2)导管末端不能插入饱和NaCO 溶液中,防止挥发出来的CHCOOH、CHCHOH
2 3 3 3 2
溶于水,造成溶液倒吸。
(3)浓HSO 的作用
2 4
①催化剂——加快反应速率。
②吸水剂——提高CHCOOH、CHCHOH的转化率。
3 3 2
(4)饱和NaCO 溶液的作用
2 3
①降低乙酸乙酯的溶解度,便于分层,得到酯。
②与挥发出来的乙酸反应。
③溶解挥发出来的乙醇。
(5)酯的分离
采用分液法分离试管中的液体混合物,所得上层液体即为乙酸乙酯。
核心知识点一:
1. 在探究乙醇的有关实验中,得出的结论正确的是( )
选项 实验步骤及现象 实验结论
在酒精试样中加入少量CuSO •5H O,搅拌,试 酒精试样中一定含有水
4 2
A
管底部有蓝色晶体
在乙醇燃烧火焰上方罩一冷的干燥烧杯,内壁有 乙醇由 C、H、O 三种元素
B 水珠出现。另罩一烧杯内壁涂有澄清石灰水的烧 组成
杯,内壁出现白色浑浊。
第6页将0. 01mol 金属钠加入过量的乙醇中充分反应, 乙醇分子中有1个氢原子与
C 在标准状况下收集到112mL气体。 氧原子相连,其余与碳原子
相连。
将灼热后表面变黑的螺旋状铜丝深入约50℃的乙 乙醇的催化氧化反应是放热
D
醇中,铜丝能保持红热一段时间。 反应
【答案】D
【解析】水能使无水硫酸铜变蓝,应该用无水硫酸铜检验水而不是 CuSO •5H O,A
4 2
项错误。乙醇的燃烧反应中有氧气参加,不能证明乙醇中含有氧元素,B项错误。根据C
项实验现象不能确定乙醇的分子结构,C项错误;根据D项实验现象可得出乙醇的催化氧
化反应是放热反应,D项正确。
2. A、B、C三种醇与足量的金属钠完全反应,相同条件下产生相同体积的氢气,消耗这
三种醇的物质的量之比为3∶6∶2,则三种醇分子里的羟基数之比为( )
A. 3∶2∶1 B. 2∶6∶2
C. 3∶1∶2 D. 2∶1∶3
【答案】D
【解析】由醇和钠的反应可得关系式2—OHN⃗aH
,产生相同体积的H 需要相同
2 2
物质的量的羟基,设都生成3 mol H ,则需要6 mol羟基,则需要一元醇6 mol,二元醇3
2
mol,三元醇2 mol,故选D。
某单官能团有机化合物中只含碳、氢、氧三种元素,相对分子质量为88,完全燃烧时
产生的CO 和HO的物质的量之比为5∶6,该有机物能被氧化为对应的羧酸。它可能的结
2 2
构共有( )
A. 4种 B. 5种 C. 6种 D. 7种
【答案】A
【解析】分子中碳和氢原子数比例符合n:(2n+2)。有机物完全燃烧时产生的CO 和
2
HO的物质的量之比为5:6,则其分子中C、H原子数之比为5:(6×2)=5:12,由于H
2
原子数达到饱和,该有机物分子中只能含有5个C、12个H。又由于该有机物的相对分子
质量为88,故该有机物的分子式为C H O。由于该有机物能被氧化为对应的羧酸,故其可
5 12
能的结构有CHCHCHCHCHOH、CHCHCH(CH )CHOH、(CH ) CHCH CHOH、
3 2 2 2 2 3 2 3 2 3 2 2 2
(CH)CCHOH共4种。
3 3 2
第7页核心知识点二:
1. 在同温同压下,某有机物和过量Na反应得到V L氢气,取另一份等量的有机物和足
1
量NaHCO 反应得V L二氧化碳,若V=V≠0,则有机物可能是( )
3 2 1 2
A. B. HOOC—COOH
C. HOCH CHOH D. CH COOH
2 2 3
【答案】A
【解析】1mol羟基与足量的金属钠反应产生0. 5molH ,1mol羧基与足量的金属钠反
2
应产生0. 5molH ;NaHCO 只能与有机物中的羧基反应而不与羟基反应,且1mol羧基与足
2 3
量的NaHCO 溶液反应产生1molCO ;若满足题干条件,该有机物中应既有羟基又有羧基,
3 2
故选A。
2. 某有机物的结构简式如图所示,下列说法不正确的是( )
A. 1mol该有机物和过量的金属钠反应最多可以生成1. 5mol H
2
B. 相同物质的量的该物质消耗Na、NaOH、NaHCO 的物质的量之比为3∶2∶2
3
C. 可以用酸性KMnO 溶液检验其中的碳碳双键
4
D. 该物质能够在催化剂作用下被氧化为含有-CHO的有机物
【答案】C
【解析】A项,金属钠可以和羟基、羧基反应生成H ,1mol该有机物中含有1mol羟
2
基和2mol羧基,故1mol该有机物和过量的金属钠反应最多可以生成1. 5molH ,正确。B
2
项,NaOH、NaHCO 均只能与该有机物中的羧基反应,正确。C项,该有机物中羟基和碳
3
碳双键都能是酸性KMnO 溶液褪色,故无法用酸性KMnO 溶液检验其中的碳碳双键,错
4 4
误。D项,该有机物中含有-CHOH,可以被氧化为-CHO,正确。
2
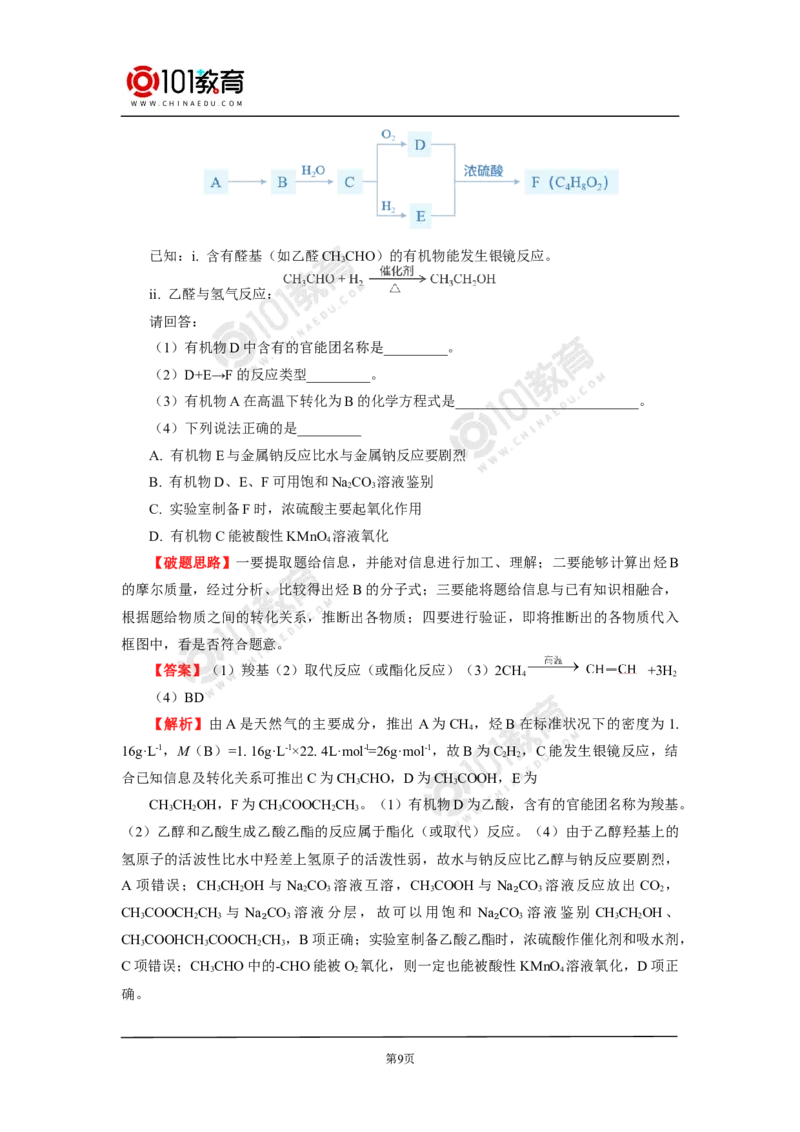
A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其
相互转化关系如图所示。已知烃B在标准状况下的密度为1. 16g/L,C能发生银镜反应,F
为有浓郁香味、不易溶于水的油状液体。
第8页已知:i. 含有醛基(如乙醛CHCHO)的有机物能发生银镜反应。
3
ii. 乙醛与氢气反应:
请回答:
(1)有机物D中含有的官能团名称是_________。
(2)D+E→F的反应类型_________。
(3)有机物A在高温下转化为B的化学方程式是__________________________。
(4)下列说法正确的是_________
A. 有机物E与金属钠反应比水与金属钠反应要剧烈
B. 有机物D、E、F可用饱和NaCO 溶液鉴别
2 3
C. 实验室制备F时,浓硫酸主要起氧化作用
D. 有机物C能被酸性KMnO 溶液氧化
4
【破题思路】一要提取题给信息,并能对信息进行加工、理解;二要能够计算出烃B
的摩尔质量,经过分析、比较得出烃B的分子式;三要能将题给信息与已有知识相融合,
根据题给物质之间的转化关系,推断出各物质;四要进行验证,即将推断出的各物质代入
框图中,看是否符合题意。
【答案】(1)羧基(2)取代反应(或酯化反应)(3)2CH +3H
4 2
(4)BD
【解析】由A是天然气的主要成分,推出A为CH ,烃B在标准状况下的密度为1.
4
16g·L-1,M(B)=1. 16g·L-1×22. 4L·mol-l=26g·mol-1,故B为C H ,C能发生银镜反应,结
2 2
合已知信息及转化关系可推出C为CHCHO,D为CHCOOH,E为
3 3
CHCHOH,F为CHCOOCH CH。(1)有机物D为乙酸,含有的官能团名称为羧基。
3 2 3 2 3
(2)乙醇和乙酸生成乙酸乙酯的反应属于酯化(或取代)反应。(4)由于乙醇羟基上的
氢原子的活波性比水中羟差上氢原子的活泼性弱,故水与钠反应比乙醇与钠反应要剧烈,
A 项错误;CHCHOH 与 NaCO 溶液互溶,CHCOOH 与 Na CO 溶液反应放出 CO ,
3 2 2 3 3 3 2
CHCOOCH CH 与 Na CO 溶液分层,故可以用饱和 Na CO 溶液鉴别 CHCHOH、
3 2 3 3 ₂3 3 2
CHCOOHCH COOCH CH,B项正确;实验室制备乙酸乙酯时,浓硫酸作催化剂和吸水剂,
3 3 2₂ 3 ₂
C项错误;CHCHO中的-CHO能被O 氧化,则一定也能被酸性KMnO 溶液氧化,D项正
3 2 4
确。
第9页(答题时间:35分钟)
一、选择题
1. 向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是
( )
A. 钠块沉在乙醇液面的下面
B. 钠块熔化成小球
C. 钠块在乙醇的液面上游动
D. 钠块表面剧烈放出气体
2. 可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A. 1 mol乙醇完全燃烧生成3 mol水
B. 乙醇可以制酒精饮料
C. 1 mol乙醇跟足量的Na作用得到0. 5 mol H
2
D. 1 mol乙醇可以生成1 mol乙醛
3. 按照下图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处
得到液体,则X气体或蒸气可能是(假设每个反应均完全)( )
A. CH CHOH B. CO或H
3 2 2
C. NH D. H
3 2
4. 乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是
( )
A. 和金属钠反应时键①断裂
B. 在铜催化共热下与O 反应时断裂①和③键
2
C. 在铜催化共热下与O 反应时断裂①和⑤键
2
D. 在空气中完全燃烧时断裂①②③④⑤键
5. 关于乙醇的说法中正确的是( )
A. 乙醇结构中有—OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B. 乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
第10页C. 乙醇与钠反应可以产生氢气,所以乙醇显酸性
D. 乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
6. 用括号内的试剂除去下列物质中的少量杂质,不正确的是( )
A. 溴苯中的溴(NaOH溶液)
B. 乙烷中的乙烯(通氢气)
C. 甲烷中的乙烯(溴水)
D. 乙酸乙酯中的乙酸(饱和碳酸钠溶液)
7. 下列物质都能与金属钠反应放出H,产生H 的速率排序正确的是( )
2 2
①C HOH ②NaOH溶液 ③醋酸溶液
2 5
A. ①>②>③ B. ②>①>③
C. ③>②>① D. ③>①>②
8. 乙酸分子的结构式为 ,下列反应及断键部位正确的是( )
a. 乙酸的电离,是①键断裂 b. 乙酸与乙醇发生酯化反应,是②键断裂 c. 在红磷
⃗红磷
存在时,Br 与CHCOOH的反应:CHCOOH+Br CHBr—COOH+HBr,是③键
2 3 3 2 2
断裂 d. 乙酸变成乙酸酐的反应:2CHCOOH―→ +HO,是①②
3 2
键断裂
A. abc B. abcd
C. bcd D. acd
9. 乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、
乙酸和浓硫酸作原料分别制备乙酸乙酯(沸点 77. 2 ℃)。下列有关说法不正确的是(
)
A. 浓硫酸能加快酯化反应速率
B. 不断蒸出酯,会降低其产率
C. 装置b比装置a原料损失的少
第11页D. 可用分液的方法分离出乙酸乙酯
10. 苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果
醋是一种常见的有机酸,其结构简式为 。
(1)苹果醋中含有的官能团的名称是______、______。
(2)苹果醋的分子式为______________。
(3)1 mol苹果醋与足量金属钠反应,能生成标准状况下的氢气__________L。
(4)苹果醋可能发生的反应是__________。
A. 与NaOH溶液反应
B. 与石蕊溶液作用
C. 与乙酸在一定条件下酯化
D. 与乙醇在一定条件下酯化
第12页1. 【答案】A
【解析】钠的密度比乙醇的大,故A正确,C错误;钠与乙醇反应产生氢气比较缓慢,
放出的热量不足以使钠熔化,故B、D错误。
2.【答案】C
【解析】一个乙醇分子中含有 6 个氢原子,分子式为 C HO,其可能的结构有
2 6
CHOCH 和C HOH。因为1 mol乙醇与足量的钠反应只得到0. 5 mol H ,说明6个氢原子
3 3 2 5 2
中只有1个氢原子可以被钠置换,这个氢原子与另外的氢原子所处环境应该不同。醇中的
氢原子只有羟基上的氢才能与钠发生反应,所以该反应经常用于判断醇分子中羟基的个数。
3. 【答案】A
【解析】选项中气体均可还原CuO,但本题的关键点是所得产物冷凝后得到液体,该
液体不可能是水(干燥管中盛有足量CuSO ),所以一定是乙醛,X气体为乙醇。
4
4. 【答案】C
【解析】乙醇与钠反应生成乙醇钠,是羟基中的 O—H键断裂,A正确;乙醇催化氧
化成乙醛时,断裂①和③化学键,B正确,C错误;乙醇完全燃烧时,化学键①②③④⑤
全部断裂。
5. 【答案】D
【解析】乙醇不能电离出氢氧根离子,—OH和OH-是完全不同的粒子;乙醇的氧化
反应表现的是乙醇的还原性;乙醇与钠反应可以产生氢气,此时,并不是氢离子的性质,
不能说明乙醇显酸性;乙醇与钠反应比水与钠反应平缓,说明乙醇羟基上的氢原子不如水
中的氢原子活泼。
6.【答案】B
【解析】溴易溶于溴苯,但可加入NaOH溶液,Br 与NaOH反应生成可溶于水的盐,
2
然后通过分液分离,故A正确;氢气的量无法控制,乙烷中会混入氢气,引入新的杂质,
故B错误;乙烯与溴水发生加成反应,可除去甲烷中混有的乙烯,故C正确;乙酸能与碳
酸钠溶液反应,可以用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,故D正确。
7.【答案】C
【解析】金属钠与NaOH溶液反应,实质上是与其中的水反应,钠与水反应的速率比
乙醇快;醋酸溶液中氢离子浓度更大,与钠反应速率更快。
8.【答案】B
【解析】乙酸电离出H+时,断裂①键;在酯化反应时酸脱羟基,断裂②键;与Br 的
2
反应,取代了甲基上的氢,断裂③键;生成乙酸酐的反应,一个乙酸分子断①键,另一个
分子断②键,所以B正确。
第13页9.【答案】B
【解析】乙酸与乙醇在浓硫酸作用下加热发生酯化反应,该反应为可逆反应,浓硫酸
吸水有利于平衡向生成乙酸乙酯的方向移动,故浓硫酸的作用为催化剂、吸水剂,浓硫酸
能加快酯化反应速率,A项正确;制备乙酸乙酯的反应为可逆反应,不断蒸出酯,有利于
反应正向进行,会提高其产率,B项错误;乙醇、乙酸易挥发,甲装置采取直接加热的方
法,温度升高快,温度不易控制,装置b采用水浴加热的方法,受热均匀,相对于装置a
原料损失的少,C项正确;分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸
钠溶液将挥发出来的乙酸转化为乙酸钠溶于水中,并溶解挥发出来的乙醇,降低乙酸乙酯
在水中的溶解度,静置分层后上层液体即为乙酸乙酯,D项正确。
10. 【答案】(1)羟基 羧基 (2)C HO (3)33. 6 (4)ABCD
4 6 5
【解析】苹果醋中含有2个—COOH和1个—OH,都可以与金属钠反应产生H ,故1
2
mol ACV与足量金属钠反应可产生H 1. 5 mol。它含有—COOH可与石蕊溶液作用,可与
2
NaOH、乙醇反应。它含有—OH可与乙酸发生酯化反应。
第14页