文档内容
物质的分离与提纯综合应用
重难点 题型 分值
1. 掌握过滤、蒸发、蒸馏、萃取和分液等分离物质
的实验技能,能独立完成一些简单的物质分离、提
重点 纯的实验操作;
2. 根据混合物的性质,选择不同的分离方法对物质
选择和填
进行分离。 6-8分
空
根据混合物的性质,选择不同的分离方法对物质进
难点
行分离
核心知识点一:
一、分离和提纯
1. 概念
(1)分离:将混合物中各组分分离开来,获得几种纯净物的过程。
第1页(2)提纯:将混合物中的杂质除去二得到纯净物的过程,也叫混合物的净化或除杂。
2. 要求
(1)“过量”(为除尽杂质,除杂试剂须过量);
(2)“后除前”(加入试剂的顺序是后面的试剂要把前面过量的试剂除尽);
(3)达标判断:沉淀完全的判断方法是在上层清液中(或取少量上层清液置于小试管
中)滴加沉淀剂,如果不再产生沉淀,说明沉淀已经完全。
3. 提纯的原则
“不增”—不引入新的杂质;
“不减”—不能减少被提纯物质;
“易分离”—原杂质或反应后生成的杂质易与被提纯物质分离;
“易复原”—被提纯的物质要容易复原
二、混合物的分离和提纯—物理方法
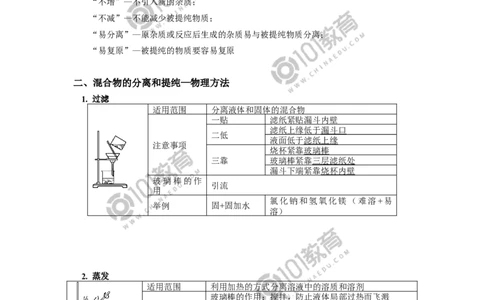
1. 过滤
适用范围 分离液体和固体的混合物
一贴 滤纸紧贴漏斗内壁
滤纸上缘低于漏斗口
二低
液面低于滤纸上缘
注意事项
烧杯紧靠玻璃棒
三靠 玻璃棒紧靠三层滤纸处
漏斗下端紧靠烧杯内壁
玻璃棒的作
引流
用
氯化钠和氢氧化镁(难溶+易
举例 固+固加水
溶)
2. 蒸发
适用范围 利用加热的方式分离溶液中的溶质和溶剂
玻璃棒的作用:搅拌,防止液体局部过热而飞溅
蒸发皿可直接加热,盛放量不超过其容积的2/3
注意事项
停止加热的标准:当有大量晶体析出时停止加热,利
用余热蒸干
①蒸发结晶:通过减少溶剂而使溶液达到过饱和,从而析出晶体,比如从硫酸铜溶液
中获取胆矾晶体(固+液互溶混合物),或是除去NaCl中的KNO(固+固加水均易溶)。
3
②冷却结晶:通过降温而使溶质的溶解度降低,从而析出晶体,如除去 KNO 晶体中
3
的NaCl。
③重结晶:将已得到的晶体用蒸馏水溶解,经过滤、加热、蒸发、冷却等步骤,再次
第2页析出晶体,得到更纯净晶体的过程。
3. 蒸馏
适用 利用混合物中各组分的沸点不同,用蒸馏的方法
范围 除去易挥发、难挥发或不挥发的杂质。
温度计的水银球在蒸馏烧瓶的支管口处
注意事项 蒸馏烧瓶中要加沸石或碎瓷片,目的是防止暴沸
冷凝管水流方向为下口进,上口出
酒精和水(液+液混合物);
举例
从海水中获取蒸馏水(固+液混合物)
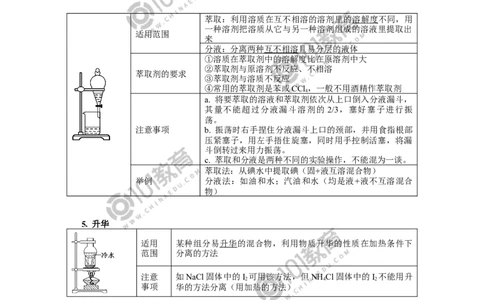
4. 萃取和分液
萃取:利用溶质在互不相溶的溶剂里的溶解度不同,用
一种溶剂把溶质从它与另一种溶剂组成的溶液里提取出
适用范围
来
分液:分离两种互不相溶且易分层的液体
①溶质在萃取剂中的溶解度比在原溶剂中大
②萃取剂与原溶剂不反应、不相溶
萃取剂的要求
③萃取剂与溶质不反应
④常用的萃取剂是苯或CCl ,一般不用酒精作萃取剂
4
a. 将要萃取的溶液和萃取剂依次从上口倒入分液漏斗,
其量不能超过分液漏斗溶剂的 2/3,塞好塞子进行振
荡。
注意事项 b. 振荡时右手捏住分液漏斗上口的颈部,并用食指根部
压紧塞子,用左手捂住旋塞,同时用手控制活塞,将漏
斗倒转过来用力振荡。
c. 萃取和分液是两种不同的实验操作,不能混为一谈。
萃取法:从碘水中提取碘(固+液互溶混合物)
举例 分液法:如油和水;汽油和水(均是液+液不互溶混合
物)
5. 升华
适用 某种组分易升华的混合物,利用物质升华的性质在加热条件下
范围 分离的方法
注意 如NaCl固体中的I 可用该方法,但NH Cl固体中的I 不能用升
2 4 2
事项 华的方法分离(用加热的方法)
三、混合物的分离和提纯—化学方法
方法 原理 杂质成分
沉淀法 将杂质离子转化为沉淀 Cl-、SO 、CO 及能形成弱碱的
阳离子
CO 、HCO 、SO 、HSO 、S2
气化法 将杂质离子转化为气体
-、NH
用氧化剂(还原剂)除去具有还原 如用酸性 KMnO 溶液除去 CO 中的
氧化还原法 4 2
性(氧化性)的杂质 SO ,用灼热的铜网除去N 中的O
2 2 2
第3页如除去NaCl中的NH Cl;除去碳酸钠
热分解法 加热使不稳定的物质分解除去 4
中的碳酸氢钠等
混合物中各组分酸碱性不同,用减 如用过量的 NaOH溶液可除去 Fe O
酸碱处理法 2 3
或酸处理 中的Al O
2 3
核心知识点
下列实验中,所选装置不合理的是( )
A. 分离NaCO 溶液和CHCOOC H,选④
2 3 3 2 5
B. 用CCl 提取碘水中的碘,选③
4
C. 用FeCl 溶液吸收Cl,选⑤
2 2
D. 粗盐提纯,选①和②
【答案】A
【解析】CHCOOCH CH 难溶于NaCO 溶液,二者会分层,可以用分液法分离,选
3 2 3 2 3
择③,A错误;用CCl 萃取碘水中的碘,选择③,B正确;⑤可以用作洗气瓶,也可用作
4
FeCl 溶液吸收Cl 的装置,C正确;粗盐提纯需要过滤、蒸发结晶,选择①和②,D正确。
2 2
1. 下对说法正确的是( )
A. 为测定新制氯水的pH,与标准比色卡对照即可
B. 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防爆沸。如果在沸腾前发现忘记加沸
石,应立即停止加热,冷却后补加
C. 在未知液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶
2
液中存在SO 2-
4
D. 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓硫酸再冷却结晶、过滤
干燥的方法
【答案】B
【解析】A项,氯水中含有HC1O,HClO具有漂白性,可将pH试纸漂白,无法测出
氯水的pH,A错;B项,做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸,如果在沸
腾前发现忘记加沸石,应立即停止加热,冷却后补加,正确;C项,Ba2++SO 2- = BaSO ,
4 4
Ag++Cl-=AgCl↓,两者均不溶于稀硝酸,此时说法错误,C错;D项,氯化钠的溶解度受温
度变化影响不大,而KNO 的溶解度随温度升高而增大,因此应用蒸发结晶的方法,不能
3
第4页用冷却结晶的方法(从KNO 溶液中除去少量NaCl可用冷却结晶的方法)。
3
2. 某硝酸钠固体中混有少量硫酸铵和碳酸氢钠杂质,现设计一实验方案,既除去杂质,
又配成硝酸钠溶液。实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完
成表格中各步实验。
选择试剂 ① NaCO 溶液 ④
2 3
实验操作 ② ③ 加热
下列试剂或操作不合理的是( )
A. 试剂①为Ba(OH) 溶液 B. 操作②为结晶
2
C. 操作③为过滤 D. 试剂④为稀HNO
3
【答案】B
【解析】选B 选择Ba(OH) 溶液除去SO 、NH 和HCO ,NH ·H O通过加热
2 3 2
除去,操作②为加热。过量的Ba2+用NaCO 溶液除去,过量的OH-和CO 用硝酸除去,
2 3
则操作③为过滤,试剂④为HNO。
3
(答题时间:25分钟)
一、选择题
1. 下列分离混合物的方法中不正确的是( )
A. 从酒精和水的混合物中分离出酒精——蒸馏法
B. 使浑浊的食盐水变澄清——过滤法
C. 从溴水中分离出溴——萃取、分液法
D. 把硝酸钾和氯化钾从同一溶液中分离开来——蒸发结晶法
2. 下列实验操作中正确的是( )
A. 蒸馏操作时,应向蒸馏烧瓶中加入几块沸石,以防止暴沸
B. 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
C. 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出
D. 萃取操作时,可以选用CCl 或酒精作为萃取剂从溴水中萃取溴
4
3. 下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)( )
选项 待提纯的物质 选用的试剂 操作方法
A NaCl(NaCO) 盐酸 蒸发
2 3
B CO(CO) O 点燃
2 2
C Fe(Zn) 稀硫酸 过滤
D CO(SO ) NaOH溶液 洗气
2 2
第5页4. 用四氯化碳取溴萃水中的溴,下列说法不正确的是( )
A. 实验使用的主要仪器是分液漏斗
B. 溴在四氯化碳中的溶解度比在水中的溶解度大
C. 溴的四氯化碳溶液呈橙红色
D. 分液时,水从分液漏斗的下端流出,溴的四氯化碳溶液从分液漏斗的上口倒出
5. 下列实验操作中正确的是( )
A. 蒸馏操作时,应向蒸馏烧瓶中加入几块沸石,以防止暴沸
B. 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
C. 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出
D. 萃取操作时,可以选用CCl 或酒精作为萃取剂从溴水中萃取溴
4
6. 提纯含有少量Mg(NO ) 杂质的KNO 溶液,可使用的方法为( )
3 2 3
A. 加入过量NaOH溶液,过滤,除去沉淀,溶液中补加适量的硝酸
B. 加入过量KOH溶液,过滤,除去沉淀,溶液中补加适量硝酸
C. 加入过量NaSO 溶液,过滤,除去沉淀,溶液中补加适量硝酸
2 4
D. 加入过量KSO 溶液,过滤,除去沉淀,溶液中补加适量硝酸
2 4
二、填空题
7. 为了除去粗盐中的Ca2+、Mg2+、SO 以及泥沙等杂质,某同学设计了一种制备精盐
的实验方案,步骤如下(所加的试剂BaCl 、NaCO、NaOH均稍过量):
2 2 3
(1)②③④步操作中所加入的试剂顺序为:
________________________________________________________________________。
(2)判断BaCl 已过量的方法是______________________________________________
2
________________________________________________________________________。
8. 除去下列物质中混有的少量杂质(杂质不要求回收),把适用的试剂、操作方法的序
号写在相应的括号内:
a. 加适量盐酸、过滤 b. 加适量水、过滤、蒸发
c. 加适量水、过滤 d. 加热(高温或灼烧) e. 加适量盐酸、蒸发
f. 冷却热的饱和溶液、过滤
(1)碳酸钙中混有少量的碳酸钠( )
(2)氯化钾粉末中混有碳酸钾( )
(3)氧化钙中混有少量的碳酸钙( )
(4)二氧化锰中混有少量的炭粉( )
第6页(5)硝酸钾中混有少量的食盐( )
第7页1.【答案】D
【解析】用蒸馏法可以把酒精从酒精和水的混合物中分离出来;食盐水浑浊,用过滤
法可除去混在食盐水里的固体物质;溴水是溴和水形成的均匀液态混合物,可先用萃取剂
(如CCl )将溴从溴水中萃取出来,然后再进行分液;硝酸钾和氯化钾都易溶于水,硝酸
4
钾的溶解度受温度的影响较大,氯化钾的溶解度受温度的影响较小,由此可以用蒸发结晶
浓缩冷却的方法把硝酸钾和氯化钾从同一溶液中分离开来。
2.【答案】A
【解析】蒸馏时若不加沸石或碎瓷片,液面容易剧烈翻滚,若加入沸石就比较平稳,
可防止暴沸,A正确;蒸发时溶液剩少许就要停止加热,利用余热将水分蒸干,B错误;
分液操作时,将分液漏斗中下层液体从下口放出,再将上层液体从上口倒出,C错误;萃
取操作时,能选用CCl 作为萃取剂从溴水中萃取溴,酒精与水互溶,不可作萃取剂,D错
4
误。
3.【答案】A
【解析】B项错误,实际上不能完成操作,因CO量少,反应的O 量又不易控制;C
2
项错误,主要成分Fe也能与稀硫酸反应而消耗;D项错误,NaOH在吸收SO 的同时也吸
2
收主要成分CO。
2
4.【答案】D
【解析】利用四氯化碳萃取溴水中的溴时,四氯化碳层在下面,先打开分液漏斗下端
的旋塞放出溴的四氯化碳溶液,水从分液漏斗的上口倒出,D项不正确。
5.【答案】A
【解析】蒸馏时若不加沸石或碎瓷片,液面容易剧烈翻滚,若加入沸石就比较平稳,
可防止暴沸,A正确;蒸发时溶液剩少许就要停止加热,利用余热将水分蒸干,B错误;
分液操作时,将分液漏斗中下层液体从下口放出,再将上层液体从上口倒出,C错误;萃
取操作时,能选用CCl 作为萃取剂从溴水中萃取溴,酒精与水互溶,不可作萃取剂,D错
4
误。
6.【答案】B
【解析】A、C引入Na+无法除去;C、D引入SO 无法除去。
7.【答案】(1)BaCl 、NaOH、NaCO 或NaOH、BaCl 、NaCO 或BaCl 、NaCO 、
2 2 3 2 2 3 2 2 3
NaOH (2)取加入BaCl 后的上层清液1~2滴于点滴板上,再滴入1~2滴BaCl 溶液,
2 2
若溶液未变浑浊,则表明BaCl 已过量
2
【解析】加入除杂试剂需过量,前面操作引入的杂质要在后续操作中除去。故NaCO
2 3
应在BaCl 之后加入,以除去过量的Ba2+。
2
第8页8.【答案】(1)c (2)e (3)d (4)d (5)f
【解析】(1)碳酸钙难溶于水,而杂质碳酸钠易溶于水,因此应加适量水,充分振荡,
使碳酸钠完全溶解,然后过滤,留在滤纸上的是纯净的碳酸钙,选c;(2)主体物质氯化
钾和杂质碳酸钾均易溶于水,不能用过滤法分离,但碳酸钾易跟盐酸反应放出二氧化碳,
留在溶液中的为氯化钾,将该溶液蒸发,即可得到氯化钾晶体,选e;(3)根据碳酸钙高
温分解,能生成氧化钙和二氧化碳,CO 逸出后只剩下氧化钙,便达到了除杂提纯的目的,
2
选d;(4)二氧化锰和炭粉均不溶于水,但炭粉易燃,因此可选用方法 d;(5)硝酸钾的
溶解度随温度升高明显增大,而食盐的溶解度受温度变化影响不大,因此,可选用结晶法
分离除杂,若要提高硝酸钾的纯度,还可将滤纸上得到的硝酸钾晶体再结晶 1~2次,结晶
次数越多,纯度越高,选f。
第9页