文档内容
《原子结构》第二课时 教学设计
课题 《原子结构》 单元 1 学科 化学 年级 高二
本节教学内容是人教版高中化学选择性必修第二册第一章《原子结构与性质》第一
节《原子结构》第二课时。这一课时的教学内容主要是电子云与原子轨道、泡利原理、
洪特规则与能量最低原理。前一课时已经学习了 “能层、能级、构造原理”的概念和内
容,了解了原子基态、激发态、原子光谱等基础知识,理解构造原理并会根据构造原理
进行原子核外电子排布。在此基础上本节内容介绍原子核外电子的运动状态,本节重点
掌握原子核外电子运动特点,基态原子中核外电子的排布遵循泡利原理、洪特规则、能
教材 量最低原理。
分析 本节安排了“电子云与原子轨道、泡利原理、洪特规则与能量最低原理”这部分内
容。学生通过学习这部分知识,了解有关核外电子运动模型的发展历史,认识核外电子
的运动特点。知道电子的运动状态(空间分布及能量)。可通过原子轨道和电子云模型
来描述。
认识基态原子中核外电子的排布遵循泡利原理、洪特规则、能量最低原理。
证据推理与模型认知:通过认识核外电子的运动特点初步建立通过原子轨道和电子
教学目 云模型来描述运动状态的思维模型。理解原子核外电子排布遵循泡利原理、洪特规则、
能量最低原理。
标与核
心素养 科学精神与社会责任:通过了原子核外电子运动模型等的发展史,认识到科学是在
不断发展的,培养求真务实、不断进步的科学精神与社会责任感。
重点 电子云与原子轨道、泡利原理、洪特规则与能量最低原理。
难点
教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 提问:原子核外的电子运动状态是怎么样呢? 了解科学 通过了原
【科学史】 史 子核外电
1911年,英国物理学家卢瑟福根据 1910年进行的α粒 子运动模
子散射实验,提出了原子结构的行星模型。在这个模型里, 型等的发
电子像太阳系的行星围绕太阳转一样围绕着原子核旋转。 展史,认
1913年,丹麦科学家玻尔在卢瑟福模型的基础上,他提 识到科学
出了氢原子模型,电子在线性轨道上运行,解决了原子结构 是在不断
的稳定性问题,描绘出了完整而令人信服的原子结构学说。 发展的,
氢原子结构理论成功的阐述了原子的稳定性,氢原子光谱的 培养求真
产生和不连续性。 务实、不
1926年,量子力学推翻了玻尔的氢原子模型,指出一定 断进步的
空间运动状态的电子并不在玻尔假定的线性轨道上运行,而 科学精神
在核外空间各处都可能出现,但出现的概率不同,可以算出 与社会责
它们的概率密度分布。 任感。
概率密度:
P表示电子在某处出现的概率;V表示该处的体积;
讲授新课 第一节 原子结构
第二课时 电子云与原子轨道、泡利原理、洪特规则、
能力最低原理
一、电子云
【问题】图1-7 中的小点是什么呢?是电子吗? 认识核外
小点是 1s 电子在原子核外出现的概率密度的形象描 电子的运
述。小点越密,表明概率密度越大。由于核外电子的概率密 思考 动特点。
度分布看起来像一片云雾,因而被形象的称作“电子云”。 知道电子
1.电子云概念 的运动状
态(空间
电子云是处于一定空间运动状态的电子在原子核外空间
分布及能
的概率密度分布的形象化描述。
量)。
电子在原子核外一定空间范围内出现的概率统计起来,
好似在原子核外笼罩着一团带负电的云雾,形象称为“电子
云”。
2.电子云轮廓图
电子云图很难绘制,使用不便,我们常使用电子云轮廓
图。
为了表示电子云轮廓的形状,对核外电子的空间运动状
态有一个形象化的简便描述。把电子在原子核外空间出现概
率P=90%的空间圈出来,即电子云轮廓图。
【过渡】所有原子的任意能层的s电子的电子云轮廓图
都是一个球形,只是球的半径不同。同一原子的能层越高,
s电子云半径越大,是由于电子的能量依次增高,电子在离
核更远的区域出现的概率逐渐增大,电子云越来越向更大的
空间扩展。
类比 形象化的
就像宇宙飞船必须提供能量推动才能克服地球引力上
理解同一
天,2s电子比1s电子能量高,克服原子核的吸引在离核更
原子的能
远的空间出现的概率就比1s大,因而2s电子云必然比1s电
层越高,s
子云更弥散。
电子云半
二、原子轨道
径越大,
1.定义:电子在原子核外的一个空间运动状态称为一个
是由于电
原子轨道。
子的能量
2.形状:
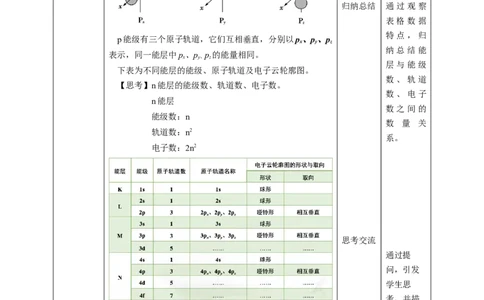
依 次 增
(1)s电子的原子轨道呈球形,能层序数越大,原子轨道
高。
的半径越大。思考交流
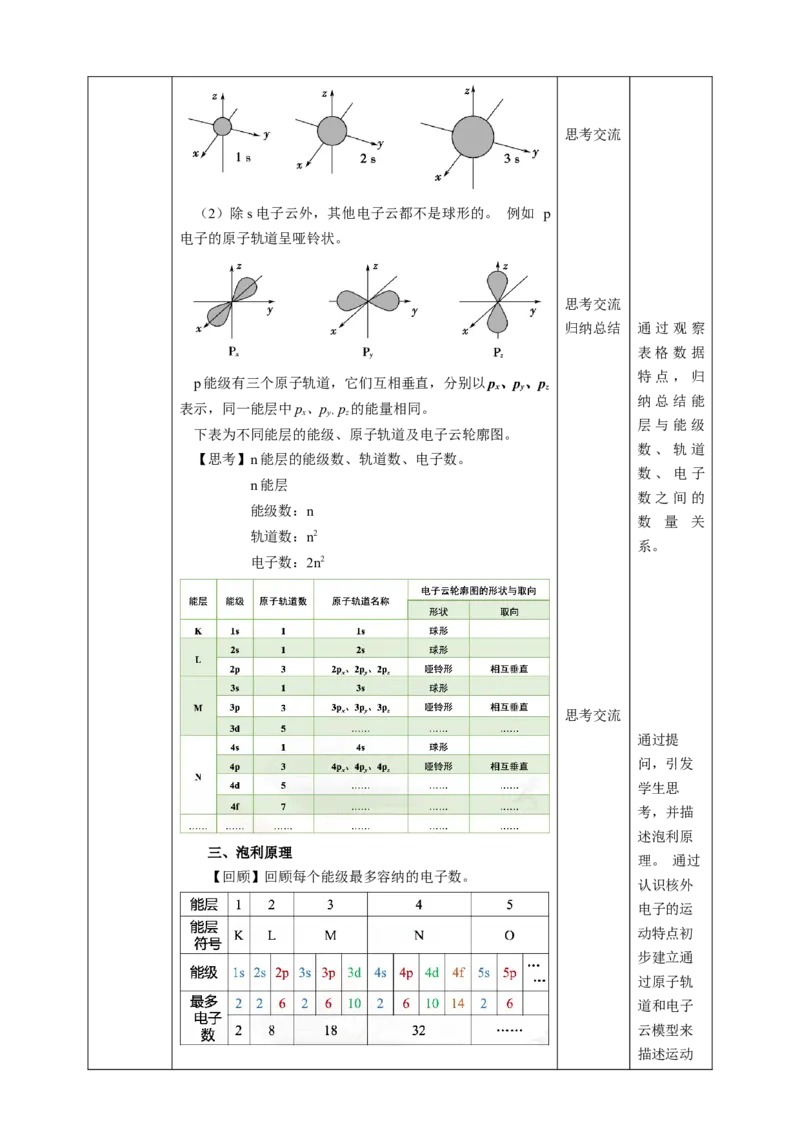
(2)除s电子云外,其他电子云都不是球形的。 例如 p
电子的原子轨道呈哑铃状。
思考交流
归纳总结 通过观察
表格数据
特点,归
p能级有三个原子轨道,它们互相垂直,分别以p、p、p
x y z
纳总结能
表示,同一能层中p、p p 的能量相同。
x y、 z
层与能级
下表为不同能层的能级、原子轨道及电子云轮廓图。
数、轨道
【思考】n能层的能级数、轨道数、电子数。
数、电子
n能层
数之间的
能级数:n
数 量 关
轨道数:n2
系。
电子数:2n2
思考交流
通过提
问,引发
学生思
考,并描
述泡利原
三、泡利原理
理。 通过
【回顾】回顾每个能级最多容纳的电子数。
认识核外
电子的运
动特点初
步建立通
过原子轨
道和电子
云模型来
描述运动【思考】为什么一个轨道允许容纳2个电子呢? 状态的思
【过渡】1925年,两个荷兰年轻人提出:电子除了空间 维模型。
运动状态外,还有一种状态叫做自旋。
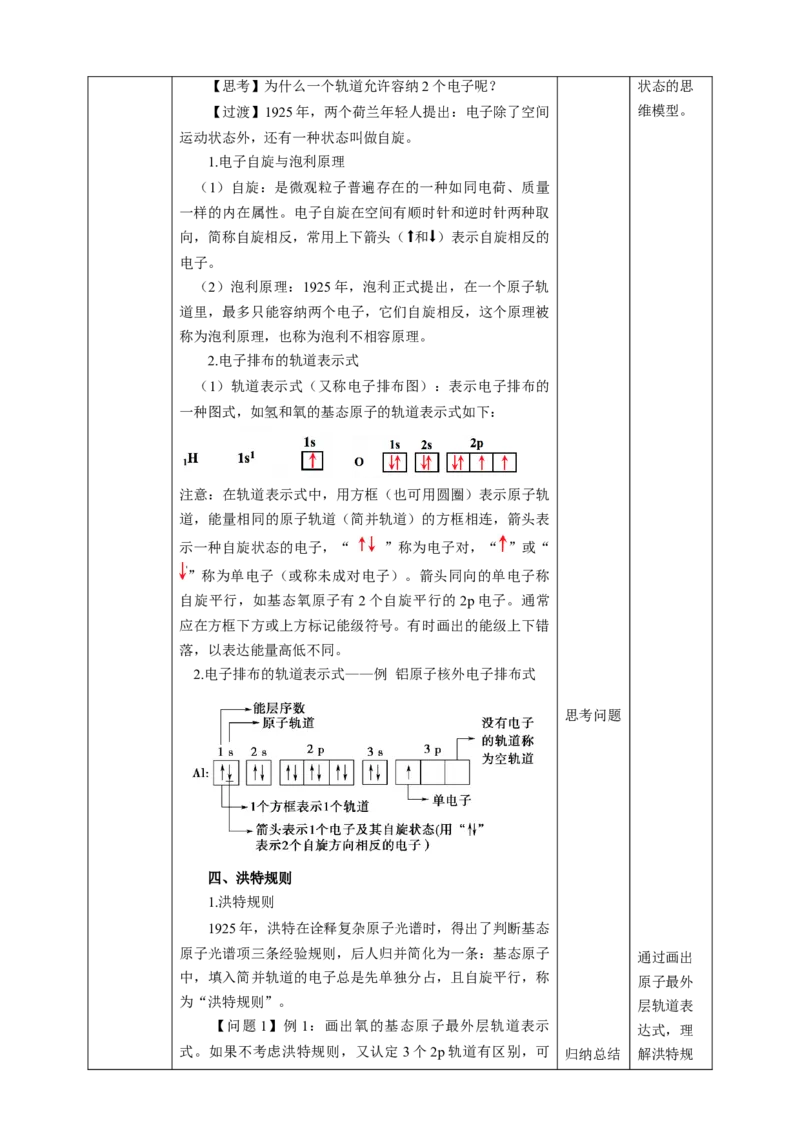
1.电子自旋与泡利原理
(1)自旋:是微观粒子普遍存在的一种如同电荷、质量
一样的内在属性。电子自旋在空间有顺时针和逆时针两种取
向,简称自旋相反,常用上下箭头(⬆和⬇)表示自旋相反的
电子。
(2)泡利原理:1925年,泡利正式提出,在一个原子轨
道里,最多只能容纳两个电子,它们自旋相反,这个原理被
称为泡利原理,也称为泡利不相容原理。
2.电子排布的轨道表示式
(1)轨道表示式(又称电子排布图):表示电子排布的
一种图式,如氢和氧的基态原子的轨道表示式如下:
注意:在轨道表示式中,用方框(也可用圆圈)表示原子轨
道,能量相同的原子轨道(简并轨道)的方框相连,箭头表
示一种自旋状态的电子,“ ”称为电子对,“ ”或“
”称为单电子(或称未成对电子)。箭头同向的单电子称
自旋平行,如基态氧原子有2个自旋平行的2p电子。通常
应在方框下方或上方标记能级符号。有时画出的能级上下错
落,以表达能量高低不同。
2.电子排布的轨道表示式——例 铝原子核外电子排布式
思考问题
四、洪特规则
1.洪特规则
1925年,洪特在诠释复杂原子光谱时,得出了判断基态
原子光谱项三条经验规则,后人归并简化为一条:基态原子
通过画出
中,填入简并轨道的电子总是先单独分占,且自旋平行,称
原子最外
为“洪特规则”。
层轨道表
【问题1】例1:画出氧的基态原子最外层轨道表示
达式,理
式。如果不考虑洪特规则,又认定3个2p轨道有区别,可 归纳总结 解洪特规画出怎样的轨道表示式? 则。
若遵循洪特规则,且不区分 3个2p轨道,只需画出轨
道表示式:
注意:
①洪特规则不仅适用于基态原子,也适用于基态离子。
②洪特规则是针对电子填入简并轨道而言的,并不适用
于电子填入能量不同的轨道。
思考与讨
【问题2】例2:请写出24、29号元素原子的电子排布
论
式。
Cr 1s22s22p63s23p63d54s1
24
Cu 1s22s22p63s23p63d104s1
29
【归纳】在简并轨道(同一能级)上的电子排布处于全
充满、半充满和全空状态时,具有较低的能量和较大的稳定
性。
【思考与讨论】
1.下列轨道表示式中,哪个是硼的基态原子 ?为什么?
应用所学
知识判断
基态原子
答案:A。基态原子核外电子排布要遵循泡利不相容原理,
的轨道表
即在一个原子轨道里,最多只能容纳两个电子,它们自旋相
达式的正
反。
确与否。
2.下列轨道表示式中,哪个是氧的基态原子 ?为什么?
答案:A。基态原子核外电子排布要遵循洪特规则,即基态
原子中,填入简并轨道的电子总是先单独分占,且自旋平
行。
【过渡】基态是能量最低的状态,所以,基态原子的电
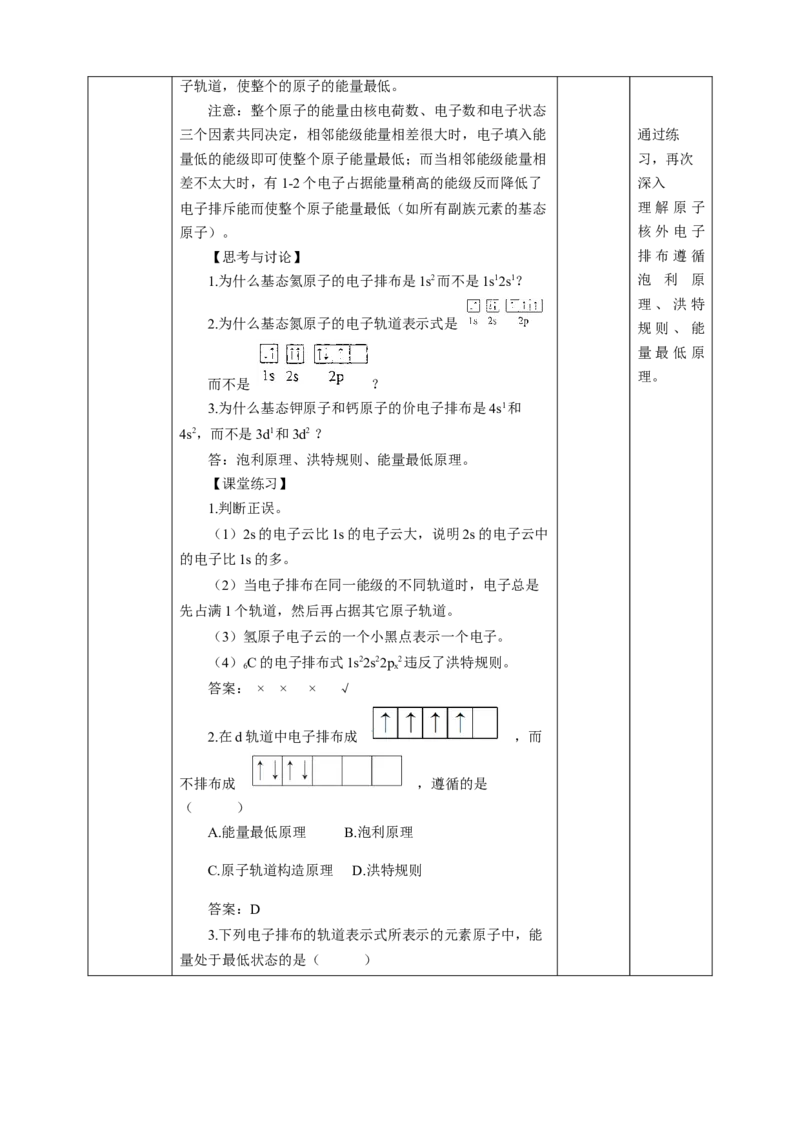
子排布是能量最低的原子轨道组合。
五、能量最低原理
1.内容
在构建基态原子时,电子将尽可能的占据能量最低的原子轨道,使整个的原子的能量最低。
注意:整个原子的能量由核电荷数、电子数和电子状态
三个因素共同决定,相邻能级能量相差很大时,电子填入能 通过练
量低的能级即可使整个原子能量最低;而当相邻能级能量相 习,再次
差不太大时,有1-2个电子占据能量稍高的能级反而降低了 深入
电子排斥能而使整个原子能量最低(如所有副族元素的基态 理解原子
原子)。 核外电子
【思考与讨论】 排布遵循
1.为什么基态氦原子的电子排布是1s2而不是1s12s1? 泡 利 原
理、洪特
2.为什么基态氮原子的电子轨道表示式是
规则、能
量最低原
理。
而不是 ?
3.为什么基态钾原子和钙原子的价电子排布是4s1和
4s2,而不是3d1和3d2 ?
答:泡利原理、洪特规则、能量最低原理。
【课堂练习】
1.判断正误。
(1)2s的电子云比1s的电子云大,说明2s的电子云中
的电子比1s的多。
(2)当电子排布在同一能级的不同轨道时,电子总是
先占满1个轨道,然后再占据其它原子轨道。
(3)氢原子电子云的一个小黑点表示一个电子。
(4)C的电子排布式1s22s22p2违反了洪特规则。
6 x
答案: × × × √
2.在d轨道中电子排布成 ,而
不排布成 ,遵循的是
( )
A.能量最低原理 B.泡利原理
C.原子轨道构造原理 D.洪特规则
答案:D
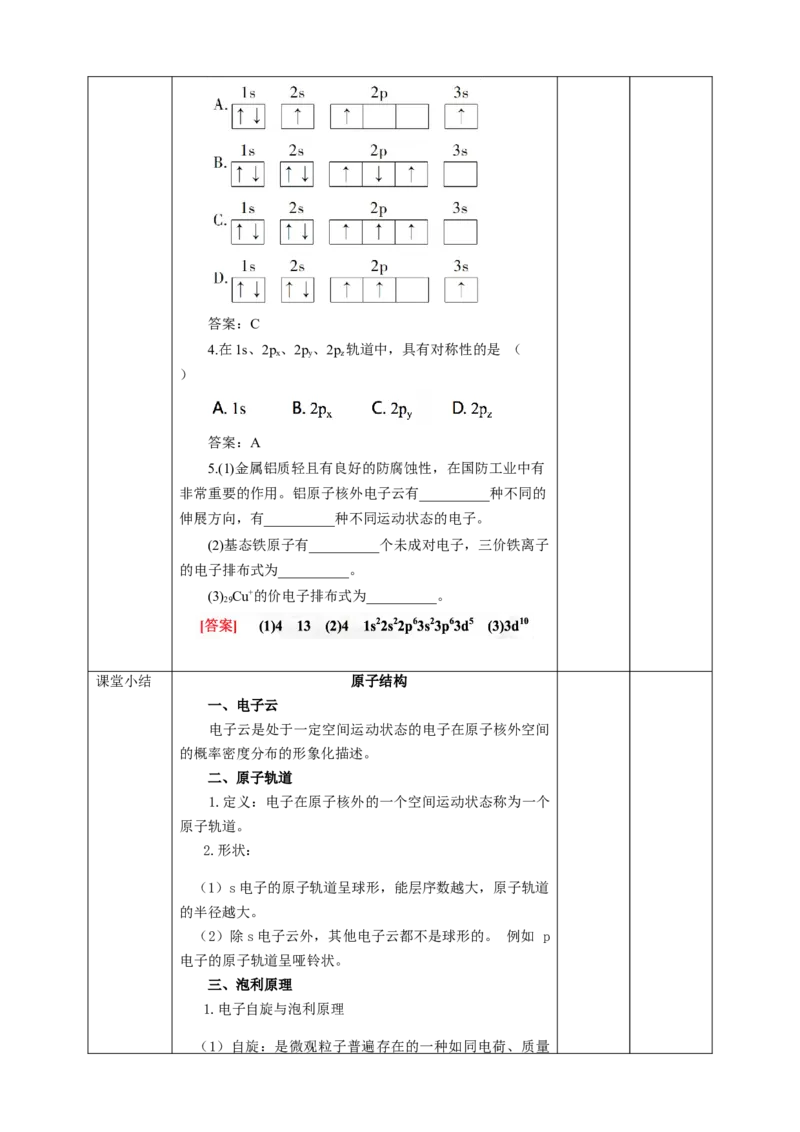
3.下列电子排布的轨道表示式所表示的元素原子中,能
量处于最低状态的是( )答案:C
4.在1s、2p、2p、2p 轨道中,具有对称性的是 (
x y z
)
答案:A
5.(1)金属铝质轻且有良好的防腐蚀性,在国防工业中有
非常重要的作用。铝原子核外电子云有__________种不同的
伸展方向,有__________种不同运动状态的电子。
(2)基态铁原子有__________个未成对电子,三价铁离子
的电子排布式为__________。
(3) Cu+的价电子排布式为__________。
29
课堂小结 原子结构
一、电子云
电子云是处于一定空间运动状态的电子在原子核外空间
的概率密度分布的形象化描述。
二、原子轨道
1.定义:电子在原子核外的一个空间运动状态称为一个
原子轨道。
2.形状:
(1)s电子的原子轨道呈球形,能层序数越大,原子轨道
的半径越大。
(2)除s电子云外,其他电子云都不是球形的。 例如 p
电子的原子轨道呈哑铃状。
三、泡利原理
1.电子自旋与泡利原理
(1)自旋:是微观粒子普遍存在的一种如同电荷、质量一样的内在属性。
(2)泡利原理:在一个原子轨道里,最多只能容纳两个
电子,它们自旋相反。
2.电子排布的轨道表示式
四、洪特规则
基态原子中,填入简并轨道的电子总是先单独分占,且
自旋平行。
五、能量最低原理
在构建基态原子时,电子将尽可能的占据能量最低的原
子轨道,使整个的原子的能量最低。
板书 原子结构
一、电子云
二、原子轨道
1.定义:
2.形状:
s电子的原子轨道呈球形。
p电子的原子轨道呈哑铃状。
三、泡利原理
1.电子自旋与泡利原理
(1)自旋:是微观粒子普遍存在的一种如同电荷、质量
一样的内在属性。
(2)泡利原理:在一个原子轨道里,最多只能容纳两个
电子,它们自旋相反。
2.电子排布的轨道表示式
四、洪特规则
五、能量最低原理