文档内容
第一章 原子结构与性质
第一节 原子结构
第三课时 电子云与原子轨道 泡利原理、洪特规则、能量最低原理
【学习目标】1.了解核外电子运动、电子云轮廓图和核外电子运动的状态 。
2. 了解泡利原理和洪特规则,会书写和说明1-36号元素基态原子的核外电子排布式和
轨道表示式
【学习重点】泡利原理和洪特规则在轨道表示式书写中的应用
【学习难点】电子的运动状态和电子云轮廓图
【课前预习】
旧知回顾:
1、能级能量大小的判断方法:
①先看能层,一般情况下,能层序数越大,能量越 ;
再看同一能层各能级的能量顺序为:E(ns) E(np) E(nd) E(nf) ……
②不同能层中同一能级,能层序数越大,能量越 。
③不同原子同一能层,同一能级的能量大小 。
2、构造原理示意图中,从1s至5s电子的排布顺序:
新知预习:
1、电子云:
2、原子轨道:
3、泡利原理:
4、洪特规则:
5、能量最低原理:
【课中探究】
情景导入:通过刚才的视频,我们发现,电子的运动状态是很复杂的,那么电子到底是如何运动的,
视频中提到的电子构成的概率云,自旋又指的是什么,通过今天的学习,我们就能解决这些问题。
一、电子云与原子轨道任务一、了解电子云的相关内容
【学生活动】阅读教材P 第1-4自然段,了解电子云,回答下列问题:
12
1、概率密度的表达式及相关物理量的含义?
2、电子云的概念?
3、电子云与概率密度的关系?
4、电子云中的小点与概率密度的关系?
任务二、认识电子云轮廓图
【学生活动】阅读教材P 第5,6自然段,和P 第1,2自然段,了解电子云轮廓图的内容,回答下
12 13
列问题:
1、绘制电子云轮廓图的目的?
2、绘制电子云轮廓图的方法?
3、s、p电子云轮廓图的形状?
4、p电子云轮廓图有几种,如何表示,什么关系?
5、电子云轮廓图的大小与能层序数的关系及产生这种变化的原因?
关系:
原因:
【对应训练1】下列说法中正确的是( )
A.电子云通常是用小黑点来表示电子的多少
B.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动
C.处于最低能量状态的原子叫基态原子
D.电子仅由激发态跃迁到基态时才会产生原子光谱
【对应训练2】下列关于电子云的叙述中不正确的是( )
A.电子云是用小黑点的疏密程度来表示电子在核外空间出现概率大小的图形
B.电子云实际上是电子运动形成的类似云一样的图形
C.电子云图说明离核越近,电子出现概率越大;离核越远,电子出现概率越小
D.能级类别不同,电子云的形态也不一样
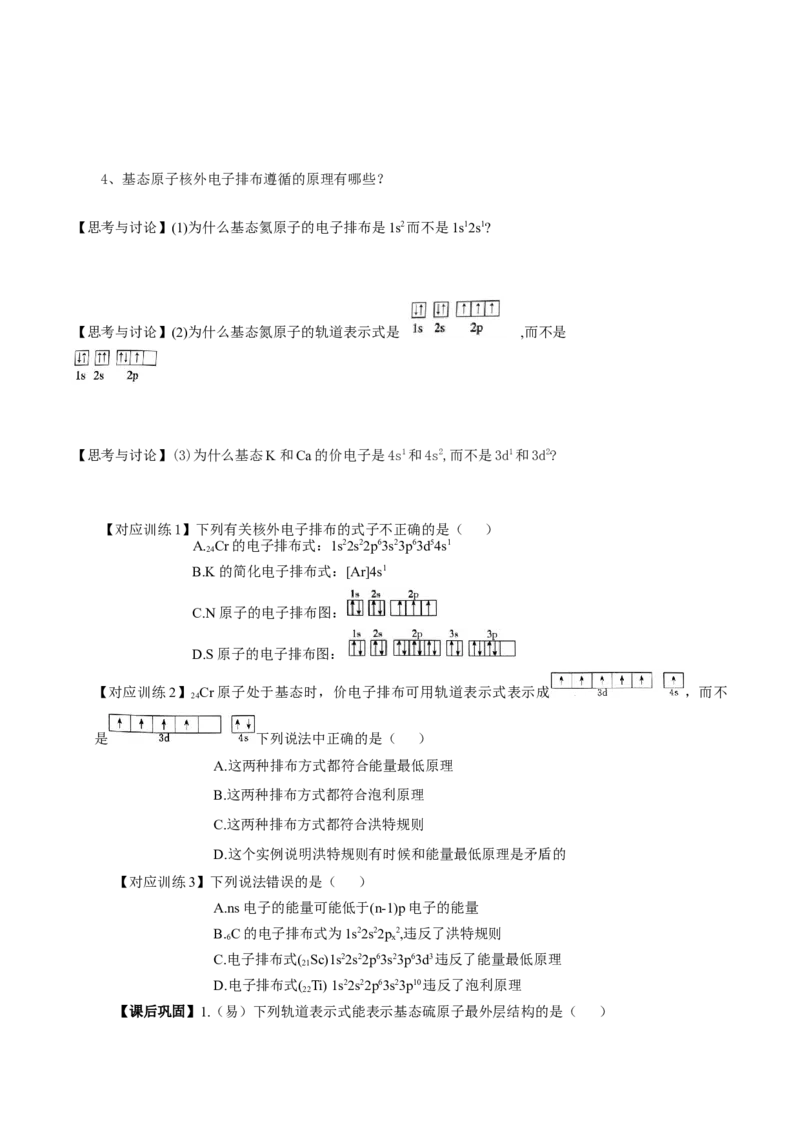
【对应训练3】下列关于1s电子在原子核外出现的概率分布图,也称电子云示意图(如图所示)
的有关说法中,正确的是( )
A.通常用小点来表示电子的多少,小点越密,电子数目越多B.小点越密,单位体积内电子出现的机会越大
C.氢原子核外电子绕核做高速圆周运动
D.氢原子的电子云就是氢原子的核外电子分布图
任务三、探究原子轨道
【学生活动】阅读教材P 表1-2,小组讨论归纳,回答下列问题:
14
1、原子轨道的形状有哪些?
2、同一能层,不同能级的原子轨道个数有什么规律?
3、不同能层,相同能级的原子轨道个数有什么规律?
4、原子轨道的个数由什么决定?
【思考题】1、同一能层不同能级的原子轨道,能量大小如何判断?
【思考题】2、同一能层相同能级的原子轨道,能量大小如何判断,例如:2p、2p、2p,这三个原子
x y z
轨道的能量大小关系如何?
【对应训练1】如图是s能级和p能级的原子轨道图,下列说法正确的是( )
A.s能级和p能级的原子轨道形状相同
B.每个p能级都有6个原子轨道
C.s能级的原子轨道半径与能层序数有关
D.钠原子的电子在11个原子轨道上高速运动
【对应训练2】下列轨道上的电子在xy平面上出现的机会为零的是( )
A. 3p B.3p C.3p D. 3s
z x y
【对应训练3】符号3p 所代表的含义是( )
x
A.p 轨道上有3个电子
x
B.第三能层p 轨道有3个伸展方向
x
C.p 电子云有3个伸展方向
x
D.第三能层沿x轴方向伸展的p轨道
【对应训练4】下列说法中正确的是( )
A.s电子云是在空间各个方向上伸展程度相同的对称形状B.p电子云的形状是对顶双球
C.L能层有d轨道
D.2d能级包含5个原子轨道,最多容纳10个电子
【对应训练5】下列说法正确的是( )
A.不同的原子轨道形状一定不相同
B.p轨道呈哑铃形,因此p轨道上的电子运动轨迹呈哑铃形
C.2p能级有3个p轨道
D.氢原子的电子运动轨迹呈球形
任务四、探究泡利原理
【学生活动】阅读教材P 第1,2自然段,回答下列问题:
14
1、电子自旋的含义?
2、电子自旋的取向?
3、电子自旋的表示方法?
4、泡利原理的内容?
任务五、探究电子排布的轨道表示式
【学生活动】阅读教材P 第1,2自然段,回答下列问题:
15
1、轨道表示式的含义?
2、轨道表示式的书写要求?
【学生活动】举一反三,通过教师讲授一个轨道表达式,学生能够自己书写下列原子的电子排布图
Na、Ar、F、Al、O、N
Na:
Ar:
F:
Al:
O:N:
任务六、探究洪特规则
【学生活动】阅读教材P 第3,4, P 前三个自然段,回答下列问题:
15 16
1、洪特规则的内容?
2、洪特规则适用的粒子范围?
3、洪特规则适用的轨道范围?
【学生活动】书写下列原子价层电子的轨道表示式?
C、P、S、As、Si、Se
C:
P:
S:
As:
Si:
Se:
【思考与讨论】(1)下列轨道表示式中哪个是硼的基态原子?为什么?
【思考与讨论】(2)下列轨道表示式中哪个是氧的基态原子?为什么?
任务七、探究能量最低原理
【学生活动】阅读教材P 第4,5,6三个自然段,回答下列问题:
16
1、能量最低原理的内容?
2、原子能量的决定因素有哪些?
3、电子填入能级的方式有哪些?4、基态原子核外电子排布遵循的原理有哪些?
【思考与讨论】(1)为什么基态氦原子的电子排布是1s2而不是1s12s1?
【思考与讨论】(2)为什么基态氮原子的轨道表示式是 ,而不是
【思考与讨论】(3)为什么基态K和Ca的价电子是4s1和4s2,而不是3d1和3d2?
【对应训练1】下列有关核外电子排布的式子不正确的是( )
A. Cr的电子排布式:1s22s22p63s23p63d54s1
24
B.K的简化电子排布式:[Ar]4s1
C.N原子的电子排布图:
D.S原子的电子排布图:
【对应训练2】 Cr原子处于基态时,价电子排布可用轨道表示式表示成 ,而不
24
是 下列说法中正确的是( )
A.这两种排布方式都符合能量最低原理
B.这两种排布方式都符合泡利原理
C.这两种排布方式都符合洪特规则
D.这个实例说明洪特规则有时候和能量最低原理是矛盾的
【对应训练3】下列说法错误的是( )
A.ns电子的能量可能低于(n-1)p电子的能量
B. C的电子排布式为1s22s22p2,违反了洪特规则
6 x
C.电子排布式( Sc)1s22s22p63s23p63d3违反了能量最低原理
21
D.电子排布式( Ti) 1s22s22p63s23p10违反了泡利原理
22
【课后巩固】1.(易)下列轨道表示式能表示基态硫原子最外层结构的是( )2.(易)下列有关碳原子的电子排布图中,能量最低的是( )
3.(易)图①和图②分别是1s电子的概率密度分布及图和电子云轮廓图。下列认识正确的是(
)
A.图①中的每个小黑点表示1个电子
B.图②表明1s电子云呈球形,有无数条对称轴
C.图②表示1s电子只能在球体内出现
D.不同能层的s电子云的半径相等
4.(易)下列排布不符合泡利原理的是( )
A.2p能级:
B.3d能级:
C.2p能级:
D.3d能级:
5.(中)下列叙述正确的是( )
A.可能存在基态核外电子排布为1s22s22p63s23p64s24p1的原子
B.在氢原子的电子云图中,小黑点的疏密程度表示电子在该区域出现的概率密度
C.当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,而且自旋方向相反
D.1个原子轨道里最多只能容纳2个电子,而且自旋方向相同
6.(易)正误判断,正确的打“√”,错误的打“×”。
(1)从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道。( )
(2)p能级能量一定比s能级的能量高。( )
(3)2p、3p、4p能级的轨道数依次增多。( )
(4)2p和3p轨道形状均为哑铃形。( )
(5)2p、2p、2p 轨道相互垂直,但能量相等。( )
x y z7.(中)基态原子的核外电子填充在6个轨道中的元素有 种,填充在7个轨道中的元素有 种。
8.(易)基态钾原子中,其电子占据的最高能层的符号是 ;基态钾离子的电子占据的最高能级共
有 个原子轨道,其形状是 。
9.(易)请写出下列基态粒子的简化电子排布式和价层电子的轨道表示式:
(1)Ti:
(2)Cr:
(3)Zn2+:
10.(难) A、B、C、D、E、F均为36号以前的元素。请完成下列空白:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的原子最外层电子排布式为nsnpn+1,其元素符号为
(3)C元素基态的正三价离子的3d轨道为半充满(即有5个电子),其元素符号为 ,其
基态原子的电子排布式为 。
(4)D 元素基态原子的 M 层全充满;N 层没有成对电子,只有一个未成对电子。D 的元素符号为
,其基态原子的价层电子的轨道表示式为 。
(5)E、F元素的基态原子都只有一个未成对电子;它们相互作用形成的离子的电子层结构相同,并且最高
能级的电子对数等于其最高能层的电子层数。E、F的元素符号分别为 。