文档内容
第二章 化学物质及其变化
第二节 离子反应
第二课时 离子反应及离子方程式
【学习目标】1.通过分析酸、碱、盐之间的反应事实及
硫酸
钠溶 液与氯化钡溶液反应实质探究,认
识离子反应,理解离子反应的定义及实质。
2.通过阅读思考,实例分析,知道离子方程式的定义、意义及书写步骤,理解离子反应发生的条
件,掌握常见离子方程式的书写及正误判断的基本方法。
3.通过实验探究、讨论交流、分析归纳等一系列科学研究过程,体验科学研究的基本方法,初步掌握
溶液中离子反应的基本类型。
【学习重点】离子反应的概念、发生条件、书写及正误判断
【学习难点】离子方程式的书写及正误的判断。
【课前预习】
旧知回顾:1.在酸的溶液里,酸根离子所带________的总数等于酸电离时生成的________的总数;在
碱的溶液里,跟金属离子结合的_______的总数等于这种金属离子所带的_____________的总数;在盐的溶
液中,金属(或铵根)离子所带的__________的总数等于酸根离子所带的__________的总数。
2.电解质电离方程式的书写规律:
(1)强酸、强碱、盐_______电离,用“===”表示。如HSO 、NaOH、(NH )SO 的电离方程式分别
2 4 4 2 4
为:
__________________________________________________________________________________。
(2)弱酸、弱碱_______电离,用“ ”表示。如 CHCOOH _____________、NH .H O
3 3 2
___________。
(3)多元弱酸分步电离______写,且电离程度逐步减弱,以第_____步电离为主。如HS电离方程式为
2
HS _________________________________ 。 多 元 弱 碱 ___ 步 电 离 ____ 步 写 。 如 Cu(OH)
2 2
__________。
新知预习:1.酸、碱、盐在水溶液中发生的复分解反应,实质是两种电解质在溶液中
_______________ , 该 类 离 子 反 应 发 生 的 条 件 是
____________________________________________________。
2.离子方程式:(1)定义是 ;
(2)离子方程式的特点① ;
② ;
(3)离子方程式的书写除了应遵守 定律外,还应遵守 。
【同步学习】
情景导入:传说三国时,诸葛亮为了擒拿南王孟获(历史上有名的七擒七纵),率军南征至云南西洱
河,遇四口毒泉,其中一口为哑泉。时逢天气好生炎热,人马饮用了哑泉水后,全都中毒,将士们都说不出话来。后来幸得一智者指教,复饮安乐泉水,“随即吐出恶涎,便能言语”。你知道其中的化学原理
吗?通过本节课的学习,我们就能解开这个谜团!(见PPT图片)
一、离子反应
活动一、探究离子反应的实质
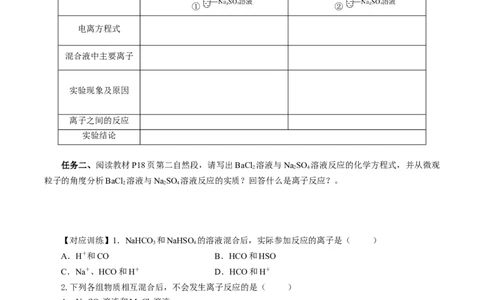
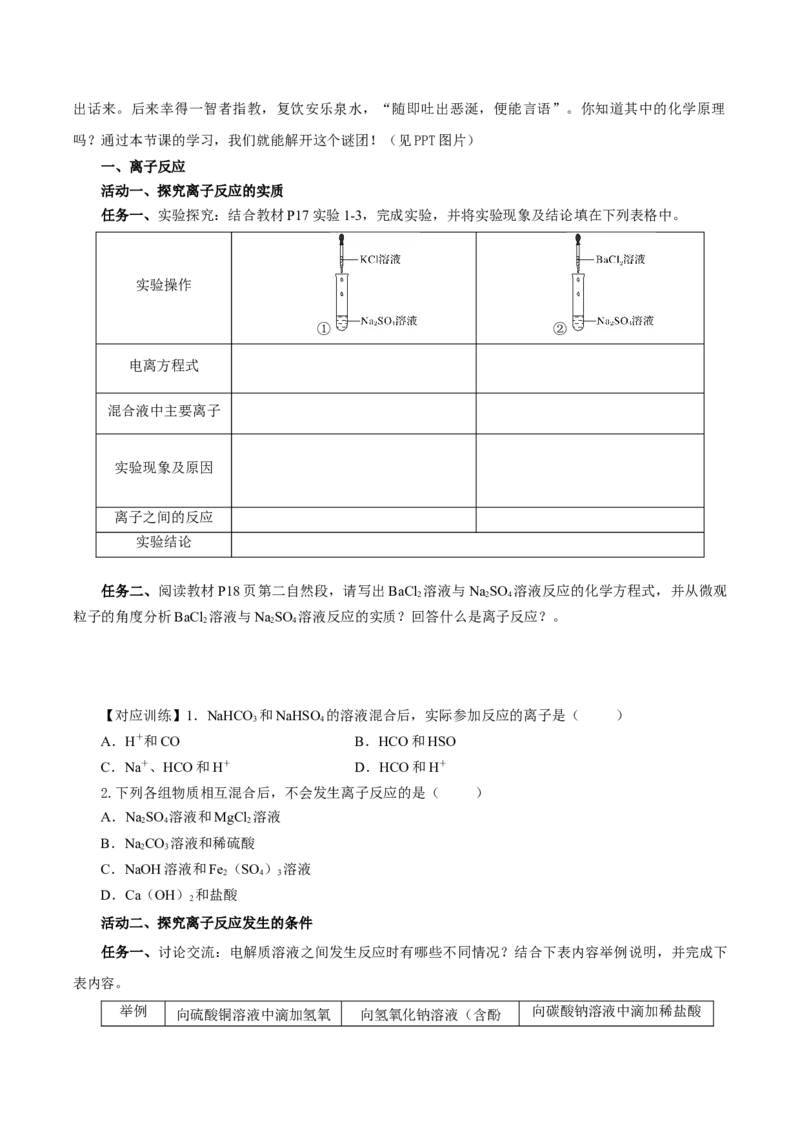
任务一、实验探究:结合教材P17实验1-3,完成实验,并将实验现象及结论填在下列表格中。
实验操作
① ②
电离方程式
混合液中主要离子
实验现象及原因
离子之间的反应
实验结论
任务二、阅读教材P18页第二自然段,请写出BaCl 溶液与NaSO 溶液反应的化学方程式,并从微观
2 2 4
粒子的角度分析BaCl 溶液与NaSO 溶液反应的实质?回答什么是离子反应?。
2 2 4
【对应训练】1.NaHCO 和NaHSO 的溶液混合后,实际参加反应的离子是( )
3 4
A.H+和CO B.HCO和HSO
C.Na+、HCO和H+ D.HCO和H+
2.下列各组物质相互混合后,不会发生离子反应的是( )
A.NaSO 溶液和MgCl 溶液
2 4 2
B.NaCO 溶液和稀硫酸
2 3
C.NaOH溶液和Fe (SO ) 溶液
2 4 3
D.Ca(OH) 和盐酸
2
活动二、探究离子反应发生的条件
任务一、讨论交流:电解质溶液之间发生反应时有哪些不同情况?结合下表内容举例说明,并完成下
表内容。
举例 向硫酸铜溶液中滴加氢氧 向氢氧化钠溶液(含酚 向碳酸钠溶液中滴加稀盐酸化钠溶液 酞)中滴加酚酞
现象
离子方
程式
分析
任务二、归纳总结:结合上面分析,阅读教材P19页第二自然段,你认为酸、碱、盐在水溶液中发生
的复分解反应的条件及结果分别是什么?
任务三、应用探究:已知,铜为重金属,可溶性的Cu2+会使蛋白质变性,因此,如果人和动物喝了含
Cu2+的水就会中毒。哑泉水是一种含铜盐的泉水,主要成分为硫酸铜,称为胆水。这种胆水饮用后会使人
恶心、呕吐、腹泻,言语不清,直至虚脱、痉挛而死。而安乐泉水中含有大量的石灰水,请你用所学知识
解释用安乐泉水给哑泉水解毒的原理。
【对应训练】1.下列不能发生离子反应的是( )
①NaCl溶液与AgNO 溶液 ②KNO 溶液与NaOH溶液 ③稀硫酸与BaCl 溶液 ④盐酸与NaCO 溶
3 3 2 2 3
液 ⑤NaCO 溶液与Ca(OH) 溶液 ⑥NaOH溶液与稀HNO 溶液 ⑦锌与CuSO 溶液 ⑧稀HSO 和
2 3 2 3 4 2 4
NaCl溶液 ⑨NaSO 溶液和CuCl 溶液
2 4 2
2.在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液或通入一种气
体时,则灯泡由亮变暗至熄灭后又逐渐变亮的是( )A.稀盐酸中逐滴加入食盐溶液 B.稀硫酸中逐滴加入氢氧化钠溶液
C.饱和石灰水中不断通入CO D.稀硝酸中逐滴加入氢氧化钡溶液
2
二、离子方程式
活动一、探究离子方程式书写
任务一、思考交流:阅读教材P18页内容,结合离子反应的实质回答离子方程式的定义及意义是什
么?
任务二、讨论交流:阅读教材P18页第三自然段,思考书写离子方程式有哪些步骤?并举例说明。
任务三、拓展探究:在书写离子方程式时,有哪些特殊的物质需“拆”或“不拆”?
【对应训练】1.下列指定溶液之间的反应不能用离子方程式SO +Ba2+=BaSO ↓表示的是( )
4
A.NaSO 与Ba(OH) B.MgSO 与BaCl
2 4 2 4 2
C.HSO 与Ba(OH) D.HSO 与Ba(NO )
2 4 2 2 4 3 2
2.下列反应的离子方程式书写正确的是( )
A.氧化铜与稀硫酸反应:CuO+4H++SO =Cu2++SO↑+2H O
2 2B.二氧化碳通入足量澄清石灰水中:Ca2++2OH-+CO =CaCO ↓+H O
2 3 2
C.铁和盐酸反应:2Fe+6H+=2Fe3++3H ↑
2
D.氢氧化钡溶液与硫酸反应:OH-+H+=H O
2
活动二、探究离子方程式正误的判断
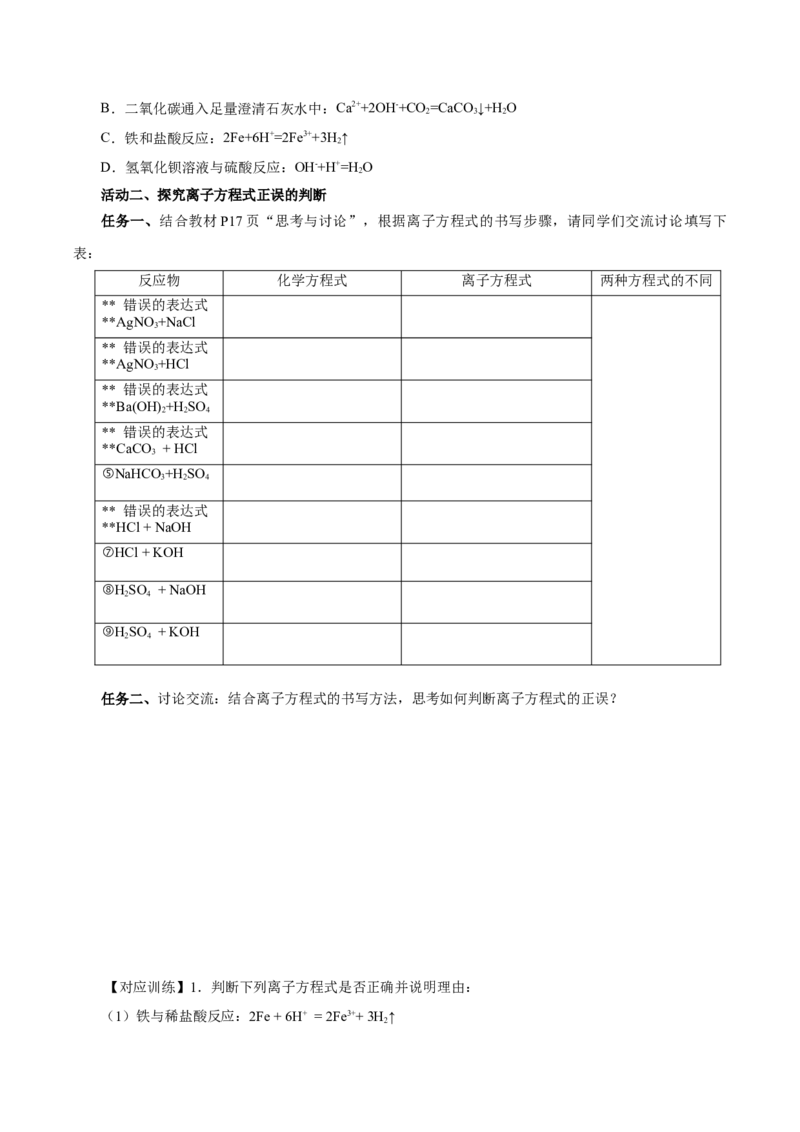
任务一、结合教材P17页“思考与讨论”,根据离子方程式的书写步骤,请同学们交流讨论填写下
表:
反应物 化学方程式 离子方程式 两种方程式的不同
** 错误的表达式
**AgNO+NaCl
3
** 错误的表达式
**AgNO+HCl
3
** 错误的表达式
**Ba(OH) +H SO
2 2 4
** 错误的表达式
**CaCO + HCl
3
⑤NaHCO +H SO
3 2 4
** 错误的表达式
**HCl + NaOH
⑦HCl + KOH
⑧HSO + NaOH
2 4
⑨H SO + KOH
2 4
任务二、讨论交流:结合离子方程式的书写方法,思考如何判断离子方程式的正误?
【对应训练】1.判断下列离子方程式是否正确并说明理由:
(1)铁与稀盐酸反应:2Fe + 6H+ = 2Fe3++ 3H ↑
2(2)铝与稀盐酸反应:Al + 3H+ = Al3+ + H ↑
2
(3)澄清石灰水与盐酸反应:Ca(OH) +2H+===2HO+Ca2+
2 2
(4)硫酸和Ba(OH) 溶液反应:Ba2+ + OH-+ H+ + SO 2-= BaSO↓ + H O
2 4 4 2
(5)碳酸钡和稀硝酸反应:CO2-+2H+ = H O+CO↑
3 2 2
2.下列离子方程式正确的是( )
A.石灰石与盐酸反应:CO+2H+===CO ↑+HO
2 2
B.铜和硝酸银溶液反应:Cu+Ag+===Cu2++Ag
C.向Ba(OH) 溶液中逐滴滴加NaHSO 溶液至SO恰好沉淀完全:Ba2++2OH-+2H++SO===BaSO ↓
2 4 4
+2HO
2
D.NH HCO 溶液与过量稀盐酸混合:HCO+H+===CO ↑+HO
4 3 2 2
【课后巩固】1.(易中)教材作业:P20-21页练习3、6、7、8
2.(易)下列物质混合后,不会发生离子反应的是( )
A.NaOH溶液和FeCl 溶液 B.NaCO 溶液和稀硫酸
3 2 3
C.NaSO 溶液和MgCl 溶液 D.澄清的石灰水和盐酸
2 4 2
3.(易)下列反应属于离子反应的是( )
A.HO和CO 气体的反应 B.NH 溶于水的反应
2 2 3
C.硝酸与Ca(OH) 溶液的反应 D.H 在O 中燃烧
2 2 2
4.(中)下列符合离子方程式Ba2++SO===BaSO ↓的化学反应是(均指溶液间)( )
4
A. HSO 和Ba(OH) 混合 B.HSO 与BaCl 混合
2 4 2 2 4 2
C.Ba(OH) 与NaSO 混合 D.Ba(OH) 与NaHSO 混合
2 2 4 2 4
5.(中)下列反应的离子方程式书写正确的是( )
A.稀硫酸滴在铜片上:Cu+2H+===Cu2++H↑
2
B.稀硫酸与氢氧化钡溶液混合:SO+Ba2+===BaSO ↓
4
C.稀硝酸滴在大理石上:CaCO +2H+===Ca2++HCO
3 2 3
D.氧化铁与稀盐酸混合:Fe O+6H+===2Fe3++3HO
2 3 2
6.(中)下列反应的离子方程式中,正确的是( )
A.氢氧化钡溶液和稀硫酸Ba2++OH-+H++SO2-==BaSO↓+2H O
4 4 2
B.氯化铁溶液中加铁粉 Fe3+ + Fe == 2Fe2+
C.少量CO 通入NaOH溶液中 CO + 2OH-== CO2- + H O
2 2 3 2D.澄清石灰水与稀盐酸反应Ca(OH) +2H+== Ca2++2H O
2 2
7.(难)下列反应的离子方程式书写正确的是( )
A.向NaHSO 溶液中滴入Ba(OH) :H++OH-=H O
4 2 2
B.碳酸钙溶于醋酸:CaCO +2H+=Ca2++H O+CO↑
3 2 2
C.NaOH溶液与少量CO 反应的离子方程式:OH-+CO =H O+CO2-
2 2 2 3
D.碳酸氢钠溶液与少量澄清石灰水混合出现白色沉淀: +Ca2++OH-=CaCO ↓+H O
3 2
8.(难)♦向Ba(OH) 溶液中逐滴加入稀硫酸,请完成下列问题:
2
(1)写出反应的离子方程式:____________________________________________________。
(2)下列三种情况下,离子方程式与(1)相同的是______(填字母)。
A.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至溶液显中性
4 2
B.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至SO恰好完全沉淀
4 2
C.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至过量
4 2
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似用上图中
的________曲线表示(填字母)。
(4)若向装有Ba(OH) 溶液的烧杯里缓缓滴入KAl(SO ) 溶液至Ba2+恰好完全反应。则反应的离子方程
2 4 2
式是__________________________________________。