文档内容
第二章 分子结构与性质
第二节 分子的空间结构
第一课时 分子结构的测定、多样的分子空间结构、价层电子对互斥模型
【学习目标】1. 结合实例了解共价分子具有特定的空间结构,并可运用相关理论和模型进行解释和预测。
2. 知道分子的结构可以通过波谱、晶体X射线衍射等技术进行测定。
【学习重点】应用价层电子对互斥模型预测简单分子或离子的空间结构。
【学习难点】中心原子上的孤电子对数的计算。
【课前预习】
旧知回顾:
1、H、HCl、CH、HO、CO 的分子结构:
2 4 2 2
H:直线形 HCl:直线形 CH:正四面体形 HO:V形 CO:直线形
2 4 2 2
2、常见物质电子式的书写:H、Cl、N、HCl、CH、NH、HO、CO、HO、HClO、HCHO
2 2 2 4 3 2 2 2 2
新知预习:
1、红外光谱的测定原理?
分子中的原子不是固定不动的,而是不断地振动着的。当一束红外线透过分子时,分子会吸收跟它的
某些化学键的振动频率相同的红外线,再记录到图谱上呈现吸收峰。通过和已有谱图库比对,或通过
量子化学计算,可以得知各吸收峰是由哪种化学键、哪种振动方式引起的。
2、红外光谱的应用?
分析出分子中含有何种化学键或官能团的信息
3、价层电子对互斥模型的应用?
预测分子的空间结构
4、价层电子对互斥模型的内容?
价层电子对互斥模型认为,分子的空间结构是中心原子周围的“价层电子对”相互排斥的结果。
VSEPR的“价层电子对”是指分子中的中心原子与结合原子间的 σ键电子对和中心原子上的孤电子对。
多重键只计其中的σ键电子对,不计π键电子对。
5、中心原子的价层电子对数如何确定?
σ键电子对数+孤电子对数=价层电子对数【课中探究】
情景导入:播放多样的分子结构视频,导入新课。
一、分子结构的测定
任务一、探究分子结构测定的方法
【学生活动】阅读教材P 第1、2、3自然段和P 图2-6,回答下列问题:
41 42
1、常见的测定分子结构的方法?
红外光谱、晶体X射线衍射
2、红外光谱的测定原理?
分子中的原子不是固定不动的,而是不断地振动着的。当一束红外线透过分子时,分子会吸收跟它的
某些化学键的振动频率相同的红外线,再记录到图谱上呈现吸收峰。通过和已有谱图库比对,或通过
量子化学计算,可以得知各吸收峰是由哪种化学键、哪种振动方式引起的。
3、红外光谱的应用?
分析出分子中含有何种化学键或官能团的信息
任务二、探究质谱法测定分子的相对分子质量
【学生活动】阅读教材P 科学技术社会,回答下列问题:
42
1、质谱法的测定内容?
利用质谱仪测定分子的相对分子质量
2、质谱法的测定原理?
在质谱仪中使分子失去电子变成带正电荷的分子离子和碎片离子等粒子。由于生成的离子具有不同的
相对质量,它们在高压电场加速后,通过狭缝进入磁场得以分离,在记录仪上呈现一系列峰,化学家
对这些峰进行系统分析,便可得知样品分子的相对分子质量。
3、质谱图中横纵坐标的含义?
纵坐标是相对丰度(与粒子的浓度成正比)
横坐标是粒子的相对质量与其电荷数之比,简称质荷比
4、质谱图的使用方法?
质谱图中,横坐标最右侧,数值最大的质荷比,就是该分子的相对分子质量
【对应训练1】在研究有机物的组成和结构时,可用于确定化学键和官能团信息的方法是( )
A.质谱法 B.红外光谱法 C.核磁共振氢谱法 D.燃烧法
【答案】B
【解析】A.质谱法用于测定有机物的相对分子质量,不能测定出有机物的化学键和官能团,A错误;B.红
外光谱法能测定出有机物的官能团和化学键,B正确;C.核磁共振氢谱法用于测定有机物分子中氢原子的
种类和数目,不能测定出有机物的化学键和官能团,C错误;D.燃烧法用于元素的定性分析和定量测定,
不能确定化学键和官能团信息,D错误。
【对应训练2】能够快速、微量、精确测定有机物相对分子质量的物理方法是 ( )
A.红外光谱法 B.质谱法 C.核磁共振氢谱法 D.色谱法【答案】B
【解析】红外光谱法主要用于鉴定官能团;质谱法其实是把有机物打成很多带正电荷的粒子,在记录仪上
会有很多不同的峰出现,从而推测出该有机物的相对分子质量,所以能够快速、微量、精确测定有机物相
对分子质量的物理方法是质谱法;核磁共振氢谱法用于判断等效氢种类;色谱法是分离混合物的一种方法。
综上所述,B项符合题意。
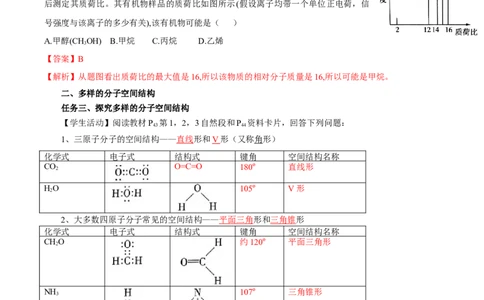
【对应训练3】质谱法能够对有机分子结构进行分析,其方法是让极少量的(10-9g)
化合物通过质谱仪的离子化室,样品分子大量离子化,少量分子碎裂成更小的离子,然
后测定其质荷比。其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信
号强度与该离子的多少有关),该有机物可能是( )
A.甲醇(CHOH) B.甲烷 C.丙烷 D.乙烯
3
【答案】B
【解析】从题图看出质荷比的最大值是16,所以该物质的相对分子质量是16,所以可能是甲烷。
二、多样的分子空间结构
任务三、探究多样的分子空间结构
【学生活动】阅读教材P 第1,2,3自然段和P 资料卡片,回答下列问题:
43 44
1、三原子分子的空间结构——直线形和V 形(又称角形)
化学式 电子式 结构式 键角 空间结构名称
CO O=C=O 180º 直线形
2
HO 105º V形
2
2、大多数四原子分子常见的空间结构——平面三角形和三角锥形
化学式 电子式 结构式 键角 空间结构名称
CHO 约120º 平面三角形
2
NH 107º 三角锥形
3
3、五原子分子常见的空间结构——四面体形
化学式 电子式 结构式 键角 空间结构名称
CH 109º28´ 正四面体形
4
4、C H 的椅式和船式的稳定性强弱?
2 6C H 的椅式比船式稳定
2 6
【对应训练1】下列分子的空间结构模型正确的是 ( )
A.CO 的空间结构模型
2
B.H O的空间结构模型
2
C.NH 的空间结构模型
3
D.CH 的空间结构模型
4
【答案】D
【解析】CO 的空间结构模型为直线形,A项错误;HO的空间结构模型为V形,B项错误;NH 的空间
2 2 3
结构模型为三角锥形,C项错误;CH 的空间结构模型为正四面体形,D项正确。
4
【对应训练2】下列分子的空间结构与分子中共价键键角对应正确的是 ( )
A.V形:105°
B.平面正三角形:120°
C.三角锥形:109°28´
D.正四面体形:109°28´
【答案】B
【解析】A.二氧化硫分子为V形,键角不是105°,故A错误;C.氨气分子为三角锥形,键角为107°,故C错
误;D.白磷分子为正四面体形,键角为60°,故D错误。
【对应训练3】下列物质分子的空间结构与CH 相同的是( )
4
A. H O B. P C. NH D. CO
2 4 3 2
【答案】B
【解析】CH 是正四面体形结构,HO是V形结构,NH 是三角锥形结构,P 是正四面体形结构,CO 是直
4 2 3 4 2
线形结构。
三、价层电子对互斥模型
任务四、探究价层电子对互斥模型的相关内容
【学生活动】阅读教材P 和P 及表格2-3,小组合作,回答下列问题:
44 45
1、价层电子对互斥模型的应用?
预测分子的空间结构
2、价层电子对互斥模型的内容?价层电子对互斥模型认为,分子的空间结构是中心原子周围的“价层电子对”相互排斥的结果。
VSEPR的“价层电子对”是指分子中的中心原子与结合原子间的σ键电子对和中心原子上的孤电
子
对。多重键只计其中的σ键电子对,不计π键电子对。
3、σ键电子对数如何确定?
由化学式确定
4、中心原子上的孤电子对数如何确定,公式中各个字母代表的涵义?
1
(a−xb)
2
中心原子上的孤电子对数=
公式中各字母的含义:
中心原子的价层电子数
主族元素 =最外层电子数
a
阳离子 =中心原子的价电子数-离子的电荷数
阴离子 =中心原子的价电子数+︱离子的电荷数︱
x 与中心原子结合的原子数
与中心原子结合的原子最多能接受的电子数
b H =1
其他原子 =8-该原子的价层电子数
【思考与讨论】
(1)以S和P为例,说明如何根据主族元素在周期表中的位置确定它的价电子数。
依据元素周期表可判断主族元素的族序数等于最外层电子数,也等于价电子数。S和P都分别处于
第三周期第VIA族和第VA族,因此S和P的价电子数分别为6和5。
(2)以N和C1为例,说明如何根据主族元素在周期表中的位置确定它最多能接受的电子数。
首先依据N和Cl在元素周期表中的位置,判断其价电子数分别为5和7,它们最多能接受的电子数
为“8减去原子的价电子数”,因此N和Cl最多能接受的电子数分别为3和1。
【对应训练1】下列分子或离子中含有孤电子对的是( )
A.HO B. CH C. SiH D.NH +
2 4 4 4
【答案】A
【解析】HO有2对孤电子对,其余均无孤电子对。
2
【对应训练2】SO 2—的中心原子孤电子对计算公式为1/2(a-xb)中,下列对应的数值正确的是(
3
)
A.a=8 x=3 b=2 B.a=6 x=3 b=2
C.a=4 x=2 b=3 D.a=6 x=2 b=3
【答案】A
【解析】SO 2—的中心原子孤电子对计算公式1/2(a-xb)中,a指中心原子价电子个数,x指配原子个数,b指
3
配原子形成稳定结构需要的电子个数,因此a=6+2=8,x=3,b=2。
【对应训练3】下列有关价层电子对互斥模型的描述正确的是( )
A.价层电子对就是σ键电子对 B.孤电子对数由分子式来确定C.分子的空间结构是价层电子对互斥的结果 D.孤电子对数等于π键数
【答案】C
【解析】价层电子对数是σ键电子对数与孤电子对数之和,孤电子对数是指没有成键的价电子对数,其与
中心原子价层电子总数、与中心原子结合的原子最多能接受的电子数及与中心原子结合的原子数有关,
A、B、D项错误。
任务五、探究用价层电子对互斥模型判断分子的空间结构
【学生活动】阅读教材P 第一自然段和P 第一自然段及表2-4,回答下列问题:
46 47
1、中心原子的价层电子对数如何确定?
σ键电子对数+孤电子对数=价层电子对数
2、VSEPR模型与分子的空间构型有什么关系?
略去VSEPR模型中的中心原子上的孤电子对,便可得到分子的空间结构
3、价层电子对互斥模型不能用于预测什么样的分子?
价层电子对互斥模型对分子空间结构的预测少有失误,但它不能用于预测以过渡金属为中心原子的分
子
【思考与讨论】确定BF、NH +和SO 2-的VSEPR模型和它们的空间结构,并与同学讨论
3 4 3
BF 的σ键电子对数为 3,中心原子 B的孤电子对数为 0,所以BF 的价层电子对数为 3。BF 的
3 3 3
VSEPR模型为平面三角形,BF 的空间结构为平面三角形。
3
NH +的σ键电子对数为4,中心原子N的孤电子对数为 0,所以NH +的价层电子对数为 4。NH +的
4 4 4
VSEPR模型为正四面体形,NH +的空间结构为正四面体形。
4
SO 2-的σ键电子对数为3,中心原子S的孤电子对数为1,所以SO 2-的价层电子对数为4。SO 2-的
3 3 3
VSEPR模型为四面体形,SO 2-的空间结构为三角锥形。
3
【对应训练1】用价层电子对互斥模型预测HS和COCl 的空间结构,两个结论都正确的是( )
2 2
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
【答案】D
【解析】HS中的中心原子S上的孤电子对数是1/2×(6-1×2)=2,则说明HS中的中心原子的价层电子对数为
2 2
4,因此空间结构是V形;而COCl 中的中心原子C上的孤电子对数是1/2×(4-2×1-1×2)=0,因此COCl 中的中
2 2
心原子的价电子对数是3,是平面三角形结构。
【对应训练2】下列分子的空间结构为正四面体形的是( )
①P ②NH ③CCl ④CH ⑤HS ⑥CO
4 3 4 4 2 2
A.①③④⑤ B.①③④⑤⑥ C.①③④ D.④⑤
【答案】C
【解析】P 白磷的结构,正四面体形;氨气三角锥形,四氯化碳和甲烷是正四面体形,硫化氢是 V形,二
4
氧化碳是直线形。
【对应训练3】用 VSEPR模型预测下列分子或离子的空间结构,其中不正确的是( )A. NH+为正四面体形 B.CS 为直线形
4 2
C.HCN为V形 D.PCl 为三角锥形
3
【答案】C
【解析】NH +、CS 、HCN中心原子上的价电子都用于形成共价键,没有孤电子对,所以其空间结构分别
4 2
为正四面体形、直线形、直线形;PCl 中心P原子上有一对孤电子对,未用于形成共价键,其空间结构为
3
三角锥形。
【课后巩固】1.(易)下列离子的VSEPR模型与离子的空间结构一致的是( )
A.SO 2- B.ClO- C.NO- D.ClO -
3 4 2 3
【答案】B
【解析】SO 2-中S原子价层电子对数为3+1/2(6+2-3×2)=4,含有1对孤电子对,VSEPR模型是四面体形,
3
SO 2-的空间结构是三角锥形,A错误:ClO-中Cl原子价层电子对数为4+1/2(7+1-4×2)=4,不含孤电子对,
3 4
VSEPR模型和ClO-的空间结构都是四面体形,B正确;NO -中N原子价层电子对数为2+1/2(5+1-2×2)=3,
4 2
含有1对孤电子对,VSEPR模型是平面三角形,NO -的空间结构是V形,C错误;ClO-中Cl原子价层电
2 3
子对数为3+1/2(7+1-3×2)=4,有1对孤电子对, VSEPR模型是四面体形,而ClO-的空间结构是三角锥形,
3
D错误。
2.(易)下列粒子的VSEPR模型为四面体且其空间结构为V形的是( )
A .SO B.NF C.H O+ D.OF
2 3 3 2
【答案】D
【解折】SO 中S原子的价层电子对数为2+1/2 (6-2×2)=3,含有1对孤电子对,VSEPR模型是平面三角形,
2
SO 的空间结构是V形,A错误:NF 中N原子的价层电子对数为3+1/2 (5-3×1)=4,含有1对孤电子对,
2 3
VSEPR模型是四面体形,NF 的空间结构是三角锥形,B错误;HO+中O原子的价层电子对数为3+1/2 (6-
3 3
1-3×1)=4,含有1对孤电子对,VSEPR模型是四面体形,HO+的空间结构是三角锥形,C错误;OF 中O
3 2
原子的价层电子对数为2+1/2 (6-2×1)=4,含有2对孤电子对,VSEPR模型是四面体形,OF 的空间结构是V
2
形, D正确。
3.(易)下列各组粒子的空间结构相同的是( )
①NH 和HO;②NH +和HO+;③NH 和HO+;④O 和SO ;⑤CO 和BeCl
3 2 4 3 3 3 3 2 2 2
A.全部 B.①②③⑤ C.③④⑤ D.②⑤
【答案】C
【解析】NH 和HO的VSEPR模型都是四面体形,前者空间结构是三角锥形,后者是 V形,①错误;
3 2
NH +和HO+的VSEPR模型都是四面体形,前者空间结构是正四面体形,后者是三角锥形,②错误;NH
4 3 3
和HO+的VSEPR模型都是四面体形,空间结构都是三角锥形, ③正确;O 和SO 的VSEPR模型都是平
3 3 2面三角形,二者空间结构都是V形,④正确;CO 和BeCl 的VSEPR模型、分子的空间结构都是直线形,
2 2
⑤正确。
4.(中)下列说法中不正确的是( )
A.测定分子结构的现代仪器和方法有红外光谱、晶体X射线衍射等
B.红外光谱属于原子光谱中的吸收光谱
C.红外光谱可测定分子中含有化学键或官能团的信息
D.当红外光束透过分子时,分子会吸收与它的某些化学键的振动频率相同的红外线
【答案】B
【解析】原子光谱是原子中的电子在不同能级轨道上跃迁时吸收或释放能量所得到的光谱,红外光谱不是
原子光谱,属于分子光谱。
5.(易)下列说法中不正确的是( )
A.早年科学家主要靠对物质的化学性质进行系统总结得出规律后推测分子的结构
B.CH CHOH的红外光谱图中显示含有C-H、C-O、O-H等键
3 2
C.质谱仪的基本原理是在质谱仪中使分子得到电子变成分子离子和碎片离子等粒子
D.化学家根据质谱图中最大质荷比推测被测物的相对分子质量
【答案】C
【解析】质谱仪的基本原理是在质谱仪中使分子失去电子变成带正电荷的分子离子和碎片离子等粒子,C
错误。
6.(多选)(中)下列有关键角与分子空间结构的说法不正确的是( )
A.键角为180°的分子,空间结构是直线形
B.键角为120°的分子,空间结构是平面三角形
C.空间结构是正四面体形,键角一定是109°28´
D.键角在90°~109°28´之间的分子,空间结构可能是V形
【答案】BC
【解析】A.键角为180°的分子,空间结构是直线形,例如二氧化碳等,A正确;B.乙烯分子的键角为120°,
但它的空间结构并不是平面三角形,B错误;C.正四面体形分子键角可能为109°28´,如甲烷,也可能为
60°,如白磷,C错误;D.键角在90°~109°28´之间的分子,空间结构可能是V形,例如水等,D正确。
7.(易)下列分子或离子中,空间结构是平面三角形的是( )
A. CH B. NH + C. NO — D. CO
4 4 3 2
【答案】C
【解析】CH 中C原子孤电子对数为1/2×(4-4×1)=0,价层电子对数为4,分子为正四面体结构,A项错误;
4NH +中N原子孤电子对数为1/2×(5-1-4×1)=0,价层电子对数为4,离子为正四面体结构,B项错误;NO —中
4 3
N原子孤电子对数为1/2×(5+1-2×3)=0,价层电子对数为3,离子为平面三角形,C项正确;CO 中C原子孤电
2
子对数为1/2×(4-2×2)=0,价层电子对数为2,分子呈直线形,D项错误。
8.(易)下列分子或离子的中心原子,带有一对孤电子对的是( )
A.HO B. BeCl C. CH. D. PCl
2 2 4 3
【答案】D
【解析】HO有2对孤电子对,BeCl 和CH 没有孤电子对。
2 2 4
9.(中)下列有关分子空间结构说法中正确的是( )
A.HClO、BF、NCl 分子中所有原子的最外层电子都满足了8电子稳定结构
3 3
B.SO 与CO2—的空间结构均为平面三角形
3 3
C.分子中键角的大小:BeCl >SnCl >SO>NH >CCl
2 2 3 3 4
D.BF 键角大于120°
3
【答案】B
【解析】A.HClO分子中的H原子和BF 分子中的B原子的最外层都未达到8电子稳定结构,A项错误。
3
B.SO 与CO2—中心原子价层电子对数均为3,无孤电子对,都是平面三角形的分子,B项正确。C.BeCl 的
3 3 2
空间结构为直线形,键角为180°;SnCl 呈V形,分子中含有1对孤电子对,由于该孤电子对的存在,使键
2
角小于120°;SO 的空间结构为平面正三角形,键角为120°;NH 的空间结构为三角锥形,键角为107°;CCl
3 3 4
的空间结构为正四面体形,键角为109°28´;故分子中键角的大小为:BeCl >SO>SnCl >CCl >NH,C项错误。
2 3 2 4 3
D.BF 分子中的中心原子 B价层电子对数为 3+1/2×(3-3×1)=3,无孤电子对,是平面三角形分子,键角为
3
120°,D项错误。
10.(中)(1)用 VSEPR模型推测下列分子或离子的空间结构。
①HCN(H-C≡N) ; ②AlBr (共价分子) ;
3
③CO2— ; ④SO 2—
3 4
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种
微粒的球棍模型,写出相应的化学式。
;
(3)按要求写出第二周期非金属元素构成的中性分子的化学式。
平面三角形分子 ;三角锥形分子 ;四面体形分子 。
【答案】(1)直线形 平面三角形 平面三角形 正四面体形(2)CH+ CH—(3)BF NF CF
3 3 3 3 4