文档内容
第二章 分子结构与性质
第三节 分子结构与物质的性质
第二课时 分子间的作用力、分子的手性
【学习目标】1.认识分子间存在相互作用,知道范德华力和氢键是两种常见的分子间作用力
2.了解分子内氢键和分子间氢键在自然界中的广泛存在及重要作用
【学习重点】分子间作用力、氢键及其对物质性质的影响
【学习难点】手性分子的概念
【课前预习】
旧知回顾:
1、分子间作用力的定义及最初的叫法?
2、范德华力与化学键的强弱?
3、氢键与范德华力、化学键的强弱?
4、氢键对物质熔沸点的影响及原因?
5、冰能浮在水面上的原因?
新知预习:
1、范德华力与化学键的大小关系?
2、相对分子质量和分子的极性对范德华力的影响方式?3、氢键的定义?
4、氢键的形成条件?
5、氢键与化学键的关系?
6、“相似相溶”规律的内容?
7、手性异构体的定义?
【课中探究】
情景导入:播放世界上最粘的不粘材料视频,导入新课
一、分子间的作用力
任务一、探究范德华力及其对物质性质的影响
【学生活动】阅读教材P 自然段和P 表2-7,回答下列问题:
55-56 56
1、范德华力的定义?
2、范德华力的特征?
3、影响范德华力的因素?
【思考与讨论】怎样解释卤素单质从F 到I 的熔点和沸点越来越高?
2 2
任务二、探究氢键及其对物质性质的影响
【学生活动】阅读教材P 自然段和图2-26和2-27及P 资料卡片,小组讨论,回答下列问题:
57 581、氢键的定义?
2、氢键的形成条件?
3、氢键的表达方式?
4、氢键的特征?
5、氢键的存在范围及对物质沸点的影响,举例说明?
6、氢键的键长表达式?
7、氢键对物质性质的影响?
【学生活动】阅读教材P 科学技术社会——生物大分子中的氢键,了解氢键在生命活动中的重要作
58
用。
任务三:探究物质溶解性的规律
【学生活动】阅读教材P 自然段和图2-30,小组讨论,回答下列问题:
59
1、“相似相溶”规律的内容?
2、影响溶解度的因素,从内因和外因两部分进行思考,提示,外因可以从温度压强等因素考虑?
【思考与讨论】(1)比较NH 和CH 在水中的溶解度。怎样用“相似相溶”规律理解它们的溶解度不同?
3 4(2)为什么在日常生活中用有机溶剂(如乙酸乙酯等)溶解油漆而不用水?
(3)在一个小试管里放入一小粒碘晶体,加入约 5mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,
可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约 1mL四氯化碳(CCl ),振
4
荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1mL浓碘化
钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I +I-I- 。
2 3
实验表明碘在纯水还是在四氯化碳中溶解性较好?为什么?
【对应训练1】下列叙述正确的是( )
A.F、Cl、Br 、I 单质的熔点依次升高,与分子间作用力大小有关
2 2 2 2
B.H S的相对分子质量比HO的大,其沸点比水的高
2 2
C.稀有气体的化学性质比较稳定,是因为其键能很大
D.干冰汽化时破坏了共价键
【对应训练2】下列有关范德华力的叙述正确的是( )
A.范德华力的实质也是一种电性作用,所以范德华力是一种特殊的化学键
B.范德华力与化学键的区别是作用力的强弱不同
C.任何分子间在任意情况下都会产生范德华力
D.范德华力非常微弱,故破坏范德华力不需要消耗能量
【对应训练3】下列说法正确的是( )
A.正是由于氢键的存在,冰能浮在水面上 B.氢键是自然界中最重要、存在最广泛的化学键之一
C.由于氢键的存在,沸点:AsH >PH>NH D.由于氢键的存在,水分子中氢氧键键角是105°
3 3 3
【对应训练4】下列现象中,不能用“相似相溶”规律解释的是( )
A.乙醇与水以任意比例互溶 B.用纯碱洗涤油脂
C.氨气易溶于水 D.用苯将溴水中的溴萃取出来
任务三、探究分子的手性对生产生活的影响
【学生活动】阅读教材P 至P 自然段和图2-32,2-33,2-34,2-35,回答下列问题:
60 61
1、手性异构体的定义2、手性分子的定义?
3、手性催化剂的特点?
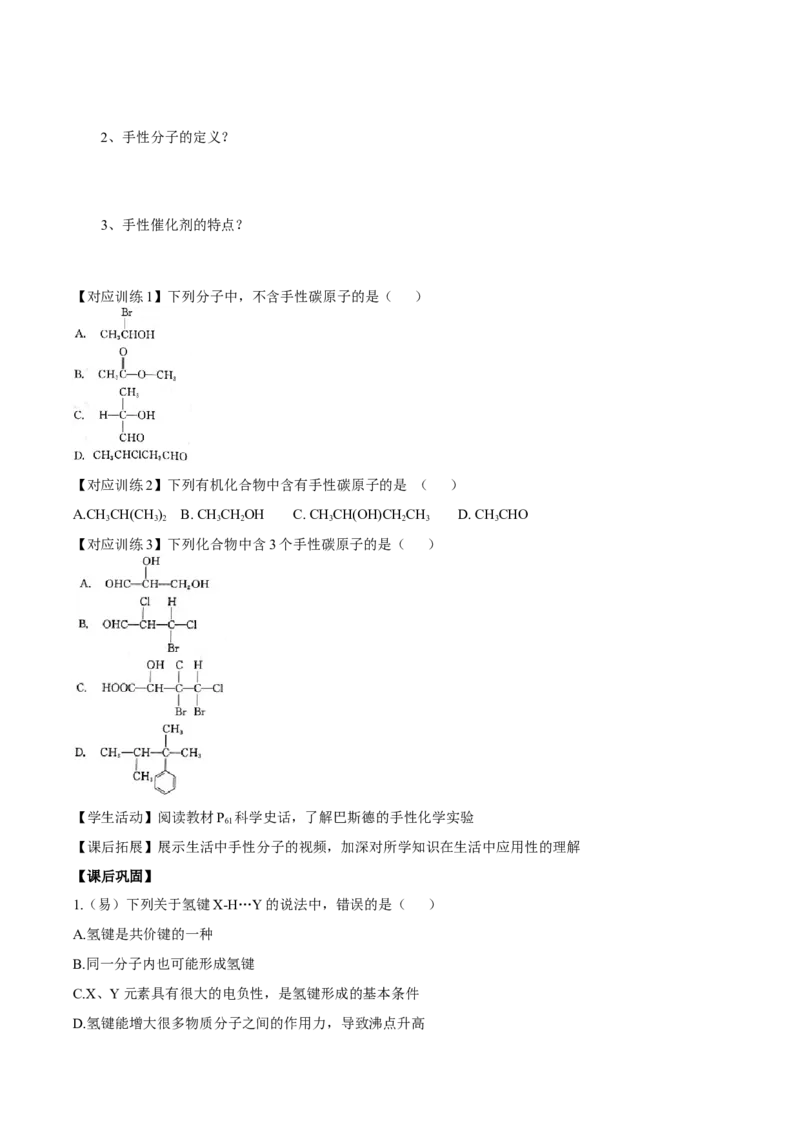
【对应训练1】下列分子中,不含手性碳原子的是( )
【对应训练2】下列有机化合物中含有手性碳原子的是 ( )
A.CHCH(CH ) B. CHCHOH C. CHCH(OH)CH CH D. CH CHO
3 3 2 3 2 3 2 3 3
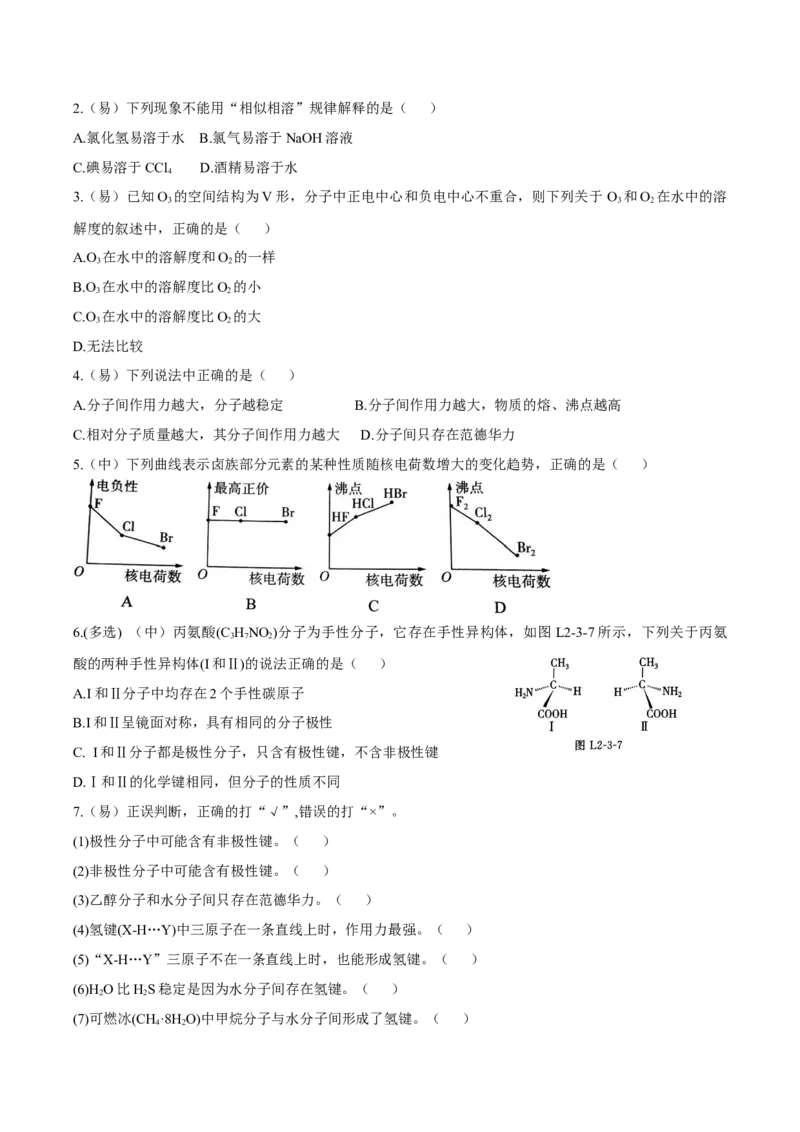
【对应训练3】下列化合物中含3个手性碳原子的是( )
【学生活动】阅读教材P 科学史话,了解巴斯德的手性化学实验
61
【课后拓展】展示生活中手性分子的视频,加深对所学知识在生活中应用性的理解
【课后巩固】
1.(易)下列关于氢键X-H…Y的说法中,错误的是( )
A.氢键是共价键的一种
B.同一分子内也可能形成氢键
C.X、Y元素具有很大的电负性,是氢键形成的基本条件
D.氢键能增大很多物质分子之间的作用力,导致沸点升高2.(易)下列现象不能用“相似相溶”规律解释的是( )
A.氯化氢易溶于水 B.氯气易溶于NaOH溶液
C.碘易溶于CCl D.酒精易溶于水
4
3.(易)已知O 的空间结构为V形,分子中正电中心和负电中心不重合,则下列关于 O 和O 在水中的溶
3 3 2
解度的叙述中,正确的是( )
A.O 在水中的溶解度和O 的一样
3 2
B.O 在水中的溶解度比O 的小
3 2
C.O 在水中的溶解度比O 的大
3 2
D.无法比较
4.(易)下列说法中正确的是( )
A.分子间作用力越大,分子越稳定 B.分子间作用力越大,物质的熔、沸点越高
C.相对分子质量越大,其分子间作用力越大 D.分子间只存在范德华力
5.(中)下列曲线表示卤族部分元素的某种性质随核电荷数增大的变化趋势,正确的是( )
6.(多选) (中)丙氨酸(C HNO )分子为手性分子,它存在手性异构体,如图L2-3-7所示,下列关于丙氨
3 7 2
酸的两种手性异构体(I和Ⅱ)的说法正确的是( )
A.I和Ⅱ分子中均存在2个手性碳原子
B.I和Ⅱ呈镜面对称,具有相同的分子极性
C. I和Ⅱ分子都是极性分子,只含有极性键,不含非极性键
D.Ⅰ和Ⅱ的化学键相同,但分子的性质不同
7.(易)正误判断,正确的打“√”,错误的打“×”。
(1)极性分子中可能含有非极性键。( )
(2)非极性分子中可能含有极性键。( )
(3)乙醇分子和水分子间只存在范德华力。( )
(4)氢键(X-H…Y)中三原子在一条直线上时,作用力最强。( )
(5)“X-H…Y”三原子不在一条直线上时,也能形成氢键。( )
(6)H O比HS稳定是因为水分子间存在氢键。( )
2 2
(7)可燃冰(CH·8H O)中甲烷分子与水分子间形成了氢键。( )
4 2(8)卤素单质、卤素氢化物、卤素碳化物(即 CX )的熔、沸点均随着相对分子质量的增大而升高。
4
( )
8.(易)请解释下列现象:
(1)同样是三原子分子,水分子有极性而二氧化碳分子没有极性。
(2)同样是直线形非极性分子,常温下二氧化碳是气体而二硫化碳是液体。
(3)乙醇与水互溶,而1-戊醇在水中的溶解度却很小。
(4)同样是三角锥形的氢化物,氨气在水中极易溶解,并且很容易液化(常用作冷库中的制冷剂),而同主
族的磷化氢(PH )却没有这些性质。
3
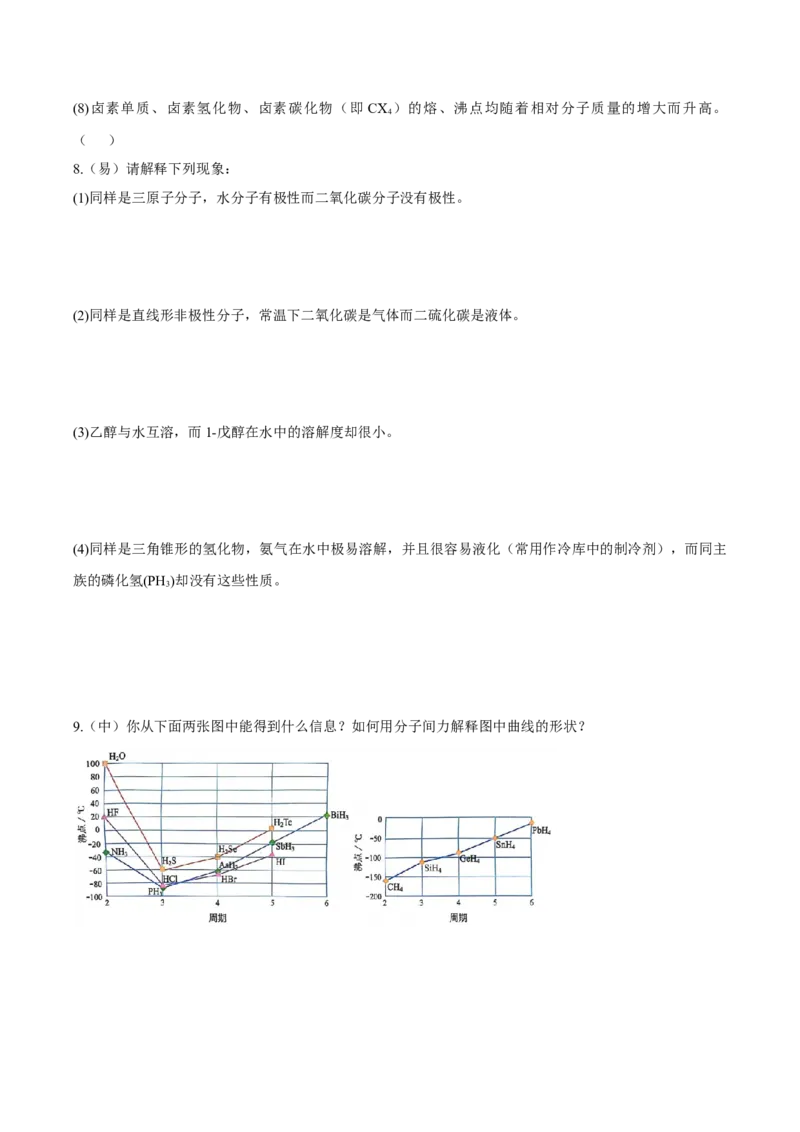
9.(中)你从下面两张图中能得到什么信息?如何用分子间力解释图中曲线的形状?