文档内容
期末备考试卷
期末备考试卷(一)
测试时间:90分钟 满分:100分
一、选择题(本题包括18小题,每小题3分,共54分。每小题只有一个选项符
合题意)
1.在①丙烯 ②氯乙烯 ③苯 ④乙酸四种有机化合物中,分子内所有原子
均在同一平面的是( )
A.①② B.②③ C.③④ D.②④
答案 B
解析 丙烯:CH —CH===CH ,含有甲基,甲基上的所有原子不共面;氯乙烯:
3 2
CH ===CHCl,是平面形的,6个原子共面;苯是平面正六边形的,12个原子共面;
2
乙酸: ,甲基上所有原子不共面;故选项B正确。
2.对下列事实的解释错误的是( )
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定
C.常温下浓硫酸、浓硝酸可以用铝罐储存,说明浓硫酸、浓硝酸与铝不反应
D.反应CuSO +H S===CuS↓+H SO 说明硫化铜既不溶于水,也不溶于稀
4 2 2 4
硫酸
答案 C
解析 常温下Al和浓H SO 、浓HNO 反应生成了致密的Al O 保护膜,阻止
2 4 3 2 3
反应进一步发生。
3.下列实验过程中始终无明显现象的是( )
A.NO 通入FeSO 溶液中
2 4
B.CO 通入CaCl 溶液中
2 2
C.NH 通入AlCl 溶液中
3 3
D.SO 通入已酸化的Ba(NO ) 溶液中
2 3 2
答案 B
解析 A项,NO 溶于水生成硝酸,HNO 具有强氧化性,能将Fe2+氧化成Fe3+
2 3
(棕黄色),同时放出无色气体NO,NO遇空气变红棕色;B项,CO 与CaCl 不反应,
2 2
无明显现象;C项,NH 溶于水生成NH ·H O,显碱性,与Al3+作用产生Al(OH) 沉
3 3 2 3
淀;D项,在酸性条件下,NO具有强氧化性,能将SO 氧化成SO,SO与Ba2+作用
2
生成BaSO 白色沉淀。
44.下表中对应关系正确的是( )
答案 B
解析 CH ===CH +HCl―→CH CH Cl属于加成反应,A错误;油脂得到甘油、
2 2 3 2
淀粉得到葡萄糖均属于水解反应,B正确;C项,第一个反应是氧化反应,第二个
反应是还原反应,C错误;D项,二者均是取代反应,D错误。
5.海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是(
)
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl
2
D.无论是海水波浪发电还是潮汐发电都是将化学能转化为电能
答案 C
解析 若制备钾单质需将K+转化成钾单质,发生化学反应,A错误;海水蒸发制NaCl发生物理变化,B错误;D错误,应为势能、动能转化为电能。
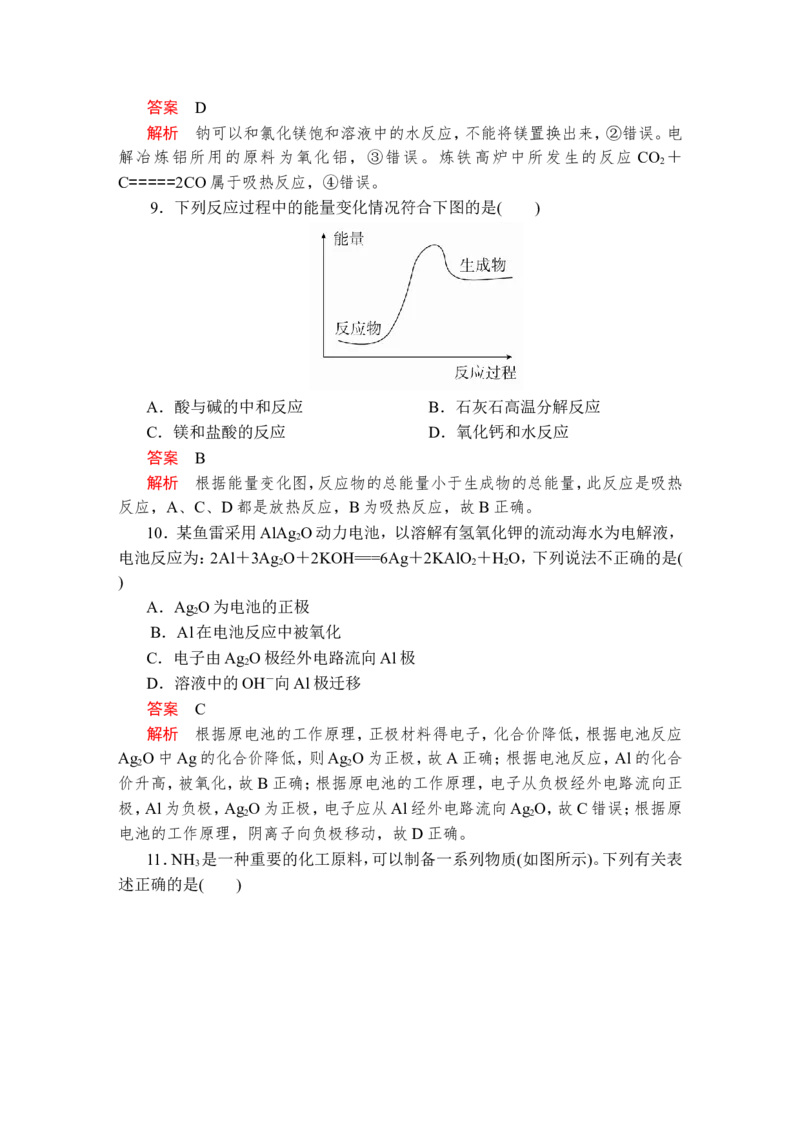
6.干电池原理示意图如右图,电池总反应为 Zn+2NH===Zn2++2NH ↑+
3
H ↑,下列说法正确的是( )
2
A.碳为电池的负极
B.Zn极上发生氧化反应
C.电流由锌极流向碳极
D.H 在Zn片上生成
2
答案 B
解析 根据原电池构成条件,锌为负极,故A错误;根据电池总反应,锌的化
合价升高,被氧化,发生氧化反应,故B正确;电流是从正极流向负极,即从碳流向
锌,故C错误;正极反应:2H++2e-===H ↑,H 应在碳棒上产生,故D错误。
2 2
7.聚丙烯酸酯的结构简式可表示为 ,由丙烯酸酯加
聚得到。下列关于聚丙烯酸酯的说法不正确的是( )
A.属于高分子化合物
B.链节为—CH —CH—
2
C.单体为CH ===CH—COOR
2
D.n为聚合度
答案 B
解析 链节为 。
8.下列化工生产原理错误的是( )
①可以用电解熔融氯化钠的方法来制取金属钠 ②可以用钠加入氯化镁饱和
溶液中的方法制取镁 ③用电冶铝时,原料是氯化铝 ④炼铁高炉中所发生的反
应都是放热的,故无需加热
A.②③ B.①③
C.①②③ D.②③④答案 D
解析 钠可以和氯化镁饱和溶液中的水反应,不能将镁置换出来,②错误。电
解冶炼铝所用的原料为氧化铝,③错误。炼铁高炉中所发生的反应 CO +
2
C=====2CO属于吸热反应,④错误。
9.下列反应过程中的能量变化情况符合下图的是( )
A.酸与碱的中和反应 B.石灰石高温分解反应
C.镁和盐酸的反应 D.氧化钙和水反应
答案 B
解析 根据能量变化图,反应物的总能量小于生成物的总能量,此反应是吸热
反应,A、C、D都是放热反应,B为吸热反应,故B正确。
10.某鱼雷采用AlAg O动力电池,以溶解有氢氧化钾的流动海水为电解液,
2
电池反应为:2Al+3Ag O+2KOH===6Ag+2KAlO +H O,下列说法不正确的是(
2 2 2
)
A.Ag O为电池的正极
2
B.Al在电池反应中被氧化
C.电子由Ag O极经外电路流向Al极
2
D.溶液中的OH-向Al极迁移
答案 C
解析 根据原电池的工作原理,正极材料得电子,化合价降低,根据电池反应
Ag O中Ag的化合价降低,则Ag O为正极,故A正确;根据电池反应,Al的化合
2 2
价升高,被氧化,故B正确;根据原电池的工作原理,电子从负极经外电路流向正
极,Al为负极,Ag O为正极,电子应从Al经外电路流向Ag O,故C错误;根据原
2 2
电池的工作原理,阴离子向负极移动,故D正确。
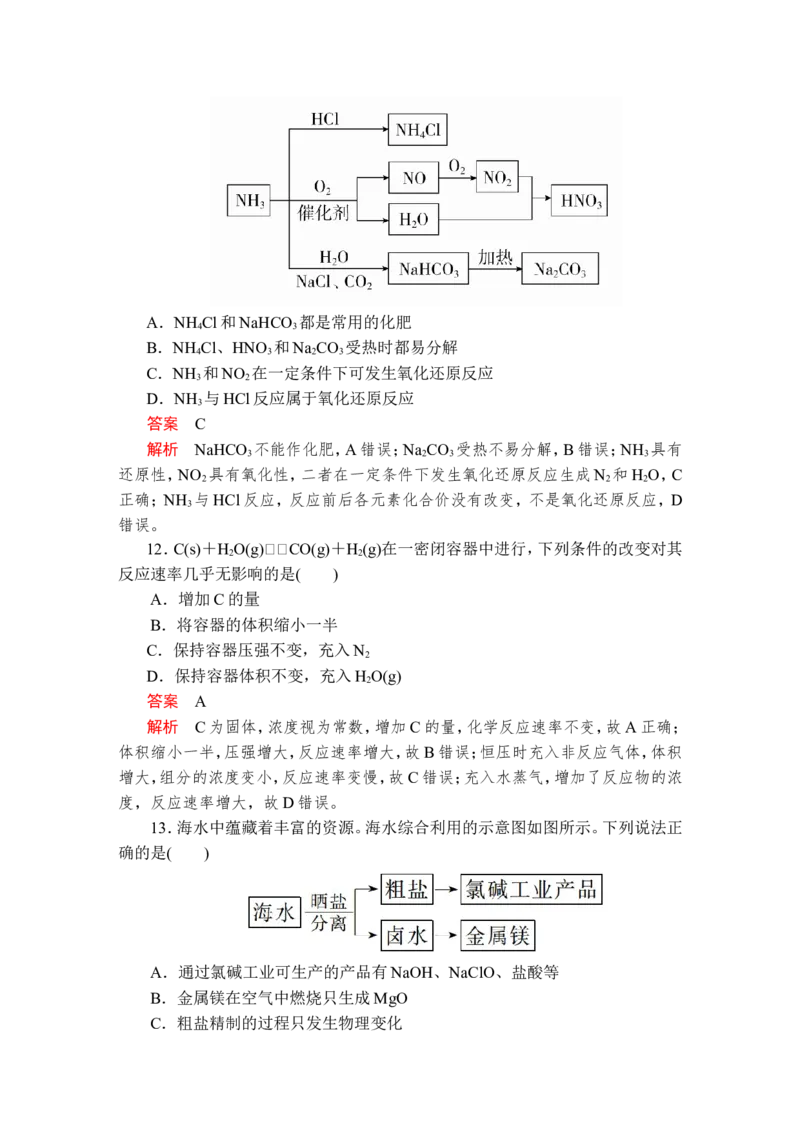
11.NH 是一种重要的化工原料,可以制备一系列物质(如图所示)。下列有关表
3
述正确的是( )A.NH Cl和NaHCO 都是常用的化肥
4 3
B.NH Cl、HNO 和Na CO 受热时都易分解
4 3 2 3
C.NH 和NO 在一定条件下可发生氧化还原反应
3 2
D.NH 与HCl反应属于氧化还原反应
3
答案 C
解析 NaHCO 不能作化肥,A错误;Na CO 受热不易分解,B错误;NH 具有
3 2 3 3
还原性,NO 具有氧化性,二者在一定条件下发生氧化还原反应生成N 和H O,C
2 2 2
正确;NH 与HCl反应,反应前后各元素化合价没有改变,不是氧化还原反应,D
3
错误。
12.C(s)+H O(g)CO(g)+H (g)在一密闭容器中进行,下列条件的改变对其
2 2
反应速率几乎无影响的是( )
A.增加C的量
B.将容器的体积缩小一半
C.保持容器压强不变,充入N
2
D.保持容器体积不变,充入H O(g)
2
答案 A
解析 C为固体,浓度视为常数,增加C的量,化学反应速率不变,故A正确;
体积缩小一半,压强增大,反应速率增大,故B错误;恒压时充入非反应气体,体积
增大,组分的浓度变小,反应速率变慢,故C错误;充入水蒸气,增加了反应物的浓
度,反应速率增大,故D错误。
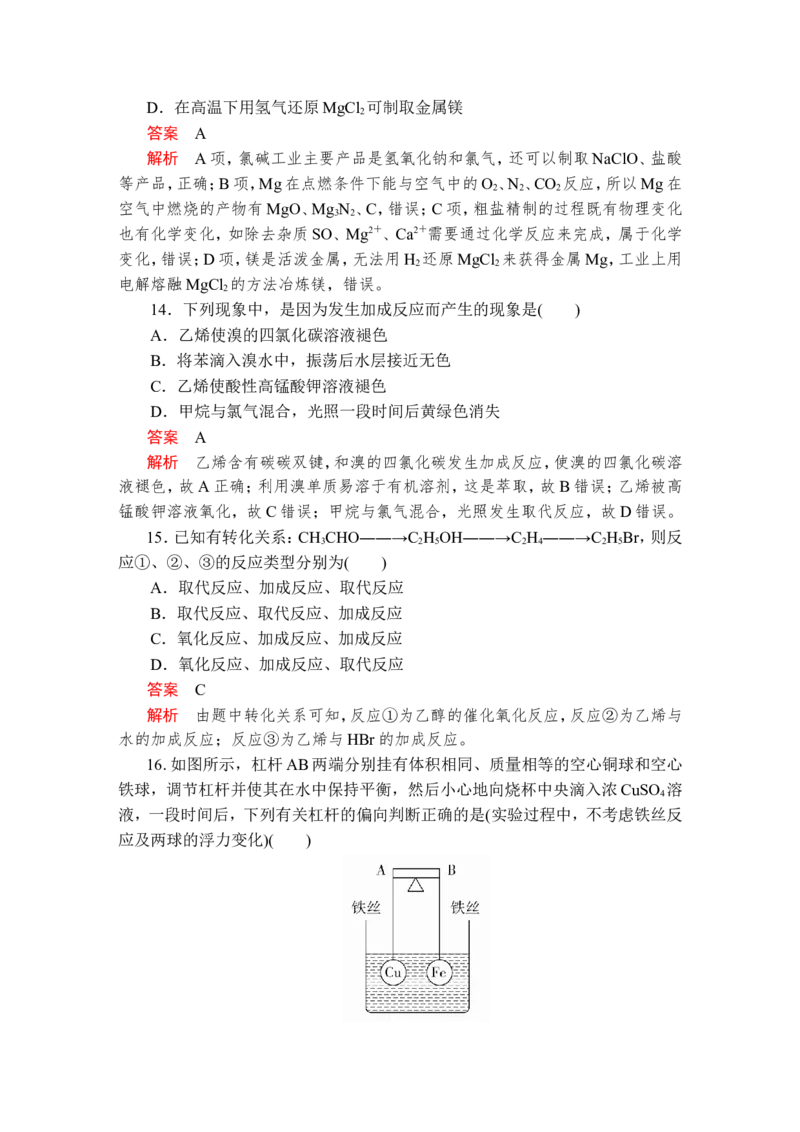
13.海水中蕴藏着丰富的资源。海水综合利用的示意图如图所示。下列说法正
确的是( )
A.通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等
B.金属镁在空气中燃烧只生成MgO
C.粗盐精制的过程只发生物理变化D.在高温下用氢气还原MgCl 可制取金属镁
2
答案 A
解析 A项,氯碱工业主要产品是氢氧化钠和氯气,还可以制取NaClO、盐酸
等产品,正确;B项,Mg在点燃条件下能与空气中的O 、N 、CO 反应,所以Mg在
2 2 2
空气中燃烧的产物有MgO、Mg N 、C,错误;C项,粗盐精制的过程既有物理变化
3 2
也有化学变化,如除去杂质SO、Mg2+、Ca2+需要通过化学反应来完成,属于化学
变化,错误;D项,镁是活泼金属,无法用H 还原MgCl 来获得金属Mg,工业上用
2 2
电解熔融MgCl 的方法冶炼镁,错误。
2
14.下列现象中,是因为发生加成反应而产生的现象是( )
A.乙烯使溴的四氯化碳溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使酸性高锰酸钾溶液褪色
D.甲烷与氯气混合,光照一段时间后黄绿色消失
答案 A
解析 乙烯含有碳碳双键,和溴的四氯化碳发生加成反应,使溴的四氯化碳溶
液褪色,故A正确;利用溴单质易溶于有机溶剂,这是萃取,故B错误;乙烯被高
锰酸钾溶液氧化,故C错误;甲烷与氯气混合,光照发生取代反应,故D错误。
15.已知有转化关系:CH CHO――→C H OH――→C H ――→C H Br,则反
3 2 5 2 4 2 5
应①、②、③的反应类型分别为( )
A.取代反应、加成反应、取代反应
B.取代反应、取代反应、加成反应
C.氧化反应、加成反应、加成反应
D.氧化反应、加成反应、取代反应
答案 C
解析 由题中转化关系可知,反应①为乙醇的催化氧化反应,反应②为乙烯与
水的加成反应;反应③为乙烯与HBr的加成反应。
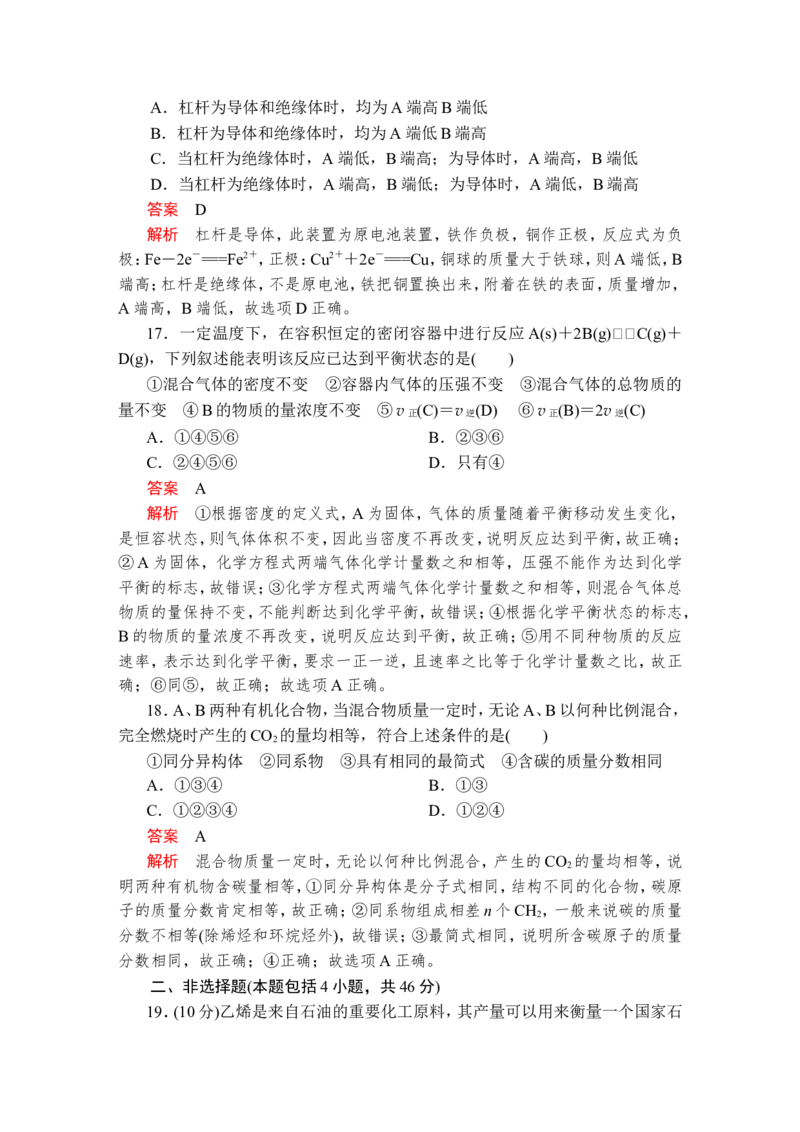
16. 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心
铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO 溶
4
液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反
应及两球的浮力变化)( )A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低
D.当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高
答案 D
解析 杠杆是导体,此装置为原电池装置,铁作负极,铜作正极,反应式为负
极:Fe-2e-===Fe2+,正极:Cu2++2e-===Cu,铜球的质量大于铁球,则A端低,B
端高;杠杆是绝缘体,不是原电池,铁把铜置换出来,附着在铁的表面,质量增加,
A端高,B端低,故选项D正确。
17.一定温度下,在容积恒定的密闭容器中进行反应A(s)+2B(g)C(g)+
D(g),下列叙述能表明该反应已达到平衡状态的是( )
①混合气体的密度不变 ②容器内气体的压强不变 ③混合气体的总物质的
量不变 ④B的物质的量浓度不变 ⑤v (C)=v (D) ⑥v (B)=2v (C)
正 逆 正 逆
A.①④⑤⑥ B.②③⑥
C.②④⑤⑥ D.只有④
答案 A
解析 ①根据密度的定义式,A为固体,气体的质量随着平衡移动发生变化,
是恒容状态,则气体体积不变,因此当密度不再改变,说明反应达到平衡,故正确;
②A为固体,化学方程式两端气体化学计量数之和相等,压强不能作为达到化学
平衡的标志,故错误;③化学方程式两端气体化学计量数之和相等,则混合气体总
物质的量保持不变,不能判断达到化学平衡,故错误;④根据化学平衡状态的标志,
B的物质的量浓度不再改变,说明反应达到平衡,故正确;⑤用不同种物质的反应
速率,表示达到化学平衡,要求一正一逆,且速率之比等于化学计量数之比,故正
确;⑥同⑤,故正确;故选项A正确。
18.A、B两种有机化合物,当混合物质量一定时,无论A、B以何种比例混合,
完全燃烧时产生的CO 的量均相等,符合上述条件的是( )
2
①同分异构体 ②同系物 ③具有相同的最简式 ④含碳的质量分数相同
A.①③④ B.①③
C.①②③④ D.①②④
答案 A
解析 混合物质量一定时,无论以何种比例混合,产生的CO 的量均相等,说
2
明两种有机物含碳量相等,①同分异构体是分子式相同,结构不同的化合物,碳原
子的质量分数肯定相等,故正确;②同系物组成相差n个CH ,一般来说碳的质量
2
分数不相等(除烯烃和环烷烃外),故错误;③最简式相同,说明所含碳原子的质量
分数相同,故正确;④正确;故选项A正确。
二、非选择题(本题包括4小题,共46分)
19.(10分)乙烯是来自石油的重要化工原料,其产量可以用来衡量一个国家石油化工发展水平。请回答:
(1)乙烯通入溴的四氯化碳溶液中,观察到的现象是_________________;其反
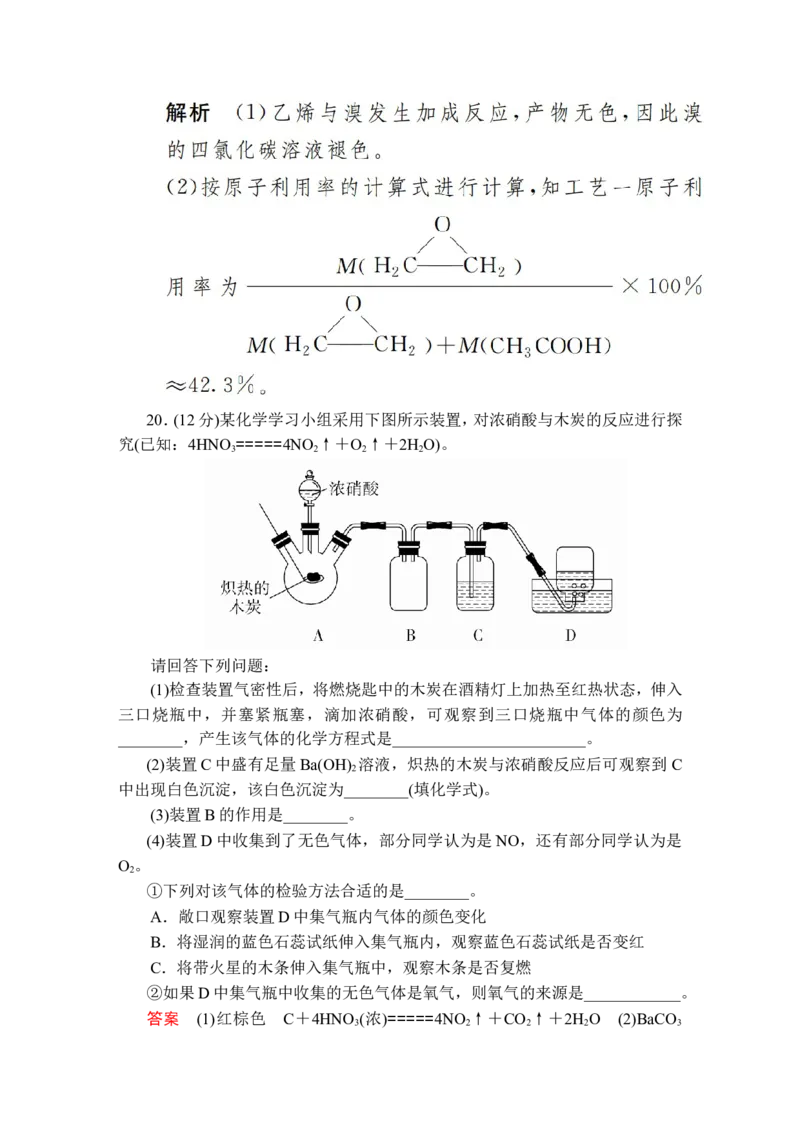
应的化学方程式为__________________________________。20.(12分)某化学学习小组采用下图所示装置,对浓硝酸与木炭的反应进行探
究(已知:4HNO =====4NO ↑+O ↑+2H O)。
3 2 2 2
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,伸入
三口烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三口烧瓶中气体的颜色为
________,产生该气体的化学方程式是________________________。
(2)装置C中盛有足量Ba(OH) 溶液,炽热的木炭与浓硝酸反应后可观察到 C
2
中出现白色沉淀,该白色沉淀为________(填化学式)。
(3)装置B的作用是________。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是
O 。
2
①下列对该气体的检验方法合适的是________。
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶中收集的无色气体是氧气,则氧气的来源是____________。
答案 (1)红棕色 C+4HNO (浓)=====4NO ↑+CO ↑+2H O (2)BaCO
3 2 2 2 3(3)防倒吸 (4)①AC ②HNO 的分解
3
解析 (1)装置A中发生的是浓硝酸与木炭的反应,生成NO 、CO 、H O,三口
2 2 2
烧瓶中显示的是NO 的红棕色。
2
(2)NO 、CO 通入Ba(OH) 溶液分别生成Ba(NO ) 和BaCO ,由于Ba(OH) 溶
2 2 2 3 2 3 2
液足量,故溶液为碱性环境,BaCO 不溶解,以沉淀形式析出。
3
(4)①NO与O 反应生成红棕色的NO ,A正确;NO和O 均不具有酸性,B错
2 2 2
误;O 能使带火星的木条复燃,而NO不能,C正确。②装置A中除木炭与浓硝酸
2
的反应外,硝酸不稳定,还会分解:4HNO =====4NO ↑+O ↑+2H O。
3 2 2 2
21.(12分)Ⅰ.下列各项分别与哪种影响化学反应速率因素的关系最为密切?
(1)夏天的食品易变霉,在冬天不易发生该现象________________。
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢
______________________。
(3)MnO 加入双氧水中放出气泡更快________。
2
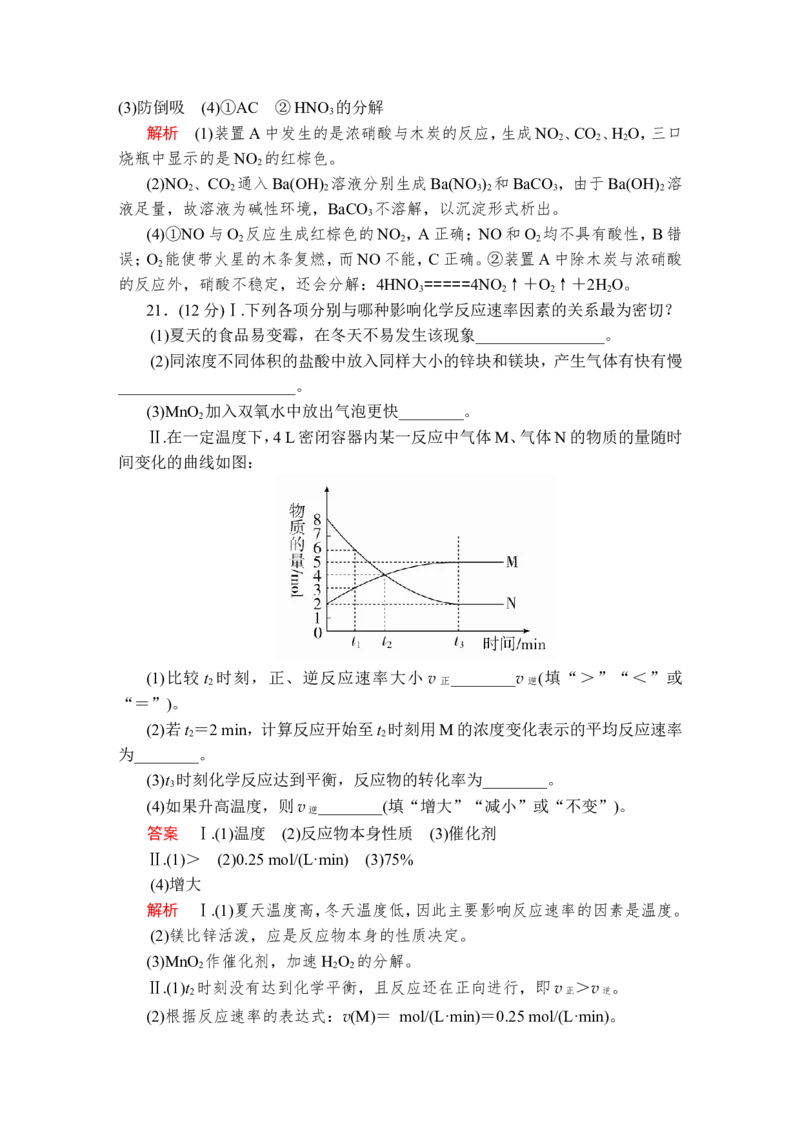
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量随时
间变化的曲线如图:
(1)比较 t 时刻,正、逆反应速率大小 v ________v (填“>”“<”或
2 正 逆
“=”)。
(2)若t =2 min,计算反应开始至t 时刻用M的浓度变化表示的平均反应速率
2 2
为________。
(3)t 时刻化学反应达到平衡,反应物的转化率为________。
3
(4)如果升高温度,则v ________(填“增大”“减小”或“不变”)。
逆
答案 Ⅰ.(1)温度 (2)反应物本身性质 (3)催化剂
Ⅱ.(1)> (2)0.25 mol/(L·min) (3)75%
(4)增大
解析 Ⅰ.(1)夏天温度高,冬天温度低,因此主要影响反应速率的因素是温度。
(2)镁比锌活泼,应是反应物本身的性质决定。
(3)MnO 作催化剂,加速H O 的分解。
2 2 2
Ⅱ.(1)t 时刻没有达到化学平衡,且反应还在正向进行,即v >v 。
2 正 逆
(2)根据反应速率的表达式:v(M)= mol/(L·min)=0.25 mol/(L·min)。(3)反应物是N,转化率为×100%=75%。
(4)升高温度,正、逆反应速率都增大。
22.(12分)资料在线:查阅资料可知以下数据:
物质 熔点(℃) 沸点(℃) 密度(g·cm-3)
乙醇 -117.0 78.0 0.79
乙酸 16.6 117.9 1.05
乙酸乙酯 -83.6 77.5 0.90
浓硫酸(98%) — 338.0 1.84
【实验步骤】
学生在实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸
的混合溶液;
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大
试管5~10 min;
③待试管B收集到一定量的产物后停止加热,撤去试管 B并用力振荡,然后
静置待分层;
④分离出乙酸乙酯层、洗涤、干燥。
【问题设计】
请根据题目要求回答下列问题:
(1)写出制取乙酸乙酯的化学方程式:_________________________。
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)________。
A.中和乙醇
B.和乙酸反应并溶解乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3) 步 骤 ② 中 需 要 小 火 均 匀 加 热 操 作 , 其 主 要 理 由 是
________________________________。
(4)指出步骤③所观察到的现象:__________________________________;分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为________(填字母)。
A.P O B.无水Na SO
2 5 2 4
C.碱石灰 D.NaOH固体
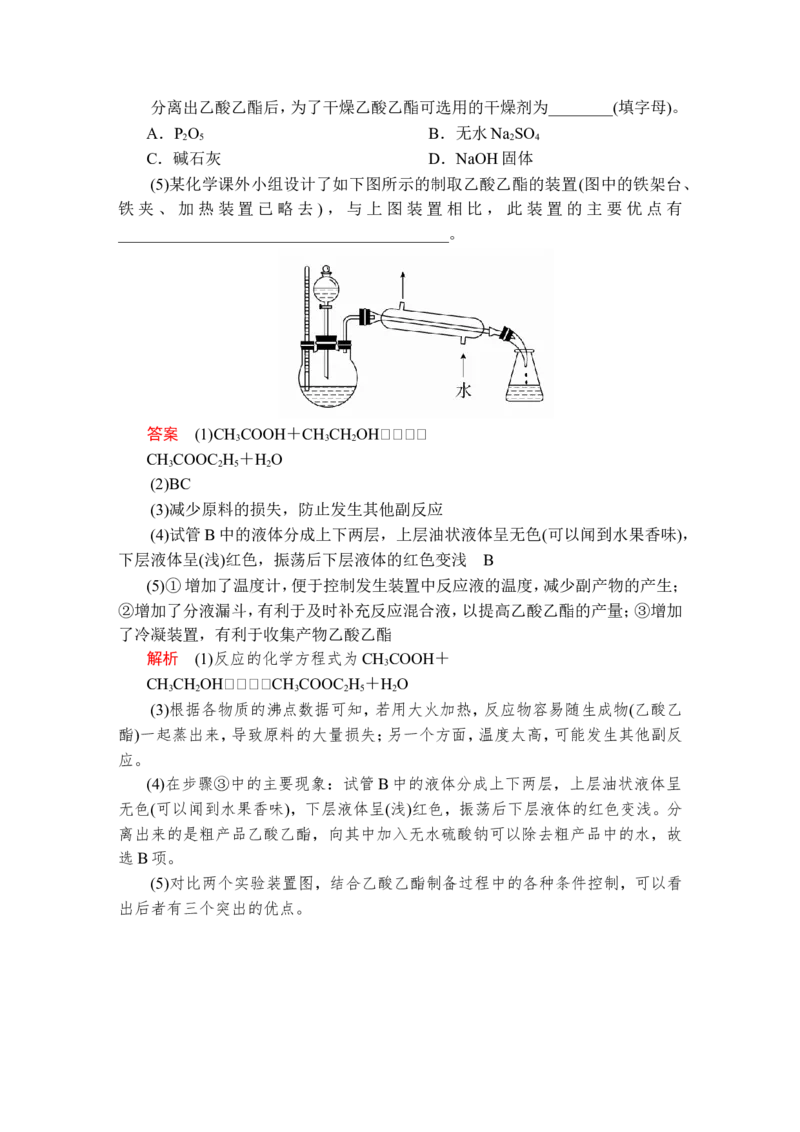
(5)某化学课外小组设计了如下图所示的制取乙酸乙酯的装置(图中的铁架台、
铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有
_________________________________________。
答案 (1)CH COOH+CH CH OH
3 3 2
CH COOC H +H O
3 2 5 2
(2)BC
(3)减少原料的损失,防止发生其他副反应
(4)试管B中的液体分成上下两层,上层油状液体呈无色(可以闻到水果香味),
下层液体呈(浅)红色,振荡后下层液体的红色变浅 B
(5)①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的产生;
②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加
了冷凝装置,有利于收集产物乙酸乙酯
解析 (1)反应的化学方程式为CH COOH+
3
CH CH OHCH COOC H +H O
3 2 3 2 5 2
(3)根据各物质的沸点数据可知,若用大火加热,反应物容易随生成物(乙酸乙
酯)一起蒸出来,导致原料的大量损失;另一个方面,温度太高,可能发生其他副反
应。
(4)在步骤③中的主要现象:试管B中的液体分成上下两层,上层油状液体呈
无色(可以闻到水果香味),下层液体呈(浅)红色,振荡后下层液体的红色变浅。分
离出来的是粗产品乙酸乙酯,向其中加入无水硫酸钠可以除去粗产品中的水,故
选B项。
(5)对比两个实验装置图,结合乙酸乙酯制备过程中的各种条件控制,可以看
出后者有三个突出的优点。