文档内容
3.2.3 酸碱中和滴定(分层作业)
1.用0.1000mol·L-1 HCl溶液滴定未知浓度的NaOH溶液。有关该实验说法中,不正确的是
A.本实验可选用酚酞作指示剂
B.用酸式滴定管盛装0.1000mol·L-1 HCl溶液
C.锥形瓶装未知浓度的NaOH溶液前必须保持干燥
D.滴定时眼睛看着锥形瓶中溶液颜色的变化
2.下列关于酸与碱中和滴定实验操作的叙述:①取一锥形瓶,用待测NaOH溶液润洗2~3次;②在锥形
瓶中加入25.00mL待测NaOH溶液;③向锥形瓶中加入2滴石蕊试液作指示剂;④取一支酸式滴定管,洗
涤干净后直接向酸式滴定管中注入标准HCl溶液,进行滴定;⑤左手控制酸式滴定管的玻璃活塞,右手摇
动锥形瓶;⑥两眼注视滴定管内的盐酸液面的下降。以上操作有错误的是
A.④⑤⑥ B.①④⑤⑥ C.③④⑥ D.①③④⑥
3.图示中是用0.1000mol·L-1 NaOH溶液滴定10.00mL未知浓度硫酸溶液(酚酞作指示剂)的滴定曲线,下列
说法正确的是
A.水电离出的氢离子浓度:a>b
B.硫酸溶液的物质的量浓度为0.1000mol·L-1
C.当滴加NaOH溶液为10.00mL时,该混合液的pH=1.0
D.当最后半滴标准NaOH溶液滴入,溶液恰好由无色变成粉红色,说明硫酸与NaOH恰好完全反应
4.实验室用基准NaCO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定NaCO 标准
2 3 2 3
溶液。下列说法错误的是
A.达到滴定终点时溶液显橙色
B.应选用烧杯而非称量纸称量准NaCO 固体
2 3
C.应选用配带塑料塞的容量瓶配制准NaCO 标准溶液
2 3
D.可用量筒量取25.00 mL Na CO 标准溶液置于锥形瓶中
2 35.如图是常温下向20.00mL的盐酸中,逐滴加入0.10mol/L的NaOH溶液时,溶液的pH随NaOH溶液的
体积V(mL)变化的曲线,根据图像所得的下列结论中正确的是
A.原盐酸的浓度为1.0mol/L
B.当NaOH滴入10.00mL时,溶液依然显酸性,且c(H+)=0.05mol/L
C.x的值为20.00
D.只能选用甲基橙作指示剂,不能用酚酞
6.中和滴定是一种操作简单,准确度高的定量分析方法。实际工作中除酸碱中和滴定外,也可利用物质
间的氧化还原反应、沉淀反应进行类似的滴定分析,下列有关滴定分析(待测液置于锥形瓶内)的说法错误
的是
A.利用2Fe3++2I-⇌I+2Fe2+反应,用FeCl 溶液测定样品中KI的百分含量时可用淀粉溶液作指示剂
2 3
B.用标准酸性KMnO 溶液测定NaSO 溶液的浓度时,滴定终点时溶液的颜色由无色变为浅红色
4 2 3
C.用标准HCl溶液滴定未知浓度的氨水溶液时,选择甲基橙作指示剂
D.利用Ag++SCN-=AgSCN↓反应,用标准KSCN溶液测定AgNO 溶液的浓度时可用Fe(NO ) 溶液作
3 3 3
指示剂
7.下列有关滴定操作的说法正确的是
A.用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL
B.酸碱中和滴定实验时,滴定管和锥形瓶水洗后都要用待装液润洗
C.用未知浓度的盐酸滴定标准KOH溶液时,若读数时,滴定前仰视,滴定到终点后俯视,会导致测
定结果偏高
D.用标准KOH溶液滴定未知浓度的盐酸,且制标准溶液的固体KOH中含有NaOH杂质,则测定结
果偏高
8.用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法不正确的是
A.可以用酚酞代替指示剂
B.滴定前不能用待测液润洗锥形瓶
C.若氢氧化钠吸收少量CO,不影响滴定结果
2D.可用量筒量取25.00mLNaOH待测液置于锥形瓶中
9.某学生用 的标准NaOH溶液滴定未知浓度的盐酸,操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00mL待测液注入洁净的存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是 (填编号)。若测定结果偏高,原因可能是 (填字母)。
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定前,滴定管尖嘴有气泡,滴定后无气泡
(2)如图是某次滴定时的滴定管中的液面,其读数为 mL。
(3)根据下列数据,请计算待测盐酸的浓度: mg·L-1。
标准烧碱溶液体积(mL)
滴定次
待测体积(mL)
数
滴定前读数 滴定后读数
第一次 20.00 0.40 20.30
第二次 20.00 2.00 24.10
第三次 20.00 4.00 24.10
(4)拓展:某同学学习了中和滴定,将该原理又应用到葡萄酒中抗氧化剂残留量(以游离SO 计算)的测定
2
准确量取100.00mL葡萄酒样品,加酸蒸馏出抗氧化剂成分,取馏分于锥形瓶中,滴加少量淀粉溶液,用
物质的量浓度为0.0100mol·L-1标准溶液滴定至终点,重复操作三次,平均消耗标准溶液22.50mL。(已知滴
定过程中所发生的反应是I+SO+2H O=2HI+HSO )。
2 2 2 2 4
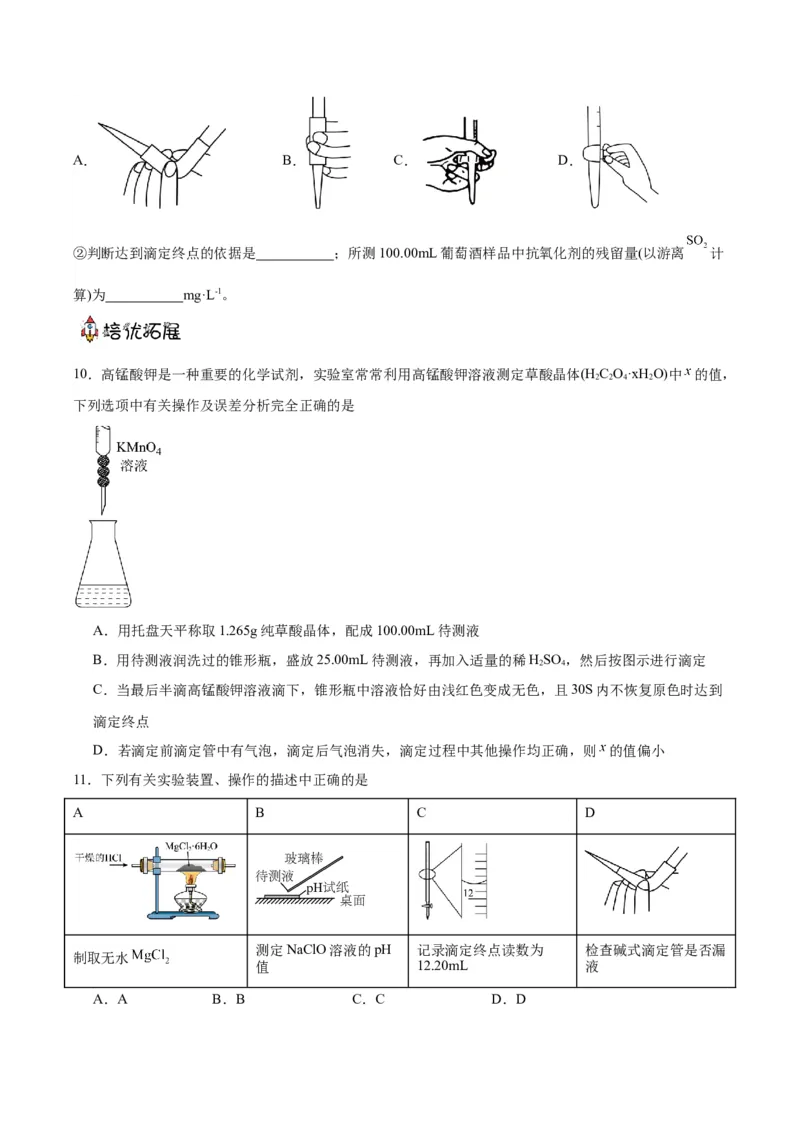
①滴定前需排放装有 溶液的滴定管尖嘴处的气泡,其正确的图示为 (填字母)。A. B. C. D.
②判断达到滴定终点的依据是 ;所测100.00mL葡萄酒样品中抗氧化剂的残留量(以游离 计
算)为 mg·L-1。
10.高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H C O·xH O)中 的值,
2 2 4 2
下列选项中有关操作及误差分析完全正确的是
A.用托盘天平称取1.265g纯草酸晶体,配成100.00mL待测液
B.用待测液润洗过的锥形瓶,盛放25.00mL待测液,再加入适量的稀HSO ,然后按图示进行滴定
2 4
C.当最后半滴高锰酸钾溶液滴下,锥形瓶中溶液恰好由浅红色变成无色,且30S内不恢复原色时达到
滴定终点
D.若滴定前滴定管中有气泡,滴定后气泡消失,滴定过程中其他操作均正确,则 的值偏小
11.下列有关实验装置、操作的描述中正确的是
A B C D
测定NaClO溶液的pH 记录滴定终点读数为 检查碱式滴定管是否漏
制取无水
值 12.20mL 液
A.A B.B C.C D.D12.在含单质碘的KI溶液中存在可逆反应: ,为测定该反应的平衡常数K进行如
下实验,实验步骤如下:
①在装有 的KI溶液的碘量瓶中加入足量 ,充分搅拌溶解,待过量的固体碘沉于瓶底后,
取42.5mL上层清液,用 萃取,充分振荡、静置、分液,得到42.5mL萃取后的水溶液、
溶液。
②取萃取后的 溶液于碘量瓶中,加水充分振荡,再加入质量分数为0.01%KI溶液,充分振荡
后,静置5分钟,注入4mL0.2%的淀粉溶液,用 的 标准溶液滴定,平行滴定3次,平均
消耗 溶液。
③将萃取后的水溶液42.5mL移入碘量瓶中,注入4mL0.2%的淀粉溶液,用 的 标准溶液滴
定,平行滴定3次,平均消耗 溶液。
已知:(1) ;(2) 与 难溶于 ;(3)达到溶解平衡后, 在 层和水
层中的分配比 为
的平衡常数K计算正确的是A. B.
C. D.
13.化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是
选
操作或做法 目的
项
向2支盛有5 mL不同浓度NaSO 溶液的试管中同时加入2 mL 5% 探究浓度对化学反应速率的
A 2 3
HO 溶液,观察实验现象 影响
2 2
取5 mL0.1 mol/L KI溶液于试管中,加入1mL0.1 mol/L FeCl 溶液,充 探究KI与FeCl 的反应是否
B 3 3
分反应后滴入5滴15% KSCN溶液 为可逆反应
C 用玻璃棒蘸取NaClO溶液点到干燥的pH试纸中间 测定NaClO溶液的pH
在50mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩
D 量取20.00 mL盐酸
余盐酸全部放入锥形瓶中
A.A B.B C.C D.D
14.以氧化剂或还原剂为滴定剂,可以滴定一些具有还原性或氧化性的物质。某二氧化锰矿粉中 含
量测定实验流程如图。下列说法错误的是
A.NaC O 将MnO 还原为Mn2+
2 2 4 2
B.滴定终点溶液的颜色从无色变为浅紫色
C.若滴定终点时滴定管尖嘴处出现气泡,则测得MnO 含量偏小
2
8.7
D.MnO 含量为 %
2 m
15.某实验小组用如下实验测定海带预处理后所得溶液的碘含量,实验步骤及现象如下:已知:I+2Na SO=2NaI+Na SO,下列说法不正确的是:
2 2 2 3 2 4 6
A.溶液b为蓝色是因为发生了反应:HO+2I-+2H+=I +2H O
2 2 2 2
B.该实验可证明蓝色恢复与空气无关
C.溶液反复由无色变蓝的原因可能是HO 氧化I-的反应速率比NaSO 还原I 的反应速率快
2 2 2 2 3 2
D.上述实验不能准确测定待测液中的碘含量,应补充实验步骤:滴定前向溶液b中加少量MnO ,反
2
应至不再产生气泡,过滤,对滤液进行滴定
16.25℃时,等体积两种一元酸HA和HB分别用等浓度的NaOH溶液滴定,滴定曲线如图所示。下列说
法正确的是
A.酸性:HA