文档内容
4.3 化学键
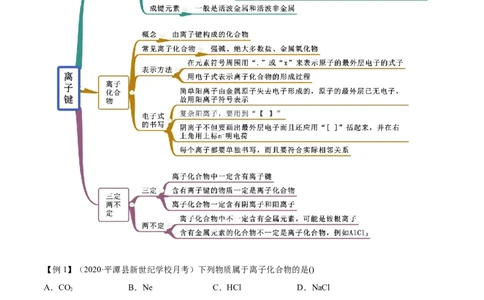
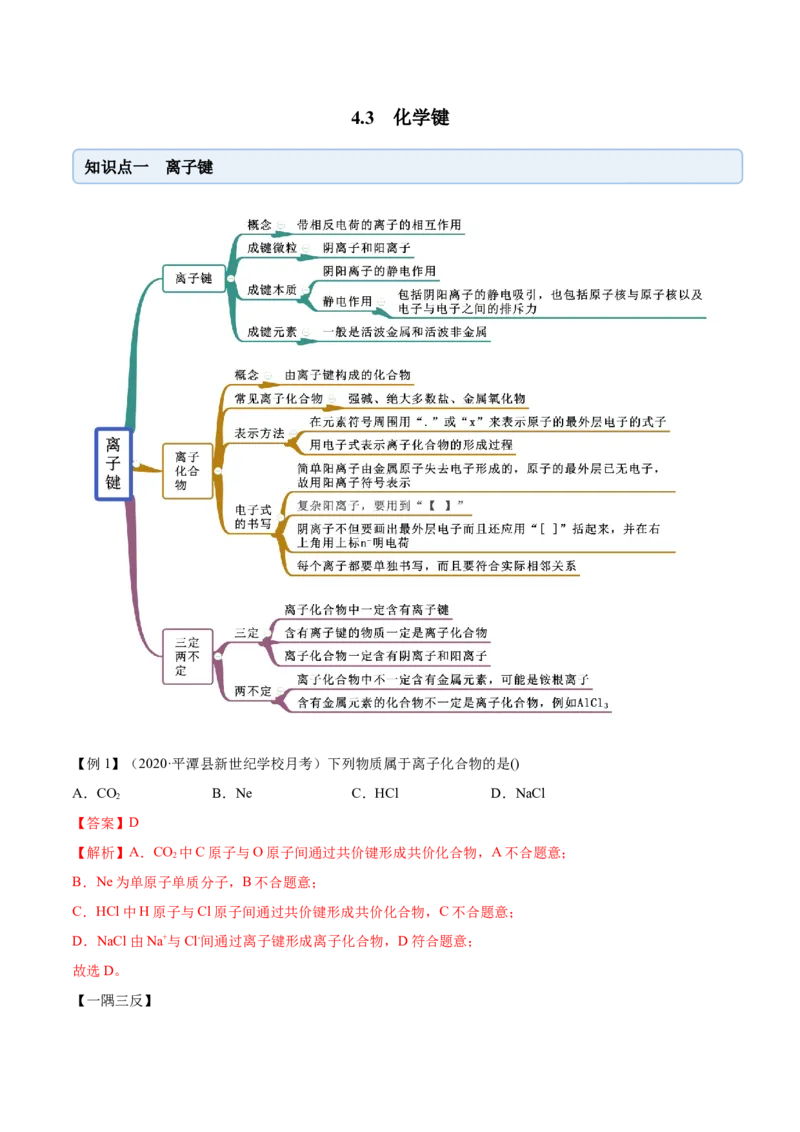
知识点一 离子键
【例1】(2020·平潭县新世纪学校月考)下列物质属于离子化合物的是()
A.CO B.Ne C.HCl D.NaCl
2
【答案】D
【解析】A.CO 中C原子与O原子间通过共价键形成共价化合物,A不合题意;
2
B.Ne为单原子单质分子,B不合题意;
C.HCl中H原子与Cl原子间通过共价键形成共价化合物,C不合题意;
D.NaCl由Na+与Cl-间通过离子键形成离子化合物,D符合题意;
故选D。
【一隅三反】1.(2020·吉林农安·高一期末)下列含有离子键的物质是 。
A.Fe B. C.HCl D.NaCl
【答案】D
【解析】A.Fe是金属单质,只含有金属键,故A不符合题意;
B.二氧化硅中存在的化学键是非金属元素之间形成的共价键,即硅原子和氧原子形成共价键,为共价化
合物,故B不符合题意;
C.HCl中存在的化学键是非金属元素之间形成的共价键,即H与Cl形成共价健,为共价化合物,故C不
符合题意;
D.氯化钠中存在的化学键是活泼金属和活泼非金属之间形成的离子键,即钠离子与氯离子之间形成的离
子键,故D符合题意;
答案为D。
2.(2020·全国高一课时练习)下列各数值表示有关元素的原子序数,其所表示的各原子间能形成离子键
的是( )
A.10和19 B.6和16 C.14和8 D.11和17
【答案】D
【解析】A.原子序数为10和19的元素为Ne和K,Ne为稀有气体元素,难以形成化合物,A与题意不符;
B.原子序数为6和16的元素为C和S,可形成二硫化碳,共价化合物,B与题意不符;
C.原子序数为14和8的元素为Si和O,都为非金属元素,可形成二氧化硅,为共价化合物,C与题意不
符;
D.原子序数为11和17的元素为Na和Cl,能形成氯化钠,为离子化合物,存在离子键,D符合题意;
答案为D。
3.(2020·陕西安康·期末)NaOH溶于水的过程中,破坏了
A.离子键 B.共价键 C.金属键和共价键 D.离子键和共价键
【答案】A
【解析】A.NaOH是含有离子键和共价键的离子化合物,溶于水电离出钠离子和氢氧根离子,破坏了离子
键,故A正确;
B.NaOH是含有离子键和共价键的离子化合物,溶于水电离出钠离子和氢氧根离子,破坏了离子键,共价
键没有破坏,故B错误;
C.NaOH是含有离子键和共价键的离子化合物,溶于水电离出钠离子和氢氧根离子,破坏了离子键,没有
金属键,故C错误;D.NaOH是含有离子键和共价键的离子化合物,溶于水电离出钠离子和氢氧根离子,破坏了离子键,共价
键没有破坏,故D错误;
故答案:A。
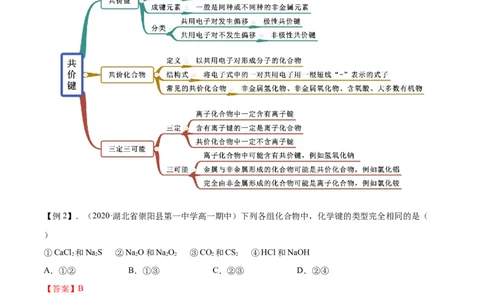
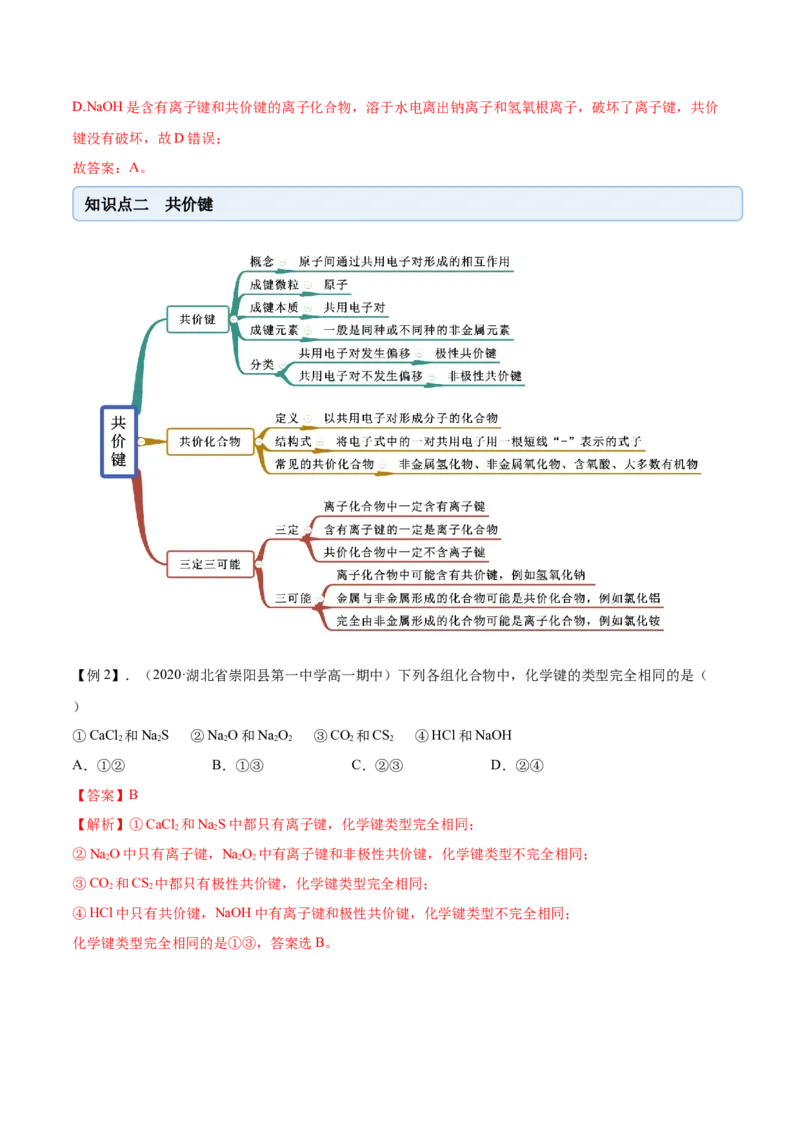
知识点二 共价键
【例2】.(2020·湖北省崇阳县第一中学高一期中)下列各组化合物中,化学键的类型完全相同的是(
)
①CaCl 和NaS ②NaO和NaO ③CO 和CS ④HCl和NaOH
2 2 2 2 2 2 2
A.①② B.①③ C.②③ D.②④
【答案】B
【解析】①CaCl 和NaS中都只有离子键,化学键类型完全相同;
2 2
②NaO中只有离子键,NaO 中有离子键和非极性共价键,化学键类型不完全相同;
2 2 2
③CO 和CS 中都只有极性共价键,化学键类型完全相同;
2 2
④HCl中只有共价键,NaOH中有离子键和极性共价键,化学键类型不完全相同;
化学键类型完全相同的是①③,答案选B。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键
【一隅三反】
1.(2020·湖南雨花·高一期末)下列化合物中既含有离子键又含有共价键的是 ( )
A.HNO B.CaCl C.NH Cl D.HSO
3 2 4 2 4
【答案】C
【解析】A.HNO 为共价化合物,只含有共价键,选项A不符合;
3
B.CaCl 是离子化合物,只有离子键,选项B不符合;
2
C.NH Cl是离子化合物,但含有离子键和共价键,选项C符合;
4
D.HSO 是共价化合物,只含有共价键,选项D不符合;答案选C。
2 4
2.(2020·全国高一课时练习)下列每组物质中含有的化学键类型相同的是( )
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】C
【解析】A. 、 、 、 分别含有离子键、共价键、共价键、离子键和共价键,选项A
不符合题意;
B. 、 、 、 分别含有共价键、离子键、共价键、共价键,选项B不符合题意;
C. 、 、 、 均含有共价键,选项C符合题意;
D. 、 、 、 分别含有离子键和共价键、共价键、共价键、共价键,选项D 不符合题
意。
答案选C。
3.(2020·全国高一课时练习)下列各组物质都是共价化合物的是( )
A.HS和NaO B.HO 和NH Cl
2 2 2 2 2 4
C.NH 和N D.HNO 和HCl
3 2 3
【答案】D
【解析】A. H S为共价化合物,NaO 为离子化合物,故A不符合题意;
2 2 2B.H O 为共价化合物,NH Cl、NaO 为离子化合物,故B不符合题意;
2 2 4 2 2
C.NH 为共价化合物, N 为单质,故C不符合题意;
3 2
D.HNO 和HCl都为共价化合物,故D符合题意;故选:D。
3
4.(2020·宁夏兴庆·长庆高中高一期中)下列物质中,属于含有共价键的离子化合物的是
A.HSO B.NaOH C.HBr D.NaCl
2 4
【答案】B
【解析】A.HSO 中只含共价键,为共价化合物,A不符合题意;
2 4
B.NaOH中氢氧根离子和钠离子之间存在离子键,氢原子和氧原子之间存在共价键,所以为离子化合物,
B符合题意;
B.HBr中只含共价键,为共价化合物,C不符合题意;
C.NaCl中只含离子键,为离子化合物,D不符合题意;答案选B。
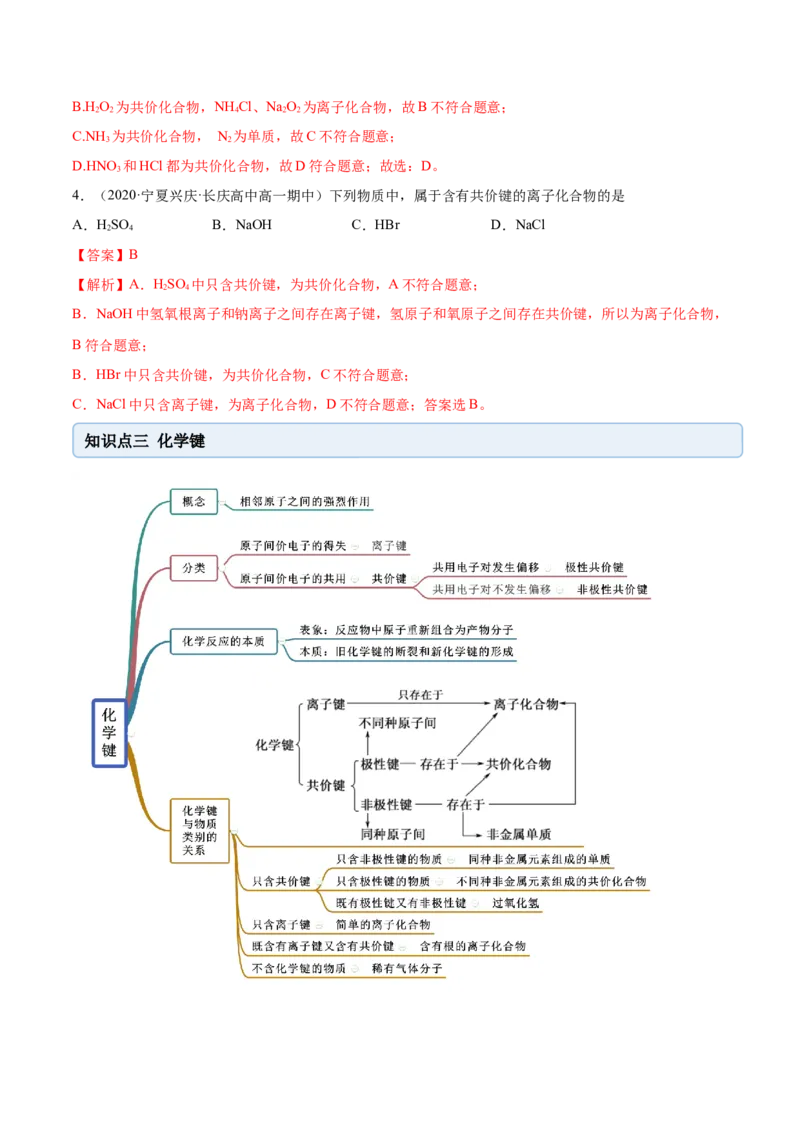
知识点三 化学键【例3】.(2020·全国高一课时练习)下列关于化学键的叙述正确的是
①化学键只存在于分子之间
②化学键是相邻原子之间强烈的相互作用
③化学键是一种静电作用
④化学键是相邻分子之间强烈的相互吸引
⑤离子化合物中可能含有共价键
⑥共价化合物中可能含有离子键
⑦离子化合物中只含离子键
⑧共价化合物中不含离子键
A.②③④⑦ B.②③⑤⑧
C.②④⑤⑥ D.①③⑤⑧
【答案】B
【解析】化学键是相邻原子之间强烈的相互作用,不存在于分子之间,这种相互作用的实质是一种静电作
用,故①④错误,②③正确;离子化合物中一定含有离子键,可能含有共价键,但共价化合物中一定只含
共价键,不含离子键,故⑤⑧正确,⑥⑦错误;因此正确的是:②③⑤⑧,故答案为:B。
【一隅三反】
1.(2020·全国高一课时练习)现有下列物质:① ② ③NaOH ④HCl ⑤ ⑥
(1)只由离子键构成的物质是________(填序号,下同)。
(2)只由极性键构成的物质是_________ 。
(3)只由非极性键构成的物质是________。
(4)由极性键和非极性键构成的物质是________。
(5)由离子键和极性键构成的物质是_______。
(6)由离子键和非极性键构成的物质是______。
(7)属于离子化合物的物质是_______。
(8)属于共价化合物的物质是_______。
【答案】(1)⑥ (2) ④ (3) ① (4) ⑤ (5) ③ (6) ② (7)②③⑥ (8)
④⑤【解析】① 属于单质,只含有非极性共价键;② 属于离子化合物,含有离子键和非极性共价键;
③NaOH属于离子化合物,含有离子键和极性共价键;④HCl属于共价化合物,只含极性共价键;⑤
属于共价化合物,含有极性共价键和非极性共价键;⑥ 属于离子化合物,只含有离子键;
(1)只由离子键构成的物质是⑥;
(2)只由极性键构成的物质是④;
(3)只由非极性键构成的物质是①;
(4)由极性键和非极性键构成的物质是⑤;
(5)由离子键和极性键构成的物质是③;
(6)由离子键和非极性键构成的物质是②;
(7)属于离子化合物的物质是②③⑥;
(8)属于共价化合物的物质是④⑤。
2.(2020·湖北武汉·高一期中)已知 A、B、C、D、E 是五种短周期的主族元素,它们的原子序数依次
增大, A 是所有元素中原子半径最小的元素,B、C 组成的某一种化合物能引起温室效应;常温下,
金属 D 单质投入水中能与水剧烈反应;E 的单质在常温下是一种有色的气体。请按要求回答下列几个问
题:
(1)B、D 的元素名称分别为:_____、_____;
(2)E 的最高价氧化物对应的水化物的化学式为:_____;
(3)C 离子的结构示意图为:_____;
(4)B、C、D 三种元素的原子半径从大到小的顺序为_____(用元素符号表示);
(5)B、E 的最高价氧化物对应水化物的酸性从强到弱的顺序为:_____(用对应的化学式表示)
(6) 写出 C、D 两种元素组成的阴、阳离子个数比为 1:2 且既含离子键又含有非极性共价键的化合
物的电子式:_____。
【答案】(1)碳 钠 (2)HClO (3) (4)Na>C>O (5) HClO>
4 4
HCO
2 3
(6)【解析】(1)B、D的元素名称分别为:碳、钠;故答案为:碳、钠;
(2)E为氯元素,在周期表中的位置为:第三周期第ⅦA族;故答案为:第三周期第ⅦA族;
(3)氧离子的核内质子数为8,核外电子数为10,离子结构示意图为: ;故答案为: ;
(4)原子的核外电子层数越多,原子半径越大,同一周期随着原子序数的增大,原子半径逐渐减小,因
此C、O、Na三种元素的原子半径从大到小的顺序为:Na>C>O;故答案为:Na>C>O;
(5)元素的非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性:Cl>C,因此最高价氧化物
对应水化物的酸性从强到弱的顺序为:HClO>HCO;故答案为:HClO>HCO;
4 2 3 4 2 3
(6)C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物为NaO,电子式为:
2
;故答案为: 。
知识点四 电子式
【例4-1】(2020·全国高一课时练习)用电子式表示下列离子化合物的形成过程。
(1)碘化钙:____________。
(2)硫化钠:____________。
(3)氯化钾:____________。【答案】(1)
(2)
(3)
【解析】(1)Ca最外层有2个电子,I最外层有7个电子,1个Ca失去最外层的2个电子,被2个I得到,
每个I最外层均达到8电子稳定结构,故其形成过程可表示为 ;
(2)Na最外层有1个电子,S最外层有6个电子,2个Na各失去最外层的1个电子成为 ,1个S得到2
个电子成为 ,进而通过离子键形成 ,
其形成过程可表示为 ;
(3)K最外层有1个电子,Cl最外层有7个电子,二者通过电子得失成为 和 ,进而形成离子键,其
形成过程可表示为 。
【例4-2】(2020·江西渝水·新余一中高一月考)请写出电子式
(1)原子的电子式
H____ 、Ca ____、N____、 O____、 Cl____ 、C____ 、 Al____
(2)离子的电子式
①简单阳离子:氢离子____ 钾离子____ 钙离子____
②简单阴离子:氯离子____ 氧离子____
③复杂阴、阳离子:铵根离子____ 氢氧根离子____ 过氧根离子( )____
(3)离子化合物的电子式
NaCl____ CaO____ CaCl _____ CaF ____ Na O ____ Na O____
2 2 2 2 2
【答案】(1)
(2)① H+ K+ Ca2+ ②③
(3)
【解析】(1)书写原子的电子式时,一般讲原子的最外层电子写在元素符号的上、下、左、右四个位置
上;H、Ca、N、 O、Cl、C、Al电子式分别为: 、 、 、 、 、 、 ;
(2)①简单阳离子是原子失去最外层电子后形成的,其电子式即为离子符号本身;氢离子、钾离子、钙
离子的电子式分别为:H+、K+、Ca2+;
②简单阴离子因为得到电子后最外层一般为8电子结构,书写时要在元素符号周围标出电子,用“[ ]”括上,
并在[ ]右上角标明电性和所带电荷数;氯离子、氧离子的电子式分别为: 、 ;
③复杂阴、阳离子中存在共用电子对,要注意H稳定结构最外层2个电子,其他非金属元素稳定结构一般
最外层为8电子,复杂阴、阳离子用“[ ]”括上,并在[ ]右上角标明电性和所带电荷数;铵根离子、氢氧根
离子、过氧根离子( )的电子式分别为: 、 、 ;
(3)离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后)拼在一起;对于不同价态的离子,
也按其绝对值,遵照“大值在中间、小值在周边”的原则书写;NaCl、CaO、CaCl 、CaF 、NaO、NaO
2 2 2 2 2
电子式分别为: 、 、 、 、
、 。电子式书写:
①书写原子的电子式时,一般讲原子的最外层电子写在元素符号的上、下、左、右四个位置上;
②简单阳离子是原子失去最外层电子后形成的,其电子式即为离子符号本身;
③简单阴离子因为得到电子后最外层一般为8电子结构,书写时要在元素符号周围标出电子,用“[ ]”括上,
并在[ ]右上角标明电性和所带电荷数;
④复杂阴、阳离子中存在共用电子对,要注意H稳定结构最外层2个电子,其他非金属元素稳定结构一般
最外层为8电子,复杂阴、阳离子用“[ ]”括上,并在[ ]右上角标明电性和所带电荷数;
⑤离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后)拼在一起;对于不同价态的离子,也
按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
【一隅三反】
1.(2020·全国高一课时练习)下列关于电子式的相关描述正确的是( )。
A. CCl 的电子式为
4
B. CaCl 的电子式为
2
C.由NH 的电子式 可知每个 分子中含8个电子
3
D.用电子式表示HCl的形成过程为
【答案】A
【解析】A.共价化合物的电子式应把组成化合物的各个原子的最外层电子数均表示出来,CCl 的电子式
4
为: ,故A正确;
B.电子式中相同离子不能合并,故氯化钙的电子式为 ,故B错误;
C.氨气的电子式为 ,故每个NH 分子中有10个电子,故C错误;
3D.HCl为共价化合物,用电子式表示HCl形成过程为 ,故D错误;
答案选A。
2.(2020·全国高一课时练习)下列关于电子式的描述正确的是
A.CC1 的电子式为
4
B.CaC1 的电子式为
2
C.CO 的电子式为
2
D.用电子式表示HCl的形成过程为
【答案】A
【解析】A. CC1 分子中C原子与4个Cl形成4对共用电子对,每个原子都达到最外层8个电子的稳定结
4
构,因此其电子式为 ,A正确;
B.CaC1 是离子化合物,Ca2+与Cl-形成离子键,在离子晶体中阴、阳离子要间隔排列,故2个Cl-不能合写
2
在一起,因此电子式为 ,B错误;
C.CO 分子中C原子与2个O原子形成4对共用电子对,使每个原子都达到最外层8个电子的稳定结构,
2
其电子式为 ,C错误;
C.HCl是共价化合物,H原子与Cl原子间共用1对电子,形成过程表示为 ,D
错误;
故合理选项是A。
3.(2020·全国高一课时练习)下列叙述正确的是( )
A. 的结构示意图为B. 的电子式为
C.硫离子的电子式为
D. 的电子式为
【答案】B
【解析】A. 粒子结构示意图中,“圆”代表原子核,中间数值是核电荷数,由 可知,氧离子的质子
数即核电荷数是8,质量数为18,结构示意图为 ,A错误;
B. 是共价化合物,电子式为 ,B正确;
C. 硫离子是阴离子,书写电子式时应加上“[]”,即 ,C错误;
D. 的电子式为: :,D错误。
答案为B。