文档内容
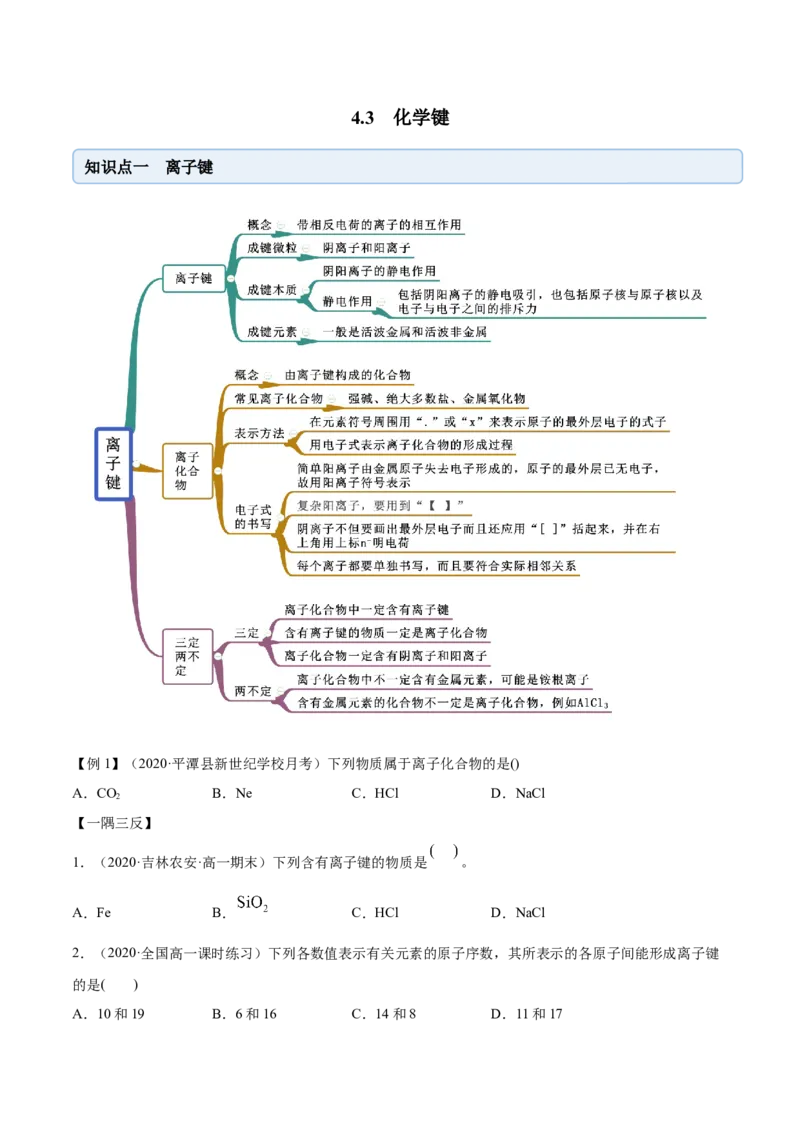
4.3 化学键
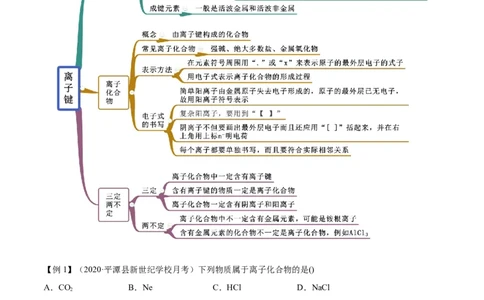
知识点一 离子键
【例1】(2020·平潭县新世纪学校月考)下列物质属于离子化合物的是()
A.CO B.Ne C.HCl D.NaCl
2
【一隅三反】
1.(2020·吉林农安·高一期末)下列含有离子键的物质是 。
A.Fe B. C.HCl D.NaCl
2.(2020·全国高一课时练习)下列各数值表示有关元素的原子序数,其所表示的各原子间能形成离子键
的是( )
A.10和19 B.6和16 C.14和8 D.11和173.(2020·陕西安康·期末)NaOH溶于水的过程中,破坏了
A.离子键 B.共价键 C.金属键和共价键 D.离子键和共价键
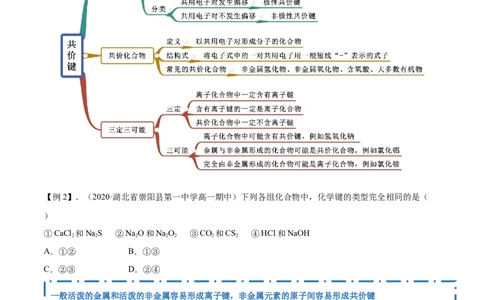
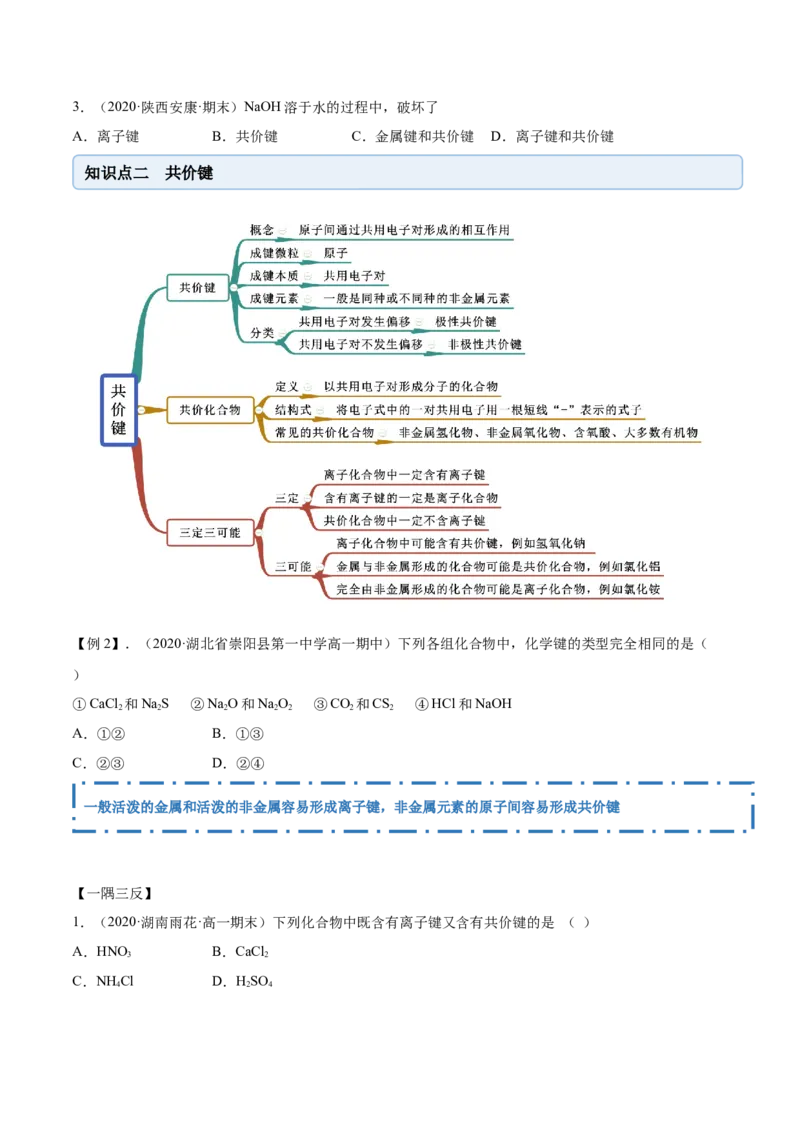
知识点二 共价键
【例2】.(2020·湖北省崇阳县第一中学高一期中)下列各组化合物中,化学键的类型完全相同的是(
)
①CaCl 和NaS ②NaO和NaO ③CO 和CS ④HCl和NaOH
2 2 2 2 2 2 2
A.①② B.①③
C.②③ D.②④
一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键
【一隅三反】
1.(2020·湖南雨花·高一期末)下列化合物中既含有离子键又含有共价键的是 ( )
A.HNO B.CaCl
3 2
C.NH Cl D.HSO
4 2 42.(2020·全国高一课时练习)下列每组物质中含有的化学键类型相同的是( )
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
3.(2020·全国高一课时练习)下列各组物质都是共价化合物的是( )
A.HS和NaO B.HO 和NH Cl
2 2 2 2 2 4
C.NH 和N D.HNO 和HCl
3 2 3
4.(2020·宁夏兴庆·长庆高中高一期中)下列物质中,属于含有共价键的离子化合物的是
A.HSO B.NaOH C.HBr D.NaCl
2 4
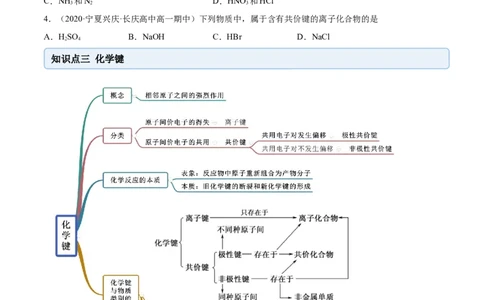
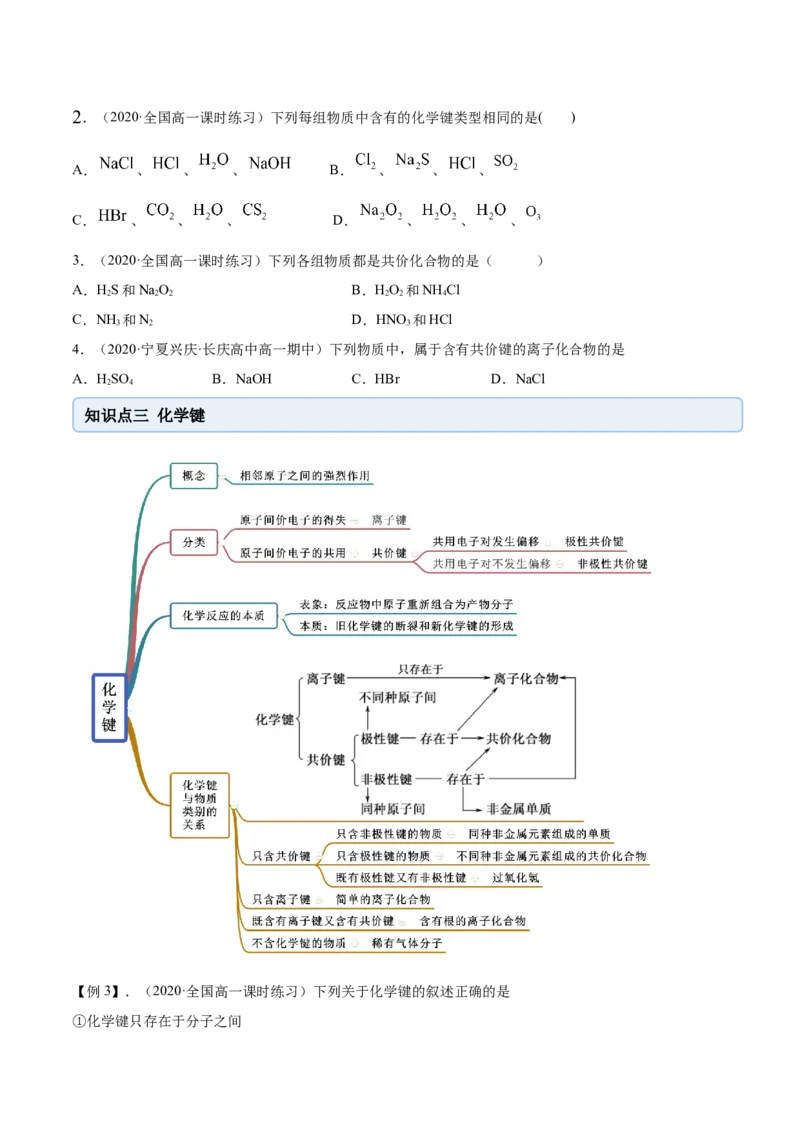
知识点三 化学键
【例3】.(2020·全国高一课时练习)下列关于化学键的叙述正确的是
①化学键只存在于分子之间②化学键是相邻原子之间强烈的相互作用
③化学键是一种静电作用
④化学键是相邻分子之间强烈的相互吸引
⑤离子化合物中可能含有共价键
⑥共价化合物中可能含有离子键
⑦离子化合物中只含离子键
⑧共价化合物中不含离子键
A.②③④⑦ B.②③⑤⑧
C.②④⑤⑥ D.①③⑤⑧
【一隅三反】
1.(2020·全国高一课时练习)现有下列物质:① ② ③NaOH ④HCl ⑤ ⑥
(1)只由离子键构成的物质是________(填序号,下同) 。
(2)只由极性键构成的物质是_________。
(3)只由非极性键构成的物质是________。
(4)由极性键和非极性键构成的物质是________。
(5)由离子键和极性键构成的物质是_______。
(6)由离子键和非极性键构成的物质是______。
(7)属于离子化合物的物质是_______。
(8)属于共价化合物的物质是_______。
2.(2020·湖北武汉·高一期中)已知 A、B、C、D、E 是五种短周期的主族元素,它们的原子序数依次
增大, A 是所有元素中原子半径最小的元素,B、C 组成的某一种化合物能引起温室效应;常温下,
金属 D 单质投入水中能与水剧烈反应;E 的单质在常温下是一种有色的气体。请按要求回答下列几个问
题:
(1)B、D 的元素名称分别为:_____、_____;
(2)E 的最高价氧化物对应的水化物的化学式为:_____;
(3)C 离子的结构示意图为:_____;
(4)B、C、D 三种元素的原子半径从大到小的顺序为_____(用元素符号表示);(5)B、E 的最高价氧化物对应水化物的酸性从强到弱的顺序为:_____(用对应的化学式表示)
(6) 写出 C、D 两种元素组成的阴、阳离子个数比为 1:2 且既含离子键又含有非极性共价键的化合
物的电子式:_____。
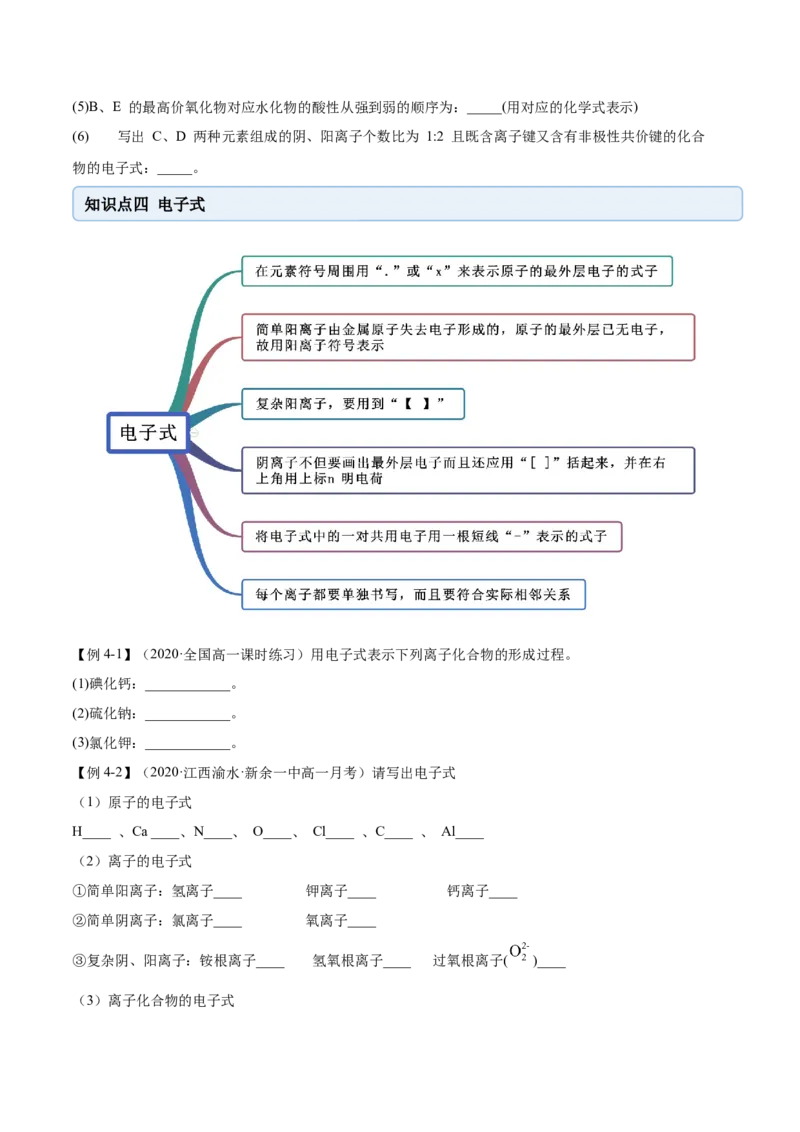
知识点四 电子式
【例4-1】(2020·全国高一课时练习)用电子式表示下列离子化合物的形成过程。
(1)碘化钙:____________。
(2)硫化钠:____________。
(3)氯化钾:____________。
【例4-2】(2020·江西渝水·新余一中高一月考)请写出电子式
(1)原子的电子式
H____ 、Ca ____、N____、 O____、 Cl____ 、C____ 、 Al____
(2)离子的电子式
①简单阳离子:氢离子____ 钾离子____ 钙离子____
②简单阴离子:氯离子____ 氧离子____
③复杂阴、阳离子:铵根离子____ 氢氧根离子____ 过氧根离子( )____
(3)离子化合物的电子式NaCl____ CaO____ CaCl _____ CaF ____ Na O ____ Na O____
2 2 2 2 2
电子式书写:
①书写原子的电子式时,一般讲原子的最外层电子写在元素符号的上、下、左、右四个位置上;
②简单阳离子是原子失去最外层电子后形成的,其电子式即为离子符号本身;
③简单阴离子因为得到电子后最外层一般为8电子结构,书写时要在元素符号周围标出电子,用“[ ]”括上,
并在[ ]右上角标明电性和所带电荷数;
④复杂阴、阳离子中存在共用电子对,要注意H稳定结构最外层2个电子,其他非金属元素稳定结构一般
最外层为8电子,复杂阴、阳离子用“[ ]”括上,并在[ ]右上角标明电性和所带电荷数;
⑤离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后)拼在一起;对于不同价态的离子,也
按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
【一隅三反】
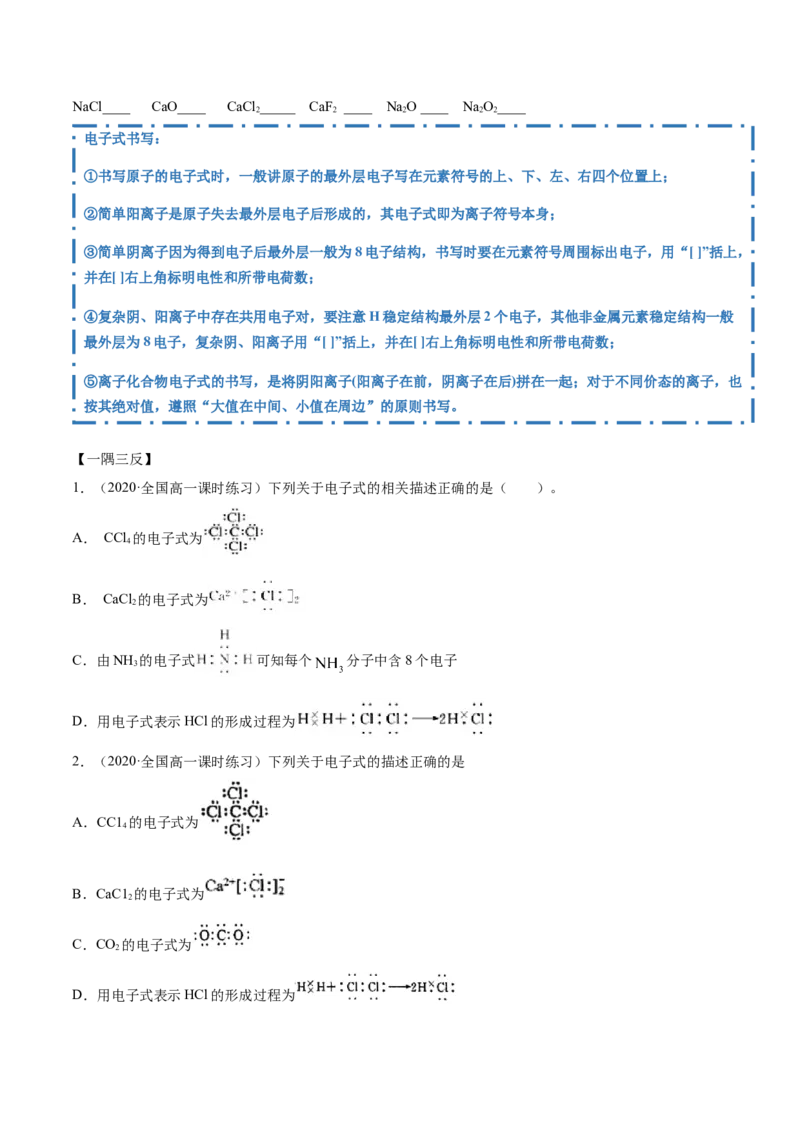
1.(2020·全国高一课时练习)下列关于电子式的相关描述正确的是( )。
A. CCl 的电子式为
4
B. CaCl 的电子式为
2
C.由NH 的电子式 可知每个 分子中含8个电子
3
D.用电子式表示HCl的形成过程为
2.(2020·全国高一课时练习)下列关于电子式的描述正确的是
A.CC1 的电子式为
4
B.CaC1 的电子式为
2
C.CO 的电子式为
2
D.用电子式表示HCl的形成过程为3.(2020·全国高一课时练习)下列叙述正确的是( )
A. 的结构示意图为
B. 的电子式为
C.硫离子的电子式为