文档内容
第四章 元素周期律
第 3 节 化学键
物质结构是化学的重要理论知识,也是中学化学教学的重要内容,化学键的相关知识在必修模块中起
到承上启下的作用,化学键概念的建立,不仅能使学生了解化学反应中物质变化和能量变化的实质,还为
学生认识有机化合物的结构打下基础。化学键的相关知识在整套高中化学教材中以螺旋式上升的形式呈现。
《普通高中化学课程标准(2017版)》对本节的要求:认识构成物质的微粒之间存在相互作用,结合典型实
例认识离子键和共价键的形成,建立化学键概念。知道分子存在一定的空间结构。认识化学键的断裂和形
成是化学反应中物质变化的实质及能量变化的主要原因。根据课程标准,有关化学键的知识,在必修模块
和选修模块中均有教学要求,作为必修模块中的内容,比较简单、基础,较系统地知识将在选修模块中安
排。
本节教材内容分为三个部分:
第一部分是关于离子键的内容。教材先从钠与氯气反应的实验入手,说明钠与氯气反应生成氯化钠,
然后在复习初中知识的基础上,提出离子键和离子化合物的概念,能用电子式表示常见物质的组成,以及
常见离子化合物的形成过程,。
第二部分是关于共价键的内容。教材以氯原子为例分析氯分子的形成,并由此得出共价键和共价化合
物的概念,能够用电子式表示常见物质的组成,以及常见共价分子的形成过程。然后通过分析氢气和氯化
氢中的共价键,引出非极性键和极性键的概念,对这两个概念知道即可。
第三部分是关于化学键的内容。在学生学习了离子键和共价键的基础上,教材归纳出了化学键的概念,
并指出化学反应的过程,包含了反应物分子内化学键的断裂和产物分子中化学键的形成。
离子键的教学流程:钠与氯气的反应→提出问题→思考、讨论→得出结论(离子键的定义)→用电子
式表示NaCl的形成过程→离子键的形成条件→离子键的实质→构成离子键的粒子的特点→离子化合物的
概念→实例→反思与评价。
共价键的教学流程:复习离子键→提出新问题(氯分子的形成)→思考、讨论→得出结论(共价键的
定义)→ 举例说明HCl的形成过程→共价键的形成条件→构成共价键的粒子的特点→共价键的实质→共
价化合物的概念→共价键的种类(极性共价键和非极性共价键)→离子键和共价键的概念辨析→归纳总结
出化学键的定义→化学反应的实质→教学评价。【证据推理与模型认知】
1、知道离子键、共价键、离子化合物、共价分子的概念。
2、能用电子式表示离子化合物、共价分子的形成过程。
3、用结构式表示简单的共价分子结构。
4、能从化学键的角度理解化学反应的本质。
【科学态度与社会责任】
1、了解共价分子的分子结构模型。
2、了解分子间作用力的发展。
1、知道离子键、共价键、离子化合物、共价分子的概念。
2、能写出常见物质的电子式。
投影、电脑视频
【引入】
从元素周期表可以看出,到目前为止,已经发现的元素有一百多种。然而,由这一百多种元素的原
子构成的物质已超过1亿种。那么,元素的原子之间通过什么作用形成如此丰富的物质呢?
【思考】
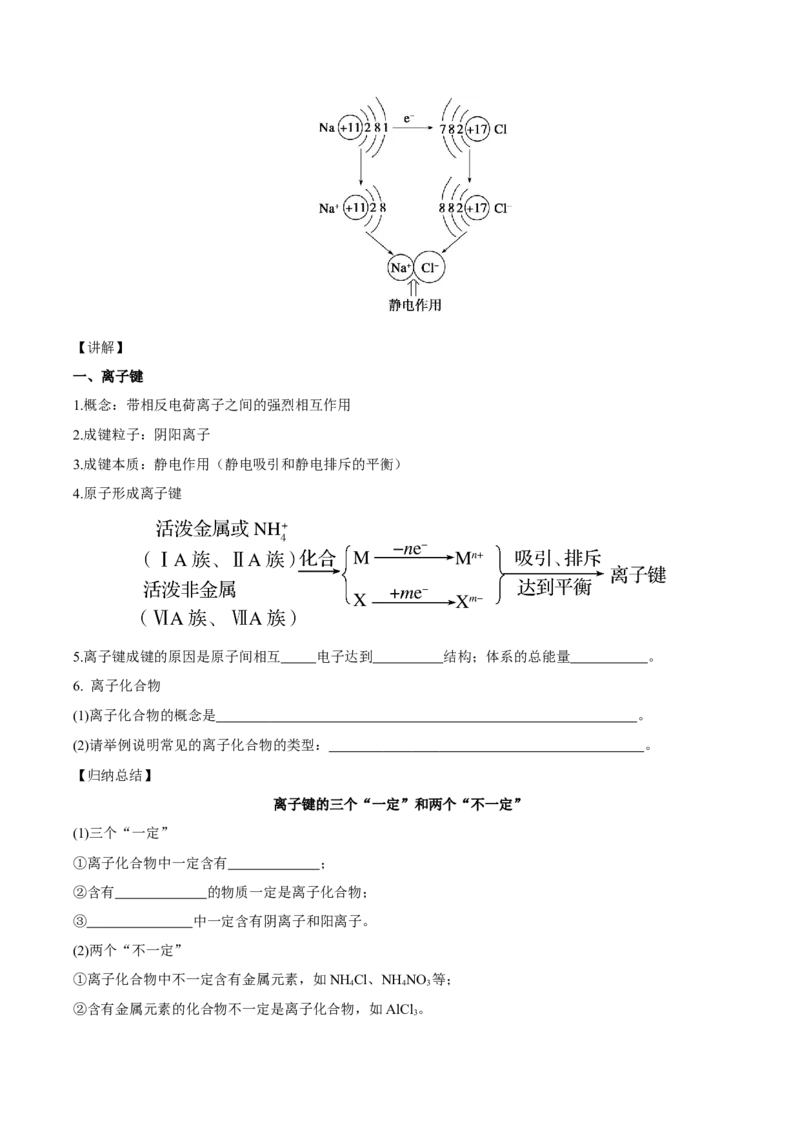
从原子结构的角度来看,钠原子和氯原子是怎样形成NaCl的呢?【讲解】
一、离子键
1.概念:带相反电荷离子之间的强烈相互作用
2.成键粒子:阴阳离子
3.成键本质:静电作用(静电吸引和静电排斥的平衡)
4.原子形成离子键
5.离子键成键的原因是原子间相互 电子达到 结构;体系的总能量 。
6. 离子化合物
(1)离子化合物的概念是 。
(2)请举例说明常见的离子化合物的类型: 。
【归纳总结】
离子键的三个“一定”和两个“不一定”
(1)三个“一定”
①离子化合物中一定含有 ;
②含有 的物质一定是离子化合物;
③ 中一定含有阴离子和阳离子。
(2)两个“不一定”
①离子化合物中不一定含有金属元素,如NH Cl、NH NO 等;
4 4 3
②含有金属元素的化合物不一定是离子化合物,如AlCl 。
3二、电子式
在元素符号周围用小黑点 · (或×)来表示原子的最外层电子的式子。
(1)原子的电子式:在元素符号四个方向逐一放置电子
(2)简单离子的电子式
简单阳离子:直接用离子符号,如Na+
简单阴离子:
【课堂练习】
1、写出下列微粒的电子式:
硫原子、 溴原子、氟原子、 铝原子、硫离子、 溴离子、氟离子、 铝离子
2、写出下列微粒的电子式:氢化钠、氧化钠。
【课堂练习】【思考与交流】
为什么2个氢原子结合成氢分子,2个氯原子结合成氯分子,而不是3个、4个呢?为什么1个氢原子
和1个氯原子结合成氯化氢分子,而不是以其他的个数比相结合呢?
H + Cl = 2HCl
2 2
在HCl分子的形成过程中,没有发生电子的得失,而是通过共用电子对双方达到稳定结构
【讲解】
1、共价键定义:原子之间通过共用电子对所形成的强烈相互作用,叫共价键。
2、共价键的成键特点
成键微粒:原 子
成键本质:共用电子对
成键条件:一般由非金属元素形成
3、共价化合物:不同原子之间以共用电子对形成分子的化合物。
4、共价键的存在:(1) 共价化合物HCl、 CO 、NH
2 3
(2) 多原子非金属单质Cl、 O、 P
2 3 4
(3) 含根的离子化合物 NaOH 、 NaO 、 NH Cl 、NH NO
2 2 4 4 3
注意:含有共价键的化合物不一定是共价化合物
【归纳总结】
共价键的两个“一定”和两个“不一定”
(1)两个“一定”
①共价化合物中一定 共价键;
②共价化合物中一定 离子键。
(2)两个“不一定”
①含共价键的物质不一定是共价化合物,也可能是单质,如O、N、H、Cl 等;
2 2 2 2
②含共价键的化合物不一定是共价化合物,也可能是离子化合物,如 NaOH中含有O—H共价键,NaO
2 2
中含有O—O共价键,NH Cl中含有N—H共价键,但它们都是离子化合物。
4
5、共价键的分类
非极性键:共用电子对不发生偏移
极性键:共用电子对偏向某一方
【共价键形成的分子及其结构模型】【课堂练习】
6、指出下列物质中的共价键类型
O
2
CH
4
CO
2
HO
2 2
NaO
2 2
NaOH
7、用电子式表示原子形成共价键
H
2
HCl
HO
2
CO
2
NH
3
四、化学键【归纳总结1】离子键和共价键的比较
【归纳总结2】离子化合物与共价化合物的比较
离子化合物 共价化合物
化学键 离子键或离子键与共价键 共价键
由离子键构成的化合物叫离子化 以共用电子对形成分子的化合物
概念
合物 叫共价化合物
通过形成共用电子对达到稳定结
达到稳定结构的途径 通过电子得失达到稳定结构
构
构成微粒 阴、阳离子 原子
一般为活泼金属元素与活泼非金
构成元素 一般为不同种非金属元素
属元素
以HCl为例:电子式为
以NaCl为例:电子式为
表示方法
NaCl的形成过程为 HCl的形成过程为【资料卡片】
【课堂练习】
2、判断以下说法的正误
A、离子化合物一定含离子键,共价化合物一定含共价键。
B、含离子键的化合物一定为离子化合物。
C、金属元素与非金属元素之间一定形成离子键。
D、由非金属元素组成的化合物一定不含离子键。
E、有离子就一定可以形成离子键。
3、下列说法正确的是( )
A、含有金属元素的化合物一定是离子化合物B、第ⅠA族和第ⅦA族原子化合时,一定生成离子键
C、由非金属元素形成的化合物一定不是离子化合物
D、活泼金属与非金属化合时,能形成离子键
4、下列说法正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属原子之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.钠原子与氯原子结合成氯化钠后体系能量降低
【学习小结】
在本节课中我先从问题入手,激发学生的学习兴趣,调动学生的积极性。从浅入深的讲解化学键、离
子键、电子式的书写。在讲解化学键时从例子总结入手,掌握化学键。利用微观粒子原子结构讲解离子键
的实质。总结离子键判断规律:含有金属阳离子和铵根离子的化合物就一定属于离子键。引出电子式,可
以表示原子、离子、化合物以及形成过程。以及电子式书写的规律和注意事项。
每讲解一个定义时,都让学生找出其关键词,并总结学习规律或经验。在今后的教学中注重定义的打
实,在语气中强调定义中的关键语。在讲解电子式的点或叉时,没有完全到位,应该强调在书写时都可以
写,但由于书写时容易书写混乱,所以都可以写成点的形式。在讲解离子键引力和斥力时,如果引用动画,
效果能好一些。从而达到落实学生学科素养的培养。