文档内容
2019-2020学年高一化学期末复习专项提升卷(人教版2019必修第二册)
专项 02 化学反应中能量变化关系的判断及计算
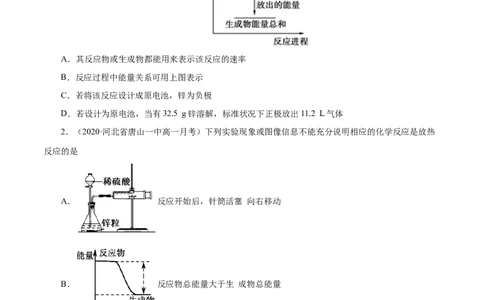
1.对于反应Zn(s)+HSO (aq)=ZnSO(aq)+H(g),下列叙述不正确的是( )
2 4 4 2
A.其反应物或生成物都能用来表示该反应的速率
B.反应过程中能量关系可用上图表示
C.若将该反应设计成原电池,锌为负极
D.若设计为原电池,当有32.5 g锌溶解,标准状况下正极放出11.2 L气体
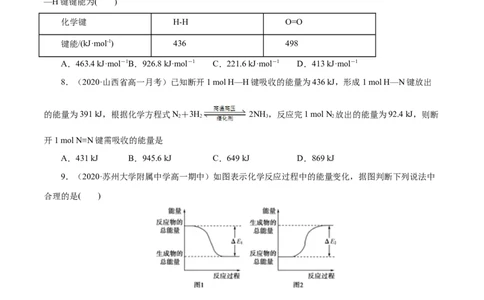
2.(2020·河北省唐山一中高一月考)下列实验现象或图像信息不能充分说明相应的化学反应是放热
反应的是
A. 反应开始后,针筒活塞 向右移动
B. 反应物总能量大于生 成物总能量
C. 反应开始后,甲处液面 低于乙处液面
1
原创精品资源学科网独家享有版权,侵权必究!D. 温度计的水银柱不断 上升
3.(2020·青海省平安一中高一期中)已知2SO +O =2SO 为放热反应,对该反应的下列说法中正确的
2 2 3
是( )
A.SO 和O 的总能量一定高于SO 的总能量
2 2 3
B.为了提高SO 的转化率,应使用催化剂
2
C.此反应达到平衡时,SO 的浓度与SO 的浓度一定相等
2 3
D.因该反应为放热反应,故不必加热就可发生
4.(2020·山东省淄博第七中学高一月考)工业上由CO 和H 合成气态甲醇的化学方程式为CO+
2 2 2
3H===CH OH+HO,已知该反应是放热反应。下面表示合成甲醇的反应的能量变化示意图,其中正确的
2 3 2
是( )
A. B.
C. D.
5.如图是金属镁和卤素单质(X )反应的能量变化示意图。下列叙述中,正确的说法有几项( )
2
①Mg(s)所具有的能量高于MgX (s)所具有的能量
2
②MgCl 电解制Mg(s)和Cl(g)是吸热过程
2 2
2
原创精品资源学科网独家享有版权,侵权必究!③热稳定性:MgI >MgBr >MgCl >MgF
2 2 2 2
④断裂Mg(s)和X(g)的化学键放出的能量比形成MgX (s)的化学键吸收的能量多
2 2
A.1项 B.2项 C.3项 D.4项
6.已知一定温度时:2SO (g)+O(g) 2SO (g),当生成2mol SO 时,放出热量197kJ,在相同温度和
2 2 3 3
压强下,向密闭容器中通入2mol SO 和1m⇌olO ,达到平衡时放出热量Q,则下列关系式中正确的是
2 2
A.Q=197 kJ B.Q<197×2 kJ C.Q<197 kJ D.Q>197 kJ
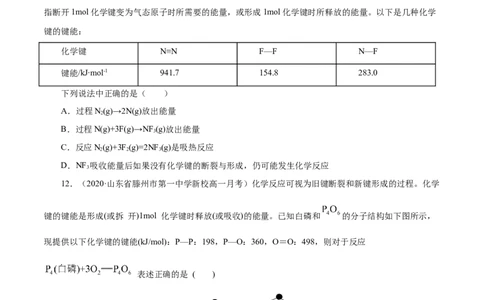
7.已知:2H(g)+O(g)=2HO(g)反应放出的热量为483.6 kJ。有关键能数据如表所示:则水分子中O
2 2 2
—H键键能为( )
化学键 H-H O=O
键能/(kJ·mol-1) 436 498
A.463.4 kJ·mol-1B.926.8 kJ·mol-1 C.221.6 kJ·mol-1 D.413 kJ·mol-1
8.(2020·山西省高一月考)已知断开1 mol H—H键吸收的能量为436 kJ,形成1 mol H—N键放出
的能量为391 kJ,根据化学方程式N+3H 2NH ,反应完1 mol N 放出的能量为92.4 kJ,则断
2 2 3 2
开1 mol N≡N键需吸收的能量是
A.431 kJ B.945.6 kJ C.649 kJ D.869 kJ
9.(2020·苏州大学附属中学高一期中)如图表示化学反应过程中的能量变化,据图判断下列说法中
合理的是( )
A.铵盐和碱混合即可反应,其能量变化符合图 1
B.0.1mol H SO 溶液和 0.1mol Ba(OH) 溶液的反应符合图 2,且吸收热量为ΔE
2 4 2 2
C.0.1mol HCl 溶液和 0.1mol NaOH 溶液的反应符合图 1,且放出热量为ΔE
1
D.发生图 1 能量变化的任何反应,一定不需要加热即可发生
10.(2020·河南省高一月考)氢气和氟气混合在黑暗处即可爆炸并放出大量的热。在反应过程中,断
3
原创精品资源学科网独家享有版权,侵权必究!裂 中的化学键消耗的能量为 ,断裂 中的化学键消耗的能量为 ,形成
中的化学键释放的能量为 ,下列关系式中,一定正确的是( )
A. B. C. D.
11.(2020·黑龙江省大庆实验中学高一月考)生产液晶显示器的过程中使用的化学清洗剂NF 是一种
3
温室气体,其储存能量的能力是CO 的12000~20000倍,在大气中的寿命可长达740年之久,已知键能是
2
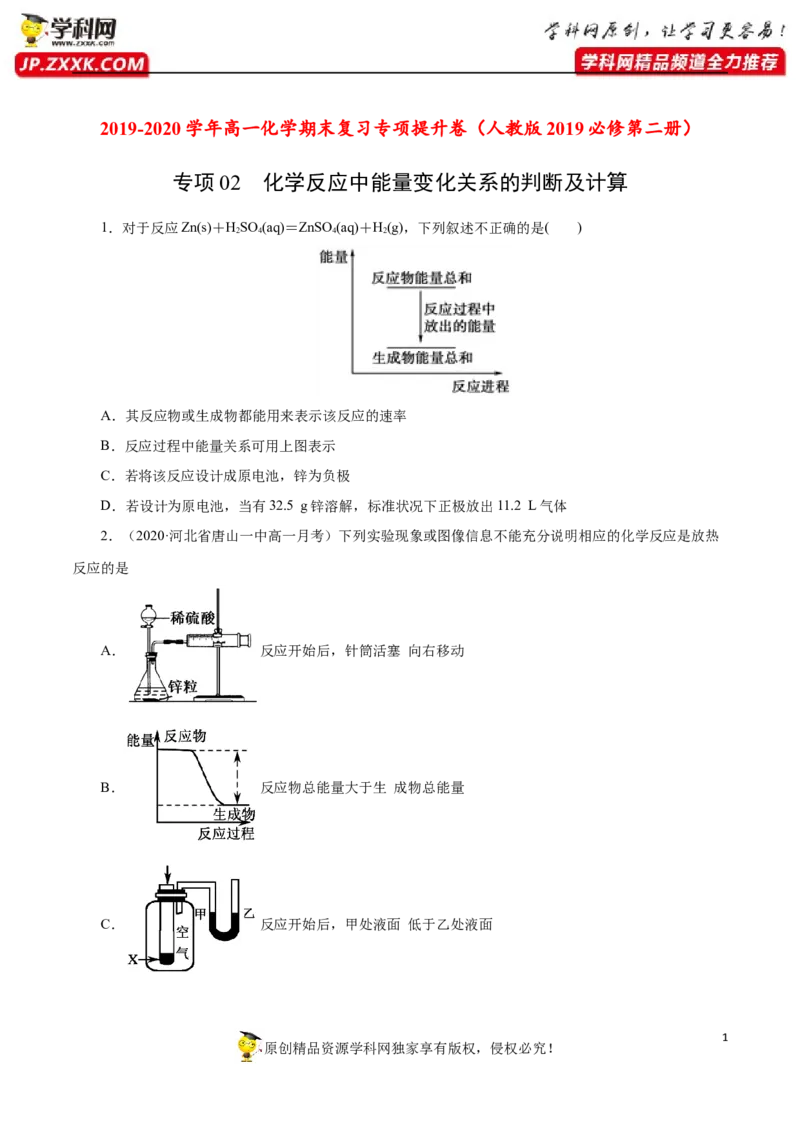
指断开1mol化学键变为气态原子时所需要的能量,或形成1mol化学键时所释放的能量。以下是几种化学
键的键能:
化学键 N≡N F—F N—F
键能/kJ∙mol-1 941.7 154.8 283.0
下列说法中正确的是( )
A.过程N(g)→2N(g)放出能量
2
B.过程N(g)+3F(g)→NF (g)放出能量
3
C.反应N(g)+3F (g)=2NF (g)是吸热反应
2 2 3
D.NF 吸收能量后如果没有化学键的断裂与形成,仍可能发生化学反应
3
12.(2020·山东省滕州市第一中学新校高一月考)化学反应可视为旧键断裂和新键形成的过程。化学
键的键能是形成(或拆 开)1mol 化学键时释放(或吸收)的能量。已知白磷和 的分子结构如下图所示,
现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则对于反应
表述正确的是 ( )
A.放出1638 kJ 的热量 B.吸收1638 kJ 的热量
C.放出126 kJ 的热量 D.吸收126 kJ 的热量
13.某反应由两步反应A B C构成,它的反应能量曲线如图,下列叙述正确的是
4
原创精品资源学科网独家享有版权,侵权必究!A.三种化合物中C最稳定
B.两步反应均为吸热反应
C.A与C的能量差为E
4
D.A B反应,反应条件一定要加热
14.(2020·天津市第二南开中学高一月考)已知断裂 1 mol 共价键所需要吸收的能量分别为 H-H 键:
436 kJ;I-I 键:153 kJ;H-I 键:299 kJ。下列对反应 H(g)+I(g) 2HI(g)的判断中,错误的是( )
2 2
A.该反应是放出能量的反应 ⇌
B.该反应是吸收能量的反应
C.该反应是氧化还原反应
D.I 与 H 具有的总能量大于生成的 HI 具有的总能量
2 2
15.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量
不同引起的。下图为N(g)和O(g)反应生成NO(g)过程中的能量变化,下列说法正确的是
2 2
A.1 mol N (g)和N 个O(g)反应放出的能量为180 kJ
2 A 2
B.1 mol N (g)和1 mol O (g)具有总能量小于2 mol NO(g)具有的总能量
2 2
C.通常情况下,N(g)和O(g)混合能直接生成NO(g)
2 2
D.吸热反应一定需要加热才能发生
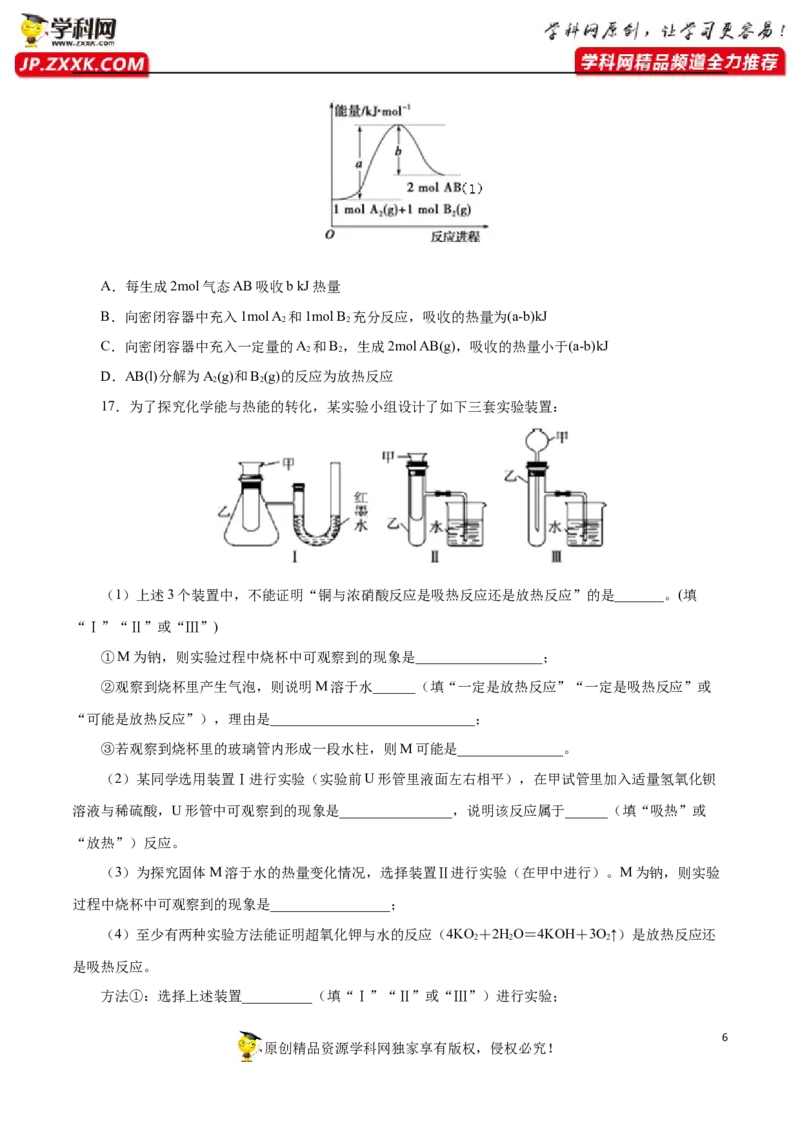
16.(2020·四川省成都外国语学校高一期中)已知化学反应A(g)+B (g) 2AB(l)的能量变化如图所示,
2 2
判断下列叙述中正确的是 ⇌
5
原创精品资源学科网独家享有版权,侵权必究!A.每生成2mol气态AB吸收b kJ热量
B.向密闭容器中充入1mol A 和1mol B 充分反应,吸收的热量为(a-b)kJ
2 2
C.向密闭容器中充入一定量的A 和B ,生成2mol AB(g),吸收的热量小于(a-b)kJ
2 2
D.AB(l)分解为A(g)和B (g)的反应为放热反应
2 2
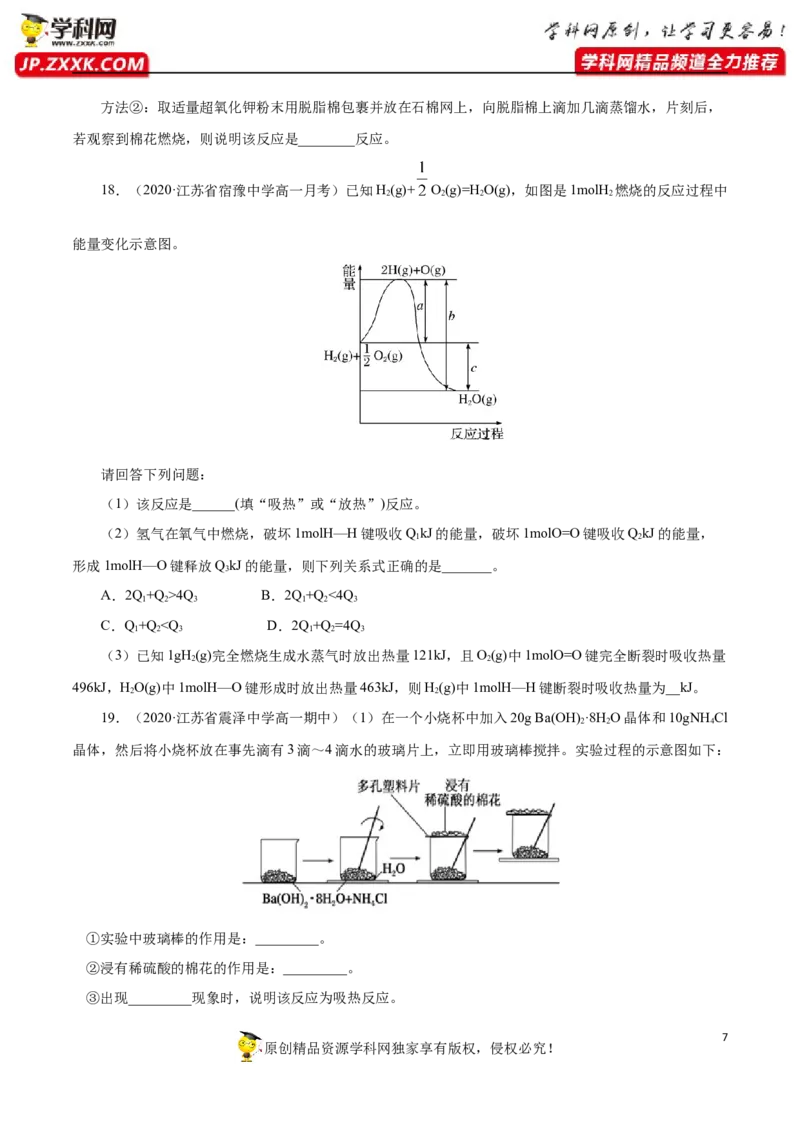
17.为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是_______。(填
“Ⅰ”“Ⅱ”或“Ⅲ”)
①M为钠,则实验过程中烧杯中可观察到的现象是__________________;
②观察到烧杯里产生气泡,则说明M溶于水______(填“一定是放热反应”“一定是吸热反应”或
“可能是放热反应”),理由是_____________________________;
③若观察到烧杯里的玻璃管内形成一段水柱,则M可能是_______________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡
溶液与稀硫酸,U形管中可观察到的现象是________________,说明该反应属于______(填“吸热”或
“放热”)反应。
(3)为探究固体M溶于水的热量变化情况,选择装置Ⅱ进行实验(在甲中进行)。M为钠,则实验
过程中烧杯中可观察到的现象是_________________;
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO +2HO=4KOH+3O↑)是放热反应还
2 2 2
是吸热反应。
方法①:选择上述装置__________(填“Ⅰ”“Ⅱ”或“Ⅲ”)进行实验;
6
原创精品资源学科网独家享有版权,侵权必究!方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,
若观察到棉花燃烧,则说明该反应是________反应。
18.(2020·江苏省宿豫中学高一月考)已知H(g)+ O(g)=HO(g),如图是1molH 燃烧的反应过程中
2 2 2 2
能量变化示意图。
请回答下列问题:
(1)该反应是______(填“吸热”或“放热”)反应。
(2)氢气在氧气中燃烧,破坏1molH—H键吸收QkJ的能量,破坏1molO=O键吸收QkJ的能量,
1 2
形成1molH—O键释放QkJ的能量,则下列关系式正确的是_______。
3
A.2Q+Q >4Q B.2Q+Q <4Q
1 2 3 1 2 3
C.Q+Q