文档内容
2009 年全国初中学生化学素质和实验能力竞赛
(第十九届天原杯)初赛试题(广东卷)
说明:1.本卷分两部分,共32小题。满分为130分,考试时间为120分钟。
2.可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 I-127
第一部分 (共计100分)
一.选择题(本大题包括14小题,每小题2分,共28分。每小题只有一个选项符合题意,请将
正确选项的字母填在该题后的括号内)
1.生活中常见的下列现象,属于化学变化的是 ( )
A .冰雪融化 B.矿井瓦斯爆炸 C.湿衣服晾干 D.玻璃杯爆裂
2.下列物质,属于纯净物的是 ( )
A. 空气 B. 石油 C. 酒精 D. 石灰水
3.能证明分子在化学变化中可分的是 ( )
A、打开汽水瓶,有气体逸出 B、10mL水与10mL酒精混合,体积小于20mL
C、加热氧化汞得银白色汞与氧气 D、水蒸发为水蒸气
4.人类探测月球发现,月球土壤中含有较丰富的质子数为2、中子数为l的氦原子。则氦原子
中的电子数为 ( )
A.1 B.2 C.3 D.4
5.下列实验操作正确的是 ( )
A.未说明药品用量时,液体取10mL左右,固体只需盖满试管底部
B.用滴管滴加液体时,为防止液滴飞溅应将滴管口紧贴试管内壁
C.酒精灯用完后,立即用嘴吹灭
D.玻璃仪器内壁附着的水既不聚成水滴,也不成股流下时,表示仪器洗涤干净
6.酒后驾车是非常严重的违章行为,交警常用“司机饮酒验测仪”检查司机呼出的气体以
判断他是否饮酒。司机呼出的乙醇分子能在硫酸存在的条件下,使红色的三氧化铬变为绿
色的硫酸铬[Cr(SO )]。则硫酸铬中Cr元素的化合价为 ( )
2 4 3
A.+3 B.+5 C.+6 D.+7
7.某饮料的配料表:纯净水、蔗糖、苹果汁、维生素C、维生素A、乳酸钙。此饮料不含
有的营养素是 ( )
A.糖类 B.维生素 C.水 D.油脂
8.“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝制易拉罐、铜导线可
以归为一类加以回收,因为它们属于 ( )
A.氧化物 B.化合物 C.混合物 D.金属或合金
9.碳的单质中,质地较软,常用作电极的是 ( )
A.金刚石 B.活性炭 C.炭黑 D.石墨
10.托盘天平调零后,在左盘衬纸上置氧化铜粉末,右盘衬纸上置1个5 g砝码,游码标尺示数如下,此时天平平衡。则被称量的氧化铜质量为 ( )
A.8.3 g B.7.7 g C.3.3 g D.2.7 g
11.实验室制取气体选择收集方法时,对气体的下列性质不必考虑的是 ( )
A.颜色 B.密度 C.溶解性 D.是否与水反应
12.扑灭图书档案、贵重设备、精密仪器等火灾,不会留下任何痕迹而使物品损坏,最适宜的
灭火器是 ( )
A、高压水枪 B、液态二氧化碳灭火器
C、干粉灭火器 D、泡沫灭火器
13.t℃时,向一支盛有0.1g熟石灰的试管内加入10mL水,充分振荡后,静置,试管底部仍有
未溶解的白色固体。对于试管内上层澄清液体的叙述正确的是 ( )
A、溶液是t℃时的饱和溶液
B、升高温度溶液变为不饱和溶液
C、溶液中溶质的质量等于0.1g
D、溶液中溶质的质量分数等于1%
14.冬天,人们常用甘油溶液护肤,使皮肤保持湿润。质量分数为80%的甘油溶液护肤效果最
佳。配制80%的甘油溶液500g,所需甘油的质量为 ( )
A.80 g B.40 g C.100 g D.400 g
二、填空题(本大题包括5小题,共20分)
15.(4分)有机合成材料的出现是材料发展史上的一次重大突破。人们常说的三大合成材料
是指塑料、 和 。合成材料的应用与发展,大大方便了人类
的生活。但是,合成材料废弃物的急剧增加也带来了环境问题,废弃塑料带来的环境问题
一般称为“___________________”。为了解决这一问题,你认为塑料的发展方向是(只要
求谈其中一点) 。
16.(5分) 某乡镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含 SO 的废气和含
2
HSO 的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该乡
2 4
镇环境造成极大破坏。
(1)分析该乡镇下酸雨的原因: 。
(2)举一例说明酸雨对环境造成的危害: 。
(3)该乡镇某中学环保小组提出了治理酸雨的下列措施,你认为其中不妥的是 。
A.将硫酸厂搬离该乡镇 B.建议环保部门限令整改
C.将硫酸厂排出的废气中的SO 处理后排放 D.工厂和居民改用较清洁的燃料
2
(4)浓硫酸弄到手上后应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液。若是稀
硫酸弄到手上,_______(填“需要”或“不需要”)这样做,理由是
____
。
17.(5分)为保证长时间潜航,在潜水艇里要配备氧气再生装置,有以下几种制取氧气的方法:
①加热高锰酸钾,②电解水,③在常温下过氧化钠固体(NaO)与二氧化碳反应生成碳酸
2 2钠和氧气。
(1)写出方法③的化学方程式_______________________________________________。
(2)你认为适合在潜水艇里制取氧气的方法是(填序号)_______,与其他两种方法相比,
这种方法的优点是_________________________________________________________;
________________________________________________________________________。
18.(4分)阅读表格,综合考虑下表各方面的因素,回答以下问题。
金 全球产量 密度 熔点(℃) 导热性能 导电性能 市场价格
属 (104t) (103㎏·m-3) (元/t)(大约)
铝 15000 2.7 660 4 4 16000
铜 8000 8.9 1083 2 2 17700
铁 301430 7.9 1540 8 7 2200
银 8 10.5 961 1 1 1365000
注:导热性能1→8表示表示导热性由强到弱,导电性能1→8表示导电性由强到弱。
(1)导电性能好的两种金属是________________,其中更适宜做导线的是_________,
理由是__________________________________________________________。
(2)用铝锅炒菜时锅底易变形,而用铁锅则不会,主要原因是___________________
____________________________________________________________。
19.(2分)某中学的同学自制成一种黄色的花汁,加入到不同试剂中,观察到的现象如下:
试剂 稀盐酸 食盐水 蒸馏水 草木灰水 石灰水
颜色 红 黄 黄 绿 绿
小强同学依据上表信息进行如下实验:
(1) 用该花汁去检验附近小化工厂排放废水的酸碱性,显浅红色,则此废水显____性
(2) 用该花汁测知家中花盆土壤显酸性,打算加入上表中的____________(写物质名称)来
改良。
三、(本大题包括2小题,共15分)
20.(8分)有 A、B、C、D、E五种常见物质,它们有如下图所示关系:
已知:C是一种金属,气体D可以使澄清石灰水变浑浊。
(1) 写出物质的名称: A 、 C 、D 、E 。
(2) 写出 A和B、 A和E反应的化学方程式:_________________________________;
______________________________________。
21.(7分)某同学用空塑料饮料瓶做简易净水器,设计图如下。(1)请你帮他继续设计:把小卵石、活性炭、石英沙三种材料放置在装置相应的位置
以获得较好的净水效果,则图中的①②③位置放置的材料依次是____________、
______________ 、_____________。
(2)小卵石、石英沙和膨松棉的作用是____________; 活性炭的作用是___________。
(3)净化后是硬水还是软水,可用___________________来检验。
(4)长期饮用硬水对人体健康不利,要降低水的硬度,可采用____________方法。
四、(本大题包括2小题,共23分)
22.(14分)根据下列装置图回答问题(所用装置图用序号表示)
(1)写出图中标号的仪器名称:
①____________,②____________ , ③____________。
(2)利用装置A可制得的气体是__________ ,该反应的化学方程式是_____________
__________________________,反应类型是____________。
(3)制取CO 可选用装置_________,检验CO 可选用装置________,收集CO 可选用装置
2 2 2
________。
(4)查阅以下资料回答下列问题:
物质 制取气体的药品 制取气体的反应条件 气体的物理性质
氯气 MnO 固体和浓盐酸 需要加热 可溶于水,密度比空气大
2
①制取氯气____________(可以或不可以)采用装置A,理由是________________。
②制取氯气____________(可以或不可以)采用装置B,理由是_________________。
23.(9分)化学科代表小聪与小明同学帮助实验老师整理化学药品室时,发现分别放在两个
试剂瓶中的两片用砂纸磨得光亮的银白色金属,未贴标签。到底它们是哪种金属?两位
同学首先对这两种金属X和Y的金属活动性顺序进行实验探究。
(1)进行猜想:
①科代表小聪猜想:活动性X大于Y。
②小明同学猜想:活动性Y大于X。(2)设计实验方案、进行实验、获得知识。完成如下实验报告,并回答后续有关问题。
①实验步骤 ②实验操作 ③结论
金属Y表面无明显变化,
金属X的表面有气泡冒
__
__ 出。将燃着的木条放在装
金属X的试管口,气体燃
__ 烧
科代表小聪的猜想:_______
(“正确”或“不正确”)
(3)上述实验之前,实验老师只知道X、Y是银铁中的各一种,则根据实验结果说明Y就是
_______。实验室急需一定量的Y粉末,科代表小聪认为可用现有的X金属粉末和Y的盐
溶液、蒸馏水等药品,配以必要的仪器来制得急需的Y粉末,原因是(用反应的化学方程式
表示)____________________________________________。
(4)实验老师经实验分析得知制得的Y粉末中含有未反应完的X粉末,若用化学方法将杂
质X粉末除去,两个同学经讨论、交流一致认为可选用的除杂质试剂是_________。
五、(本大题包括2小题,共14分)
24.(6分)青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物
主要是尿素[CO(NH)]。若从食物中摄取的蛋白质经体内新陈代谢后完全转化为尿素排出
2 2
体外,每人每天相当于排出尿素30g。
(1)30g尿素中含氮元素_____克。
(2)已知蛋白质中氮元素的平均质量分数为16%,则每人每天至少应从食物里摄取的蛋白
质为多少克?
(3)请你根据下表中几种常见食物的蛋白质含量,计算出每天至少应摄入多少克下列食
物才能满足你对蛋白质的需求(可以只摄取一种食物,也可同时摄取几种食物)。
食物 白面 鸡蛋 瘦猪肉 牛奶
蛋白质含量 10% 14% 20% 3%25.(8分)我国目前使用的燃料主要是煤和石油,含有硫的煤燃烧时生成的SO 会污染空气。
2
(1)某火力发电厂每天燃烧含硫1.6%的煤100 t,若煤中的硫全部转化为SO ,则该厂每天
2
产生SO t。为防止SO 污染,可将SO 通入石灰乳中生成Ca(HSO ),则该反应的化学
2 3 2 3 2
方程式为 。
(2)国家标准规定工业废气中SO 含量不得超过0.15 mg/m3。工业上测量SO 的含量时,可
2 2
以根据反应:SO +2H O+I =H SO +2HI。现取该厂废气样品1000 L,用0.0254%的碘(I)溶
2 2 2 2 4 2
液2g刚好完全反应。试计算该厂排放的废气中SO 的含量是否符合国家标准。
2
第二部分 (共计30分)
六、选择题(本大题包括5小题,每小题2分,共10分。每小题有1个或2个选项符合题
意,请将正确选项的字母填在该题后的括号内。错选得0分,漏选且正确得1分)
26.我们在实验室看到的浓硝酸往往呈黄色,这是由于硝酸的化学性质不稳定、分解生成
NO 的缘故。纯净的硝酸或浓硝酸在常温下见光或受热就会分解,有关反应为:
2
见光或受热4HNO ===2HO + 4NO ↑+ O ↑。为防止硝酸的分解,下列贮存硝酸的方法中
3 2 2 2
你认为合理的是 ( )
A.无色试剂瓶 B.棕色试剂瓶C.无色试剂瓶并置于阴凉处 D.棕色试剂瓶并置于阴凉处
27.下列化学实验基本操作中,正确的是 ( )
A. 加热试管里的固体时,试管口应稍稍向下倾斜
B. 把氢氧化钠固体放在天平右盘的纸上称量
C. 给试管里的液体加热时 ,试管口不要对着人
D. 稀释浓硫酸时,把水迅速地倒入浓硫酸中
28.能使农作物枝叶繁茂、叶色浓绿,还能提高产量的化学肥料是 ( )
A.尿素 B.钙镁磷肥 C.硫酸钾 D.碳酸氢铵
29.鉴别下列各组物质,选用试剂(括号内的物质)正确的是 ( )
A.氢氧化钠溶液和澄清石灰水(稀盐酸)
B.氯化钠溶液和稀盐酸(无色酚酞)
C.硝酸铵固体和氢氧化钠固体(水)
D.硬水与软水(肥皂水)
30.下列各图所示装置的气密性检查中,漏气的是 ( )
A. B. C. D.
七、(本大题包括2小题,共20分)
31.(6分)某化学小组同学按下图所示装置和表中所给试剂进行实验(图中铁架台等夹持仪
器均已略去):
组别 A组 B组 C组 D组
试管I Ca(OH) CaCO Zn Cu
2 3
稀HCl 稀HCl 稀HSO 稀HSO
2 4 2 4
试管Ⅱ KNO 溶 Ca(OH) 溶 Ba(OH) 溶 Ba(OH) 溶
3 2 2 2
液 液 液 液
(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止
水夹b,试管Ⅱ中液面上升,溶液变浑浊。符合以上实验现象的试
剂 是 组 , 此 时 Ⅱ 中 发 生 反 应 的 化 学 方 程 式 为
____________ __________ _ _ ,出
现上述现象的原因是 ____________________________________ _。
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,试管Ⅱ
中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是 组。
32.(14分)在学了盐的性质以后,某校化学兴趣小组的同学开展了测定NaCO 和NaCl的固
2 3
体混合物中质量分数的探究实验。他们设计了如下的实验方案:
[方案一]气体分析法。
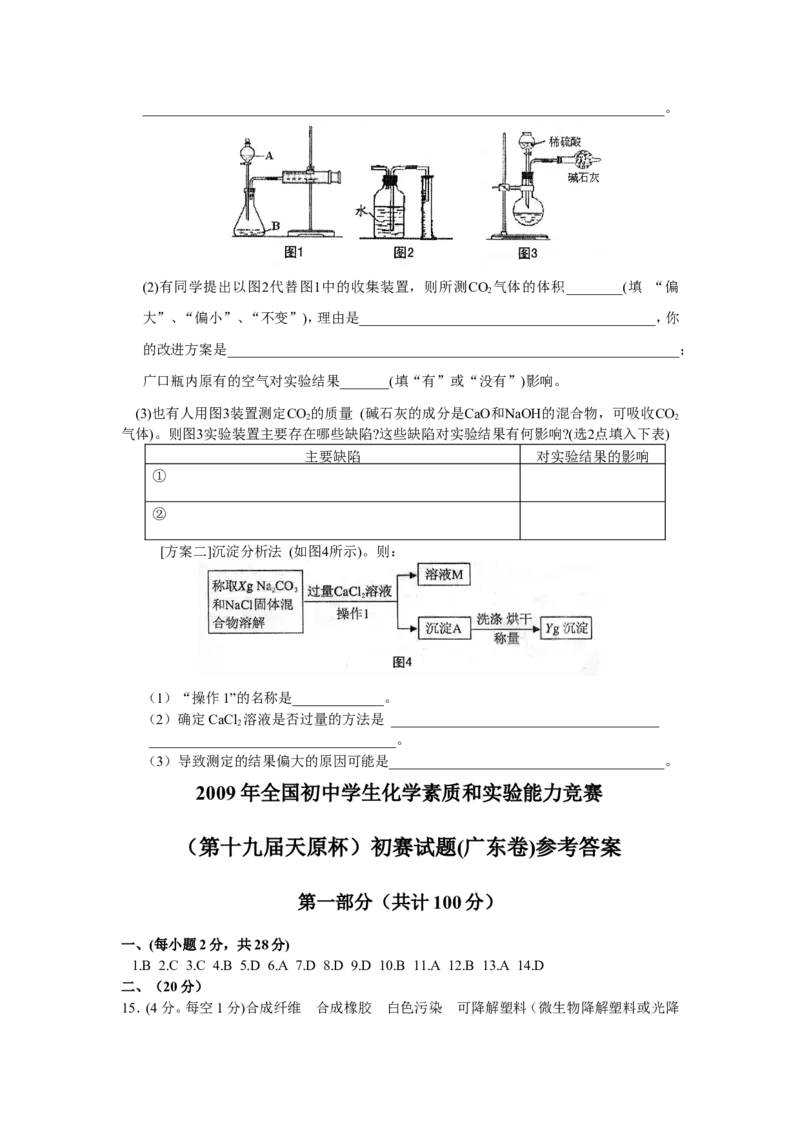
(1)如下图1所示(铁夹夹持的仪器是注射器),把X g的混合物与足量稀硫酸反应后,测定
产生的CO气体的体积。检查该装置的气密性的方法是________________________
2__________________________________________________________________________。
(2)有同学提出以图2代替图1中的收集装置,则所测CO 气体的体积________(填 “偏
2
大”、“偏小”、“不变”),理由是__________________________________________,你
的改进方案是________________________________________________________________;
广口瓶内原有的空气对实验结果_______(填“有”或“没有”)影响。
(3)也有人用图3装置测定CO 的质量 (碱石灰的成分是CaO和NaOH的混合物,可吸收CO
2 2
气体)。则图3实验装置主要存在哪些缺陷?这些缺陷对实验结果有何影响?(选2点填入下表)
主要缺陷 对实验结果的影响
①
②
[方案二]沉淀分析法 (如图4所示)。则:
(1)“操作1”的名称是_____________。
(2)确定CaCl 溶液是否过量的方法是 ______________________________________
2
___________________________________。
(3)导致测定的结果偏大的原因可能是_______________________________________。
2009年全国初中学生化学素质和实验能力竞赛
(第十九届天原杯)初赛试题(广东卷)参考答案
第一部分(共计100分)
一、(每小题2分,共28分)
1.B 2.C 3.C 4.B 5.D 6.A 7.D 8.D 9.D 10.B 11.A 12.B 13.A 14.D
二、(20分)
15.(4分。每空1分)合成纤维 合成橡胶 白色污染 可降解塑料(微生物降解塑料或光降解塑料等)
16.(5分)(1)排放二氧化硫废气、用煤作燃料
(2)酸化土壤、腐蚀、破坏森林植物、腐蚀建筑物(答出一点即可)
(3)A (4)需要 稀硫酸中的水蒸发后会变成浓硫酸(意对即可)
17.(5分) (1)2NaO+2CO===2Na CO+O (2分)
2 2 2 2 3 2
(2)③ (1分) 将人呼出的CO 转化为O (1分)
2 2
反应容易,不需要加热和消耗电能(1分)
18.(4分。每空1分)
(1)银和铜 铜 铜的产量比银的产量高,铜的价格比银的价格低
(2)因为铝锅的熔点低,故在炒菜时容易软化,而铁锅的熔点高(从硬度角度解释也可)
19.(2分,每空1分)(1) 酸 (2) 熟石灰(或石灰水) 或 草木灰 (或草木灰水)
三、(15分)
20.(8分)氧化铜 铜 二氧化碳 一氧化碳(每空1分)
C + 2CuO 2Cu + CO ↑ CuO + CO Cu + CO (每空2分)
2 2
21.(7分。每空1分)(1)小卵石 石英沙 活性炭 (2)过滤 吸附 (3)肥皂水
(4)蒸馏
四、(27分)
22.(14分。方程式2分,其余每空1分)(1)酒精灯 试管 长颈漏斗
(2)O 2KClO 2KCl+3O ↑ 分解反应
2 3 2
(3)B D E
(4)①不可以 浓盐酸是液体 ②不可以 反应需要加热
23.(2)①将金属片X、Y分别放入两支试管中,再分别加入稀硫酸(或稀盐酸)2mL(2分)
③在金属活动顺序里,X排在氢前,Y排在氢后(或金属的活动性为X大于Y)(2分)
正确(1分)
(3)银(1分) Fe + 2 AgNO === Fe(NO ) + 2Ag(2分) (4)盐酸(或稀硫酸)(1分)
3 3 2
五、(14分)
24.(6分)(1) 14 (2分)
(2)至少应摄取的蛋白质质量为:14g/16% = 87.5g(2分)
(3)若只摄取白面,摄取量至少为:87.5/10% =875g (2分。其它正确方案也得分)
25. (8分)(1) 3.2 2SO +Ca(OH) ===Ca(HSO )(每空2分)
2 2 3 2
(2) 设1000L废气样品中SO 质量为X。
2
SO + 2H O + I === H SO + 2HI
2 2 2 2 4
64 254
X 2g×0.0254%
(2分) X=1.28×10-4 g (1分)
l000 L废气中SO 的质量为1.28×10-4 g 即O.128 mg/m3,小于0.15 mg/m3,符合国家标准。
2
(1分)
第二部分(共计30分)六、(10分,每小题2分)
26.D 27.AC 28.AD 29.CD 30.D
七、(20分)
31.(6分)
(1)C(1分) Ba(OH) + H SO = BaSO ↓+ 2H O 或写Ba(OH) 与ZnSO 反应(2分)
2 2 4 4 2 2 4
Zn和稀HSO 反应产生H 使I中溶液排到Ⅱ中使液面上升,两溶液混合发生反应生成不
2 4 2
溶于水的BaSO 使溶液变浑浊(2分)
4
(2)B (1分)
32.(14分)
[方案一]
(1)将注射器活塞拉出一定距离,一段时间后松开活塞,活塞能回到原位则不漏气(2分)
(2)偏小 CO 能溶于水且与水反应 将广口瓶中的水改为饱和的CO 水溶液(或在水
2 2
面上覆盖一层植物油) 没有 (4分。每空1分)
(3)①产生的CO 气体中混有水蒸气,同时被碱石灰吸收 导致结果偏大
2
②反应结束后装置内残留的CO 气体不能全部排出 导致结果偏小
2
③球形干燥管与空气相通,也会吸收空气中的CO 和水蒸气,导致结果偏大
2
(4分。每空1分。答其中两点或其他合理答案均可)
[方案二]
(1)过滤 (1分)
(2)静置,向上层清液中继续滴加CaCl 溶液,若无沉淀说明CaCl 溶液已过量(2分)
2 2
(3)沉淀未洗涤干净(或沉淀干燥不充分)(1分)