文档内容
湖南省南县2008年学科知识竞赛初赛试题
九 年 级 化 学
时量:120分钟 总分:100分
注意:①本试卷分为第Ⅰ卷和第Ⅱ卷两卷,第Ⅰ卷的答案必须填在第Ⅱ卷的指定答案栏内,
考试结束后,只交第Ⅱ卷
②本试卷可能需要的相对原子质量:H(1)、O(16)、Mg(24)、N(14)、Cu(64)、S(16)
第Ⅰ卷(选择题,共 50 分)
一、选择题(每题只有一个选项符合题意,每题2分,共20分
1.现代医学证明,人类牙齿由一层称为碱式磷酸钙的坚硬物质保护着。碱式磷酸钙的化学
式中除钙离子外,还含有一个氢氧根离子和三个磷酸根离子,则其化学式正确的是
A.Ca (PO )(OH) B.Ca (PO )(OH)
2 4 3 3 4 3
C.Ca (PO )(OH) D.Ca (PO )(OH)
4 4 3 5 4 3
2.某星期天,小明同学回家发现自家田里的小麦出现大面积倒伏现象,就向其父提出了
一条合理化建议:明年应在小麦生长期增施抗倒伏的化肥。从各类化肥的性能来看,你认为
应该施用的化肥是
A.NH NO B.CO(NH) C.Ca(HPO ) D.(NH )SO
4 3 2 2 2 4 2 4 2 4
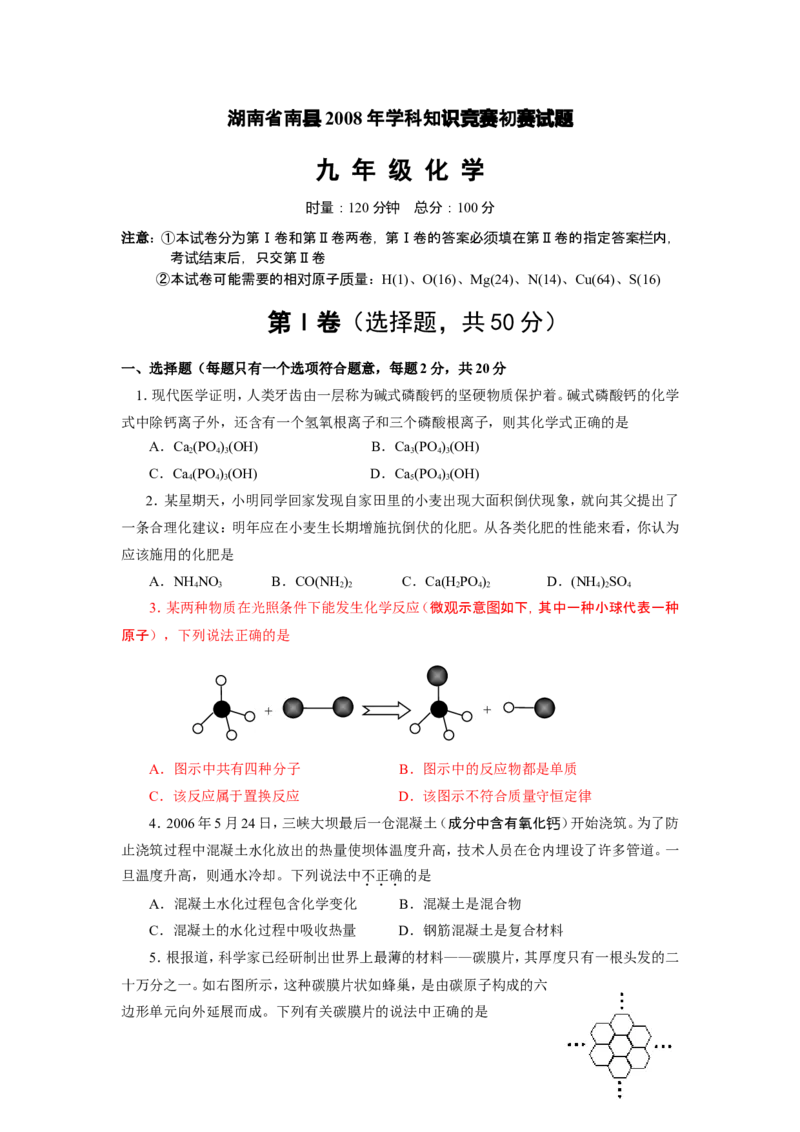
3.某两种物质在光照条件下能发生化学反应(微观示意图如下,其中一种小球代表一种
原子),下列说法正确的是
+ +
A.图示中共有四种分子 B.图示中的反应物都是单质
C.该反应属于置换反应 D.该图示不符合质量守恒定律
4.2006年5月24日,三峡大坝最后一仓混凝土(成分中含有氧化钙)开始浇筑。为了防
止浇筑过程中混凝土水化放出的热量使坝体温度升高,技术人员在仓内埋设了许多管道。一
旦温度升高,则通水冷却。下列说法中不正确的是
A.混凝土水化过程包含化学变化 B.混凝土是混合物
C.混凝土的水化过程中吸收热量 D.钢筋混凝土是复合材料
5.根报道,科学家已经研制出世界上最薄的材料——碳膜片,其厚度只有一根头发的二
十万分之一。如右图所示,这种碳膜片状如蜂巢,是由碳原子构成的六
边形单元向外延展而成。下列有关碳膜片的说法中正确的是A.碳膜片属于单质
B.碳膜片与C 是同一种物质
60
C.碳膜片属于人工合成的有机高分子材料
D.碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同
6.近段时间,我国猪内价格上涨幅度已超过50%,猪肉价格的不断上涨对国民的生活带
来了一定的负面影响。猪肉的新鲜度可以通过测试pH来判断。有资料显示,pH与肉类新鲜
度的关系为:
名称 新鲜肉 次鲜肉 变质肉
pH 5.8~6.2 6.3~6.6 >6.7
新鲜肉在变质过程中酸性强弱的变化为
A.变强 B.变弱 C.不变 D.无法确定
7.珍珠是一种名贵的中药材,其主要成分是一种含钙的化合物。把盐酸滴在珍珠粉上,
产生大量气泡。若将生成的气体通入澄清的石灰水,澄清的石灰水变浑浊。据此推断,珍珠的
主要成分可能是
A.KCO B.Ca(OH) C.CaCO D.Ca(NO )
2 3 2 3 3 2
8.科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型为,其中每个
代表一个碳原子,每个 代表一个氢原子。下列说法中不正确的是
A.该分子的分子式为C H
4 5
B.该分子中碳元素的质量分数是93.75%
C.该分子中的氢原子与碳原子的个数比是4:5
D.等质量的该物质与甲烷相比,燃烧时消耗的氧气更多
9.有一溶液是由HCl、HSO 、Fe (SO ) 、FeCl 、HNO 、
2 4 2 4 3 3 3
Fe(NO ) 几种中的两种混合而成,向该溶液中加 Ba(OH) 溶液 的
3 3 2
体积与生成沉淀的质量关系如右图所示,则该溶液是
A.HNO、Fe(NO ) B.HSO 、FeCl
3 3 3 2 4 3
C.Fe (SO )、Fe(NO ) D.HCl、Fe (SO )
2 4 3 3 3 2 4 3
10.有质量相等的两份氯酸钾,只向其中一份加入少量二氧化锰,同时放在两只试管内
加热。下列有关放出氧的质量(g)与反应时间(t)的关系图象(图中a是纯氯酸钾的曲线,b是
混有二氧化锰的曲线)中正确的是
A BD C
二、选择题(每题只有一个选项符合题意,每题3分,共30分)11.1952年,美国洛杉矶爆发了光化学烟雾事件。当时,不少老人和儿童眼睛红肿,呼吸
困难;蔬菜由绿色变成黄色,菠菜到了不能吃的地步;橡胶制品失去弹性而龟裂;仅加利福尼
亚,就有190成棵松树爱害,其中30%枯死。下列关于光化学烟雾的形成原因的说法中正确
的是
A.光化学烟雾是由SO 造成的
2
B.光化学烟雾是由汽车排出的NO 和C H 在阳光照射下发生光化学反应造成的
X X Y
C.光化学烟雾是一种自然现象,但可以通过化学方法加以控制
D.光化学烟雾是一种不可抗拒的超自然现象
12.自然界各种水体都有一定的自净能力,这是由水自身的理化特征决定的,同时也是
自然界赋予人类的宝贵财富。水体自净大致可分为三类,即物理净化、化学净化和生物净化。
它们同时发生,相互影响,共同作用。下列净化过程属于化学净化的是
A.可沉性固体在水流紊动较弱的地方逐渐沉入水底,形成污泥
B.流动的水体从水面上大气中溶于氧气,使污染物中的某些物质氧化,形成沉淀
C.水中一部分有机物消耗于腐生微生物的繁殖,转化为细菌有机体
D.悬浮体、胶体和溶解性污染物因混合、稀释,浓度逐渐降低
13.CO 就像温室的玻璃一样,并不影响太阳对地球表面的辐射,但却能阻碍由地面反射
2
回高空的红外辐射,这就像给地球罩上了一层保温膜,使地球表面气温增高,产生“温室效
应”。能产生“温室效应”的气体当然不只有CO 一种,请你指出下列气体中不可能产生
2
“温室效应”的是
A.O B.CH C.N D.CCl F
3 4 2 3
14.若在宇宙飞船的太空实验室(失重条件下)进行以下实验,其中最难完成的是
A.将金粉和铜粉混合 B.将牛奶加入水中混合
C.将氯化钠晶体溶于水中 D.用漏斗、滤纸过滤除去水中的泥沙
15.两位美国科学家彼得·阿格雷和罗德里克·麦金农,因为发现细胞膜水通道,以及对离
子通道结构和机理研究作出的开创性贡献而获得 2003年诺贝尔化学奖。他们之所以获得诺
贝尔化学奖而不是生理学或医学奖是因为
A.他们的研究和化学物质水有关
B.他们的研究有利于研制针对一些神经系统疾病和心血管疾病的药物
C.他们的研究深入到分子、原子的层次
D.他们的研究深入到细胞的层次
16.当水的温度和压强升高到临界点(£=374.3℃,p=22.05MPa)以上时,水就处于超临界
状态,该状态的水即称之为超临界水。超临界水具有通常状态下水所没有的特殊性质,它可
以和空气、氧气及一些有机物质均匀混合。如果超临界水中同时溶有氧气和有机物,则有机
物可迅速被氧化,生成二氧化碳、氮气、水等。有关超临界水的叙述错误的是
A.超临界水可处理有机废物 B.超临界水是一种新物质
C.超临界水是水的一种状态 D.超临界水氧化技术不形成二次污染17.镁在空气中燃烧不仅生成氧化镁,还有少量的镁与氮气化合生成氮化镁(3Mg+N
2
MgN)。由此推知 6 g镁在空气中完全燃烧后所得产物的质量可能是
3 2
A.8.3 g B.9.7 g C.10 g D.10.3 g
18.将镁粉放入瓷坩埚(主要成分之一为SiO)中充分加热,使其完全反应。取出生成的
2
氧化镁,然后用盐酸清洗坩埚,这时常会出现着火燃烧的现象。研究证实是SiH 发生自燃。下
4
列反应中与此着火燃烧无关的是
A.SiO+ 4Mg 2MgO+MgSi B.MgSi十4HCl=2MgCl 十SiH↑
2 2 2 2 4
C.2Mg+O 2MgO D.SiH+2O=SiO 十2HO
2 4 2 2 2
19.为了使经济可持续发展,生产过程应尽量减少对环境的负面作用。由单质铜制取硫
酸铜有下列几种步骤,其中可行且符合以上要求的是
A.Cu→CuSO
4
B.Cu→CuO→CuSO
4
C.Cu→Cu (OH)CO→CuSO
2 2 3 4
D.Cu→Cu(NO )→Cu(OH)→CuSO
3 2 2 4
20.测得某溶液中仅含有 Na+ 、Mg2+、SO 2-、Cl-四种离子,其中离子个数比为
4
Na+∶Mg2+∶Cl-=4∶5∶8,若没Na+为4n个,则SO 2-离子个数可能是
4
A.2n B.3n
C.6n D.8n
南县2008年学科知识竞赛初赛试题
九 年 级 化 学
一 二 三 四 五 总分
请将第Ⅰ卷答案填在下面的空格中
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
第Ⅱ卷(非选择题,共 50 分)
得分 评卷人
三、填空题(每空2分,共24分)
21.下表数据是在某温度下,金属镁和镍(Ni)分别在氧气中进行氧化反
应时,在金属表面生成氧化薄膜的实验记录:
反应时间/h 1 4 9 16 25MgO层厚/nm 0.005a 0.02a 0.45a 0.80a 1.25a
NiO层厚/nm b 2b 3b 4b 5b
注:a和b均为与温度有关的常数,nm表示“纳米”
请回答;Mg与Ni比较,哪一种更易氧化?其理由是____________________________
_______________________________________________________________。
22.地球的外层空间存在微量的臭氧和氧原子(称为“臭氧层”),“臭氧层”能吸收和
阻挡太阳有害的紫外线的强烈辐射。可是人为的大气污染物会破坏“臭氧层”,如超音速飞
机排放的氮氧化物(NO和NO ),它们和O 及O发生如下反应:O + NO = NO + O ;O +
2 3 3 2 2
NO = NO + O ;这两个反应反复循环,其总反应方程式为: _
2 2
___________________________________________。氮的氧化物在破坏臭氧层的过程中起了
_______________作用。
23.磷酸二氢铵是一种含有氮、磷两种营养元素的复合肥,熟石灰常可用来中和土壤的
酸性,但是这两种物质不宜混合使用,试写出有关反应的化学方程式 __
______________________ _____ ,并说明原因 ______________________________ _
_____________________________________________________________。
24.吸烟有害健康,科学实验表明香烟所产生的烟雾中,至少有300多种化合物不同程
度的对人体有害。为了检验该烟雾中是否存在CO 和CO,某实验小组对香烟燃烧产生的烟
2
雾进行适当处理后,依次通过足量的以下试剂(假设每次吸收都是完全的):①澄清石灰水,
②浓硫酸,③灼热的黑色氧化铜粉末,④澄清石灰水,发现①④变浑浊。试回答:
(1)①中发生的现象说明 _ 。
(2)烟雾中是否存在CO? ,做出此判断依据的实验现象为
____________________________________________________________________________。
25.为防止大气污染,工业上产生的硫化氢(HS)要经过处理,使其变成硫单质。富玛克
2
斯法治理硫化氢的方法和步骤如下:
① 用2%~3%的NaCO 溶液作吸收剂生成两种酸式盐,其中一种为NaHS;
2 3
② 再加入一种RNO(液)(R表示一种有机基团)与生成的这种酸式盐的水溶液反应生
成硫、碱和RNHOH;
③ 第二步生成的碱在溶液中与另一种酸式盐反应生成正盐;
④ RNHOH与空气中的氧发生反应又得到RNO。
写出上述四步反应的化学方程式。
①;
② ;
③ ;
④
。
得分 评卷人
四、实验题(每空2分,共18分)
26.现在许多食品都采用密封包装,但包装袋中的空气、水蒸气仍会使食
品氧化、受潮变质,因此一些食品包装袋中需放入一些脱氧剂,以使食品保质期更长一些。甲、
乙、丙三同学为了探究“脱氧剂”的成分,从某食品厂的月饼包装袋中取出“脱氧剂”一袋,
打开封口,将其倒在滤纸上,仔细观察,脱氧剂为灰黑色粉末,还有少量的红色粉末。
[提出问题]:该脱氧剂中的黑色、红色粉末各是什么?
[作出猜想]:甲同学认为:灰黑色粉末可能是氧化铜、红色粉末可能是铜。
乙同学认为:灰黑色粉末可能是铁粉,也可能还有少量的活性炭粉;红
色物质是氧化铁。
丙同学认为:灰黑色物质可能是氧化铜、活性炭粉,红色粉末可能是铜。
(1)你认为 同学的猜想正确,其理由是:
。
(2)设计一个实验方案来验证该同学的猜想是正确的。请填写以下实验报告:
实验步骤 预期的实验现象 结 论
②
绝大部分黑色物质被吸引
②将红色物质放入小试管中,加
入足量稀硫酸观察现象。继续滴
加NaOH溶液并观察现象。
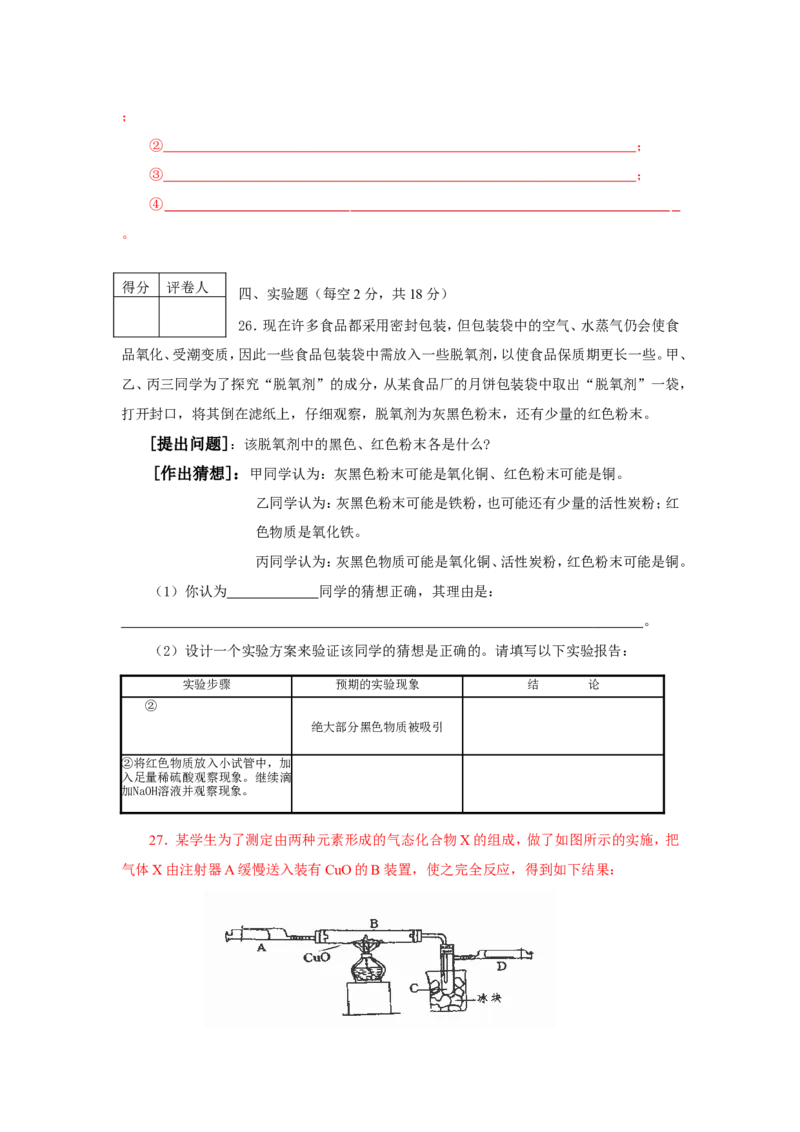
27.某学生为了测定由两种元素形成的气态化合物X的组成,做了如图所示的实施,把
气体X由注射器A缓慢送入装有CuO的B装置,使之完全反应,得到如下结果:实验前B管及药品的质量为21.32克,实验后为21.16克
① C管中收集到的物质电解后可得到H 和O,在D中收集到的是N。
2 2 2
② X中两元素的质量比是14:3。问:
(1)C中收集到的液体,质量是 克。
(2)在实验中看到的现象是 。
(3)B中反应的化学方程式是 。
得分 评卷人
五、计算题(共8分)
28.某同学用一定质量分数的稀硫酸做“氧化铜+硫酸→硫酸铜+水”的
实验,
其五次实验的结果如下表所示:
实验次数 氧化铜/g 硫酸溶液/g 硫酸铜/g
1 2.0 120 4.0
2 4.0 120 8.0
3 6.0 120 9.6
4 8.0 200 16.0
5 10.0 200 X
根据实验结果填写下列空格:
(l)哪几次反应氧化铜有剩余;
(2)哪几次反应硫酸有剩余;
(3)表中X的值是;
(4)硫酸溶液中溶质的质量分数为。南县2008年学科知识竞赛初赛试题
参考答案及平分标准
一、选择题(每题2分,共20分)
1 2 3 4 5 6 7 8 9 10
D C A C A B C A A C
二、选择题(每题3分,共30分)
11 12 13 14 15 16 17 18 19 20
B B C D C B B C B B
三、填空题(每空2分,共24分)
21.Mg比Ni更容易被氧化(1分),因为在相同的反应时间内,生成的MgO层总是比生成的
NiO层更厚(1分)
22.O + O = 2O (未写催化扣分) 催化
3 2
23.2Ca(OH) + Ca(HPO ) = Ca (PO )↓+ 4HO 生成的Ca (PO ) 不溶于水,不
2 2 4 2 3 4 2 2 3 4 2
便于作物的吸收
24.(1)香烟产生的烟雾中含有CO
2
(2)存在 ③中黑色固体变成红色(1分),④中澄清的石灰水变浑浊(1分)
25.① HS + NaCO = NaHS + NaHCO
2 2 3 3
② RNO + NaHS + HO = S↓+ NaOH + RNHOH(未打↓符号不扣分)
2
③ NaOH + NaHCO = NaCO + HO
3 2 3 2
④ 2RNHOH + O = 2RNO + 2HO
2 2
四、实验题(每空2分,共18分)
26.(1)乙 作为“脱氧剂”,它的主要成分应该是一种能与空气中的O 用水蒸气反
2
应的比较活泼的物质(未答出水蒸气者扣1分)
(2)用一块磁铁接近(或接触)该脱氧剂 灰黑色物质大部分是铁粉
红色物质溶解,得到棕黄色溶液(1分),加NaOH后,生成红褐色沉淀(1分)
脱氧剂中的红色物质是氧化铁
27.(1)0.18
(2)B中黑色固体变红色(1分),C中有无色液体凝结(1分)
(3)2NH + 3CuO 3Cu + 3HO(未写加热符号扣1分)
3 2
五、计算题(每小题2分)共8分)
28.(1)第3次与第5次氧化铜过量
(2)第1次与第2次硫酸有剩余
(3)表中的X值为16.0(未保留一位小数扣1分)
(4)w%=4.9%(没有计算过程扣1分)