文档内容
第三单元 物质构成的奥秘
知能优化训练
中考回顾
1.(2017山东枣庄中考)下列关于“酒精温度计遇热读数上升”的微观解释正确的是( )
A.分子质量增大
B.分子体积扩大
C.分子间距变大
D.分子个数增多
答案:C
2.(2017广州中考)下图是元素X的一种粒子结构示意图,下列说法正确的是( )
+11
A.X是非金属元素
B.X的最外层电子数为8
C.该粒子最外层电子层已达到相对稳定结构
D.该粒子可表示为X-
答案:C
3.(2017山东青岛中考)下列关于宏观事实的微观解释中,错误的是( )
A.自然界中水的天然循环——水分子不断运动
B.天然气经压缩储存在钢瓶中——压强增大,分子之间的间隔变大
C.电解水生成氢气和氧气——在化学反应中分子发生改变
D.通过气味辨别酒精和水——分子不断运动,不同分子的性质不同
答案:B
4.(2017湖南邵阳中考)下图中“ ”和“ ”分别表示氢原子和氮原子,能保持氨气化学性质
的微粒是( )
答案:A
5.(2017江苏连云港中考)下图是元素周期表的一部分。下列说法正确的是( )
5 6
B C
硼 碳
[来
源 1 :学科 0 网ZX . XK 8 ] 12.0
1 1
13Al
铝
26.9
8
A.硼为金属元素
B.碳的原子序数是12.01
C.铝是地壳中含量最高的元素
D.三种原子中质量最大的是铝
答案:D
6.(2017四川内江中考)下列有关说法错误的是( )
A.水的三态变化说明分子间具有间隙
B.原子不显电性是因为原子中质子数与中子数相等
C.五个二氧化硫分子可表示为5SO
2
D.Al3+可表示一个铝离子带三个单位的正电荷
答案:B
7.(2017山东潍坊中考)下列说法正确的是( )
A.同种元素可能组成性质不同的几种单质
B.物质都是由分子或原子构成的
C.核电荷数:S2->S
[来源:学科网]
D.在原子中质子数一定等于中子数
答案:A
8.(2017成都中考)下图是X、Y两种微粒的结构示意图。下列说法正确的是( )
A.X为原子,Y为离子
B.X、Y均属于非金属元素
C.X在反应中可失去6个电子
D.X与Y形成化合物的化学式为YX
答案:D
9.(2017重庆中考B卷)下图是某品牌矿泉水的标签,回答下列问题。
每100 mL含量(μg)
钙 ≥400
镁 ≥50
钾 ≥20
偏硅酸 ≥180
(1)钙、镁和钾等指的是 (填序号)。
A.分子 B.原子 C.元素
(2)已知镁原子的结构示意图为 +12 ,则Mg2+的质子数为 。
(3)已知偏硅酸的化学式为HSiO,则偏硅酸钙的化学式为 。
2 3答案:(1)C (2)12 (3)CaSiO
3
10.(2017天津中考)根据下列粒子结构示意图,回答问题。
(1)A、B、C、D所示粒子共表示 种元素(填数字)。
(2)D所示粒子在化学反应中容易 电子(填“得到”或“失去”)。
(3)若E中x=10时,则该粒子属于 (填“原子”或“离子”)。
答案:(1)3 (2)得到 (3)原子
模拟预测
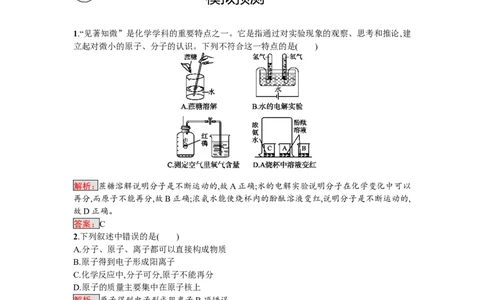
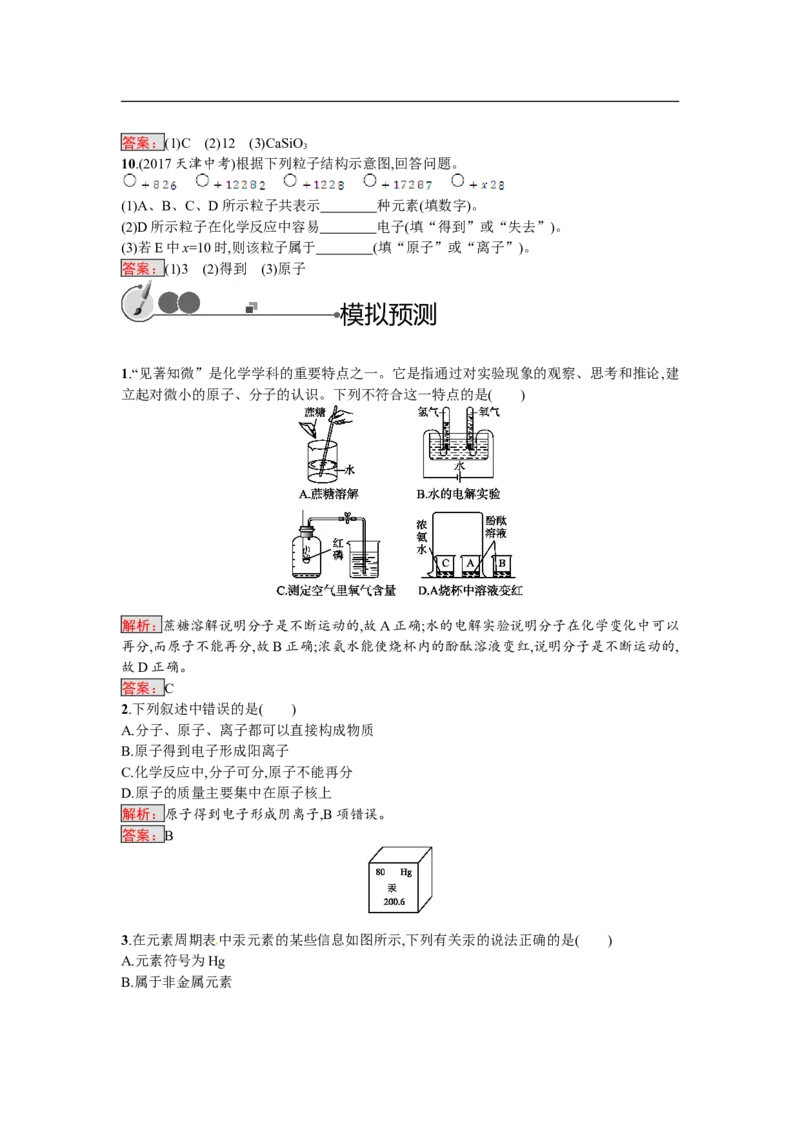
1.“见著知微”是化学学科的重要特点之一。它是指通过对实验现象的观察、思考和推论,建
立起对微小的原子、分子的认识。下列不符合这一特点的是( )
解析:蔗糖溶解说明分子是不断运动的,故A正确;水的电解实验说明分子在化学变化中可以
再分,而原子不能再分,故B正确;浓氨水能使烧杯内的酚酞溶液变红,说明分子是不断运动的,
故D正确。
[来源:学+科+网]
答案:C
2.下列叙述中错误的是( )
A.分子、原子、离子都可以直接构成物质
B.原子得到电子形成阳离子
C.化学反应中,分子可分,原子不能再分
D.原子的质量主要集中在原子核上
解析:原子得到电子形成阴离子,B项错误。
答案:B
3.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是( )
A.元素符号为Hg
B.属于非金属元素C.原子核内中子数为80
D.相对原子质量是200.6 g
解析:在周期表中的每个单元格中左上角表示的是质子数,右上角表示的是元素符号,中间是
元素名称,下面表示的是相对原子质量;汞是唯一不带“钅”字旁的金属元素。
答案:A
4.下列有关粒子结构示意图的说法正确的是( )
① +2 ② +12 ③ +11 ④ +10 ⑤ +16 ⑥ +8
A.③和④在元素周期表中属于同一族,⑤和⑥属于同一周期
B.⑤和⑥的化学性质相似,①和②属于同一种元素
C.②和⑥可以以离子的形式形成化合物
D.②③④是具有稳定结构的原子
解析:③的原子最外层电子数为1,④的原子最外层电子数为8,因此它们在元素周期表中不
属于同一族,⑤和⑥的电子层数不同,因此不属于同一周期,A项错误;核内质子数决定元素的
种类,①和②核内质子数不同,因此它们不属于同一种元素,B项错误;③中核内质子数多于核
外电子数,是阳离子不是原子,D项错误。
答案:C
5.已知钠离子(Na+)与氖原子(Ne)核外都有10个电子,下列说法正确的是( )
A.Na+与Ne核内质子数一定相同
B.Na+与Ne核内中子数一定相同
C.Na+与Ne一定属于同种元素
D.Na+与Ne核电荷数一定不同
解析:Na+带一个单位的正电荷,核外有10个电子,说明钠原子的核外有11个电子;又知,在原
子中,核电荷数=质子数=核外电子数,则钠原子的核内质子数与核电荷数均为11,则Na+的核
内质子数与核电荷数也均为11。而氖原子为原子,其核电荷数等于核内质子数等于核外电子
数,均为10。故A、C选项错,D选项对。由于核外电子数与核内中子数没有必然相等的联系,故
B选项错。
答案:D
6.下列有关符号中的数字“2”的意义,叙述正确的是( )
A.O 中的“2”表示2个氧原子
2
B.2Fe中的“2”表示2个铁原子
C.3HO中的“2”表示一个氢分子中含有2个氢原子
2
D.2N中的“2”表示2个氮分子
解析:A选项中的“2”,在化学式中元素符号的右下角,表示一个O 分子中含有两个氧原子,
2
故选项错;B选项中的“2”在元素符号的前面,表示原子的个数,故选项正确;C选项中的“2”
表示一个水分子中含两个氢原子,故选项错;D中的“2”在元素符号的前面,应表示原子的个
数,而不是分子的个数,故选项错。
答案:B
7.化学用语是学习化学的主要工具,是国际通用的化学语言。
(1)请你用化学用语填空。
①氩气 。②某气体在空气中占78%(体积百分含量),保持它的化学性质的最小粒子是 。
③地壳中含量最多的金属元素形成的离子 。
④标出氧化铁中铁元素的化合价 。
(2)请你试着写出两种带有数字“2”的粒子符号并指出其含义:
[来源:学+科+网]
① ; ;
② ; 。
解析:(1)空气中占78%的气体为氮气,保持其化学性质的最小粒子为氮气分子(N );地壳中含
2
量最多的金属是Al,它易失去电子形成Al3+;在三氧化二铁中设铁的化合价为 x,则有2x+
(-2)×3=0,x=+3。
答案:(1)①Ar ②N ③Al3+ ④ O
2 3
(2)2NH 2个氨气分子 HO 1个水分子中含有2个氢原子(凡合理答案:均可)
3 2
8.下图中A、B、C、D是四种粒子的结构示意图,E是银元素在元素周期表中的信息。
A. +13 B. +13
C. +17 D. +18
E.
请回答下列问题:
(1)图中A、B、C、D粒子共表示 种元素。
(2)D中x= 。
(3)E中银元素原子的质子数为 ,一个银原子质量是一个碳12原子质量的 倍。
解析:(1)具有相同核内质子数的原子属于同种元素,图中A、B、C、D分别表示核内质子数为
13、17、18的三种元素。(2)D是18号元素氩,核内质子数等于核外电子数,故x=8。(3)从图中看
出,银的核内质子数为47,相对原子质量为108,根据相对原子质量的含义,一个银原子的质量
是一个碳12原子质量的 =9倍。
答案:(1)3 (2)8 (3)47 9
9.下表列出了1~18号元素的原子序数和元素符号:
原
子
1 2 3 4 5 6 7 8 9
序
数
元
素 H B
H Li B C N OF
符 e e
号
原
子1011 12131415161718
序数
元
素N N M A
AlSiP S Cl
符e a g r
号
请回答下列问题:
(1)1~18号元素中属于稀有气体元素的有He、Ne、 (填元素符号)。
(2)1~18号元素中最外层有2个电子的原子有 、Be、Mg(填元素符号)。
(3)某元素的原子结构示意图为 +17 ,它在化学反应中一般易 (填“得到”或
“失去”)电子,它与地壳中含量最多的金属元素形成化合物的化学式为 。
(4)某粒子的结构示意图为 +x ,当x-y=8时,该粒子为 。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下
列各组粒子中属于等电子体的是 (填字母序号)。
A.NO和O B.CO和N
2 2[来源:学_科_网]
C.SO 和CO D.P 和S
2 2
解析:(3)17号元素为Cl,地壳中含量最多的金属元素是Al,二者形成的化合物为AlCl 。
3
(4)从结构示意图可知,电子数=10+y;从“x-y=8”可知,质子数x=8+y,质子数≠电子数,因
此该粒子为离子。离子最外层一般为8电子的稳定结构,所以y=8,x=16。
(5)判断等电子体,注意把握题目的信息“具有相同原子数和电子数的分子或离子叫等电
子体”。以上各选项中的两种分子或离子所含的原子数都相同,所含电子数是分子中原子所含
电子数的和,离子所带电子数还要考虑所带电荷数,即得失电子数。A中NO分子含7+8=15个
电子,而O 分子中含电子数为8×2=16个;B中,CO分子含电子数为6+8=14,N 分子含电子数
2 2
为7×2=14;C中,SO 分子所含电子数为16+8×2=32,CO 分子所含电子数为12+8×2=28;D中,P
2 2
所含电子数为15+8×4+3=50,S 所含电子数为16+8×4+2=50。故只有B、D正确。
答案:(1)Ar (2)He (3)得到 AlCl (4)S2-
3
(5)BD
10.元素周期表是学习和研究化学的重要工具。回答下列问题:
(1)元素周期表中不同元素间最本质的区别是 (填字母)。
A.质子数不同
B.中子数不同
C.相对原子质量不同
(2)1869年, (填字母)发现了元素周期律并编制出元素周期表。
A.张青莲
B.门捷列夫
C.拉瓦锡(3)元素周期表中氟元素的有关信息如图所示,下列说法正确的是 (填字母)。
A.氟属于金属元素
B.氟的原子序数是9
C.氟的相对原子质量是19.00 g
(4)氟原子结构示意图为 +9 ,氟原子在化学反应中易 (填“得到”或“失去”)电
子,由钠元素和氟元素组成的化合物氟化钠的化学式为 。
解析:(1)元素的种类是由质子数决定的,因此不同元素间最本质的区别是质子数不同;(2)1869
年,门捷列夫发现了元素周期律并编制出元素周期表;(3)氟字中含有“气”字头,因此它属于
非金属元素,故A错误;由元素周期表中氟元素的有关信息可知,氟的原子序数是9,故B正确;
相对原子质量的单位是“1”,常省略不写,故C错误;(4)氟原子最外层电子数为7,大于4,故在
化学反应中易得到1个电子,显-1价,钠元素为+1价,根据化合物中各元素的化合价的代数和
为零可知,钠元素和氟元素组成的化合物氟化钠的化学式为NaF。
答案:(1)A
(2)B
(3)B
(4)得到 NaF