文档内容
2018 年中考化学一轮复习·《化学计算》真题练习
一、填空题
1.(2017四川省内江市)一种新型环保材料被塑胶跑道工程广泛应用,合成
这种新材料的原料是二甲苯烷二异氰酸酯(其分子式为 C H N O )。请回答下
15 10 2 2
列问题:
(1)二甲苯烷二异氰酸酯(C H N O )中氢、氧元素的质量比为___________
15 10 2 2
(填最简整数比)。
(2)二甲苯烷二异氰酸酯(C H N O )的相对分子质量为_________。
15 10 2 2
(3)500g二甲苯烷二异氰酸酯中含氮元素的质量为____________g。
【答案】(1)5:16 (2)250 (3)56
【解析】本题考查根据化学式的计算。
( 1 ) 二 甲 苯 烷 二 异 氰 酸 酯 ( C H N O ) 中 氢 、 氧 元 素 的 质 量 比
15 10 2 2
=1×10:16×2=5:16;
( 2 ) 二 甲 苯 烷 二 异 氰 酸 酯 ( C H N O ) 的 相 对 分 子 质 量
15 10 2 2
=12×15+1×10+14×2+16×2=250;
(3)500g二甲苯烷二异氰酸酯中含氮元素的质量=500g×14×2/250=56g。
2.(2017湖南省郴州市)2017年5月18日至22日,第五届中国(湖南)国际
矿物宝石博览会在郴州成功举行。这场亚洲最大的矿物宝石博览会以“神夺的
矿晶,多彩的萤石”为主题,向世界充分展示了“矿晶之都,多彩郴州”的独
特魅力。萤石的主要成分是CaF ,试计算:
2
(1)CaF 的相对分子质量是 ;
2
(2)CaF 中钙元素和氟元素的质量比为 ;
2
(3)CaF 中氟元素的质量分数为 (结果精确到0.1%)。
2
【答案】(1)78;(1分)
(2)20:19;(1分)
(3)48.7%。(2分)
【解析】本题考查相对分子质量的概念及其计算;元素质量比的计算;元素质
量分数的计算。(1)CaF 的相对分子质量是40+19×2=78;
2
(2)CaF 中钙元素和氟元素的质量比为40:19×2=20:19;
2
192
(3)CaF 中氟元素的质量分数为 78 ×100%=48.7%。
2
3.(2017四川省自贡市) 我国科学家屠呦呦发现并提纯抗疟疾药物青蒿素
(C H O )荣获2015年诺贝尔奖,请计算青蒿素中碳、氢、氧元素的质量比
15 22 5
为____________。
【答案】96:11:40
【解析】本题是考查化学式计算的知识;青蒿素中碳、氢、氧元素的质量比为:
12×16:1×22:16×5=96:11:40。
4.(2017新疆) 每年的6-7月,新疆的许多地区都要举办“薰衣草”节。薰
衣草精油的主要成分为芳樟醇、伽罗木醇等物质。其中芳樟醇的化学式
C H O,请计算:
10 18
(1)芳樟醇分中的原子个数比为__________。
(2)芳樟醇的相对分子质量是(154),计算该物质组成中氧元素的质量分数
为__________(精确到0.1%)。
【答案】(1)10:18:1 (2)10.4%
【解析】本题属于化学式的计算题,考查了根据化学式计算分子中各原子的个
数比和化合物中某元素质量分数的计算。
(1)从芳樟醇的化学式:C H O 可以看出芳樟醇中 C、H、O 原子的个数比
10 18
=10:18:1。
16
(2)根据芳樟醇的化学式:C H O 可知,芳樟醇中氧元素的质量分数=154
10 18
×100%=10.4%。
5. (2017山东济宁市)观看足球比赛时,经常会看到绿茵场上运动员因拼抢
摔倒受伤,医生向受伤部位喷射氯乙烷(CH CH Cl),并用药棉不断揉搓,运动
3 2
员疼痛很快消除,重新投入比赛.
请阅读信息后,回答:
(1)氯乙烷中C、H、Cl三种元素的原子个数比为_________;
(2)氯乙烷中C、H、Cl三种元素的质量比为___________.【答案】(1)2:5:1;(2)48:10:71
【解析】本题考查的是化学式的计算。(1)化学式中元素符号右下角的数字表
示一个分子中的原子个数,由化学式可知,1个氯乙烷分子是由2个碳原子、5
个氢原子和1个氯原子构成的,则氯乙烷中C、H、Cl三种元素的原子个数比为
2:5:1;
(2)物质中元素的质量比等于相对原子质量和原子个数的乘积之比,氯乙烷中
碳、氢、氯三种元素的质量比为(12×2):(1×5):(35.5×1)=48:
10:71。
6.(2017年山东省泰安市)“舌尖上的中国”在央视上的热播让厨房再次成为
人们施展厨艺的舞台,大多数厨师有个工作经验;炒菜时,又加料又加醋,可
使菜变得香美可口,原因是醋中的乙酸与料酒中的乙醇生成乙酸乙酯。下表中
是几种常见的脂,请完成下列各题:
(1)甲酸甲酯(C H O )中碳元素、氢元素、氧元素的质量比为__________;
2 4 2
(2)甲酸乙酯(C H O )中碳元素的质量分数为______________(计算结果精
3 6 2
确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X的化学式为_________。
【答案】(1)6:1:8;
(2)48.6%;
(3)C H O
4 8 2
【解析】(1)化合物中元素质量比等于元素的相对原子质量×原子个数之比,
所以,甲酸甲酯中 C、H、O 三种元素的质量比为:(12×2):(1×4):
(16×2)=6:1:8;
12�3
椿100% 48.6%
12�3�1�6 16 2
(2)甲酸乙酯中碳元素的质量分数为: ;
(3)由表中化学式可知,脂分子中C和H的原子个数比均为1:2,且每个脂分
子中均含有2个O原子,每个乙酸乙酯分子中的碳原子数是4,则氢原子数为
8,氧原子数为2,由此乙酸乙酯的化学式为:C H O 。
4 8 27、(2017黑龙江省齐齐哈尔市)学生体育测试后,常会感到肌肉酸痛,这是
因为运动后产生了乳酸的原因。乳酸的化学式为C H O ,请回答:
3 6 3
(1)乳酸属于________化合物(填“有机”或“无机”)
(2)乳酸的相对分子质量是_______________。
(3)乳酸中碳、氢、氧三种元素的质量比是______________________。
(4)180g乳酸中含碳元素_____________g。
【答案】(1)有机(2)90(3)6:1:8(4)72
【解析】此题主要考查化学式的有关计算;
(1) 乳酸的化学式为C H O ,是含碳的化合物,属于有机物化合物;
3 6 3
(2) C H O 相对分质量等于各相对原子质量的总和=12×3+1x6+16x3=90;
3 6 3
(3) 化学式中物质的质量比等相对原子质量乘以原子个数的比, C H O ,中
3 6 3
C:H:O=(12×3):(1x6):(16x3)=6:1:8;
(4)物质中某元素的质量,等于该物质的质量乘以该元素的质量分数=180g×
(12÷90)=72g
8. (2017甘肃省庆阳市)今年年初,科学家利用显微镜针头手工“敲打”原
子,首次成功合成能稳定存在4天之久的三角烯分子。三角烯(化学式为
C H )将在量子计算、量子信息处理和自旋电子学等领域展现巨大应用潜力。
22 14
请计算:[来源:学科网]
(1)C H 中碳氢元素的质量比为_______。
22 14
(2)C H 中碳元素的质量分数为______(计算结果精确到0.01%)。
22 14
【答案】(1)132:7(1分) (2)94.96%(2分)
【解析】此题主要考查的是化学式的意义和计算。(1)根据化学式C H ,可
22 14
以得出三角烯中碳氢元素的质量比为12×22:1×14=132:7。(2)C H 中碳元
22 14
碳元素的相对原子质量原子个数
三角烯的相对分子质量
素的质量分数为: ×100%=
1222
100%94.96%
1222114 。9. (2017年湖南省株州市)若1个A原子的质量为akg,1个碳12原子(含
有6个质子和6个中子的碳原子)的质量为bkg。请计算:
(1)A原子的相对原子质量为________。
(2)1个碳12原子的核外电子数为_________。
12a
【答案】(1) b ;(2)6。
【解析】此题主要考查原子的相关知识。(1)因为 Ar(原子)=
aKg
m(某原子)
1 12a
bKg
m(某碳原子)1/12
;所以A原子的相对原子质量= 12 = b ;(2)1个碳12
原子(含有6个质子和6个中子的碳原子),在原子中质子数等于核外电子数,
故核外电子数为6.。
10.(2017黑龙江省龙东地区,题号33,分值3)炒菜时加入料酒和食醋,炒
出的菜別具香味,其原因之一是料酒中的乙醇与食醋中的乙酸反应生成乙
酸乙酯(C H O ),试计算:
4 8 2
(1)乙酸乙酯的相对分子质量为_________;
(2)乙酸乙酯中碳、氢元素的质量比为___________;(答最简整数比)
⑶17.6 g乙酸乙酯中所含氧元素的质量为_______g。
【答案】(1) 88(1分) (2) 6:1 (1分) (3)6.4(1分)
【解析】(1)乙酸乙酯的相对分子质量=12×4+8+16×2=88; (2)乙酸乙酯中碳、
氢元素的质量比=12×4:8= 6:1;⑶17.6 g乙酸乙酯中所含氧元素的质量=17.
162
100% 6.4g
6g× 88 。
11.(2017甘肃省兰州市)中国是把香椿当做蔬菜的唯一国家,它不仅营养丰
富,而且具有极高的药用价值,如香椿中含有的皂甙,具有抗菌、防癌的作用,
皂甙的化学式为C H O ,请你计算:
27 42 3
(1)皂甙属于_______________(填“有机物”或“无机物”);
(2)皂甙中各元素的质量之比是____________________(最简整数比);
(3)含氢元素8.4 g的皂甙的质盆为________________克(写出计算过程)
【答案】(1)有机物(1分) (2)54:7:8(1分) (3) 8.4÷42×1
27×12+42×1+3×16=82.8(2分)
【解析】(1)皂甙的化学式为C H O ,含有碳、氢、氧三种元素且不属于碳
27 42 3
酸及碳酸盐类物质,因此属于有机物;
(2)根据皂甙的化学式 C H O 可知,其组成碳、氢、氧的质量比为
27 42 3
(27×12):(4×1):(3×16)=54:7:8;
42×1
(3)皂甙中氢元素的质量分数为 27×12+42×1+3×16 ,含氢元素8.4g的皂
42×1
甙质量为8.4÷27×12+42×1+3×16=82.8g.
12.(2017年甘肃省天水市)青少年过多摄人蛋糕里的人造奶油会产生一种影
响身体发育的反式脂肪酸,其化学式为C H O ,请计算。
18 34 2
(1)该反式脂肪酸中碳、氧元素的质量比________。
(2)141g该反式脂肪酸中含氢元素的质量为_________g。
【答案】(1)27:4(1分)
(2)17g(1分)
【解析】本题考查化学式的简单计算
(1)该反式脂肪酸的化学式为:C H O ,故该反式脂肪酸中碳、氧元素的质量
18 34 2
比=12×18:(16×2)=27:4
(2)该该反式脂肪酸的化学式为:C H O 反式脂肪酸中含氢元素的质量分数
18 34 2,
34
为: 282 ×100%,根据物质中元素的质量=物质质量×元素质量分数可得 141g
34
该反式脂肪酸中含氢元素的质量为141g×282 ×10 0%=17g
二、计算题1.(2017甘肃)某化学兴趣小组同学为回收一块质量为40 g的铜锌合金中的铜,
将该合金放人烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫
酸100 g,烧杯内剩余固体27 g。请完成下列计算:
(1)40 g铜锌合金中锌的质量是________g 。
(2)计算所用稀硫酸中溶质的质量分数。
【答案】(1)40 g铜锌合金中锌的质量为40 g-27 g=13 g
(2)解:设所用稀硫酸中溶质的质量为x。
Zn+H SO ═ZnSO +H ↑
2 4 4 2
65 98
13 g x
65 98
=
13 g x
x=19.6 g
19.6 g
×100%=19.6%
100 g
所用稀硫酸中溶质的质量分数: 。
答:所用稀硫酸中溶质的质量分数是19.6%。
2.(2017河南)将30.9 g 氯酸钾(KClO )和二氧化锰的固体混合物装入试管
3
中,加热制取氧气,同时生成氯化钾。待反应完全后,将试管冷却,称
量,可以得到21.3 g 固体物质。请计算原固体混合物中氯酸钾的质量。
【答案】生成氧气的质量为30.9g-21.3g=9.6g,设原混合物中氯酸钾的质
量为x
2KClO 2KCl+3O ↑
3 2
245 96
x 9.6g
245 x
96 9.6g
= 解得x= 24.5g
3.(2017枣庄)一化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物
质),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的发案,取 100g上
述废液,向其中加入2.8g铁粉,恰好完全反应,测得反应后溶液中溶质的质量
分数为15%,求:
(1)回收得到铜的质量为 g(2)回收得到硫酸亚铁的质量是多少?(写出计算过程)
【答案】解:设2.8g铁完全反应生成的铜的质量为x
Fe+CuSO =FeSO +Cu
4 4
56 64
2.8g x
=
x=3.2g
硫酸亚铁质量为×15%=14.94g
答:(1)回收得到铜的质量为 3.2gg
(2)回收得到硫酸亚铁的质量是14.94g.
4.(2017达州)NaCl和Na CO 的固体混合物与一定质量的稀盐酸恰好完全反应,
2 3
得到4.4gCO 和100g21.1%的NaCl溶液,求:
2
⑴稀盐酸中溶质的质量为 g。
⑵原混合物中NaCl的质量分数(写出计算过程)。
【答案】⑴7.3g ⑵47%
解:设碳酸钠的质量为x,反应生成的氯化钠质量为y,参加反应的盐酸中溶质
质量为z。
Na CO +2HCl=2NaCl+H O+CO ↑
2 3 2 2
106 73 117 44
x z y 4.4g
= = = x=10.6g y=11.7g z=7.3g
原混合物中氯化钠的质量为:100g×21.1%-11.7g =9.4g
原混合物中NaCl的质量分数=×100%=47%
5.(2017南充)某化学兴趣小组欲测定一瓶过氧化氢溶液中溶质的质量分数,
实验操作及相关数据如图
所示:(1)生成氧气的质量 g;
(2)这瓶过氧化氢溶液中溶质的质量分数是多少?(写出计算过程)
. 解:(1)根据质量守恒定律,反应生成氧气的质量=68g+2g-68.4g=1.6g;故
填:1.6
(2)设68g过氧化氢溶液中含有过氧化氢的质量为x.
2H O 2H O + O ↑
2 2 2 2
68 32
x 1.6g
解得,x=3.4g
过氧化氢溶液的溶质的质量分数为
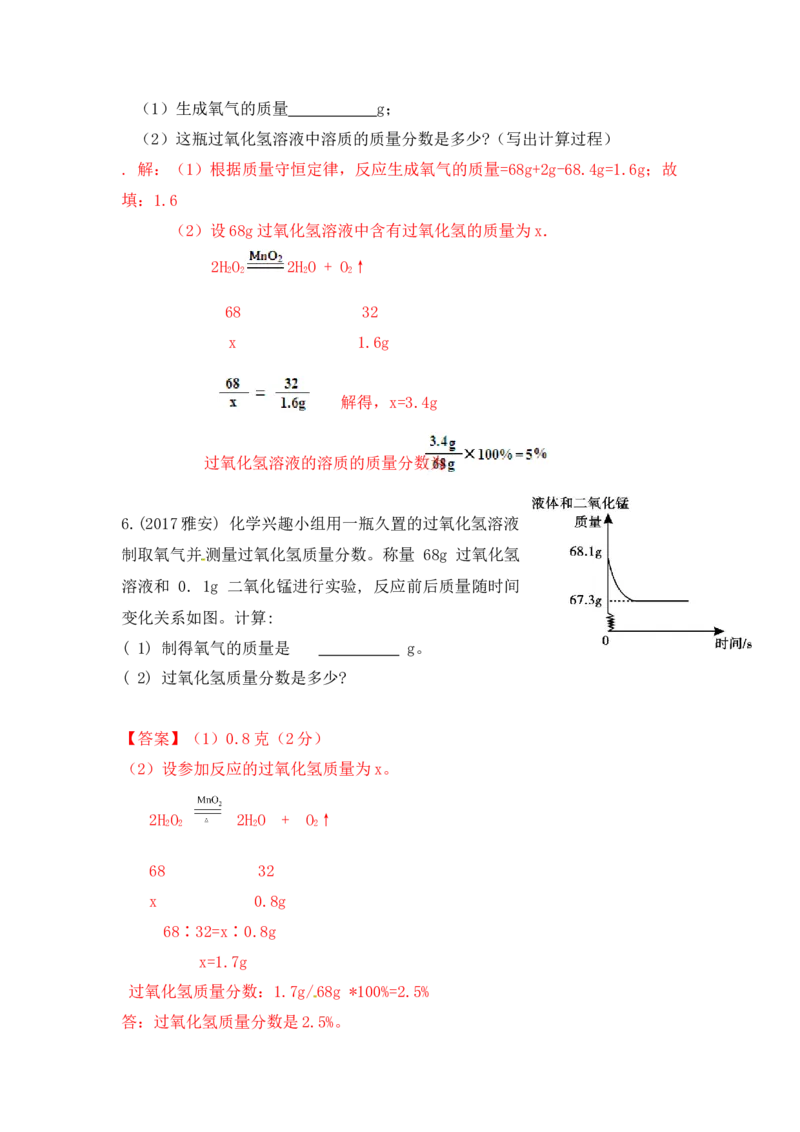
6.(2017雅安) 化学兴趣小组用一瓶久置的过氧化氢溶液
制取氧气并测量过氧化氢质量分数。称量 68g 过氧化氢
溶液和 0. 1g 二氧化锰进行实验, 反应前后质量随时间
变化关系如图。计算:
( 1) 制得氧气的质量是 g。
( 2) 过氧化氢质量分数是多少?
【答案】(1)0.8克(2分)
(2)设参加反应的过氧化氢质量为x。
2H O 2H O + O ↑
2 2 2 2
68 32
x 0.8g
68∶32=x∶0.8g
x=1.7g
过氧化氢质量分数:1.7g/68g *100%=2.5%
答:过氧化氢质量分数是2.5%。