文档内容
2018 年中考化学一轮复习·《原子、离子》真题练习
一、选择题
1.(2017长春市)下列物质中,由原子直接构成的是( )
A. 氮气 B.金刚石 C.水 D.氯化钠
【答案】B
【解析】此题主要考查物质的构成。分子、原子、离子均能直接构成物质。
A、氮气是由氮气分子构成,故错误;
B、金刚石是由碳原子构成的,故正确;
C、水是由水分子构成,故错误;
D、氯化钠是由氯离子和钠离子构成的,故错误;故选B。
2.(2017苏州)下列物质由离子构成的是( )
A. 二氧化碳B. 氯化钠C. 铁D. 水
【答案】B
【解析】本题主要考查物质构成知识的试题;二氧化碳是由二氧化碳分子构成,故
A不符合题意;氯化钠由钠离子和氯离子构成,故B符合题意;铁由铁原子构成,
故C不符合题意;水由水分子构成,故D不符合题意。
3.(2017广西省来宾市)下列各种粒子,带负电荷的是( )
A.电子 B.中子 C.质子 D.原子核
【答案】A
【解析】原子是由原子核和电子构成,原子核是由质子和中子构成,质子带正电荷
中子不带电,原子核带正电荷,电子带负电荷,A符合题意,故选A。
【知识点】原子的构成
4.(2017云南)如图是某元素的原子结构示意图,下列有关该原子的说法错误的
是( )
A.质子数为11 B.易得电子形成阴离子
C.最外层有1个电子 D.该原子有三个电子层
1【答案】B
【解答】解:A、由某元素的原子结构示意图,圆圈内的数字是11,该元素原子核内
有11个质子,故选项说法正确.
B、由某元素的原子结构示意图,最外层电子数是2,在化学反应中易失去1个电
子而形成阳离子,故选项说法错误.
C、由某元素的原子结构示意图,该原子的最外层有1个电子,故选项说法正确.
D、由某元素的原子结构示意图,该原子核外有3个电子层,故选项说法正确.
5.(2017荆州)下列说法不正确的是( )
A.原子呈电中性
B.原子中一定含有质子
C.化学反应前后原子的种类不变
D.保持水的化学性质的微粒是氢原子和氧原子
【答案】D
【解答】解:A、原子核是由质子和中子构成,质子带正电荷,中子不带电,故原子核
带正电荷,但由于原子核与核外电子所带电荷数量相等,电性相反,故整个原子
不显电性,故A正确;
B、原子中一定含有质子,故B正确;
C、化学反应前后原子的种类、数目、质量不变,故C正确;
D、保持水的化学性质的微粒是水分子,故D错误;
6.(2017昆明)某粒子的结构示意图如图所示,该粒子是( )
A.Al B.Al3+ C.Mg D.Mg2+
【答案】C
【解答】解:由粒子的结构示意图可知,该微粒的质子数=电子数=12,是镁原子,符
号为:Mg.故C正确,A、B、D错误.
7.(2017黔南)下列关于四种粒子结构示意图的说法正确的是( )
2A.①③属于不同种元素B.④属于离子,离子符号为Mg2﹣
C.②③的化学性质相似D.①④均达到相对稳定的结构
【答案】D
【解答】解:A、同种元素质子数一定相同,①③的质子数都是17,所以两者属于同
种元素,故A错误;
B、由于离子中质子数与核外电子数不等,而④中质子数比电子数多2是镁离子,
其符号应该是Mg2+,故B错误;
C、因为元素的性质和最外层电子数关系密切,所以最外层电子数相同则化学性
质相似,②③的最外层电子数分别是1、7,故性质不会相似,故C错误;
D、根据通常认为最外层有8个电子(最外层是第一电子层时有2个电子)的结构
是一种稳定结构,而①④的最外层电子数都是8,是一种稳定结构,故D正确.
8.(2017牡丹江)下面是几种粒子的结构示意图,有关说法正确的是( )
+2 2
+12 282 +12 28 +16286
① ② ③ ④
A.只有①达到了稳定结构 B.①②元素具有相似的化学性质
C.②失去电子以后形成的是阳离子 D.④属于金属元素
【答案】C
【解答】解:A、①的核外电子层数为1层,电子数为2,属于相对稳定结构,③的最
外层电子数为8,属于相对稳定结构,故A说法错误.
B、①的核外只有一个电子层,有2个电子,具有相对稳定结构;②的核外有3个电
子层,最外层的电子数是2,未达到稳定结构.故B说法错误.
C、②中最外层电子数为2,易失去电子以后形成形成稳定结构,是阳离子;故C说
法正确.
D、根据原子结构示意图的特点:金属元素的最外层电子数一般少于4,因此④不
3属于金属元素;故D说法错误.
9.(2017南宁)下列微观粒子的结构示意图中,表示阳离子的是( )
A. B. C. D.
+1028 +12 28 +16286 +17288
【答案】B
【解析】A.质子数=核外电子数=10,则为原子,故 A错误;B.质子数=12,核外电子
数=10,质子数>核外电子数,则为阳离子,故B正确;C.质子数=核外电子数=16,
则为原子,故C错误;D.质子数=17,核外电子数=18,质子数<核外电子数,则为
阴离子,故D错误。
10.(2017贺州)下列粒子不能直接构成物质的是( )
A.原子B.分子 C.电子 D.离子
【答案】C
【解答】解:构成物质的微观粒子有分子、原子和离子,电子不是构成物质的粒子;
11.(2017贺州)下列粒子结构示意图表示阴离子的是( )
A. B. C. D.
【答案】C
【解答】A、由图示可知:质子数为11而核外电子数为10,即核内质子数大于核外
电子数,所以该粒子为阳离子,故不符合题意;
B、根据粒子结构示意图,可知质子数为12,核外电子数也为12,所以该粒子为原
子,故不符合题意.
C、由图示可知:质子数为8,核外电子数为10,所以该粒子为阴离子,故符合题意;
D、由图示可知:质子数为10,核外电子数为10,所以该粒子为原子,故不符合题
意.
12.(2017山东省聊城市)李涛同学撰写的“心目中的原子”短文中,阐述了以下
观点,你认为不正确的是( )
A.原子可以转化为离子 B.原子是最小的微观粒子
C.有些物质是由原子构成的 D.原子可以“搭建”成分子
【答案】B
4【解析】此题主要考查有关原子的相关知识。
核外电子是分层排布的,最外层电子大于4个的容易得到电子,形成阴离子;最
外层电子小于4个的容易失去电子,形成阳离子,所以原子可以转化为离子,故
正确;
从结构上原子可以分为原子核和和外电子,因此它不是最小的微粒;原子是化学
变化中的最小粒子,不可再分;故错误;
构成物质的微粒有分子、原子和离子,原子是构成物质的微粒之一,如金属铁是
由铁原子构成,故正确;
分子和原子都可以构成物质,由分子构成的物质,分子由是由原子构成的,故正
确。
13. (2017浙江省温州市)5月9日,2机构发布 等四种元素的中文名称。
元素的核电荷数为118,相对原子质量为294,则 原子核外电子数为( )
A.118 B.176 C.294 D.412
【答案】A
【解析】此题主要考查的是原子的构成,原子是由具于原子中心的原子核和核外
电子构成的,原子核是由质子和中子构成的,在原子中质子数等于核电荷数等于
电子数, 元素的核电荷数为118,所以电子数为118,故选A。
14. (2017山西省)小美从某粒子结构示意图(如右图)中,获取了下列信息,其中
错误的是( )
A.它有两个电子层 B.它的核电荷数为12
C.它表示阴离子 D.它表示相对稳定结构
【答案】C
【解析】本题考查的是原子的结构示意图,从题中所给原子结构示意图中可以看
出,该粒子有两个电子层,圆圈内的数字即为核电荷数为12,核外电子数为10,
5质子数大于电子数为阳离子,12号元素为镁元素,因此该粒子为为镁离子,为阳
离子,最外层电子数为8,具有相对稳定结构。故选C。
15.(2017四川省自贡市) 铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内
有58个质子和82个中子,该原子的核外电子数为( )
A.24 B.58 C.82 D.140
【答案】B
【解析】本题主要考查构成原子的粒子种类以及各粒子之间的数量关系;在原子
中,质子数=核外电子数,所以金属铈中的质子数=核外电子数=58,所以B选项符
合题意;24是中子数与质子数之差,不等于核外电子数,故A选项错误;中子数不
等于核外电子数,故C选项错误;140是质子数与中子数之和,等于相对原子质量
故D选项错误。
【知识点】构成原子的粒子种类以及各粒子之间的数量关系
16.(2017年山东省威海市)在化学变化中,下列说法正确的是( )
①原子不能被创造也不能被消灭 ②原子核不能被创造但能被消灭
③分子既可以被创造也可以被消灭 ④电子不能被创造但能被消灭
A.②④ B.①④ C.①③ D.②③
【答案】 C
【解析】此题考查了在化学变化中分子原子之间的转化:①原子不能被创造也不
能被消灭,却可以重新组合成新分子,故正确 ;②原予核不能被创造也不能被消
灭,是组成原子的一部分,故原予核不能被创造但能被消灭错误;③分子既可以
被创造也可以被消灭,物质在发生化学变化时分子分成原子被消灭,反应后又生
成新的分子被创造,故正确;④电子知识从一个原子上转移到另一个原子上不能
被创造也不能被消灭 ,所以电子不能被创造但能被消灭错误。
A②错误,④错误,故错误。
B①正确,④错误,故错误。
C①正确,③正确,故正确。
D②错误,③正确,故错误。
17.(2017上海市)有关氧原子的描述正确的是( )
A. 一个氧原子的质量是16g
B. 1g氧原子和1g氧分子含有相同的原子个数
C. 氧原子的摩尔质量在数值上等于氧原子的质量
6D. 氧原子的相对原子质量就是1mol氧原子的质量
【答案】B
【解析】本题主要考查原子及物质的量;一个氧原子的相对原子质量是16,不是质
量,故A选项错误;每个氧分子是由2个氧原子构成,1g氧分子所含的氧原子个
数是1g氧原子个数的2倍,故B选项错误;氧原子的摩尔质量在数值上等于氧原
子的相对原子质量,不是原子质量,故C选项错误;摩尔质量是指每摩尔原子所
具有的质量,单位是g/mol,在数值上等于原子的相对原子质量,所以氧原子的相
对原子质量就是1mol氧原子的质量,正确,故D正确。
18.(2017常州)道尔顿、汤姆生和卢瑟福等科学家对原子结构进行了不断探索,
下列叙述正确的是( )
①原子由原子核和核外电子构成
②原子的质量主要集中在原子核上
③原子核在原子中所占的体积极小
A.①② B.①③ C.②③ D.①②③
【答案】D
【解析】本题主要考查原子结构;①原子是由具于原子中心的原子核和核外电子
构成的,正确;②核外电子的质量非常小,大约是质子质量的1836分之一,故通
常忽略不计,所以原子的质量主要集中在原子核上,正确;③原子核位于原子中
心,所占的体积极小,电子在核外的空间做运动,正确;所以D选项正确,ABC错误。
19.(2017怀化市)下列关于分子、原子、离子的说法正确的是( )
A.分子是保持物质性质的最小粒子 B.原子是最小的粒子
C.原子得到电子或失去电子变成离子 D.分子一定比原子大
【答案】C
【解析】此题考察各微粒的性质。
分子是保持物质化学性质的最小微粒,故A选项错误;
原子还可以分成原子核和核外电子,原子是化学变化中的最小微粒,故B选项错
误;
原子得到电子变成阴离子,失去电子变成阳离子,故C选项正确;
分子和原子都是构成物质的微粒,不同的 原子核分子体积不同,不能说分子一
定比原子大,故D选项正确,所以选择C。
720.(2017江苏省宿迁市) 下列说法正确的是( )
A.由分子构成的物质在发生化学变化时,分子种类改变,原子种类不变
B.离子是带电的原子或原子团,所以带电的微粒一定是离子
C.构成固体物质的微粒都是静止不动的
D.与元素化学性质关系最密切的是原子的核外电子数
【答案】A
【解析】本题主要考查微观粒子种类及特征;化学变化反应前后,分子种类一定改
变,原子种类不变,故A说法正确;带电的微粒不一定是离子,质子、电子都带电,
故B说法错误;构成固体物质的微粒也是在不停运动的,故C说法错误;原子的最
外成电子数决定元素的化学性质,故D说法错误。
21.(2017山东省烟台市)下图是四种粒子的结构示意图。下列说法正确的是(
)
A.②③属于同种元素 B.②④的化学性质相同
C.②的符号为Al+3 D.①③形成的化合物是MgF
2
【答案】D
【解析】由图知,②③原子核内质子数不同,不属于同一种元素,A错误;
②④最外层电子数不同,化学性质不同,B错误;
②中质子数为13,核外电子数为10,故其符号应为Al3+,C错误;
①为F-,③为Mg2+,二者形成化合物的化学式为MgF2,D正确。
22.(2017年山东省威海市)学习完“原子的构成”之后,萍萍同学形成了以下认
识,其中错误的是( )
A.原子由居于中心的原子核和核外电子构成
B.核外电子在离核远近不同的区域中运动
C.原子核的质量和电子的质量相差不大
D.原子核的体积与整个原子的体积相比要小很多
【答案】C
【解析】本题考查了原子结构,核外电子排布,原子与原子内部微粒之间比较
8A原子结构中,原子是由居于院子中心的带正电的原子核和核外带负电的电子构
成的,故正确。
B原子结构中,核外电子分层排布,并且电子的能量不同离核远近不同,故正确。
C原子中原子核几乎集中了原子的全部质量,原子核又是由质子和中子构成的,
相对于电子质量很大,故错误。
D原子的质量和体积都很小,原子是由原子核和核外电子构成的,原子核的体积
也很小,故正确。
【知识点】原子的构成
23.(2017山东省临沂市)核电荷数多于核外电子数的粒子一定是( )
A.分子 B.原子
C.阴离子 D.阳离子
【答案】D
【解析】本题主要考查阳离子和阴离子的判断。
分子和原子都是不带电的粒子,核电荷数等于电子数;阴离子带负电荷,电子数
大于核电荷数,如S2-;阳离子带正电荷,核电荷数大于电子数,如K+,故D正确。
24.(2017山东省青岛市)下列物质中, 由离子构成的是( )
A.铁 B.氯化钠 C.二氧化碳 D.金刚石
【答案】B
【解析】此题考查物质的微粒构成。构成物质的微粒有分子、原子和离子;铁是由
原子构成的,A不符合题意;氯化钠是由钠离子和氯离子构成的,B符合题意;二
氧化碳是由分子构成的,C不符合题意;金刚石是由原子构成的,D不符合题意。
故选B。
25.(2017山东省临沂市)核电荷数多于核外电子数的粒子一定是( )
A.分子 B.原子
C.阴离子 D.阳离子
【答案】D
【解析】本题主要考查阳离子和阴离子的判断。
分子和原子都是不带电的粒子,核电荷数等于电子数;阴离子带负电荷,电子数
大于核电荷数;阳离子带正电荷,核电荷数大于电子数,故D正确。
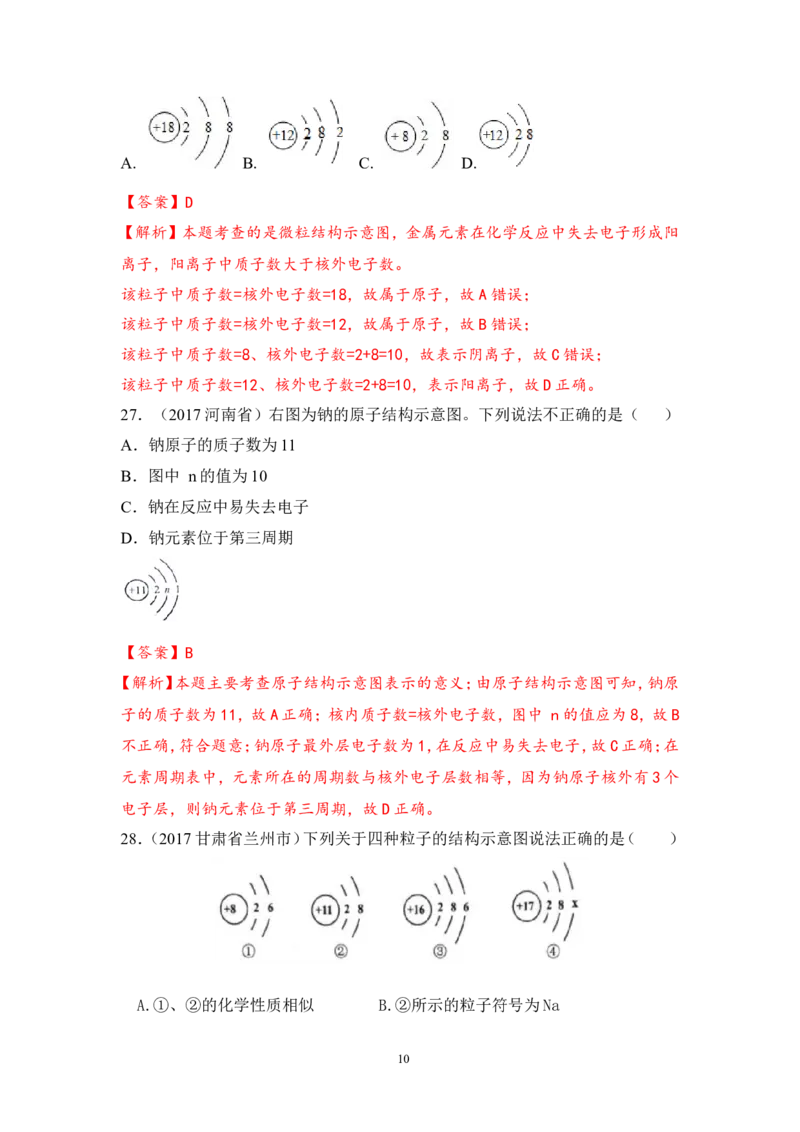
26.( 2017广安市)下列四种粒子的结构示意图中,表示金属离子的是( )
9A. B. C. D.
【答案】D
【解析】本题考查的是微粒结构示意图,金属元素在化学反应中失去电子形成阳
离子,阳离子中质子数大于核外电子数。
该粒子中质子数=核外电子数=18,故属于原子,故A错误;
该粒子中质子数=核外电子数=12,故属于原子,故B错误;
该粒子中质子数=8、核外电子数=2+8=10,故表示阴离子,故C错误;
该粒子中质子数=12、核外电子数=2+8=10,表示阳离子,故D正确。
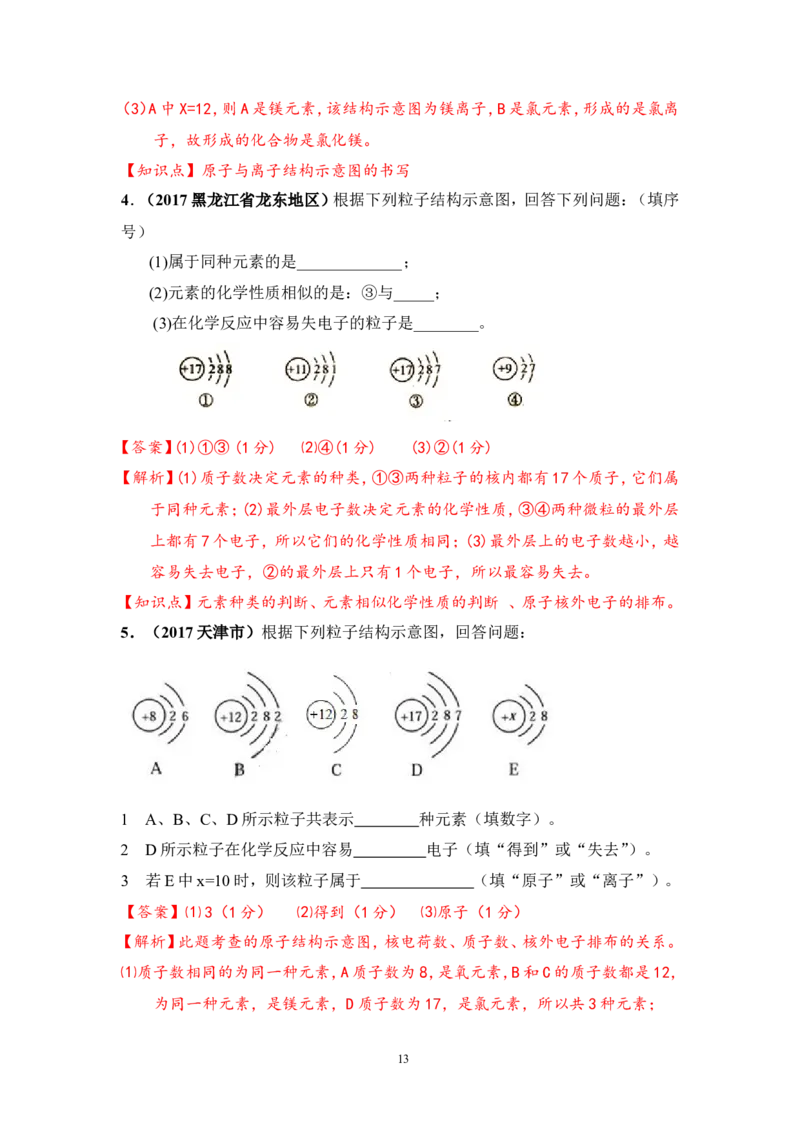
27.(2017河南省)右图为钠的原子结构示意图。下列说法不正确的是( )
A.钠原子的质子数为11
B.图中 n的值为10
C.钠在反应中易失去电子
D.钠元素位于第三周期
【答案】B
【解析】本题主要考查原子结构示意图表示的意义;由原子结构示意图可知,钠原
子的质子数为11,故A正确;核内质子数=核外电子数,图中 n的值应为8,故B
不正确,符合题意;钠原子最外层电子数为1,在反应中易失去电子,故C正确;在
元素周期表中,元素所在的周期数与核外电子层数相等,因为钠原子核外有3个
电子层,则钠元素位于第三周期,故D正确。
28.(2017甘肃省兰州市)下列关于四种粒子的结构示意图说法正确的是( )
A.①、②的化学性质相似 B.②所示的粒子符号为Na
10C.③在化学反应中易失去电子 D.④中X可能为8
【答案】D
【解析】此题考查原子结构示意图及原子的简单性质;
①表示8号元素的原子,表示氧原子;②表示11号元素的离子,即钠离子,二者化
学性质不相似,故错误;
②表示11号元素的离子即钠离子(Na+),故错误;
③表示16号元素的原子即硫原子,最外层有6个电子,在反应中容易得到两个电
子,故错误;
若④表示17号元素的离子即氯离子,则x为8;若④表示17号元素的原子即氯原
子,则x为7,因此x可能为7或8,故正确,选择D。
填空题
二、填空题
1.(2017黑龙江省龙东地区)用化学用语填空:
(1)铝离子________;
(2) 2个水分子_________;
(3)人体中含量最多的金属元素__________。
【答案】(1) Al3+ (2) 2H O ⑶ Ca
2
【解析】(1) 铝的符号是Al,在化学反应中易失去最外层上的3个电子,故其离子
符号是Al3+;(2)一个水分子可表示 为H O,所以两个水分子是2H O;⑶人体中含
2 2
量最多的金属元素是钙,其符号是Ca。
2. (2017年湖南省株州市)下图1为溴原子(Br)的结构示意图:图2为A、B、C、D
、E5种粒子的结构示意图。请回答下列问题:
(1)图1中第三层电子数与最外层电子数之差为______(注意:不能填代数
式);图2中E粒子形成的单质的化学式是______(填用元素符号表示的化学
式)。
11(2)D粒子与溴原子可以结合成化合物,该化合物的化学式为______(填用元
素符号表示的化学式)。
(3)图2的结构示意图中,______(填字母代号)表示的是非金属元素的粒子。
【答案】(1)11; Cl2; (2)NaBr ; (3)E
【解析】此题主要考查核外电子在化学反应中的作用及化学式的书写。(1)图1为
溴原子(Br)的结构示意图,在原子中质子数等于核外电子数,解得X=7,故
图1中第三层电子数与最外层电子数之差为11;图2中E粒子为氯原子,它
形成单质是氯气,故化学式为:Cl2;(2)从图知D粒子是钠原子,钠属于活泼
的金属,在反应中失去1个电子,显+1价,溴原子易得到1个电子,显-1价
故可以结合成化合物化学式为:NaBr ;(3)在原子中最外层电子小于4的为
金属元素,则A、B、D为金属元素;达到8电子或只有一层,达到2电子稳定
结构的,其性质就是稳定的,是稀有气体元素,则C为稀有气体元素;最外层
电子大于4的为非金属元素,则E为非金属元素;故填 E。
【知识点】原子结构示意图、核外电子在化学反应中的作用、化学式的书写、元素
分类
3.(2017青海省西宁市) 右图A、B是两种粒子的结构示意图,回答下列问题。
(l)若A是某阴离子的结构示意图,则x可能是下列中的____(填字母序号)。
a.8 b.10 c.11 d.12
(2)若B表示某原子的结构示意图,则y=______。
(3)若A中x=12,则A、B所表示的元素形成化合物的名称为______。
【答案】(1)a(1分)(2)7(1分)(3)氯化镁(1分)
【解析】本题主要考察原子与离子结构示意图的书写
在阴离子中,核内质子数<核外电子数,所以X小于10,故X可能是8,即a
当核电荷数=质子数=核外电子数,为原子,所以若B表示某原子的结构示意图,
则17=2+8+y,y=7
12(3)A中X=12,则A是镁元素,该结构示意图为镁离子,B是氯元素,形成的是氯离
子,故形成的化合物是氯化镁。
【知识点】原子与离子结构示意图的书写
4.(2017黑龙江省龙东地区)根据下列粒子结构示意图,回答下列问题:(填序
号)
(1)属于同种元素的是_____________;
(2)元素的化学性质相似的是:③与_____;
(3)在化学反应中容易失电子的粒子是________。
【答案】(1)①③(1分) ⑵④(1分) (3)②(1分)
【解析】(1)质子数决定元素的种类,①③两种粒子的核内都有17个质子,它们属
于同种元素;(2)最外层电子数决定元素的化学性质,③④两种微粒的最外层
上都有7个电子,所以它们的化学性质相同;(3)最外层上的电子数越小,越
容易失去电子,②的最外层上只有1个电子,所以最容易失去。
【知识点】元素种类的判断、元素相似化学性质的判断 、原子核外电子的排布。
5.(2017天津市)根据下列粒子结构示意图,回答问题:
1 A、B、C、D所示粒子共表示 种元素(填数字)。
2 D所示粒子在化学反应中容易 电子(填“得到”或“失去”)。
3 若E中x=10时,则该粒子属于 (填“原子”或“离子”)。
【答案】⑴3(1分) ⑵得到(1分) ⑶原子(1分)
【解析】此题考查的原子结构示意图,核电荷数、质子数、核外电子排布的关系。
⑴质子数相同的为同一种元素,A质子数为8,是氧元素,B和C的质子数都是12,
为同一种元素,是镁元素,D质子数为17,是氯元素,所以共3种元素;
13⑵D最外层电子数都是7,容易得到1个电子形成8电子稳定结构;
⑶根据原子的核电荷数=质子数=核外电子数,当x=10时,核电荷数=核外电子数,
表示的是原子;
【知识点】元素、原子的构成
6.(2017湖南省邵阳市)下图是 A、B、C、D四种粒子的结构示意图。
(1)属于同种元素的是_______(填序号)。
(2)A与C形成化合物的化学式是 ________。
(3)B在化学反应中易 _________(填“得”或“失”)电子。
【答案】(1) CD(或C和D) (2)MgCl2 (3)得
【解析】(1)同种元素的元素具有相同的核电荷数即质子数,C和D原子的质子数
都为17,都属于氯元素。
(2)A质子数为12,核外电子数为10,为镁离子;C的质子数为17,核外电子数为
18,为氯离子,A与C形成化合物的化学式是MgCl2。
(3)B原子的最外层有6个原子,在反应中易得到2个电子,达到8电子稳定结构,
形成阴离子。
14