文档内容
第10讲 质量守恒定律和化学方程式
命题点1 质量守恒定律及其应用(6年6考)
1.(2012·山西·8题·2分)氯碱工业的反应原理是电解饱和食盐水,下列物质不可能
是氯碱工业产品的是( C )
A.H B.Cl
2 2
C.NaCO D.NaOH
2 3
2.(2013·山西·9题·2分)对于化学反应X+NaCO===2Y+CaCO↓,分析错误的是(
2 3 3
C )
A.该反应属于复分解反应
B.Y中一定含有钠元素
C.X一定是熟石灰
D.X中阴离子化合价是-1价
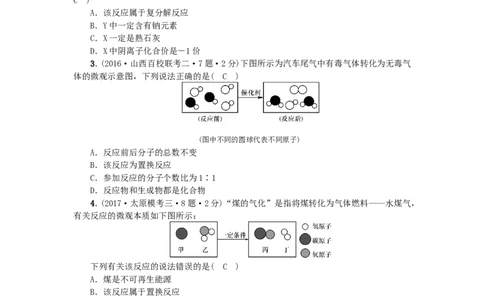
3.(2016·山西百校联考二·7题·2分)下图所示为汽车尾气中有毒气体转化为无毒气
体的微观示意图,下列说法正确的是( C )
(图中不同的圆球代表不同原子)
A.反应前后分子的总数不变
B.该反应为置换反应
C.参加反应的分子个数比为1∶1
D.反应物和生成物都是化合物
4.(2017·太原模考三·8题·2分)“煤的气化”是指将煤转化为气体燃料——水煤气,
有关反应的微观本质如下图所示:
下列有关该反应的说法错误的是( C )
A.煤是不可再生能源
B.该反应属于置换反应
C.图中只有一种氧化物
D.反应中乙、丙的质量比是9∶14
命题点2 化学方程式的书写与计算(6年6考)
5.(2017·山西·22题·3分)我们的胃液中含有盐酸,它有助于消化,但胃酸过多会引
起胃部不适。有时可以用小苏打治疗,反应的方程式为NaHCO + HC l = = =NaC l + H O + C O↑,化
3 2 2
学反应前后一定没有变化的离子是 N a + 、 C l - (离子符号表示)。
6.(2017·山西百校四·28题·6分)在实验室里加热30 g氯酸钾和二氧化锰的混合物
制取氧气,反应时间与剩余固体的质量如下表所示。反应时间/s t t t
1 2 3
剩余固体质量/g 25.2 20.4 20.4
请计算:
(1)生成氧气的质量是多少。
(2)原混合物中氯酸钾的质量分数(精确到0.1%)。
解:生成氧气的质量=30 g-20.4 g=9.6 g
设原混合物中氯酸钾的质量为x。
2KClO=====2KCl+3O↑
3 2
245 96
x 9.6 g
=
x=24.5 g
原混合物中氯酸钾的质量分数为×100%=81.7%
答:原混合物中氯酸钾的质量分数为81.7%。
提分训练1 质量守恒定律
(2017·齐齐哈尔)赤热的铁与水蒸气反应,其化学方程式为3Fe+4HO===X+
2
4H,X的化学式为( B )
2
A.FeO B.FeO C.FeO D.O
2 3 3 4 2
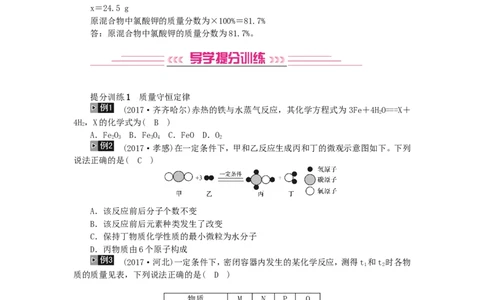
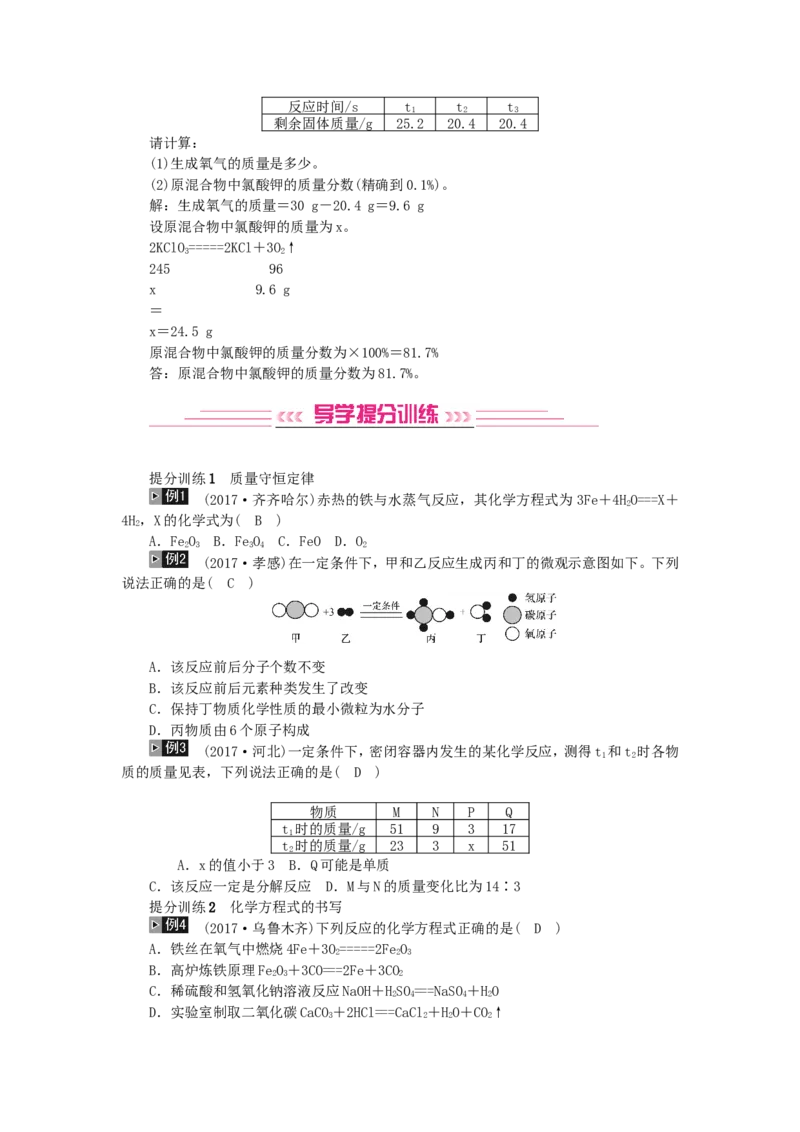
(2017·孝感)在一定条件下,甲和乙反应生成丙和丁的微观示意图如下。下列
说法正确的是( C )
A.该反应前后分子个数不变
B.该反应前后元素种类发生了改变
C.保持丁物质化学性质的最小微粒为水分子
D.丙物质由6个原子构成
(2017·河北)一定条件下,密闭容器内发生的某化学反应,测得t 和t 时各物
1 2
质的质量见表,下列说法正确的是( D )
物质 M N P Q
t 时的质量/g 51 9 3 17
1
t 时的质量/g 23 3 x 51
2
A.x的值小于3 B.Q可能是单质
C.该反应一定是分解反应 D.M与N的质量变化比为14∶3
提分训练2 化学方程式的书写
(2017·乌鲁木齐)下列反应的化学方程式正确的是( D )
A.铁丝在氧气中燃烧4Fe+3O=====2FeO
2 2 3
B.高炉炼铁原理FeO+3CO===2Fe+3CO
2 3 2
C.稀硫酸和氢氧化钠溶液反应NaOH+HSO===NaSO+HO
2 4 4 2
D.实验室制取二氧化碳CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2提分训练3 化学方程式的计算
(易错题)(2017·安徽)实验室加热氯酸钾和二氧化锰的混合物28 g制取氧气,
完全反应后剩余固体质量为18.4 g,请计算:
(1)生成氧气的质量;
(2)原混合物中氯酸钾的质量。
解:(1)生成氧气的质量为28 g-18.4 g=9.6 g
(2)设原混合物中氯酸钾的质量为x。
2KClO=====2KCl+3O↑
3 2
245 96
x 9.6 g
= x=24.5 g
答:(1)生成氧气的质量为9.6 g;(2)原混合物中氯酸钾的质量为24.5 g。
实验突破与活动建议 质量守恒定律的验证
为了研究质量守恒定律,某同学设计了如图“红磷燃烧前后质量测定”的实验,
请分析有关问题:
(1)装置:锥形瓶的底部铺有一层细沙,其作用是防止燃烧物溅落使锥形瓶底炸裂;
(2)燃烧前称量,锥形瓶的总质量为27.0 g,则图中托盘天平中游码的读数为2.0g;
(3)红磷燃烧过程中看到的现象是产生大量白烟,玻璃管上方的气球先胀大后缩小;
(4)燃烧后称量:发现托盘天平指针偏向右边,造成的原因可能是 装置漏气 ( 或锥形瓶未
冷却等 )(填一种即可);
(5)反思:红磷燃烧遵守(填“遵守”或“不遵守”)质量守恒定律,理由是在化学反应
中,反应前后原子的种类没有改变、原子的数目没有增减、原子的质量也没有变化(从微观上
解释)。
1.(2017·来宾)下列实验能够用于直接验证质量守恒定律的是( C )
A B C D2.(2017·黑龙江)实验室用浓盐酸和二氧化锰制取氯气,反应的化学方程式为MnO+
2
4HCl(浓)=====X+Cl↑+2HO,则X的化学式为( A )
2 2
A.MnCl B.ClO
2 2
C.MnCl D.HClO
4
3.(2017·连云港)我国古代典籍中有“银针验毒”的记载,“银针验毒”的反应原理
之一是4Ag+2HS+O===2X+2HO。下列有关该反应的说法不正确的是( D )
2 2 2
A.反应属于氧化反应
B.X的化学式是AgS
2
C.反应前后元素的种类不变
D.反应前后所有元素的化合价都发生了变化
4.(2017·临沂)下列化学方程式书写正确的是( C )
A.2NaOH+CuSO===Cu(OH)↓+NaSO
4 2 4
B.Ba(NO)+HSO===BaSO↓+HNO
3 2 2 4 4 3
C.C+2CuO=====2Cu+CO↑
2
D.FeO+6HCl===2FeC1+3HO
2 3 2 2
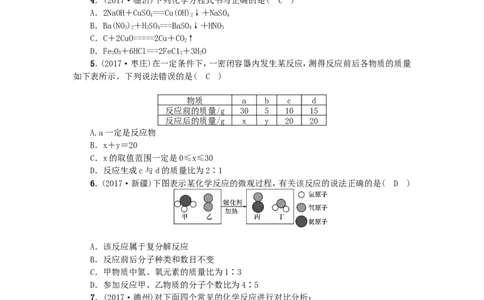
5.(2017·枣庄)在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量
如下表所示。下列说法错误的是( C )
物质 a b c d
反应前的质量/g 30 5 10 15
反应后的质量/g x y 20 20
A.a一定是反应物
B.x+y=20
C.x的取值范围一定是0≤x≤30
D.反应生成c与d的质量比为2∶1
6.(2017·新疆)下图表示某化学反应的微观过程,有关该反应的说法正确的是( D )
A.该反应属于复分解反应
B.反应前后分子种类和数目不变
C.甲物质中氮、氧元素的质量比为1∶3
D.参加反应甲、乙物质的分子个数比为4∶5
7.(2017·德州)对下面四个常见的化学反应进行对比分析:
分解反应:2KMnO=====KMnO+MnO+O↑;
4 2 4 2 2
置换反应:2CuO+C=====2Cu+CO↑;
2
复分解反应:Ca(OH)+NaCO===CaCO↓+2NaOH;
2 2 3 3
化合反应:2H+O=====2HO。
2 2 2
请从以下各项中选择恰当的内容,用对应的序号填空:
①元素的种类;②原子的种类;③原子的个数;④分子的种类;⑤物质的组成(或结构);
⑥物质的总质量;⑦元素的化合价
在化学反应过程中,一定发生变化的是④⑤;可能发生变化的是⑦。
8.(2017·天津)写出下列反应的化学方程式。
(1)镁在氧气中燃烧 2M g + O ==== = 2Mg O;
2(2)锌和稀硫酸反应 Z n + HSO = = =ZnS O + H↑;
2 4 4 2
(3)氢氧化钠溶液与稀盐酸混合 NaO H + HC l = = =NaC l + HO。
2
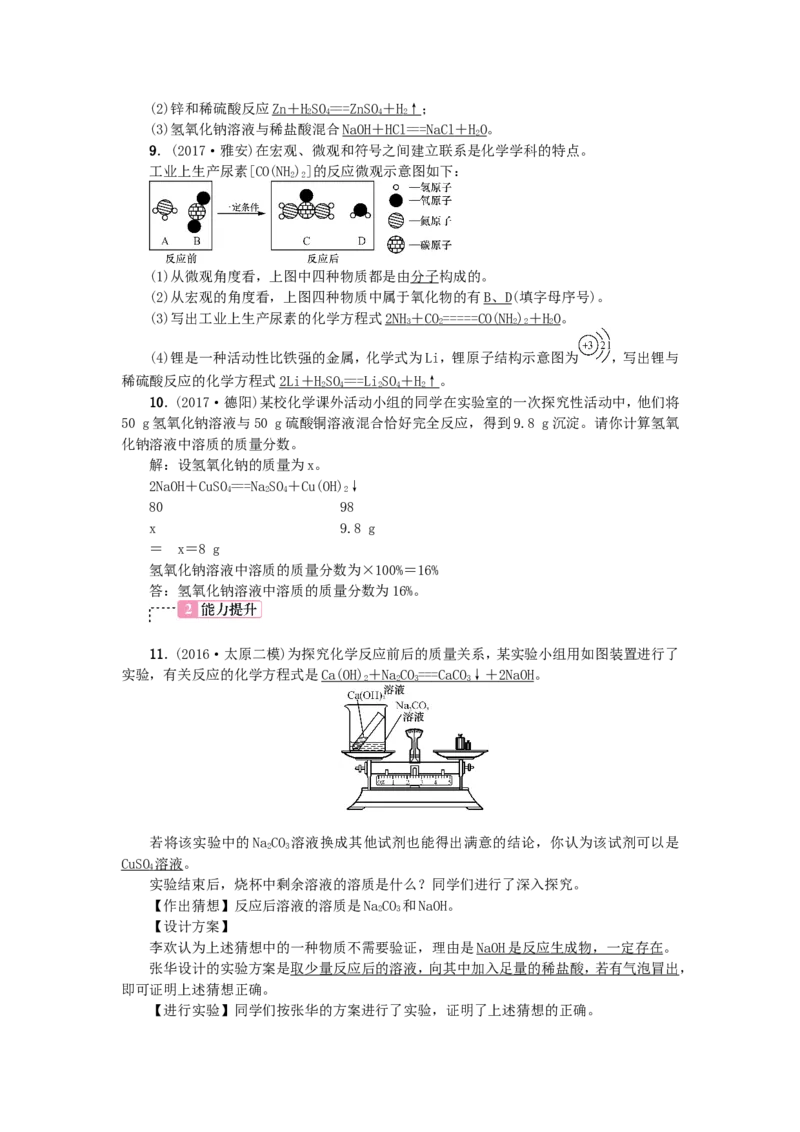
9.(2017·雅安)在宏观、微观和符号之间建立联系是化学学科的特点。
工业上生产尿素[CO(NH)]的反应微观示意图如下:
2 2
(1)从微观角度看,上图中四种物质都是由分子构成的。
(2)从宏观的角度看,上图四种物质中属于氧化物的有 B 、 D(填字母序号)。
(3)写出工业上生产尿素的化学方程式2NH + C O ==== = CO(N H) + HO。
3 2 2 2 2
(4)锂是一种活动性比铁强的金属,化学式为Li,锂原子结构示意图为 ,写出锂与
稀硫酸反应的化学方程式 2L i + HSO = = =L iSO + H↑。
2 4 2 4 2
10.(2017·德阳)某校化学课外活动小组的同学在实验室的一次探究性活动中,他们将
50 g氢氧化钠溶液与50 g硫酸铜溶液混合恰好完全反应,得到9.8 g沉淀。请你计算氢氧
化钠溶液中溶质的质量分数。
解:设氢氧化钠的质量为x。
2NaOH+CuSO===NaSO+Cu(OH)↓
4 2 4 2
80 98
x 9.8 g
= x=8 g
氢氧化钠溶液中溶质的质量分数为×100%=16%
答:氢氧化钠溶液中溶质的质量分数为16%。
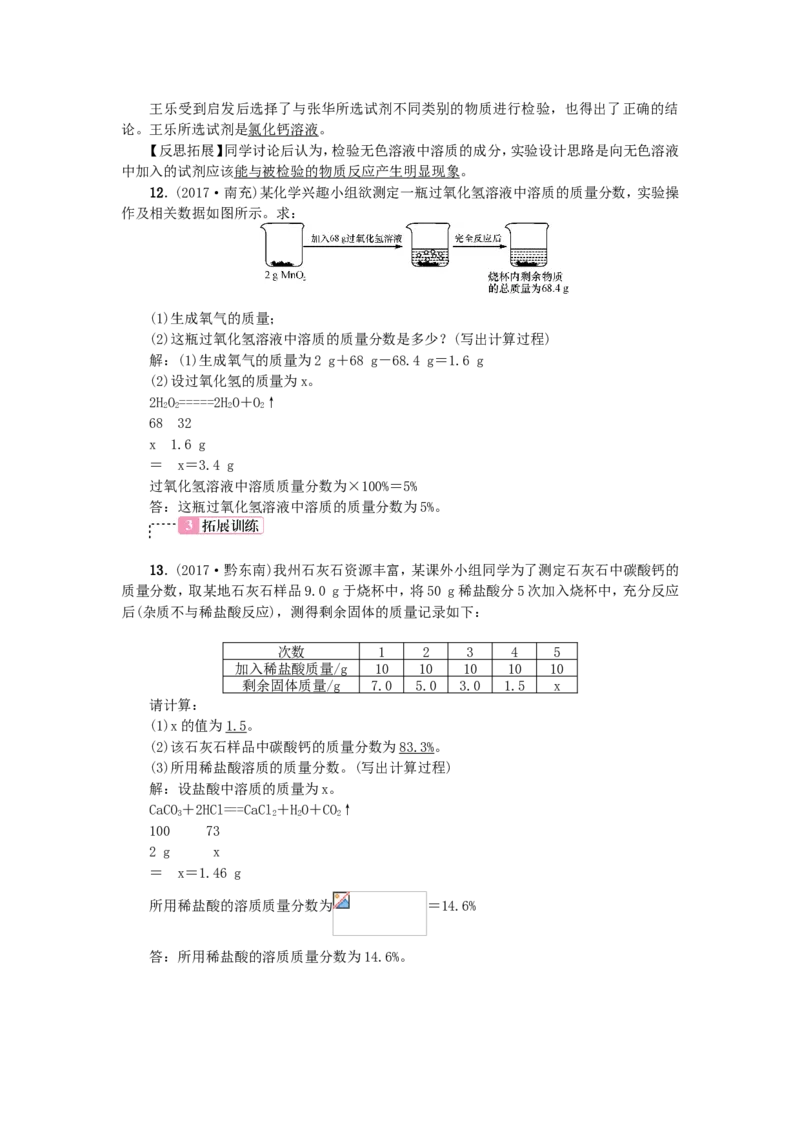
11.(2016·太原二模)为探究化学反应前后的质量关系,某实验小组用如图装置进行了
实验,有关反应的化学方程式是Ca(OH) + N aCO = = =CaC O ↓+ 2NaO H。
2 2 3 3
若将该实验中的NaCO 溶液换成其他试剂也能得出满意的结论,你认为该试剂可以是
2 3
CuSO 溶液。
4
实验结束后,烧杯中剩余溶液的溶质是什么?同学们进行了深入探究。
【作出猜想】反应后溶液的溶质是NaCO 和NaOH。
2 3
【设计方案】
李欢认为上述猜想中的一种物质不需要验证,理由是 NaO H 是反应生成物,一定存在 。
张华设计的实验方案是取少量反应后的溶液,向其中加入足量的稀盐酸,若有气泡冒出,
即可证明上述猜想正确。
【进行实验】同学们按张华的方案进行了实验,证明了上述猜想的正确。王乐受到启发后选择了与张华所选试剂不同类别的物质进行检验,也得出了正确的结
论。王乐所选试剂是氯化钙溶液。
【反思拓展】同学讨论后认为,检验无色溶液中溶质的成分,实验设计思路是向无色溶液
中加入的试剂应该能与被检验的物质反应产生明显现象。
12.(2017·南充)某化学兴趣小组欲测定一瓶过氧化氢溶液中溶质的质量分数,实验操
作及相关数据如图所示。求:
(1)生成氧气的质量;
(2)这瓶过氧化氢溶液中溶质的质量分数是多少?(写出计算过程)
解:(1)生成氧气的质量为2 g+68 g-68.4 g=1.6 g
(2)设过氧化氢的质量为x。
2HO=====2HO+O↑
2 2 2 2
68 32
x 1.6 g
= x=3.4 g
过氧化氢溶液中溶质质量分数为×100%=5%
答:这瓶过氧化氢溶液中溶质的质量分数为5%。
13.(2017·黔东南)我州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的
质量分数,取某地石灰石样品9.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应
后(杂质不与稀盐酸反应),测得剩余固体的质量记录如下:
次数 1 2 3 4 5
加入稀盐酸质量/g 10 10 10 10 10
剩余固体质量/g 7.0 5.0 3.0 1.5 x
请计算:
(1)x的值为1.5。
(2)该石灰石样品中碳酸钙的质量分数为83.3%。
(3)所用稀盐酸溶质的质量分数。(写出计算过程)
解:设盐酸中溶质的质量为x。
CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
100 73
2 g x
= x=1.46 g
所用稀盐酸的溶质质量分数为 =14.6%
答:所用稀盐酸的溶质质量分数为14.6%。