文档内容
滚动小专题(二) 溶解度曲线及其应用
一、溶解度曲线的意义
1.溶解度曲线上的每个点表示的是某温度下某种物质的溶解度,即曲线上的任意一点都对应有相应的温度和溶解度。
2.溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。曲线的坡度越大,说明溶解度受温度
影响越大;反之,说明受温度影响较小。
3.两条溶解度曲线的交点表示该点所示的温度下两物质的溶解度相同,此时两种物质饱和溶液的溶质质量分数也相
同。
4.在溶解度曲线上的每一个点都表示溶质在某温度下的溶解度,此时的溶液必然是恰好饱和的溶液;在溶解度曲线
下方的点,则表示溶液是不饱和溶液;在溶解度曲线上方的点,则表示未溶解的溶质与饱和溶液共存的混合物或过饱
和溶液。
二、溶解度曲线的应用
1.溶解度曲线上的点有三个方面的作用:(1)根据已知温度查出有关物质的溶解度;(2)根据物质的溶解度查出对应的
温度;(3)比较相同温度下不同物质溶解度的大小或者饱和溶液中溶质的质量分数的大小。
2.溶解度曲线也有三个方面的应用:(1)根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况;(2)根
据溶解度曲线,比较在一定温度范围内的物质的溶解度大小;(3)根据溶解度曲线,选择分离某些可溶性混合物的方
法。
3.如果要使不饱和溶液(曲线下方的一点)变成对应温度下的饱和溶液,方法有两种:第一种方法是向该溶液中添加溶
质使之到达曲线上;第二种方法是蒸发一定量的溶剂。
类型1 溶解度曲线的意义
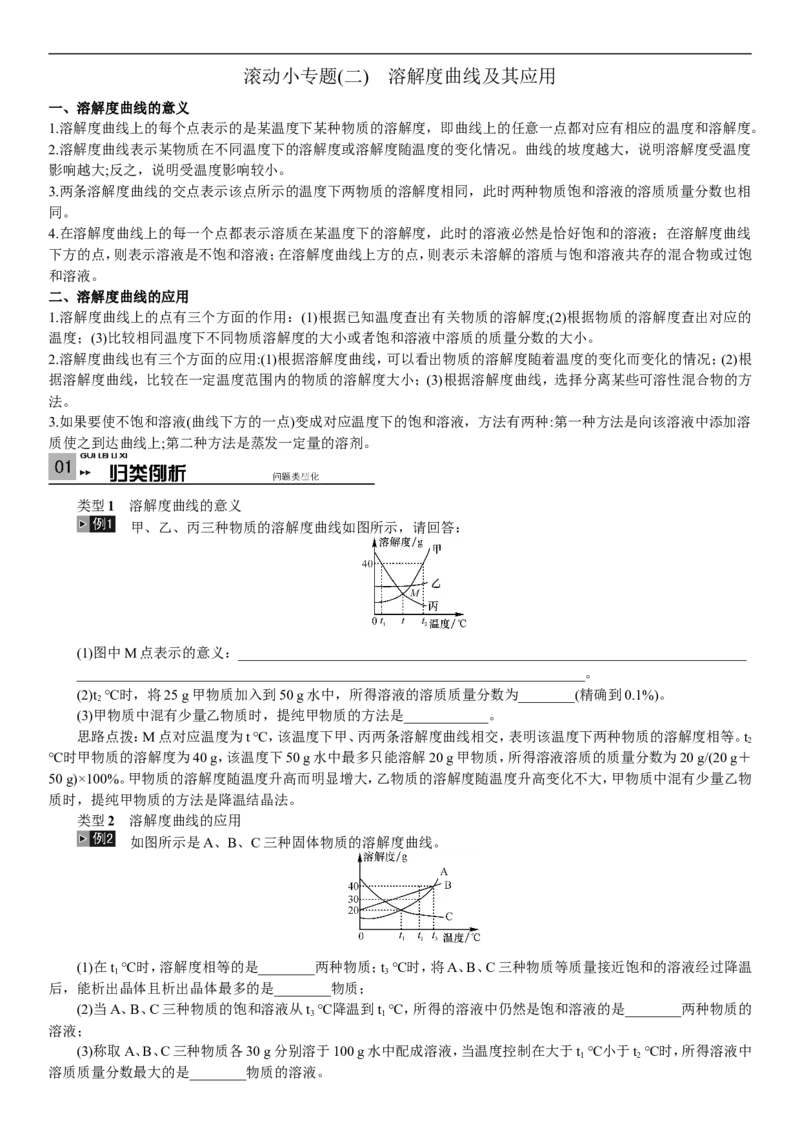
甲、乙、丙三种物质的溶解度曲线如图所示,请回答:
(1)图中M点表示的意义:________________________________________________________________________
________________________________________________________________________。
(2)t ℃时,将25 g甲物质加入到50 g水中,所得溶液的溶质质量分数为________(精确到0.1%)。
2
(3)甲物质中混有少量乙物质时,提纯甲物质的方法是____________。
思路点拨:M点对应温度为t ℃,该温度下甲、丙两条溶解度曲线相交,表明该温度下两种物质的溶解度相等。t
2
℃时甲物质的溶解度为40 g,该温度下50 g水中最多只能溶解20 g甲物质,所得溶液溶质的质量分数为20 g/(20 g+
50 g)×100%。甲物质的溶解度随温度升高而明显增大,乙物质的溶解度随温度升高变化不大,甲物质中混有少量乙物
质时,提纯甲物质的方法是降温结晶法。
类型2 溶解度曲线的应用
如图所示是A、B、C三种固体物质的溶解度曲线。
(1)在t ℃时,溶解度相等的是________两种物质;t ℃时,将A、B、C三种物质等质量接近饱和的溶液经过降温
1 3
后,能析出晶体且析出晶体最多的是________物质;
(2)当A、B、C三种物质的饱和溶液从t ℃降温到t ℃,所得的溶液中仍然是饱和溶液的是________两种物质的
3 1
溶液;
(3)称取A、B、C三种物质各30 g分别溶于100 g水中配成溶液,当温度控制在大于t ℃小于t ℃时,所得溶液中
1 2
溶质质量分数最大的是________物质的溶液。思路点拨:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;一定温度范围内,溶解度随温度变化趋势
越大,则析出晶体越多;(2)A、B的溶解度随温度的降低而减小,C的溶解度随温度的降低而增大,所以当A、B、C三
种物质的饱和溶液从t ℃降温到t ℃,所得的溶液中仍然是饱和溶液的是A和B;(3)观察图示可知:t ℃时A的溶
3 1 2
解度是30 g,当温度控制在大于t ℃小于t ℃时,A的溶解度最大是30 g,而B的溶解度始终大于30 g,C的溶解度
1 2
始终小于30 g,所以在此温度范围内,所得溶液中溶质质量分数最大的是B。
解答有关利用溶解度曲线问题时,要注意分清溶解度受温度影响的不同情况,再视具体情况分析,如饱和溶液与
不饱和溶液相互转化时,结晶时,分离混合物时都要注意“改变温度”时的不同现象与溶解度受温度影响程度有关。
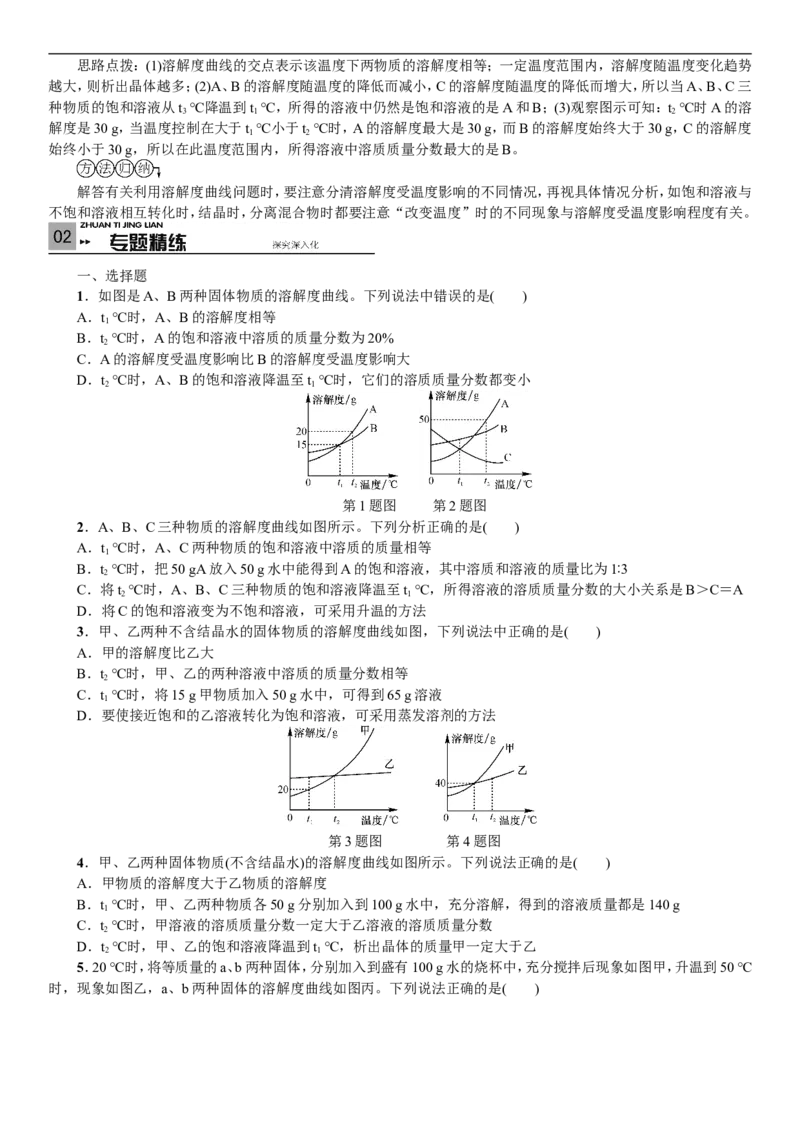
一、选择题
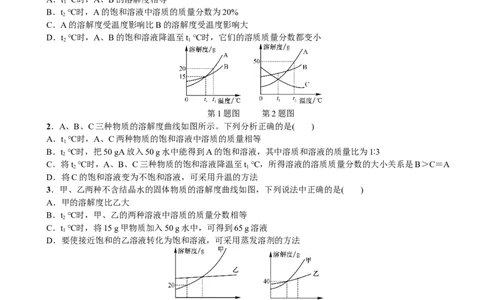
1.如图是A、B两种固体物质的溶解度曲线。下列说法中错误的是( )
A.t ℃时,A、B的溶解度相等
1
B.t ℃时,A的饱和溶液中溶质的质量分数为20%
2
C.A的溶解度受温度影响比B的溶解度受温度影响大
D.t ℃时,A、B的饱和溶液降温至t ℃时,它们的溶质质量分数都变小
2 1
第1题图 第2题图
2.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是( )
A.t ℃时,A、C两种物质的饱和溶液中溶质的质量相等
1
B.t ℃时,把50 gA放入50 g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3
2
C.将t ℃时,A、B、C三种物质的饱和溶液降温至t ℃,所得溶液的溶质质量分数的大小关系是B>C=A
2 1
D.将C的饱和溶液变为不饱和溶液,可采用升温的方法
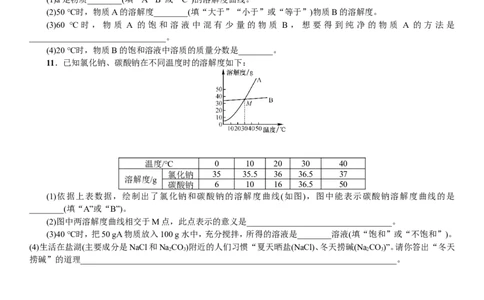
3.甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
A.甲的溶解度比乙大
B.t ℃时,甲、乙的两种溶液中溶质的质量分数相等
2
C.t ℃时,将15 g甲物质加入50 g水中,可得到65 g溶液
1
D.要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法
第3题图 第4题图
4.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t ℃时,甲、乙两种物质各50 g分别加入到100 g水中,充分溶解,得到的溶液质量都是140 g
1
C.t ℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
2
D.t ℃时,甲、乙的饱和溶液降温到t ℃,析出晶体的质量甲一定大于乙
2 1
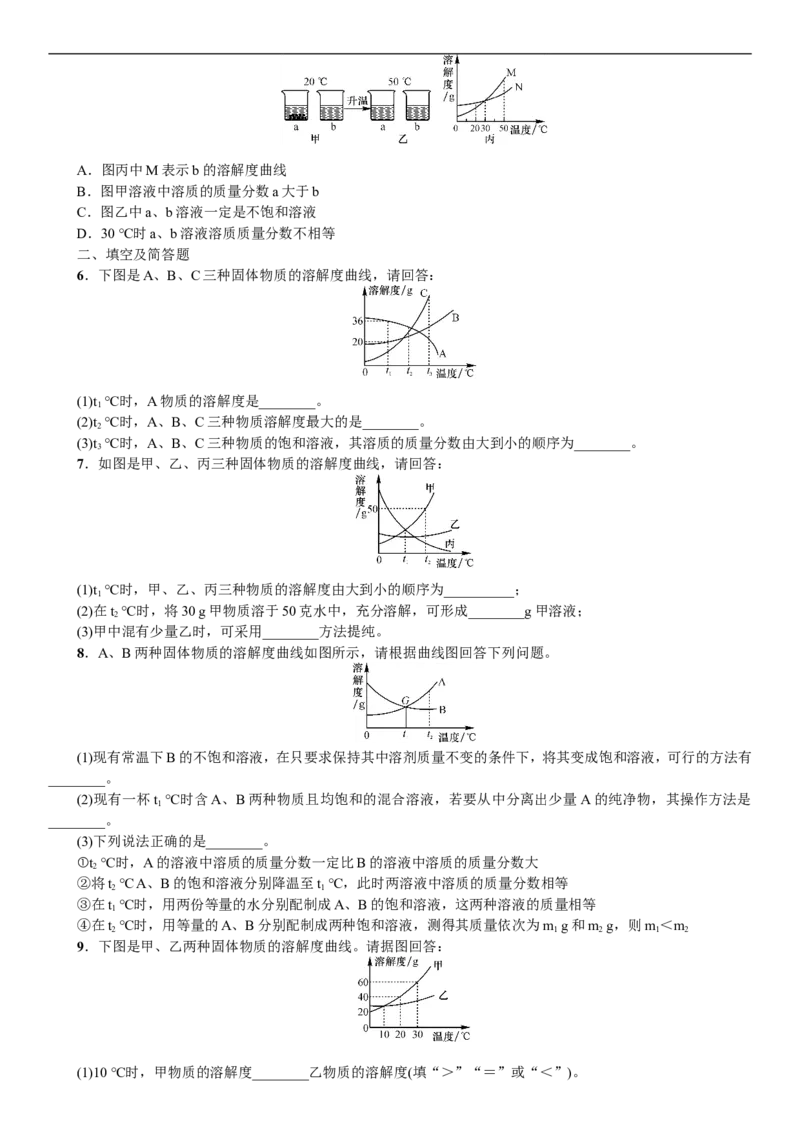
5.20 ℃时,将等质量的a、b两种固体,分别加入到盛有100 g水的烧杯中,充分搅拌后现象如图甲,升温到50 ℃
时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是( )A.图丙中M表示b的溶解度曲线
B.图甲溶液中溶质的质量分数a大于b
C.图乙中a、b溶液一定是不饱和溶液
D.30 ℃时a、b溶液溶质质量分数不相等
二、填空及简答题
6.下图是A、B、C三种固体物质的溶解度曲线,请回答:
(1)t ℃时,A物质的溶解度是________。
1
(2)t ℃时,A、B、C三种物质溶解度最大的是________。
2
(3)t ℃时,A、B、C三种物质的饱和溶液,其溶质的质量分数由大到小的顺序为________。
3
7.如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:
(1)t ℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为__________;
1
(2)在t ℃时,将30 g甲物质溶于50克水中,充分溶解,可形成________g甲溶液;
2
(3)甲中混有少量乙时,可采用________方法提纯。
8.A、B两种固体物质的溶解度曲线如图所示,请根据曲线图回答下列问题。
(1)现有常温下B的不饱和溶液,在只要求保持其中溶剂质量不变的条件下,将其变成饱和溶液,可行的方法有
________。
(2)现有一杯t ℃时含A、B两种物质且均饱和的混合溶液,若要从中分离出少量A的纯净物,其操作方法是
1
________。
(3)下列说法正确的是________。
①t ℃时,A的溶液中溶质的质量分数一定比B的溶液中溶质的质量分数大
2
②将t ℃ A、B的饱和溶液分别降温至t ℃,此时两溶液中溶质的质量分数相等
2 1
③在t ℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等
1
④在t ℃时,用等量的A、B分别配制成两种饱和溶液,测得其质量依次为m g和m g,则m<m
2 1 2 1 2
9.下图是甲、乙两种固体物质的溶解度曲线。请据图回答:
(1)10 ℃时,甲物质的溶解度________乙物质的溶解度(填“>”“=”或“<”)。(2)把30 ℃时等质量的甲、乙两物质的饱和溶液降温到10 ℃,析出晶体较多的是________。
(3)20 ℃时,将50 g甲物质放入盛有100 g水的烧杯中,最终所得溶液的质量为________g,若将烧杯内物质升温
到30 ℃(不考虑水蒸发),溶液中不变的是________(填序号)。
A.溶剂的质量 B.溶液的质量
C.溶质的质量分数 D.以上都不变
10.已知物质A的溶解度受温度影响较大,物质B的溶解度受温度影响较小,物质C的溶解度随温度升高而减
小(如图)。
(1)a是物质________(填“A”“B”或“C”)的溶解度曲线。
(2)50 ℃时,物质A的溶解度________(填“大于”“小于”或“等于”)物质B的溶解度。
(3)60 ℃ 时 , 物 质 A 的 饱 和 溶 液 中 混 有 少 量 的 物 质 B , 想 要 得 到 纯 净 的 物 质 A 的 方 法 是
________________________________。
(4)20 ℃时,物质B的饱和溶液中溶质的质量分数是________。
11.已知氯化钠、碳酸钠在不同温度时的溶解度如下:
温度/℃ 0 10 20 30 40
氯化钠 35 35.5 36 36.5 37
溶解度/g
碳酸钠 6 10 16 36.5 50
(1)依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如图),图中能表示碳酸钠溶解度曲线的是
________(填“A”或“B”)。
(2)图中两溶解度曲线相交于M点,此点表示的意义是__________________________________。
(3)40 ℃时,把50 gA物质放入100 g水中,充分搅拌,所得的溶液是________溶液(填“饱和”或“不饱和”)。
(4)生活在盐湖(主要成分是NaCl和NaCO)附近的人们习惯“夏天晒盐(NaCl)、冬天捞碱(Na CO)”。请你答出“冬天
2 3 2 3
捞碱”的道理__________________________________________________________________________。
参考答案
归类例析例1 (1)在t ℃时,甲、丙两种物质的溶解度相等 (2)28.6% (3)降温结晶法
例2 (1)A、C A (2)A、B (3)B
专题精练
1.B 2.B 3.D 4.B 5.C 6.(1)36 g (2)A (3)C>B>A 7.(1)甲=丙>乙 (2)75 (3)降温结晶 8.(1)加入
溶质 (2)降温结晶 (3)③④ 9.(1)= (2)甲 (3)140 A 10.(1)A (2)等于 (3)降温结晶(或冷却热饱和溶液法)
(4)23.1% 11.(1)A (2)30 ℃时,两物质的溶解度相等 (3)饱和 (4)冬天温度低,碳酸钠易结晶析出,而氯化钠的溶
解度变化小不析出