文档内容
、
滚动小专题(一)气体的制备与净化
一、实验室制取气体的思路和方法
1.选择适当的反应,包括反应物和反应条件。
2.选择合适的实验装置:选择气体发生装置要考虑反应物的状态和反应条件
反应物的状态 固体 固体与液体
反应条件 加热 不需加热
固液不加热制气装置
装置示意图
制取较多 可随时 可连续制取并 可控制反应的
量的气体 添加液体 控制反应速率 终止与发生
制取气体举例 加热高锰酸钾制O 实验室制取CO、H,过氧化氢制O
2 2 2 2
【温馨提示】选择气体收集装置
密度比空气大——向上排空法
排空气法
密度比空气小——向下排空法
排水法——不易溶于水、不与水反应
3.验证所制得的气体。
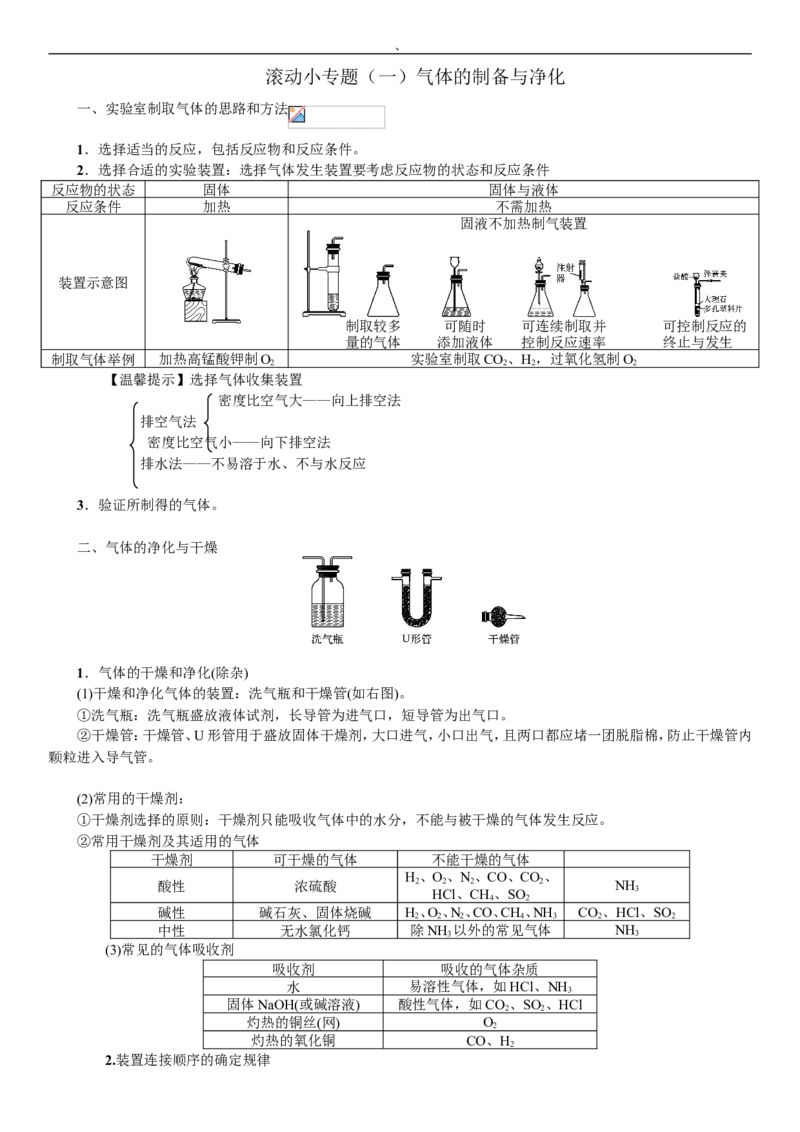
二、气体的净化与干燥
1.气体的干燥和净化(除杂)
(1)干燥和净化气体的装置:洗气瓶和干燥管(如右图)。
①洗气瓶:洗气瓶盛放液体试剂,长导管为进气口,短导管为出气口。
②干燥管:干燥管、U形管用于盛放固体干燥剂,大口进气,小口出气,且两口都应堵一团脱脂棉,防止干燥管内
颗粒进入导气管。
(2)常用的干燥剂:
①干燥剂选择的原则:干燥剂只能吸收气体中的水分,不能与被干燥的气体发生反应。
②常用干燥剂及其适用的气体
干燥剂 可干燥的气体 不能干燥的气体
H、O、N、CO、CO、
酸性 浓硫酸 2 2 2 2 NH
HCl、CH、SO 3
4 2
碱性 碱石灰、固体烧碱 H、O、N、CO、CH、NH CO、HCl、SO
2 2 2 4 3 2 2
中性 无水氯化钙 除NH 以外的常见气体 NH
3 3
(3)常见的气体吸收剂
吸收剂 吸收的气体杂质
水 易溶性气体,如HCl、NH
3
固体NaOH(或碱溶液) 酸性气体,如CO、SO 、HCl
2 2
灼热的铜丝(网) O
2
灼热的氧化铜 CO、H
2
2.装置连接顺序的确定规律、
气体净化除杂原则:不减少被净化的气体,不能引进新的杂质。
(1)除杂和干燥的先后顺序
①若用洗气装置除杂,一般除杂在前,干燥在后。原因:从溶液中出来的气体肯定混有水蒸气,干燥在后可将水
蒸气完全除去。如除去CO中混有的CO 和水蒸气,应将气体先通过NaOH溶液,再通过浓HSO 。
2 2 4
②若用加热装置除杂,一般是干燥在前,除杂在后。原因:加热时气体中最好不混有水蒸气。如除去CO 中混有
2
的CO和水蒸气,应将气体先通过浓HSO ,再通过灼热的CuO。
2 4
(2)除去多种杂质气体的顺序
一般是酸性较强的气体先除去。如N 中混有HCl、HO(气)、O 时,应先除去HCl,再除去HO(气),最后除去
2 2 2 2
O(用灼热的铜网)。
2
(3)检验多种气体的先后顺序(一般先验水)
有多种气体需要检验时,应尽量避免前步检验对后步检验的干扰。如被检验的气体中含有CO 和水蒸气时,应先
2
通过无水CuSO 检验水蒸气(由白色变成蓝色,说明有水蒸气存在),再通过澄清的石灰水检验CO。
4 2
3.尾气处理装置
(1)溶液吸收,如酸性的HCl、SO 气体可用NaOH溶液吸收。
2
(2)点燃尾气,如CO、CH 等可燃性污染物可接一尖嘴导管,将其点燃而烧掉。
4
(3)尾气回收,即在装置末端导管上接上气球或塑料袋等将尾气收集,如回收CO。
类型1 常见气体的制取
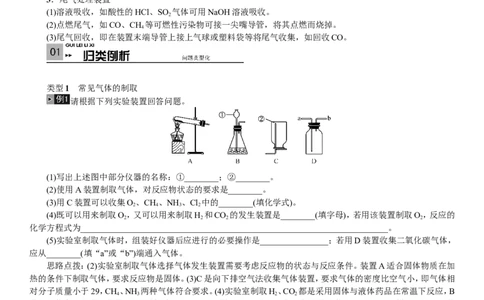
请根据下列实验装置回答问题。
(1)写出上述图中部分仪器的名称:①________;②________。
(2)使用A装置制取气体,对反应物状态的要求是________。
(3)用C装置可以收集O、CH、NH 、Cl 中的________(填化学式)。
2 4 3 2
(4)既可以用来制取O,又可以用来制取H 和CO 的发生装置是________(填字母),若用该装置制取O,反应的
2 2 2 2
化学方程式为________________________________________________________________________。
(5)实验室制取气体时,组装好仪器后应进行的必要操作是________________;若用D装置收集二氧化碳气体,
应从________(填“a”或“b”)端通入气体。
思路点拨:(2)实验室制取气体选择气体发生装置需要考虑反应物的状态与反应条件。装置A适合固体物质在加
热的条件下制取气体,要求反应物是固体。(3)C是向下排空气法收集气体装置,要求气体的密度比空气小,即气体相
对分子质量小于29,CH、NH 两种气体符合要求。(4)实验室制取H、CO 都是采用固体与液体药品在常温下反应,B
4 3 2 2
装置可作发生装置,若用该装置制取氧气,需要用过氧化氢溶液在二氧化锰的催化作用下反应。(5)制取气体时组装
好仪器后必须要检查装置的气密性。二氧化碳的密度比空气大,若用D装置排空气法收集,气体应从a端通入。
类型2 气体的净化与干燥
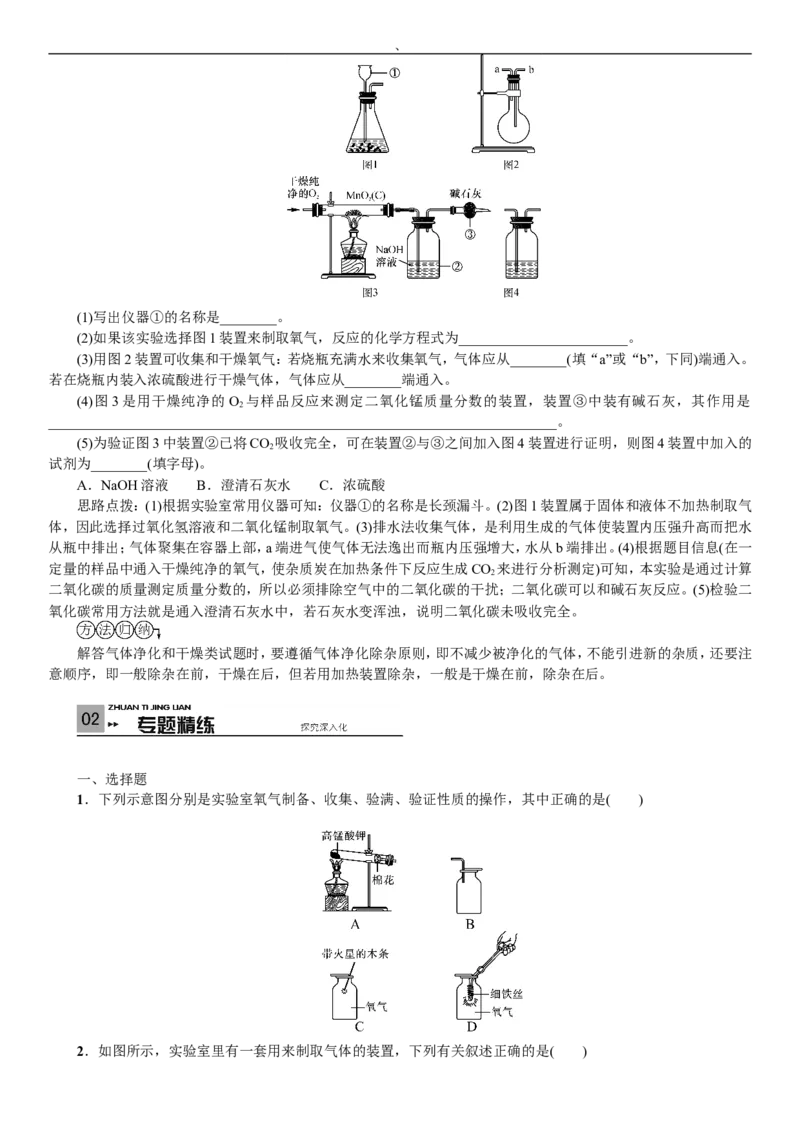
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方
案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO 来进行分析测定。
2、
(1)写出仪器①的名称是________。
(2)如果该实验选择图1装置来制取氧气,反应的化学方程式为________________________。
(3)用图2装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从________(填“a”或“b”,下同)端通入。
若在烧瓶内装入浓硫酸进行干燥气体,气体应从________端通入。
(4)图3是用干燥纯净的O 与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是
2
________________________________________________________________________。
(5)为验证图3中装置②已将CO 吸收完全,可在装置②与③之间加入图4装置进行证明,则图4装置中加入的
2
试剂为________(填字母)。
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
思路点拨:(1)根据实验室常用仪器可知:仪器①的名称是长颈漏斗。(2)图1装置属于固体和液体不加热制取气
体,因此选择过氧化氢溶液和二氧化锰制取氧气。(3)排水法收集气体,是利用生成的气体使装置内压强升高而把水
从瓶中排出;气体聚集在容器上部,a端进气使气体无法逸出而瓶内压强增大,水从b端排出。(4)根据题目信息(在一
定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO 来进行分析测定)可知,本实验是通过计算
2
二氧化碳的质量测定质量分数的,所以必须排除空气中的二氧化碳的干扰;二氧化碳可以和碱石灰反应。(5)检验二
氧化碳常用方法就是通入澄清石灰水中,若石灰水变浑浊,说明二氧化碳未吸收完全。
解答气体净化和干燥类试题时,要遵循气体净化除杂原则,即不减少被净化的气体,不能引进新的杂质,还要注
意顺序,即一般除杂在前,干燥在后,但若用加热装置除杂,一般是干燥在前,除杂在后。
一、选择题
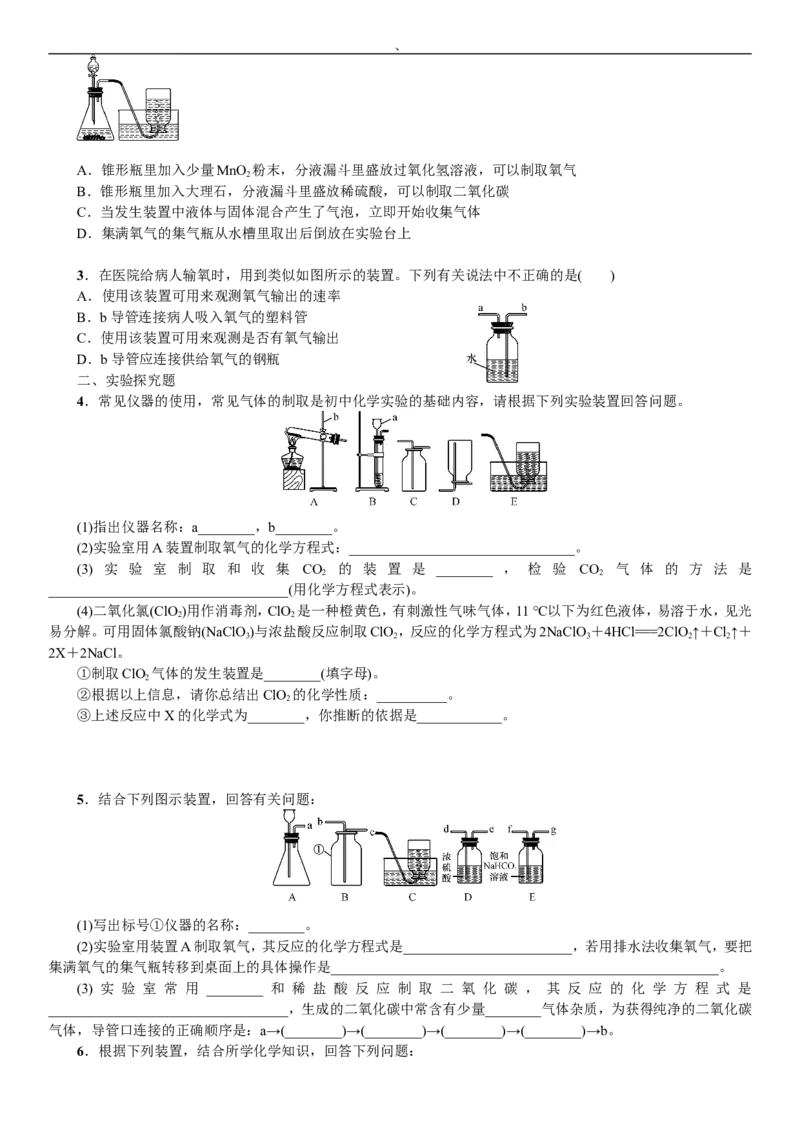
1.下列示意图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是( )
2.如图所示,实验室里有一套用来制取气体的装置,下列有关叙述正确的是( )、
A.锥形瓶里加入少量MnO 粉末,分液漏斗里盛放过氧化氢溶液,可以制取氧气
2
B.锥形瓶里加入大理石,分液漏斗里盛放稀硫酸,可以制取二氧化碳
C.当发生装置中液体与固体混合产生了气泡,立即开始收集气体
D.集满氧气的集气瓶从水槽里取出后倒放在实验台上
3.在医院给病人输氧时,用到类似如图所示的装置。下列有关说法中不正确的是( )
A.使用该装置可用来观测氧气输出的速率
B.b导管连接病人吸入氧气的塑料管
C.使用该装置可用来观测是否有氧气输出
D.b导管应连接供给氧气的钢瓶
二、实验探究题
4.常见仪器的使用,常见气体的制取是初中化学实验的基础内容,请根据下列实验装置回答问题。
(1)指出仪器名称:a________,b________。
(2)实验室用A装置制取氧气的化学方程式:________________________________。
(3) 实 验 室 制 取 和 收 集 CO 的 装 置 是 ________ , 检 验 CO 气 体 的 方 法 是
2 2
__________________________________(用化学方程式表示)。
(4)二氧化氯(ClO )用作消毒剂,ClO 是一种橙黄色,有刺激性气味气体,11 ℃以下为红色液体,易溶于水,见光
2 2
易分解。可用固体氯酸钠(NaClO)与浓盐酸反应制取ClO ,反应的化学方程式为2NaClO+4HCl===2ClO ↑+Cl↑+
3 2 3 2 2
2X+2NaCl。
①制取ClO 气体的发生装置是________(填字母)。
2
②根据以上信息,请你总结出ClO 的化学性质:__________。
2
③上述反应中X的化学式为________,你推断的依据是____________。
5.结合下列图示装置,回答有关问题:
(1)写出标号①仪器的名称:________。
(2)实验室用装置A制取氧气,其反应的化学方程式是________________________,若用排水法收集氧气,要把
集满氧气的集气瓶转移到桌面上的具体操作是_______________________________________________________。
(3) 实 验 室 常 用 ________ 和 稀 盐 酸 反 应 制 取 二 氧 化 碳 , 其 反 应 的 化 学 方 程 式 是
__________________________________,生成的二氧化碳中常含有少量________气体杂质,为获得纯净的二氧化碳
气体,导管口连接的正确顺序是:a→(________)→(________)→(________)→(________)→b。
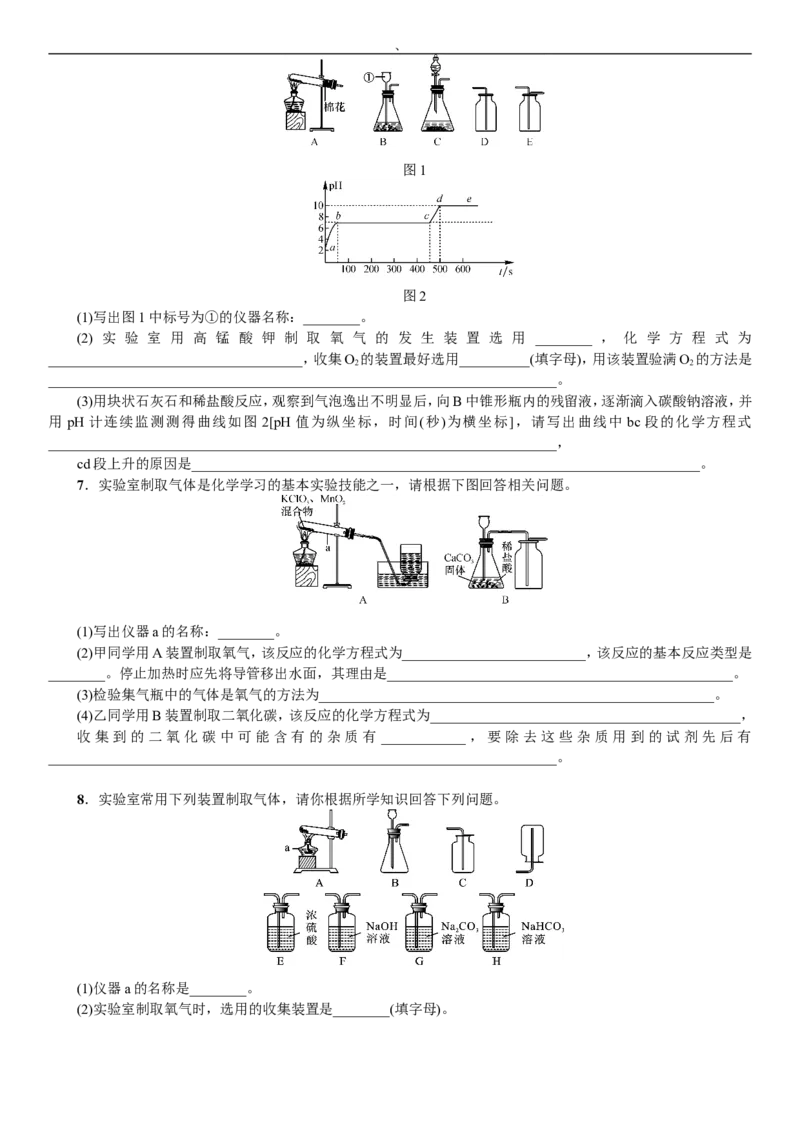
6.根据下列装置,结合所学化学知识,回答下列问题:、
图1
图2
(1)写出图1中标号为①的仪器名称:________。
(2) 实 验 室 用 高 锰 酸 钾 制 取 氧 气 的 发 生 装 置 选 用 ________ , 化 学 方 程 式 为
____________________________________,收集O 的装置最好选用__________(填字母),用该装置验满O 的方法是
2 2
________________________________________________________________________。
(3)用块状石灰石和稀盐酸反应,观察到气泡逸出不明显后,向B中锥形瓶内的残留液,逐渐滴入碳酸钠溶液,并
用 pH 计连续监测测得曲线如图 2[pH 值为纵坐标,时间(秒)为横坐标],请写出曲线中 bc 段的化学方程式
________________________________________________________________________,
cd段上升的原因是________________________________________________________________________。
7.实验室制取气体是化学学习的基本实验技能之一,请根据下图回答相关问题。
(1)写出仪器a的名称:________。
(2)甲同学用A装置制取氧气,该反应的化学方程式为__________________________,该反应的基本反应类型是
________。停止加热时应先将导管移出水面,其理由是_________________________________________________。
(3)检验集气瓶中的气体是氧气的方法为________________________________________________________。
(4)乙同学用B装置制取二氧化碳,该反应的化学方程式为____________________________________________,
收集到的二氧化碳中可能含有的杂质有 ____________,要除去这些杂质用到的试剂先后有
________________________________________________________________________。
8.实验室常用下列装置制取气体,请你根据所学知识回答下列问题。
(1)仪器a的名称是________。
(2)实验室制取氧气时,选用的收集装置是________(填字母)。、
若改用右图装置收集氧气,则气体应从________(填“a”或“b”)进。
(3)小明取一定浓度的盐酸与石灰石反应制取气体,反应的化学方程式为
________________________________________________________________________;
将生成的气体通入澄清石灰水中,未见变浑浊。为探究其原因,进行了如下过程:
【作出猜想】A.石灰水已经完全变质;B.气体中有挥发出来的HCl气体。
【实验探究】
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色。于是排除了猜想A,你
认为排除猜想A的理由是________________________________________________________________________
________________________________________________________________________。
②小明想探究所得气体中是否有挥发出来的HCl气体,设计如下实验。请你帮他完成实验,填写以下表格:
实验步骤 实验现象 实验结论
将生成的气体________________中 产生________ 气体中有HCl
【查阅资料】
碳酸钠溶液中通入二氧化碳发生反应:NaCO+CO+HO===2NaHCO
2 3 2 2 3
【拓展延伸】
如果用上述原料制得纯净的二氧化碳气体,所选仪器的连接顺序为________(填字母)。
参考答案、
归类例析
例1 (1)长颈漏斗 集气瓶 (2)固体 (3)CH 、NH (4)B 2HO=====2HO+O↑ (5)检查装置的气密性
4 3 2 2 2 2
a
例2 (1)长颈漏斗 (2)2H O=====2HO+O↑ (3)a b (4)防止空气中的二氧化碳进入②中,影响测定结果
2 2 2 2
(5)B
专题精练
1.A 2.A 3.B 4.(1)长颈漏斗 铁架台 (2)2KMnO=====KMnO +MnO +O↑ (3)BC CO +
4 2 4 2 2 2
Ca(OH) ===CaCO ↓+HO (4)B 见光易分解 HO 质量守恒定律 5.(1)集气瓶 (2)2H O=====2HO+O↑
2 3 2 2 2 2 2 2
在水中,用玻璃片的磨砂一面盖住瓶口,轻轻移出水面,正放即可 (3)石灰石(或大理石) CaCO +2HCl===CaCl +
3 2
CO↑+HO HCl f g d e 6.(1)长颈漏斗 (2)A 2KMnO =====KMnO +MnO +O↑ E 将带火星的木
2 2 4 2 4 2 2
条放在集气瓶口,木条复燃,证明氧气收集满了 (3)Na CO+CaCl ===CaCO ↓+2NaCl 碳酸钠溶液显碱性 7.(1)
2 3 2 3
试管 (2)2KClO =====2KCl+3O↑ 分解反应 防止水倒吸,使试管炸裂 (3)将带火星的木条伸入到集气瓶中,
3 2
木条复燃则说明集气瓶中的气体是氧气 (4)CaCO +2HCl===CaCl +CO↑+HO HCl和HO 饱和NaHCO 溶
3 2 2 2 2 3
液、浓硫酸 8.(1)酒精灯 (2)C b CaCO +2HCl===CaCl +CO↑+HO 【实验探究】①酚酞试液变红,说明溶
3 2 2 2
液中存在碱性物质Ca(OH) ②通入AgNO 溶液 白色沉淀 【拓展延伸】BHEC
2 3