文档内容
【同步教育信息】本周教学内容:化学计算
[复习指导]: 1. 抓好基础知识。 2. 抓好解题的基本环节。
3. 抓解题的规范 4. 加强练习,注意一题多解。
【复习内容】
一、有关化学式的计算:
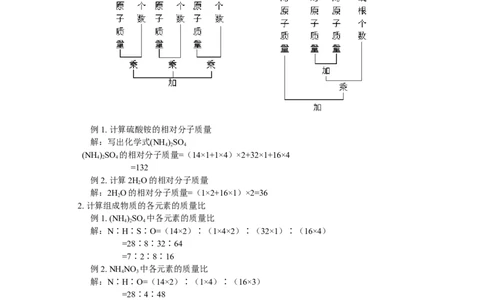
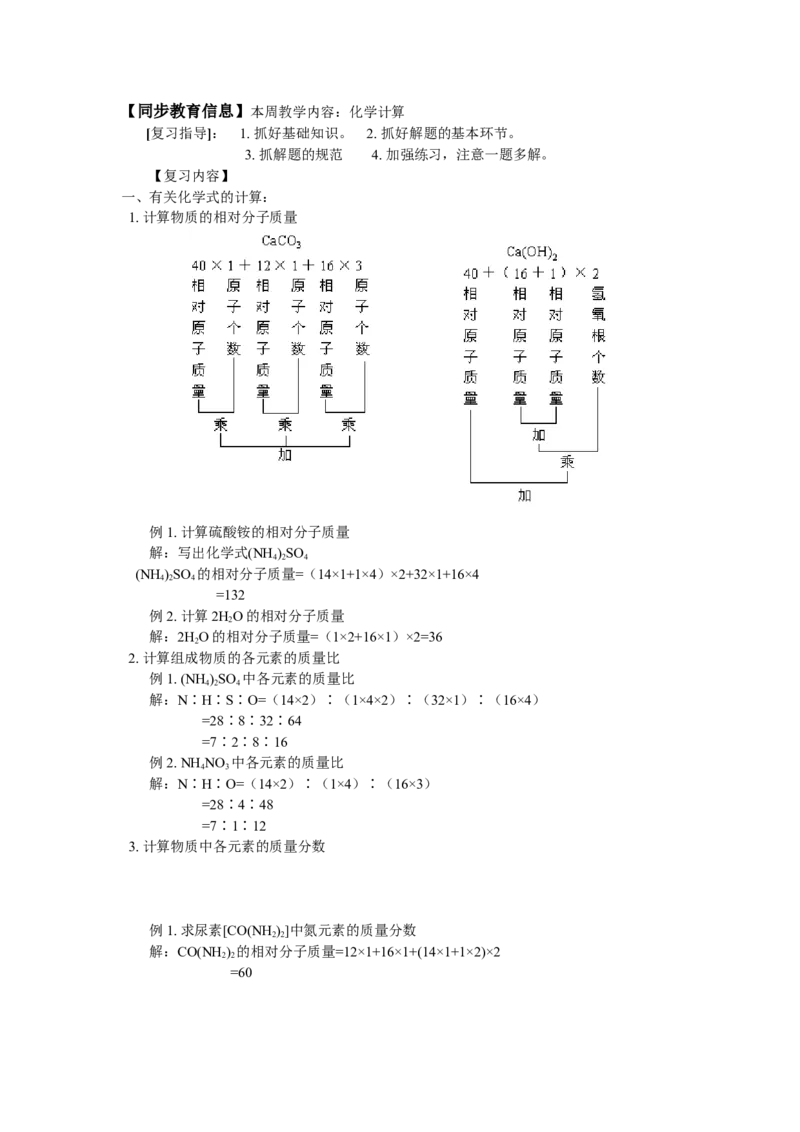
1. 计算物质的相对分子质量
例1. 计算硫酸铵的相对分子质量
解:写出化学式(NH )SO
4 2 4
(NH )SO 的相对分子质量=(14×1+1×4)×2+32×1+16×4
4 2 4
=132
例2. 计算2HO的相对分子质量
2
解:2HO的相对分子质量=(1×2+16×1)×2=36
2
2. 计算组成物质的各元素的质量比
例1. (NH )SO 中各元素的质量比
4 2 4
解:N∶H∶S∶O=(14×2)∶(1×4×2)∶(32×1)∶(16×4)
=28∶8∶32∶64
=7∶2∶8∶16
例2. NH NO 中各元素的质量比
4 3
解:N∶H∶O=(14×2)∶(1×4)∶(16×3)
=28∶4∶48
=7∶1∶12
3. 计算物质中各元素的质量分数
例1. 求尿素[CO(NH)]中氮元素的质量分数
2 2
解:CO(NH) 的相对分子质量=12×1+16×1+(14×1+1×2)×2
2 2
=60例2. 有一不纯净的硫酸铵样品,经分析知道它的含氮量为20%,求该样品中含硫酸铵的
质量分数
解法1:设100g样品中,含氮20g的硫酸铵的质量为x。
关系式 (NH )SO ~ 2N
4 2 4
关系量 132 28
x 20g
解法2:设样品中含(NH )SO 为x%
4 2 4
100% 21%
x% 20%
答:样品中含硫酸铵94.3%。
二、有关化学方程式的计算
例1. 电解9克水可以得到多少克氢气?
解:设可得到氢气的质量为x ①设未知量
2×18=36 1×2×2=4 ③写出相关物质的相对分子质量和已知量未知量
9克(纯净物) x
x=1g ④列出比例式,求解
答:得到1克氢气 ⑤简明地写出答案
例2. 有一种含水的过氧化氢样品10g,在二氧化锰的催化作用下,完全分解得到3.2g氧
气,试求该过氧化氢的质量分数
解:设样品中含有过氧化氢的质量为x68 32
x 3.2g
x=6.8g
答:该样品中过氧化氢的质量分数为68%
例3. 碳酸钙与氧化钙组成的混合物100g,测得其中钙元素质量分数为46.25%,在高温
条件下煅烧,生成的气体完全被足量的澄清石灰水吸收,称得石灰水增重 35.2g,已知
Ar(O)=16,试计算:
(1)钙元素的相对原子质量:(精确到0.01)
(2)原混合物中碳酸钙的质量分数(精确到0.01%)
解:(1)剩余固体即CaO的质量为:100g-35.2g=64.8g
设Ca的相对原子质量为x
x=39.89
Ca的相对原子质量为39.89
(2)设原混合物中CaCO 的质量为x
3
99.89 44
x 35.2g
x=79.91g
答:(1)Ca的相对原子质量为39.89 (2)原混合物中CaCO 的质量分数为79.91%
3【模拟试题】
一、选择题
Cl—35.5 O—16 Fe—56 C—12 Mg—24 N—14 H—1 S—32 Ca—40 Mn—55
1. 自1974年以来,已发现在饮水中加氯会促使一系列致癌物产生。因此,世界各国正积极
开发高效安全的二氧化氯杀菌消毒剂。二氧化氯的相对分子质量是( )
A. 51.5 B. 67.5 C. 87 D. 103
2. 血红蛋白的相对分子质量68000,含铁的质量分数为0.33%,则平均每个血红蛋白分子中
铁原子的个数是( )
A. 1 B. 2 C. 3 D. 4
3. 等质量的CO和CO 中,碳元素的质量比为( )
2
A. 1∶1 B. 11∶7 C. 7∶11 D. 11∶14
4. 下列计算错误的是( )。
A. Mg(OH) 的相对分子质量:24+(16+1)×2=58
2
B. SO 中硫元素与氧元素的质量比:1∶1
2
C. NH NO 中氮元素的质量分数:
4 3
D. 18g水(HO)中含氢元素的质量:
2
5. 我国在1993年成功制取了一种由相对原子质量为18、核电荷数为8的氧原子构成的双
原子分子,则下列说法正确的是( )
A. 这种气体的相对分子质量为32
B. 这种氧原子与氢原子构成的水分子的相对分子质量为20
C. 这种氧离子的核内质子数为10
D. 这种氧原子核外电子数为10
6. 有一种碳的氧化物,其中碳元素与氧元素的质量比为3∶4,则此碳的氧化物中碳元素的
化合价为( )
A. +2价 B. +1价 C. 0价 D. +4价
7. 已知CO气体和某气体混合物中,测得氧元素的质量分数为55%,则该气体可能是(
)
A. CO B. SO C. NO D. N O
2 2 2 2 5
8. 镁在氧气中反应生成氧化镁。在此反应中,如生成氧化镁5g,则参加反应的镁与氧气的质
量比是( )。
A. 1∶4 B. 2∶3 C. 3∶2 D. 4∶1
9. 二氧化硫是污染空气的气体。某工厂每天燃烧含硫质量分数为0.02%的煤10t,设煤中的
硫全部转为二氧化硫,则该厂每天产生的二氧化硫的质量是( )
A. 0.2g B. 2000g C. 0.4g D. 4000g
10. 碳和碳酸钙的混合物在空气中受强热后,碳酸钙完全分解,碳完全氧化,若生成二氧化
碳的总质量等于混合物的总质量,则混合物中碳的质量分数约为( )。
A. 82.6% B. 42% C. 21% D. 17.4%
二、填空题
1. 我国瓷都——江西景德镇生产的瓷器在世界上享有盛誉。景德镇的高岭土[主要成分
Al (Si O)(OH) ]是制造瓷器的优良原料。在Al (Si O)(OH) 中氢元素与氧元素的质量比为
2 2 5 4 2 2 5 4
____________。2. 天旱时,可用单级小火箭发射碘化银进行人工降雨。小火箭使用的主要燃料名叫“偏二
甲肼”。现取3.0g偏二甲肼在O 中充分燃烧后生成4.4gCO 、3.6gH O和1.4gN 三种物质,
2 2 2 2
由此可知偏二甲肼由__________种元素组成,其中碳元素的质量分数为___________。偏二
甲肼的相对分子质量为60,则其化学式为_________。
3. 实验室用高锰酸钾制取氧气。
(1)求反应中各物质间的质量比:_________________。
(2)若要制得8g氧气,最少需要高锰酸钾的质量为_________________g。
(3)反应完全后,混合物中氧化物的质量分数为________________。
三、计算题:
1. 黄曲霉素AFTB(化学式为C H O)是污染粮食(大米、花生等)的真菌霉素,人类的特殊
17 12 6
基因在黄曲霉素作用下会发生突变,继而转变为肝癌。
(1)黄曲霉素AFTB由几种元素组成?
(2)黄曲霉素AFTB分子中共有多少个原子?
(3)黄曲霉素AFTB的相对分子质量是多少?
(4)黄曲霉素AFTB分子中氧元素的质量分数是多少?
2. 一种氮的氧化物是早已被发现的古老分子,但自1987年发现它在人体内具有许多重要的
生理功能后,才备受青睐,被学术界评为1992年的明星分子,经测定在90g这种氮的氧化物
中含氮元素42g,计算求此氮的氧化物的化学式。
3. 人体缺钙易产生“骨质疏松症”。一体重为60kg的缺钙病人每天除从食物中获得钙质外,
还需从药物中补充钙质0.5g,若医生确定此人每天至少吃某种钙片6.25g,且知该钙片中的
有效成分为葡萄糖酸钙[(C H O)Ca]。试求该钙片中葡萄糖酸钙的质量分数是多少?
6 11 7 2
[(C H O)Ca的相对分子质量为430,计算结果保留两位小数]
6 11 7 2
4. 将3.6g CaCO 高温煅烧一段时间后冷却,测得固体剩余物中钙元素的质量分数为57.6%,
3
求固体剩余物中氧化钙的质量。(结果保留一位小数)
5. 已知 。现有镁和碳酸镁组成的混合物a g,当在空气中煅烧
至质量不再改变为止,冷却后称得剩余固体质量是原混合物的一半,求原混合物中镁和碳酸
镁的质量比。【试题答案】
一、选择题
1. B 2. D 3. D 4. C 5. B
6. A 7. B 8. C 9. D 10. D
二、填空:
1. 1∶36
2. 三种;40%;CHN
4
3. (1)316∶197∶87∶32 (2)79g (3)30.6%
三、计算题:
1. (1)三种;(2)35个;(3)312;(4)30.8%
2. NO
3. 86%
4. 1.4g
5. 1∶49
年级 初三 学科 化学 版本 人教实验版 期数 009
内容标题 化学计算
分类索引号 C.901 分类索引描述 学习资料
主题词 化学计算 栏目名称 同步课堂
编稿老师 华敏 审稿老师