文档内容
第三单元 物质构成的奥秘 课题 3 元素(第一课时)
教学目标:
知识与技能:
(1)了解元素的概念,将对物质的宏观组成与微观结构的认识统一起来;
(2)了解元素符号所表示的意义,学会元素符号的正确写法,逐步记住一些常见的元素符
号;
过程与方法: 学习运用对比的方法获取信息;
情感态度与价值观 逐步积累化学用语,真正进入一个化学世界。
重点:元素的概念、元素符号的书写和意义
难点: 元素概念的形成,元素符号的书写和意义,
教学方法:探究讨论法
教学过程:
一、课前复习:(提问方式,3分钟)
1、什么是分子?什么是原子?其本质区别是什么?
2、什么是原子相对质量?
二、导入新课:
利用相对原子质量概念“以一种碳原子……”这种碳原子指的是原子核内有6个质子
和6个中子的碳—12,此外还有质子数为6而中子数为7的碳—13,还有质子数为6而中子
数为8的碳—14,这是三种不同的碳原子,它们核内的中子数虽不同,但它们的核电荷数(即
质子数)都是6,凡是核电荷数(即质子数)相同的原子为同一类原子,这些同一类原子总称
为元素(即碳元素)
三、讲授新课:
一、元素(板书)
讲解:无论是木炭中的碳原子,还是二氧化碳分子里的碳原子,它们的核电荷数(即质子数)
都是6,说明它们都含有碳元素。又如:二氧化碳分子里的氧原子与氧气分子中的氧原
子其核电荷数都是8,称为氧元素。
提问:二氧化碳是由几种元素组成?(四氧化三铁、氯酸钾呢?)
小结:1、元素概念:见课文第73页(板书)
讲解:核电荷数(质子数)决定元素的种类。目前已发现的元素有一百余种,物质三千多万种,
这千千万万物质都是由一百多种元素组成的。元素只论种类,不论个数。
讲解:根据我国文字的形象化,讲解这一百余种元素分为金属元素、非金属元素。
小结:2、元素 { 金属元素:如:Na、Mg、Al、Zn、Fe、……
非金属元素:如:C、Si、S、P、Cl、N、…… (板书)
阅读:课本第73页图4-4,找出地壳中含量最多的两种非金属元素和两种金属元素。
3、元素的读法、写法(板书)
讲解:略
4、元素符号的意义:
讲解:元素符号的意义:表示一种元素,表示这种元素的一个原子。
如: 表示氢元素
H
表示一个原子
提问:如何表示几个原子呢?
小结:元素符号前边的化学计量数表示原子个数如:2H 表示两个氢原子
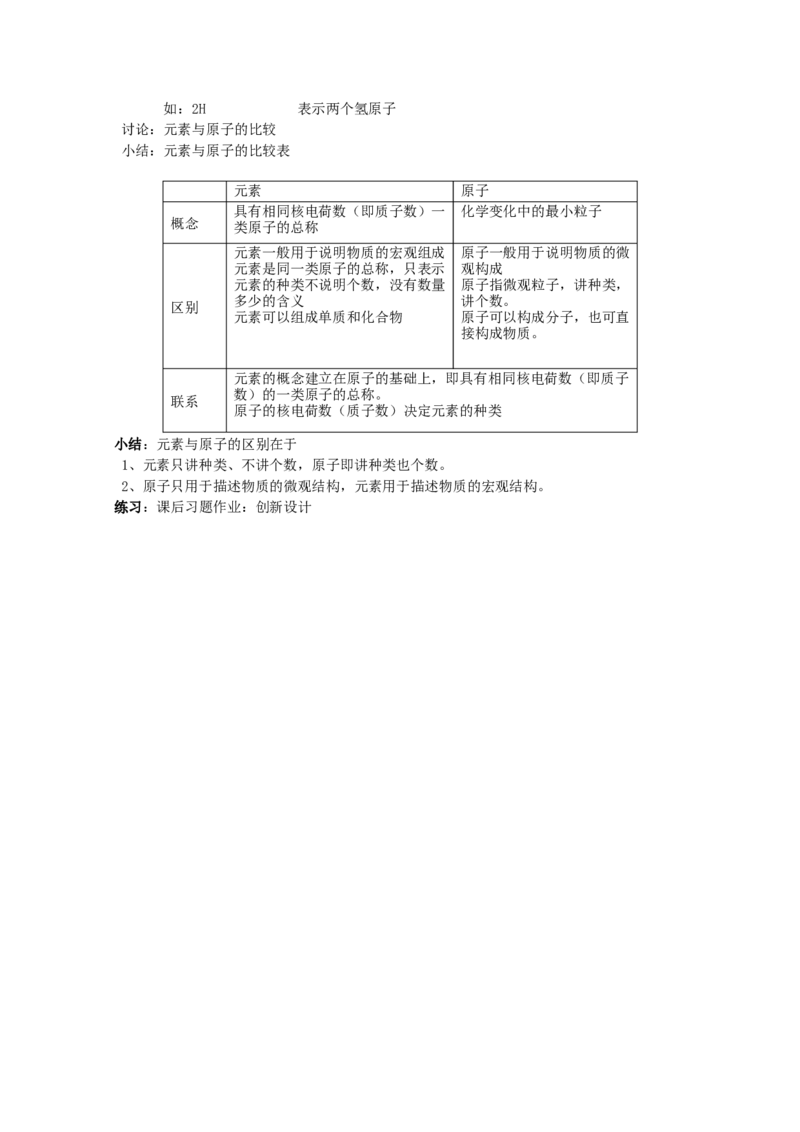
讨论:元素与原子的比较
小结:元素与原子的比较表
元素 原子
具有相同核电荷数(即质子数)一 化学变化中的最小粒子
概念 类原子的总称
元素一般用于说明物质的宏观组成 原子一般用于说明物质的微
元素是同一类原子的总称,只表示 观构成
元素的种类不说明个数,没有数量 原子指微观粒子,讲种类,
多少的含义 讲个数。
区别
元素可以组成单质和化合物 原子可以构成分子,也可直
接构成物质。
元素的概念建立在原子的基础上,即具有相同核电荷数(即质子
数)的一类原子的总称。
联系
原子的核电荷数(质子数)决定元素的种类
小结:元素与原子的区别在于
1、元素只讲种类、不讲个数,原子即讲种类也个数。
2、原子只用于描述物质的微观结构,元素用于描述物质的宏观结构。
练习:课后习题作业:创新设计