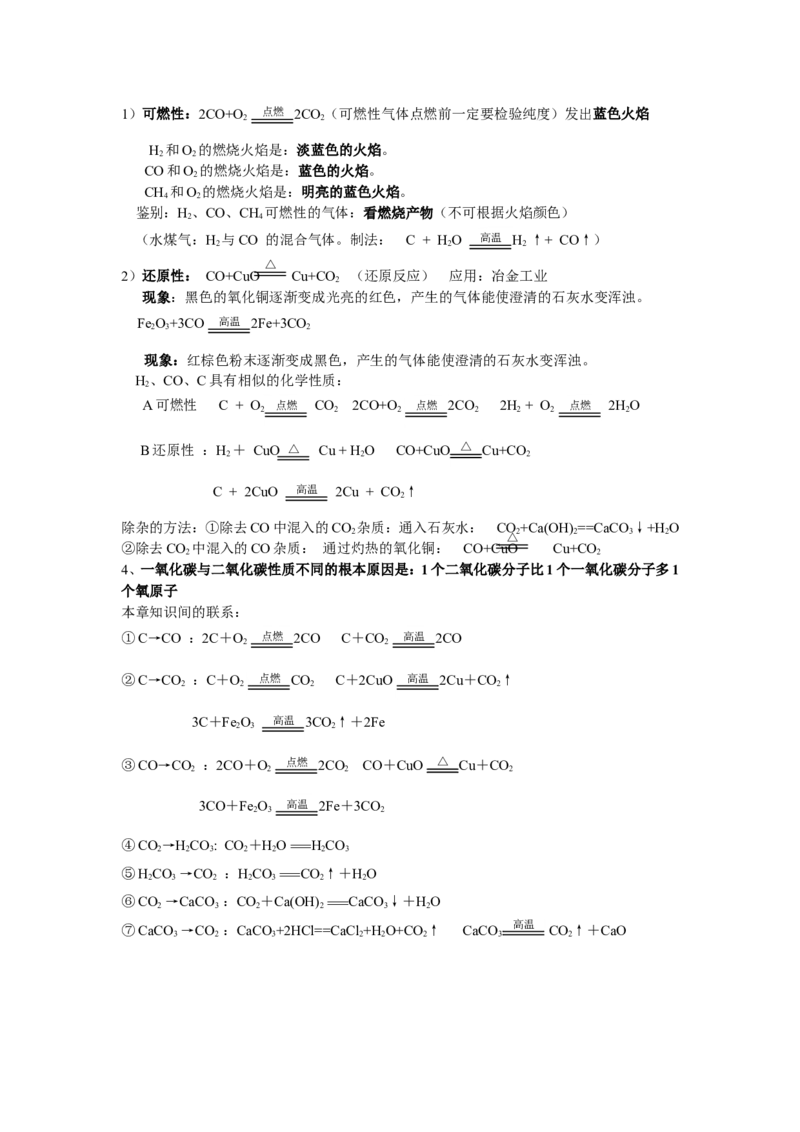文档内容
第六单元 碳和碳的氧化物
课题1 金刚石、石墨和C
60
一、碳的几种单质(金刚石、石墨、C )
60
1、金刚石(C)是自然界中最硬的物质,无色透明,正八面体。可用于制钻石、刻划玻璃、钻探
机的钻头(体现了它的硬度大)等。
2、石墨(C)是最软的矿物之一,深灰色,具有金属光泽,细鳞片状的固体,有优良的导电性,
润滑性。可用于制铅笔芯(体现了它深灰色、质软)、干电池的电极(体现了它的导电性)、电
车的电刷(体现了它的导电性,润滑性、常温下化学性质稳定)、做固体润滑剂(体现它具有润
滑性)等
金刚石和石墨的物理性质有很大差异的原因是:碳原子的排列不同。
3、无定形碳:由石墨的微小晶体和少量杂质构成.主要有:焦炭,木炭,活性炭,炭黑等.
活性炭、木炭具有强烈的吸附性(因为具有疏松多孔的结构),木炭可用于食品、工业产品
中除去色素、异味等,活性炭可用于防毒面具中除去毒气、制糖业中脱色以制白糖;焦炭用于
冶铁,炭黑加到橡胶里能够增加轮胎的耐磨性。
注意:吸附性是活性炭、木炭的物理性质而不是化学性质
4、C (也叫“足球碳”):C 分子是由60个碳原子构成的分子,形似足球,结构稳定。
60 60
二、.单质碳的化学性质:
单质碳的物理性质各异,而各种单质碳的化学性质却完全相同
1、常温下碳的化学性质比较稳定。因此古代用墨书画的字画保存时间很久仍不变色。
2、可燃性:
完全燃烧(氧气充足),生成CO : C + O 点燃 CO
2 2 2
不完全燃烧(氧气不充足),生成CO:2C + O 点燃 2CO
2
3、还原性:C + 2CuO 高温 2Cu + CO↑ (置换反应)
2
现象:黑色粉末逐渐变成光亮的红色,生成的气体能使澄清的石灰水变浑浊。
CuO在反应中失去氧元素,发生还原反应。C具有还原性。
应用:冶金工业:2Fe 2 O 3 +3C 高温 4Fe+3CO 2 ↑ C+C O高2 温 2 CO
课题2 二氧化碳制取的研究
一、实验室制取气体的思路:(原理、装置、检验)
(1)发生装置:由反应物状态及反应条件决定:
①若反应物是固体,需加热,则制气体时用高锰酸钾制O 的发生装置。
2
②若反应物是固体与液体,不需加热,则制气体时则用制CO 的发生装置。
2
(2)收集方法:气体的密度及溶解性决定:
①难溶于水的气体用排水法收集。 CO只能用排水法(因为密度约等于空气,且有毒)
②密度比空气大(或相对分子质量>29)的气体用向上排空气法收集。 CO 只能用向上
2
排空气法(因为能溶于水)
③密度比空气小(或相对分子质量<29)的气体用向下排空气法收集。
二、实验室制取二氧化碳的方法
1、药品:石灰石(或大理石)与稀盐酸①不能用HSO 与CaCO 反应的原因:生成的CaSO 微溶于水,会覆盖在CaCO 表面,阻止
2 4 3 4 3
反应的进行。
②不能用浓盐酸与CaCO 反应的原因:浓盐酸易挥发成HCl气体混入生成的CO 中。
3 2
③不能用HCl与NaCO 反应的原因:NaCO 易溶于水,与盐酸反应速率快,不利收集。
2 3 2 3
2、原理:用石灰石(或大理石)和稀盐酸反应:CaCO +2HCl==CaCl +H O+CO↑
3 2 2 2
3、装置图:
装置的注意事项:(1)若用长颈漏斗来注入盐
酸,则长颈漏斗的下端必须伸入液面以下(防
止空气混入瓶内,及生成的CO 从漏斗溢出)。
2
(2)若用试管来装药品,固定试管时,试管口
竖直向上,试管底部与铁架台面接触。
4、气体收集方法:向上排空气法
5、检验方法:将制得的气体通入澄清的石灰水,如能浑浊,则是二氧化碳。
验满方法:用点燃的木条,放在集气瓶口,木条熄灭。证明已集满二氧化碳气体。
6、二氧化碳的工业制法:
煅烧石灰石: CaCO 高温 C aO+CO ↑
3 2
课题3 二氧化碳和一氧化碳
一、二氧化碳
1、物理性质:无色,无味的气体,密度比空气大,能溶于水,高压低温下可得固体----干冰
2、化学性质:
1)一般情况下不能燃烧,也不支持燃烧,不能供给呼吸
2)与水反应生成碳酸: CO+H O==H CO 生成的碳酸能使紫色的石蕊试液变红,
2 2 2 3
碳酸不稳定,易分解 HCO == H O+ CO ↑
2 3 2 2
3)能使澄清的石灰水变浑浊:CO+Ca(OH) ==CaCO↓+H O 用于检验二氧化碳;这也
2 2 3 2
是久置装石灰水的试剂瓶壁有一层白膜的原因。要除去这白膜,用稀盐酸。其原理是
CaCO +2HCl==CaCl +H O+CO↑
3 2 2 2
4)与灼热的碳反应: C + CO 高温 2 CO
2
3、用途:①灭火(灭火器原理:NaCO+2HCl==2NaCl+HO+CO↑)既利用其物理性质(密度
2 3 2 2
比空气大),又利用其化学性质(不能燃烧,也不支持燃烧)
②干冰用于人工降雨、制冷剂(利用干冰升华时要吸收大量的热)
③温室的气体肥料 ④做碳酸型饮料(利用二氧化碳能溶于水)
1、二氧化碳对环境的影响:⑴过多排放引起温室效应。
①造成温室效应的原因:人类消耗的能源急剧增加,森林遭到破坏
②减轻温室效应的措施:减少化石燃料的燃烧;植树造林;使用清洁能源
⑵由于二氧化碳不能供给呼吸但无毒,因此在人群密集的地方注意通风换气
二、一氧化碳
1、物理性质:无色,无味的气体,密度比空气略小,难溶于水
2、有毒:吸进肺里与血液中的血红蛋白结合,使人体缺少氧气而中毒。因此在冬季用煤炉来
取暖时,要注意房间的通风和换气。
3、化学性质:1)可燃性:2CO+O 点燃 2CO(可燃性气体点燃前一定要检验纯度)发出蓝色火焰
2 2
H 和O 的燃烧火焰是:淡蓝色的火焰。
2 2
CO和O 的燃烧火焰是:蓝色的火焰。
2
CH 和O 的燃烧火焰是:明亮的蓝色火焰。
4 2
鉴别:H、CO、CH 可燃性的气体:看燃烧产物(不可根据火焰颜色)
2 4
(水煤气:H 与CO 的混合气体。制法: C + HO 高温 H ↑+ CO↑)
2 2 2
△
2)还原性: CO+CuO Cu+CO (还原反应) 应用:冶金工业
2
现象:黑色的氧化铜逐渐变成光亮的红色,产生的气体能使澄清的石灰水变浑浊。
Fe O+3CO 高温 2 Fe+3CO
2 3 2
现象:红棕色粉末逐渐变成黑色,产生的气体能使澄清的石灰水变浑浊。
H、CO、C具有相似的化学性质:
2
A可燃性 C + O
2
点燃 CO
2
2CO+O
2
点燃 2CO
2
2H
2
+ O
2
点燃 2H
2
O
B还原性 :H + CuO △ Cu + H O CO+CuO △ C u+CO
2 2 2
C + 2CuO 高温 2Cu + CO↑
2
除杂的方法:①除去CO中混入的CO 杂质:通入石灰水: CO+Ca(OH) ==CaCO↓+H O
2 △2 2 3 2
②除去CO 中混入的CO杂质: 通过灼热的氧化铜: CO+CuO Cu+CO
2 2
4、一氧化碳与二氧化碳性质不同的根本原因是:1个二氧化碳分子比1个一氧化碳分子多1
个氧原子
本章知识间的联系:
①C→CO :2C+O 点燃 2CO C+CO 高温 2 CO
2 2
②C→CO :C+O 点燃 CO C+2CuO 高温 2 Cu+CO↑
2 2 2 2
3C+Fe O 高温 3 CO↑+2Fe
2 3 2
③CO→CO :2CO+O 点燃 2CO CO+CuO △ C u+CO
2 2 2 2
3CO+Fe O 高温 2 Fe+3CO
2 3 2
④CO→HCO: CO +HO ===HCO
2 2 3 2 2 2 3
⑤HCO →CO :HCO ===CO↑+HO
2 3 2 2 3 2 2
⑥CO
2
→CaCO
3
:CO
2
+Ca(OH)
2
===CaCO
3
↓+H
2
O
⑦CaCO →CO :CaCO +2HCl==CaCl +H O+CO↑ CaCO
高温
C O ↑+CaO
3 2 3 2 2 2 3 2