文档内容
学生姓名 年级 初三 授课时间 教师姓名 伍万茹 课时 2 课时
1、碳的几种单质及化学性质;2、实验室制取气体的装置选择;3、实验室制取二氧化碳及CO2的
教学目标
工业制法(煅烧石灰石);4、二氧化碳及一氧化碳的性质。
重点:碳的几种单质及化学性质;实验室制取二氧化碳。
重点难点
难点:实验室制取二氧化碳;二氧化碳及一氧化碳化学性质。
(1)金刚石、石墨和C60
一、知识要点:
1. 碳的几种单质
(1)金刚石、石墨和C 的物理性质和用途的比较
60
名称 金刚石(由___元素组成) 石墨(由___元素组成) C
60
外观 色透明、正八面体形状 色不透明的细鳞片状 C 分子形似 。有金属光泽
60
的 体,有璀璨夺目的光泽 体,有 光泽 的固体,其微晶粉末呈黄色
导电性 几乎 几乎
硬度 天然存在的最 的物质 质 (最 的矿物之一),有 质脆
滑腻感,在纸上会留下痕迹
导热性 良好 良好 很差
物性差异 晶体中的碳原子排列方式不同 分子晶体
的原因
用途 、 、 、 、 应用于材料、医学和超导等领域
等 等
(注:人们对C 性质的认识正在不断地深入,C 是一个分子中含有60个碳原子,是单质,相对分子质量720)
60 60
由上表可知,物质的性质决定了物质的用途,其关系为:
( ) ( )
物质的结构 物质的性质 物质的用途
(2)木炭、活性炭
A. 木炭:有吸附作用,用于吸附一些食品和工业产品里的色素,吸附有异味的物质。
B. 活性炭:有较强的吸附作用,用于防毒面具、冰箱的除臭剂。
[活动与探究]
用块状木炭脱色,需要较长时间,可作如下改进:在小烧杯中注入30ml~40ml蒸馏水,加入少许红墨水至
呈现前红色为止,将其均分注入两个小锥形瓶里,取0.5g干燥木炭,在研钵中研细后,倒入其中一个小
锥形瓶里,充分振荡后过滤,可以得到无色溶液,再与另一个小锥形瓶中未加木炭的原溶液比较,可观察
到明显的现象: 加了木炭的红墨水褪色了。
(木炭和活性碳具有 的结构,因此具有较强的 能力,可以吸附气体或溶液
里的色素,其中管道越多,跟气体和溶液的接触面积越大,吸附能力越强,吸附过程属物理变化过程。因
此,木炭和活性炭在制糖工业、食品工业、防毒面具制作等方面有重要作用。 )
C. 无定形碳:由石墨的微小晶体和少量杂质构成.主要有:焦炭,木炭,活性炭,炭黑(均为混合物)等;
焦炭用于冶炼金属( 冶铁 ), 炭黑是细小的黑色粉末,含碳化合物不完全燃烧均会产生炭黑,如蜡、柴
油、煤油等。常用于制黑色颜料、墨汁、鞋油等;炭黑加到橡胶里能够增加轮胎的耐磨性。
Δ“碳”和“炭”的区别
“碳”是元素的名称,比如碳单质、含碳化合物、二氧化碳等;
“炭”表示由碳元素组成的某种物质――木炭、活性炭、焦炭、炭黑等。
(3)同一种元素可以组成不同的单质;同种元素组成的物质可能属于纯净物种的单质,也可能属于不同物质组成
的混合物。(例如: )
2. 单质碳的化学性质:单质碳的物理性质各异,而各种单质碳的化学性质却完全相同!
(1)常温下,碳的化学性质不活泼(稳定性强)(碳原子最外层电子数为4)
古代字画为什么经历几千年而不变色?档案资料为什么要求用碳素墨水书写?
(2)可燃性:
点燃
完全燃烧(氧气充足),生成CO : C+O CO 放热
2 2 2
点燃
不完全燃烧(氧气不充足),生成CO :2C+O 2CO 放热
2
(相同的反应物,因反应物的量不同,生成物不同)高温
(3)还原性:C+2CuO 2Cu+CO ↑
2
应用:冶金工业
现象:黑色粉末逐渐变成光亮红色,澄清的石灰水变浑浊。
高温
利用碳单质的还原性,可用于冶金工业。例如:用焦炭炼铁。 2Fe O + 3C 4Fe + 3CO↑
2 3 2
高温 高温
(拓展:C + CO 2CO,2Fe O + 3C 4Fe + 3CO↑)
2 2 3 2
二、典例剖析:
例1.常温下,碳的化学性质不活泼。碳单质的下列用途与这一性质有关的是( )
A、用碳素笔书写重要文件和资料 B、用金刚石切割大理石
C、用石墨为主要原料制铅笔芯 D、用活性炭脱色制白糖
例2.科学家已证实了有一种具有空心球状结构的N 分子,以下判断不正确的是( )
60
A、N 和N 都是氮元素的单质 B、N 的相对分子质量是840
60 2 60
C、N 中含有30个氮分子 D、N 中氮元素的化合价为0
60 60
例3.已知碳有如下性质:C + HO 高温 CO + H,由此推知:在火势旺盛的煤炉中,湿煤燃烧比干煤燃烧时的火焰
2 2
将( )。
A、更旺 B、不旺 C、熄灭 D、维持不变
例4.用墨汁书写的字画经久不褪色,其主要原因是 。
例5.吸烟是不良嗜好。香烟烟气中含有几百种对人体有害得物质,毒害作用较大得有CO、尼古丁和含有致癌物质的
焦油等。长期吸烟的人,易患冠心病、肺气肿、肺癌等,大量吸烟能使人中毒死亡。有一种香烟的过滤嘴中有许多
黑色的小颗粒。试问此黑色小颗粒可能是 ,它起 的作用。
例6.1999年发生在南联盟科索沃的战争中,北约使用石墨炸弹破坏了南联盟大部分电力供应,其原理就是产生了
覆盖大范围地区的碳纤维云,这些纤维因具有 性而使供电系统短路。
1、下列反应或作用中不产生二氧化碳的是( )
A、用赤热的木炭还原氧化铜 B、大理石与稀盐酸反应
C、在空气中点燃木炭 D、绿色植物的光合作用
2、下列过程中发生了化学变化的是( )
A、石墨导电 B、金刚石切割金属 C、用铅笔写字 D、用焦炭冶炼金属
3、1990年海湾战争引起科威特大量油井燃烧,造成严重的大气污染,据报道,有些地区降了黑雨。你分析形成黑雨
的主要污染物是( )
A、炭黑 B、二氧化碳 C、水蒸汽 D、石墨
4、同一种元素可以组成不同种单质。碳单质有 、 和 等,它们的性质差异是因为
,由此可知 决定物质的性质。
5、木炭具有较强的吸附性是因为它具有 结构,防毒面具是利用活性炭来吸附 ;制糖工业利用
活性炭来吸附 ;自来水厂用活性炭来吸附 。
6、1797年法国化学家谈拉德做了一个成功德实验,他称取等量的石墨和金刚石,分别使之充分燃烧,结果得到了相
等 质 量 的 气 体 , 该 气 体 都 能 使 澄 清 的 石 灰 水 变 混 浊 。 由 此 我 们 可 以 得 出 什 么 结 论 ?
。
7、具体填写(1)-(3)组物质性质不同的原因。并以此为例,再另写两组实例。
(1)金刚石、石墨、C :碳原子 不同;
60
(2)HO和HO: 分子的 不同;
2 2 2
(3)钠原子和氯原子:原子的 不同;
(4) ;
(5) 。
8、继1985年科学家发现了C 分子后,1991年科学家又发现了一种管状的碳单质――碳纳米管。
60
请你用所学知识回答下列问题。
(1) 在常温下C 分子和碳纳米管的化学性质是否活泼?简要说明理由。
60
(2) 设计一个方案,证明C 分子和碳纳米管都是由碳元素组成的。
60
9、自行车车锁使用久了不灵活,通常可用小刀削一些铅笔芯的粉末,放到锁眼后转动几下,锁就变得灵巧多了,为什
么?你也试试看。四、课后作业
1.下列不符合科学道理是( )
A.碳是非金属,但它的单质石墨能导电 B.普通大理石经“气功大师”发功能变成金刚石
C.工业上用焦炭来炼铁是利用碳的还原性 D.碳与氧气反应的生成物有时是不同的
2.下列物质的性质中,中属于物理性质的是( )
A.金刚石具有很大的硬度 B.石墨有良好的导电性
C.活性炭有碳的性质稳定 D.常温下碳的性质稳定
3.下列关于碳单质用途的叙述中,错误的是( )
① 橡胶里添加炭黑能增加耐磨性 ② 干电池里的碳棒是石墨制成的
③ 电冰箱除味剂是活性炭 ④ 防毒面具用焦炭吸收有毒气体
⑤ 制糖工业用炭黑来吸附有色物质 ⑥ 金刚石不仅能刻划玻璃,还能装在钻头上钻凿坚硬的岩层
A.②①③ B.②③④ C.③④ D.④⑤
4.有下列变化:甲→乙→丙,能满足这个变化的甲是( )
A.C B.H C.CO D.Cu
2
5.在一密闭容器内盛有等质量的碳和氧气,高温加热使之充分反应,容器内的物质是( )
A.CO B.CO 和O C.CO D.Cu
2 2
6.下列说法错误的是( )
A.同种元素组成的物质,性质不一定相同 B.同种元素组成的物质、性质一定相同
C.不同的单质可以由同一种元素组成 D.不同的单质可以有相同的化学性质
7.金刚石、石墨、C 在物理性质上存在明显差异的原因是 。
60
8.某同学自制简易净水器,除可利用 和 等疏松结构的材料做吸附剂外,还可利用我
们身边的材料如 作吸附剂。为消除室内抽香烟后或装修后难闻的气味,该同学点燃一支蜡烛,一段
时间后室内难闻气味消失,根据蜡烛在空气中燃烧的现象解释其中原因 。
9.经常不用的锁,开启比较困难时,可向锁空中加些铅笔芯粉末,便容易开启,这是因为
。
10.埋木桩前,有时把埋入地下一段的表面用火微微烧焦,这是因为 。
11.计算题:氧化铜和木炭的混合物在加热条件下恰好完全反应,生成了25.4 g铜,计算原混合物中氧化铜和木炭
粉各多少克。
(2)二氧化碳制取的研究
一、知识要点:
1. 实验室制取气体的装置选择
( 实验室里制取气体的装置包括 和 两部分。)
(1)发生装置的选择依据固体和固体反应:如:
反应物 固体和液体反应 如:
气体 的状态 液体和液体反应 如:
发生装置 ……
反应条件(是否需要加热、加催化剂等)
实验室制取气体的一般设计思路和方法
A.药品的选择原则:选择反应速度适中,价格便宜,来源广泛,污染少,实验安全,
所制气体纯净的药品。
B.实验装置的设计:根据药品的状态和反应原理,以及反应条件设计装置。
(2)收集装置的选择 装 置 设 密计度要比简空单气,大便—于—控向制上和排操气作法。 缺 纯度不高
排空气法 点 需验纯
气体 密度比空气小——向下排气法 优点:较干燥
收集装置
排水法(不易溶于水、难溶于水且不与水反应 )
优缺点:收集到的气体较纯,但含水蒸气
2. 实验室制取二氧化碳
(1)药品:______________ 原理:_______________________________________
(2)注意:A. 不能用浓盐酸代替稀盐酸,因为_____________________________________
B. 不能用稀硫酸代替稀盐酸,因为_____________________________________
C. 不能用NaCO 或CaCO 代替大理石(或石灰石),因为___________________
2 3 3
(3)发生装置:固 + 液——气体型(参看课本P 图6-10)
111
(4)收集装置:只用向上排空气法
(因为CO 能溶于水且与水反应,密度比空气大)
2
(5)CO 的检验:将气体通入_______________中,如果变浑浊,则该气体为CO。
2 2
化学方程式:CO + Ca(OH) == CaCO↓+ HO
2 2 3 2
(6)CO 的验满:用燃着的木条放在___________________,如果木条熄灭,则已充满。
2
(这样做是利用___________________的性质)。
(7)实验室制取CO 的实验操作过程(主要步骤)
2
A.按实验要求连接仪器;B.检查装置的气密性;C.装入大理石,塞紧胶塞;
D.固定装置;E.从长颈漏斗加入稀盐酸至长颈漏斗下端管口液封;
F.收集气体,导管一定要伸至集气瓶底部;G.检验是否集满。
*检查装置气密性:
常用的方法:将装置导管口的一端浸没于水中,再用双手握住容器(试管),
若导管口有_______冒出;松开双手后,管口形成一端高于水面
的________,且在一定时间内不下降,则证明连接装置不漏气。
特殊方法:使用长颈漏斗加液体的气体发生装置如何检查气密性?
(8)净化所收集的二氧化碳:
若制取的CO 中,含有少量HCl气体和水蒸气时,可先将气体通过盛NaHCO 溶液的洗气瓶(除去HCl气
2 3
体),再通过盛有浓硫酸的洗气瓶(除去水蒸气并进行干燥)
[思考]
1、 实验室常用稀盐酸与大理石或石灰石制取二氧化碳。若反应物用了浓盐酸,那么把所得的气体通入澄清石灰
水,可能会出现什么现象?为什么?
2、 如果为了避免该现象的发生一般应当采取哪些措施?
高温
3. CO 的工业制法(煅烧石灰石):CaCO CaO + CO↑
2 3 2
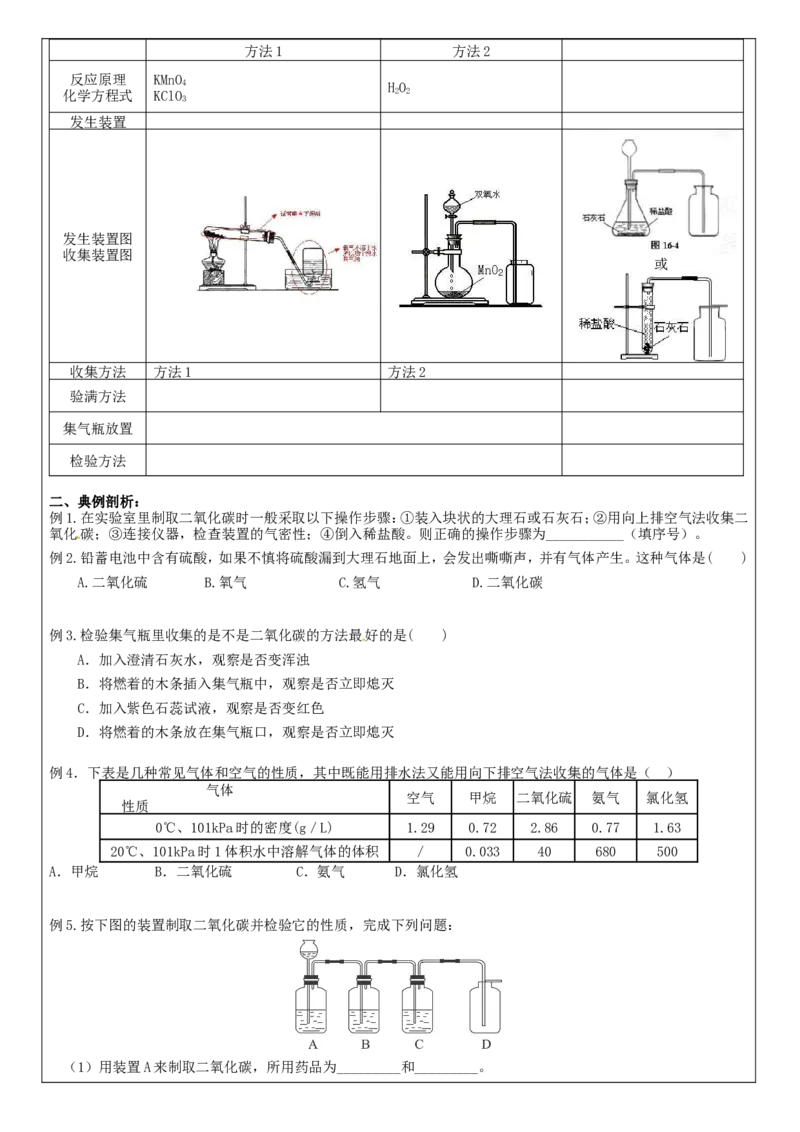
[归纳与小结] 实验室制取氧气、二氧化碳气体的反应原理、装置及验证的对比
O CO
2 2方法1 方法2
反应原理 KMnO
4 HO
化学方程式 KClO 2 2
3
发生装置
发生装置图
收集装置图
或
收集方法 方法1 方法2
验满方法
集气瓶放置
检验方法
二、典例剖析:
例1.在实验室里制取二氧化碳时一般采取以下操作步骤:①装入块状的大理石或石灰石;②用向上排空气法收集二
氧化碳;③连接仪器,检查装置的气密性;④倒入稀盐酸。则正确的操作步骤为___________(填序号)。
例2.铅蓄电池中含有硫酸,如果不慎将硫酸漏到大理石地面上,会发出嘶嘶声,并有气体产生。这种气体是( )
A.二氧化硫 B.氧气 C.氢气 D.二氧化碳
例3.检验集气瓶里收集的是不是二氧化碳的方法最好的是( )
A.加入澄清石灰水,观察是否变浑浊
B.将燃着的木条插入集气瓶中,观察是否立即熄灭
C.加入紫色石蕊试液,观察是否变红色
D.将燃着的木条放在集气瓶口,观察是否立即熄灭
例4.下表是几种常见气体和空气的性质,其中既能用排水法又能用向下排空气法收集的气体是( )
气体
空气 甲烷 二氧化硫 氨气 氯化氢
性质
0℃、101kPa时的密度(g/L) 1.29 0.72 2.86 0.77 1.63
20℃、101kPa时1体积水中溶解气体的体积 / 0.033 40 680 500
A.甲烷 B.二氧化硫 C.氨气 D.氯化氢
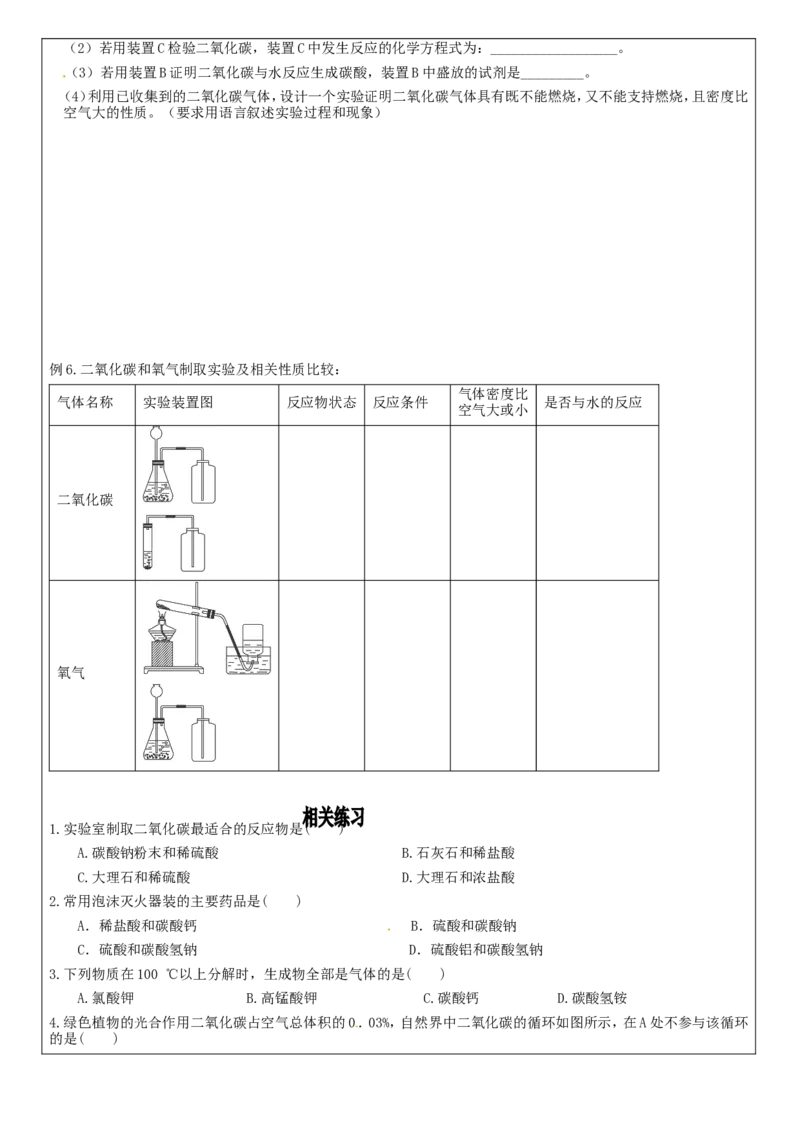
例5.按下图的装置制取二氧化碳并检验它的性质,完成下列问题:
(1)用装置A来制取二氧化碳,所用药品为_________和_________。(2)若用装置C检验二氧化碳,装置C中发生反应的化学方程式为:__________________。
(3)若用装置B证明二氧化碳与水反应生成碳酸,装置B中盛放的试剂是_________。
(4)利用已收集到的二氧化碳气体,设计一个实验证明二氧化碳气体具有既不能燃烧,又不能支持燃烧,且密度比
空气大的性质。(要求用语言叙述实验过程和现象)
例6.二氧化碳和氧气制取实验及相关性质比较:
气体密度比
气体名称 实验装置图 反应物状态 反应条件 是否与水的反应
空气大或小 ]
二氧化碳 [
氧气
1.实验室制取二氧化碳最适合的反应物是( )
A.碳酸钠粉末和稀硫酸 B.石灰石和稀盐酸
C.大理石和稀硫酸 D.大理石和浓盐酸
2.常用泡沫灭火器装的主要药品是( )
A.稀盐酸和碳酸钙 B.硫酸和碳酸钠
C.硫酸和碳酸氢钠 D.硫酸铝和碳酸氢钠
3.下列物质在100 ℃以上分解时,生成物全部是气体的是( )
A.氯酸钾 B.高锰酸钾 C.碳酸钙 D.碳酸氢铵
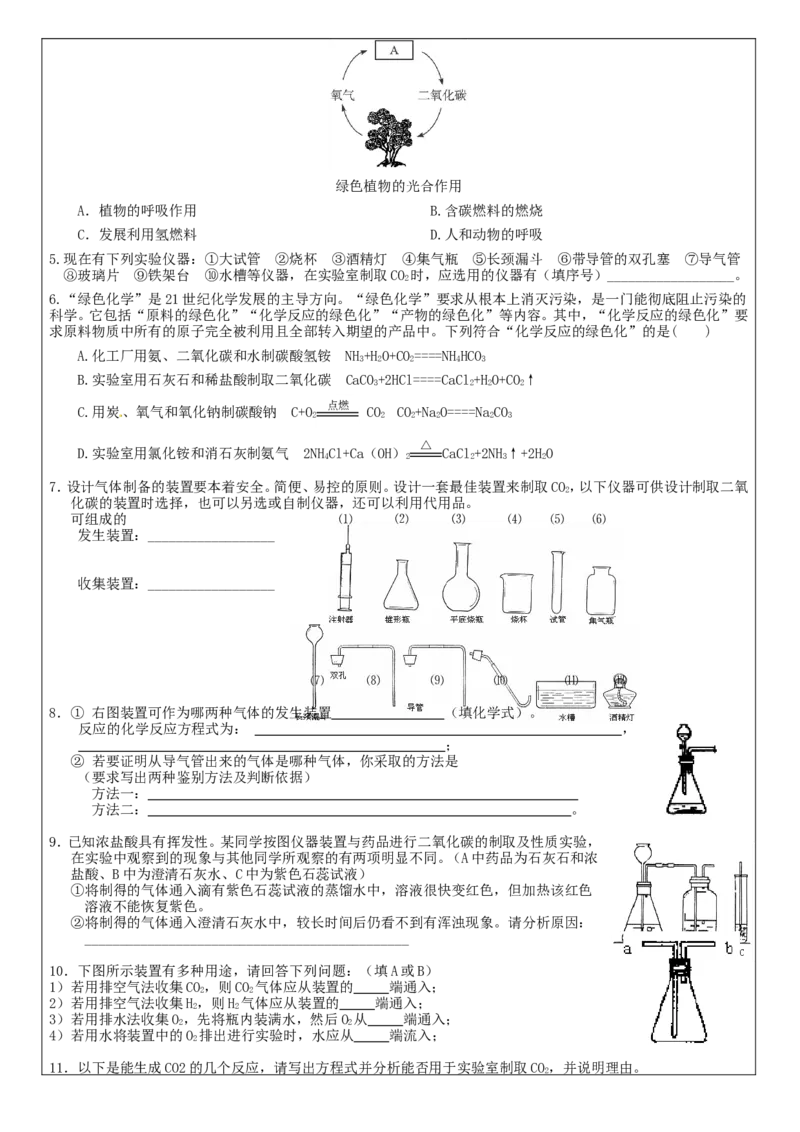
4.绿色植物的光合作用二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环
的是( )绿色植物的光合作用
A.植物的呼吸作用 B.含碳燃料的燃烧
C.发展利用氢燃料 D.人和动物的呼吸
5.现在有下列实验仪器:①大试管 ②烧杯 ③酒精灯 ④集气瓶 ⑤长颈漏斗 ⑥带导管的双孔塞 ⑦导气管
⑧玻璃片 ⑨铁架台 ⑩水槽等仪器,在实验室制取CO 时,应选用的仪器有(填序号)__________________。
2
6.“绿色化学”是21世纪化学发展的主导方向。“绿色化学”要求从根本上消灭污染,是一门能彻底阻止污染的
科学。它包括“原料的绿色化”“化学反应的绿色化”“产物的绿色化”等内容。其中,“化学反应的绿色化”要
求原料物质中所有的原子完全被利用且全部转入期望的产品中。下列符合“化学反应的绿色化”的是( )
A.化工厂用氨、二氧化碳和水制碳酸氢铵 NH+HO+CO====NHHCO
3 2 2 4 3
B.实验室用石灰石和稀盐酸制取二氧化碳 CaCO+2HCl====CaCl+HO+CO↑
3 2 2 2
点燃
C.用炭、氧气和氧化钠制碳酸钠 C+O CO CO+NaO====NaCO
2 2 2 2 2 3
△
D.实验室用氯化铵和消石灰制氨气 2NHCl+Ca(OH) CaCl+2NH↑+2HO
4 2 2 3 2
7.设计气体制备的装置要本着安全。简便、易控的原则。设计一套最佳装置来制取CO,以下仪器可供设计制取二氧
2
化碳的装置时选择,也可以另选或自制仪器,还可以利用代用品。
可组成的 ⑴ ⑵ ⑶ ⑷ ⑸ ⑹
发生装置:__________________
收集装置:__________________
⑺ ⑻ ⑼ ⑽ ⑾ ⑿
8.① 右图装置可作为哪两种气体的发生装置 (填化学式)。
反应的化学反应方程式为: ,
;
② 若要证明从导气管出来的气体是哪种气体,你采取的方法是
(要求写出两种鉴别方法及判断依据)
方法一:
方法二: 。
9.已知浓盐酸具有挥发性。某同学按图仪器装置与药品进行二氧化碳的制取及性质实验,
在实验中观察到的现象与其他同学所观察的有两项明显不同。(A中药品为石灰石和浓
盐酸、B中为澄清石灰水、C中为紫色石蕊试液)
①将制得的气体通入滴有紫色石蕊试液的蒸馏水中,溶液很快变红色,但加热该红色
溶液不能恢复紫色。
②将制得的气体通入澄清石灰水中,较长时间后仍看不到有浑浊现象。请分析原因:
______________________________________________
10.下图所示装置有多种用途,请回答下列问题:(填A或B)
1)若用排空气法收集CO,则CO 气体应从装置的 端通入;
2 2
2)若用排空气法收集H,则H 气体应从装置的 端通入;
2 2
3)若用排水法收集O,先将瓶内装满水,然后O 从 端通入;
2 2
4)若用水将装置中的O 排出进行实验时,水应从 端流入;
2
11.以下是能生成CO2的几个反应,请写出方程式并分析能否用于实验室制取CO,并说明理由。
2生成CO 的反应 化学方程式 能否用,理由
2
①
燃烧石灰石
②
燃烧木炭
石灰石与 ③
稀盐酸反应
碳酸钠与 ④
稀硫酸反应
四、课后作业
1.(黄冈初赛)已知碳酸氢钙[Ca(HCO ) ]易溶于水,受热易分解,分解反应的化学方程式为:
3 2
Ca(HCO )=====CaCO ↓+ CO↑+ H O。
3 2 3 2 2
现要用实验方法证明上述反应的产物。请回答有关问题:
(1)写出分解碳酸氢钙所需的主要仪器名称:___________________________。
(2)在实验中,有人提出必须先检验分解产物碳酸钙,再检验二氧化碳,你认为该建议是否正确?
(3)简述如何用实验方法证明分解产物中有二氧化碳?
(4)简述如何用实验方法证明分解产物中有碳酸钙?
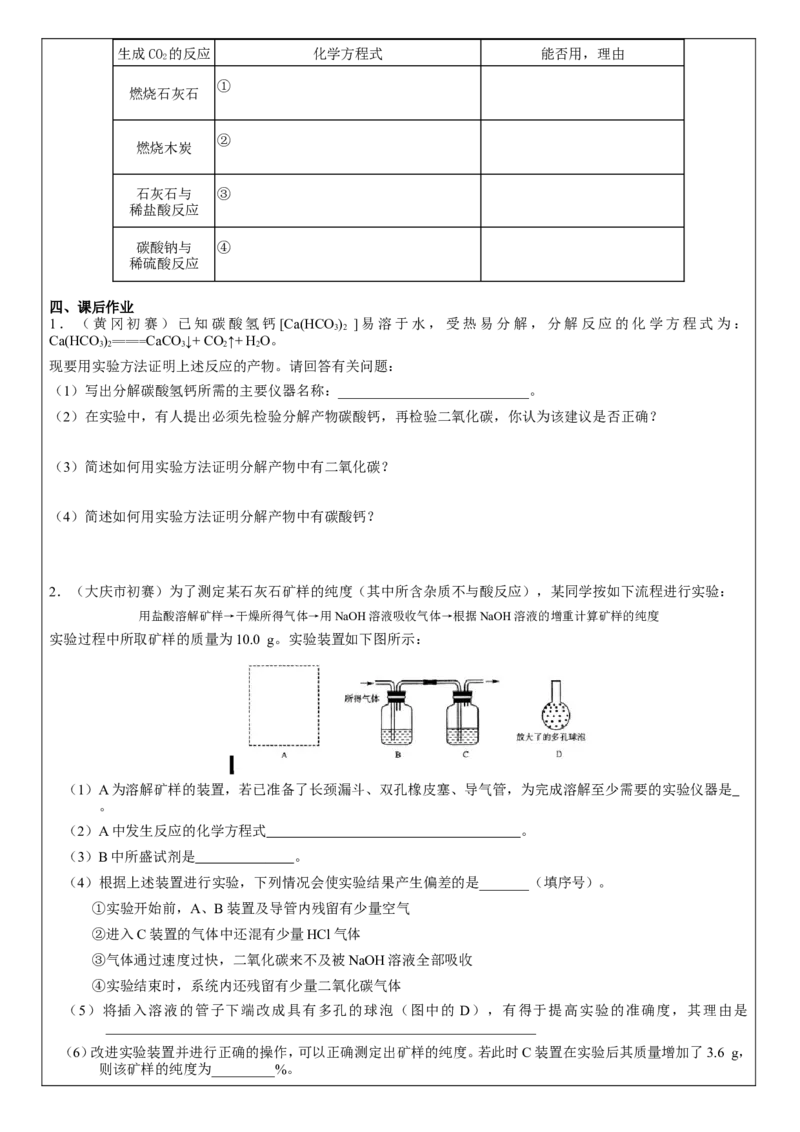
2.(大庆市初赛)为了测定某石灰石矿样的纯度(其中所含杂质不与酸反应),某同学按如下流程进行实验:
用盐酸溶解矿样→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重计算矿样的纯度
实验过程中所取矿样的质量为10.0 g。实验装置如下图所示:
(1)A为溶解矿样的装置,若已准备了长颈漏斗、双孔橡皮塞、导气管,为完成溶解至少需要的实验仪器是
。
(2)A中发生反应的化学方程式 。
(3)B中所盛试剂是 。
(4)根据上述装置进行实验,下列情况会使实验结果产生偏差的是_______(填序号)。
①实验开始前,A、B装置及导管内残留有少量空气
②进入C装置的气体中还混有少量HCl气体
③气体通过速度过快,二氧化碳来不及被NaOH溶液全部吸收
④实验结束时,系统内还残留有少量二氧化碳气体
(5)将插入溶液的管子下端改成具有多孔的球泡(图中的 D),有得于提高实验的准确度,其理由是
_____________________________________________________________
(6)改进实验装置并进行正确的操作,可以正确测定出矿样的纯度。若此时C装置在实验后其质量增加了3.6 g,
则该矿样的纯度为_________%。(3)二氧化碳和一氧化碳
一、知识要点:
1. 二氧化碳的性质
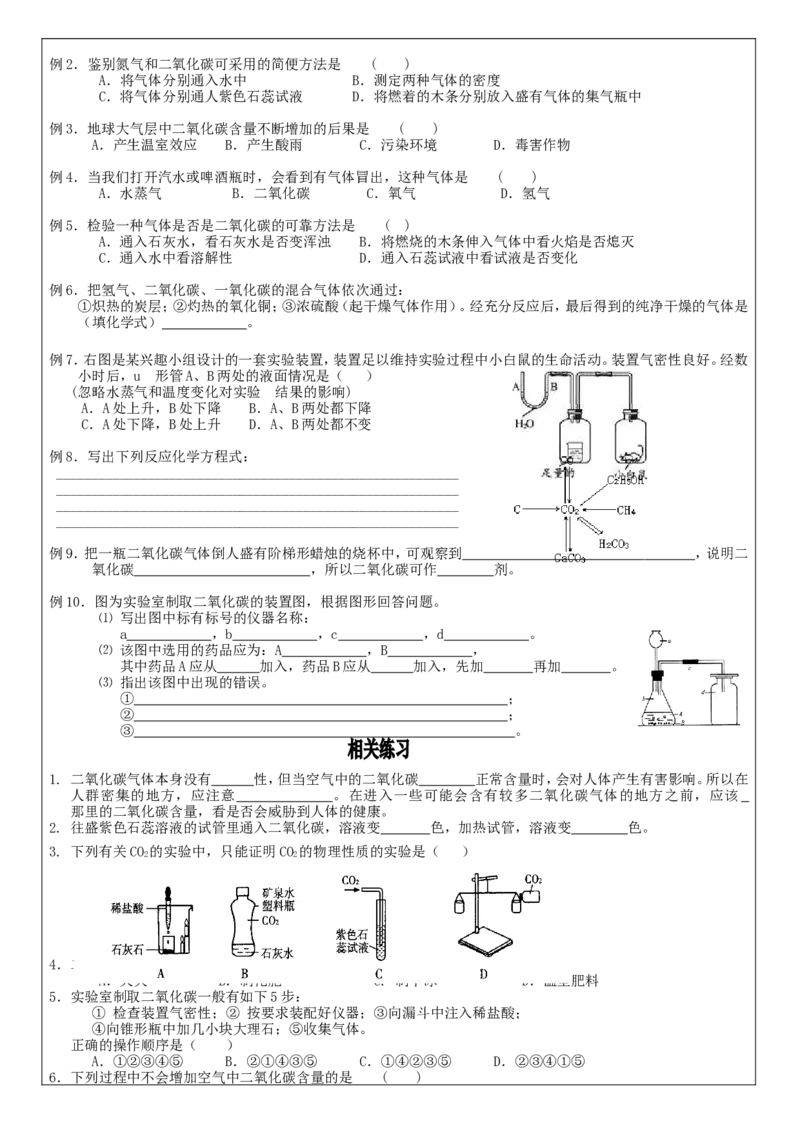
(1)二氧化碳的物理性质:
A. 常温下是无色无味的气体
B. 密度比空气大
C. 能溶于水 (设计实验证明,参看课本P 实验6-5)
114
D. CO 固体叫“干冰” (高压低温下制得固体 )
2
(2)二氧化碳的化学性质
A. 一般情况下,二氧化碳不燃烧,也不支持燃烧;(实验探究:课本P 实验6-4)
113
B. 二氧化碳不供给呼吸(“屠狗洞”现象)
C. 二氧化碳能与水反应生成碳酸(实验探究:参看课本P 实验6-6)
114
化学方程式:CO + HO == HCO ( 生成的碳酸能使紫色的石蕊试液变红 )
2 2 2 3
( 碳酸不稳定、易分解:HCO == CO↑+ HO )
2 3 2 2
D. 二氧化碳与石灰水反应
现象:澄清的石灰水变浑浊。原因:生成不溶于水的白色CaCO 沉淀。
3
化学方程式:CO + Ca(OH) == CaCO↓+ HO
2 2 3 2
① CO 气体的检验
2
此反应 ② 长期放置的石灰水,瓶壁会出现一层白色物质( 如何清洗?)
的应用 ③ 刚抹过石灰浆的墙壁,生上炭火炉时,墙壁反而更潮湿
④ 建筑工人在没有用完的石灰浆上覆盖一层土
⑤ 鸡蛋放入石灰水中一会儿取出,可以保鲜
E. 二氧化碳能与炽热的碳反应:CO + C 高温 2CO(吸热反应)
2
(3)用途:灭火(灭火器原理:NaCO+2HCl==2NaCl+HO+CO↑)既利用其物理性质,又利用其化学性质,干冰用于人
2 3 2 2
工降雨、制冷剂、温室肥料
(4)二氧化碳对生活和环境的影响:过量排放引起温室效应。
全球变暖,两极冰川融化
温室效应的危害 海平面升高,淹没沿海地带
土地沙漠化,农业减产
减少煤、石油、天然气等化石燃料的使用
控制温室效应措施 开发利用太阳能、风能等清洁能源
大力植树造林,严禁乱砍滥伐
2. 一氧化碳的性质
(1)物理性质:通常情况下是无色无味的气体,难溶于水,密度比空气略小。
想一想:水能防止CO中毒吗? 实验室制取CO用什么方法收集?
(2)化学性质(H、CO、C具有相似的化学性质:① ② )
2
A. 可燃性: 2CO + O 点燃 2CO —— 作燃料(是煤气的主要成分)
2 2
现象:产生蓝色火焰,放出热量。
注意:CO和H 一样与空气(或氧气)混合时,遇明火可能发生爆炸,点燃前必须验纯。
2
( 可燃性气体点燃前一定要检验纯度,方法与H 一样 )
2
水煤气:H 与CO 的混合气体 ( C + HO高温 H + CO )
2 2 2
B. 还原性: 应用于冶炼金属
CO + CuO △ Cu + CO (现象:黑色粉末变光亮红色,澄清的石灰水变浑浊)
2
高温
FeO + 3CO 2Fe + 3CO (现象:红棕色粉末逐渐变成黑色,石灰水变浑浊)
2 3 2注意:
① 实验操作顺序:
1)通入一氧化碳;
2)点燃酒精灯;
3)氧化铜还原;
4)撤去酒精灯、停止加热;
5)停止通入一氧化碳;
6)让还原出来的铜完全冷却。
② 但需对尾气处理,方法是将CO点燃转变CO(或收集起来)。
2
C. 毒性:CO能与血液中的血红蛋白结合,使血红蛋白失去运输氧气的能力,使人因缺氧而中毒。
(正常的血液呈深红色,当通入一氧化碳后,血液由深红色变成鲜红色)
* 鉴别:H 、 C O 、 C H 可燃性的气体:看燃烧产物(不可根据火焰颜色)
2 4
H 和O 的燃烧火焰是:发出淡蓝色的火焰。CO和O 的燃烧火焰是:发出蓝色的火焰。
2 2 2
CH 和O 的燃烧火焰是:发出明亮的蓝色火焰。
4 2
* 除杂:CO [CO] 通入石灰水 或 氢氧化钠溶液: CO + 2NaOH == NaCO + HO
2 2 2 3 2
△
CO [CO] 通过灼热的氧化铜 CO + CuO Cu + CO
2 2
高温
CaO [CaCO] 只能煅烧(不可加盐酸) CaCO CaO + CO↑
3 3 2
CuO [C] 在氧气流中加热。
* 检验CaO是否含CaCO 加盐酸 :CaCO + 2HCl == CaCl + HO + CO↑
3 3 2 2 2
[归纳与小结]
①二氧化碳和一氧化碳性质的比较
对比项目 一氧化碳 二氧化碳
物理 状态 无色、无味气体 无色、无味气体
性质 密度 1.025 g/L(略________空气) 1.977g/L(________空气)
溶解性 在1体积水里溶解0.02体积 在1体积水里溶解1体积二氧化碳
可燃性 有可燃性2CO + O === 2CO 一般情况下,既不燃烧也不支持燃烧
2 2
化学 还原性 有还原性CuO + CO === Cu + CO 没有还原性
2
性质 与水反应 不能跟水反应 跟水反应CO+ HO===HCO
2 2 2 3
跟石灰水 跟石灰水反应
不能跟石灰水反应
反应 CO + Ca(OH) === CaCO ↓+ HO
2 2 3 2
碳元素的化合价
又无毒性 有剧毒 无毒
主要用途
从上表看出,一氧化碳和二氧化碳同属碳的氧化物,其组成 相同,但因 不同,性质差异很大。
② 单质碳和一氧化碳、氢气性质的比较
碳 一 氧 化 碳 氢 气
物
理
性
质
化
学
性
质
③ 物质的性质决定物质的用途,物质的用途就是物质性质的科学利用。
列举本课题所学物质的性质及对应用途。
物质的性质 用 途
二、典例剖析:
例1. 氧气和二氧化碳在性质上的相似点是( )
① 都易溶于水 ②都能跟澄清石灰水反应 ③ 都是气体 ④都是氧化物
⑤ 都可用于灭火 ⑥通常状况下密度都比空气大
A.②③⑤ B.③⑥ C.①④⑤ D.②④⑤例2.鉴别氮气和二氧化碳可采用的简便方法是 ( )
A.将气体分别通入水中 B.测定两种气体的密度
C.将气体分别通人紫色石蕊试液 D.将燃着的木条分别放入盛有气体的集气瓶中
例3.地球大气层中二氧化碳含量不断增加的后果是 ( )
A.产生温室效应 B.产生酸雨 C.污染环境 D.毒害作物
例4.当我们打开汽水或啤酒瓶时,会看到有气体冒出,这种气体是 ( )
A.水蒸气 B.二氧化碳 C.氧气 D.氢气
例5.检验一种气体是否是二氧化碳的可靠方法是 ( )
A.通入石灰水,看石灰水是否变浑浊 B.将燃烧的木条伸入气体中看火焰是否熄灭
C.通入水中看溶解性 D.通入石蕊试液中看试液是否变化
例6.把氢气、二氧化碳、一氧化碳的混合气体依次通过:
①炽热的炭层;②灼热的氧化铜;③浓硫酸(起干燥气体作用)。经充分反应后,最后得到的纯净干燥的气体是
(填化学式) 。
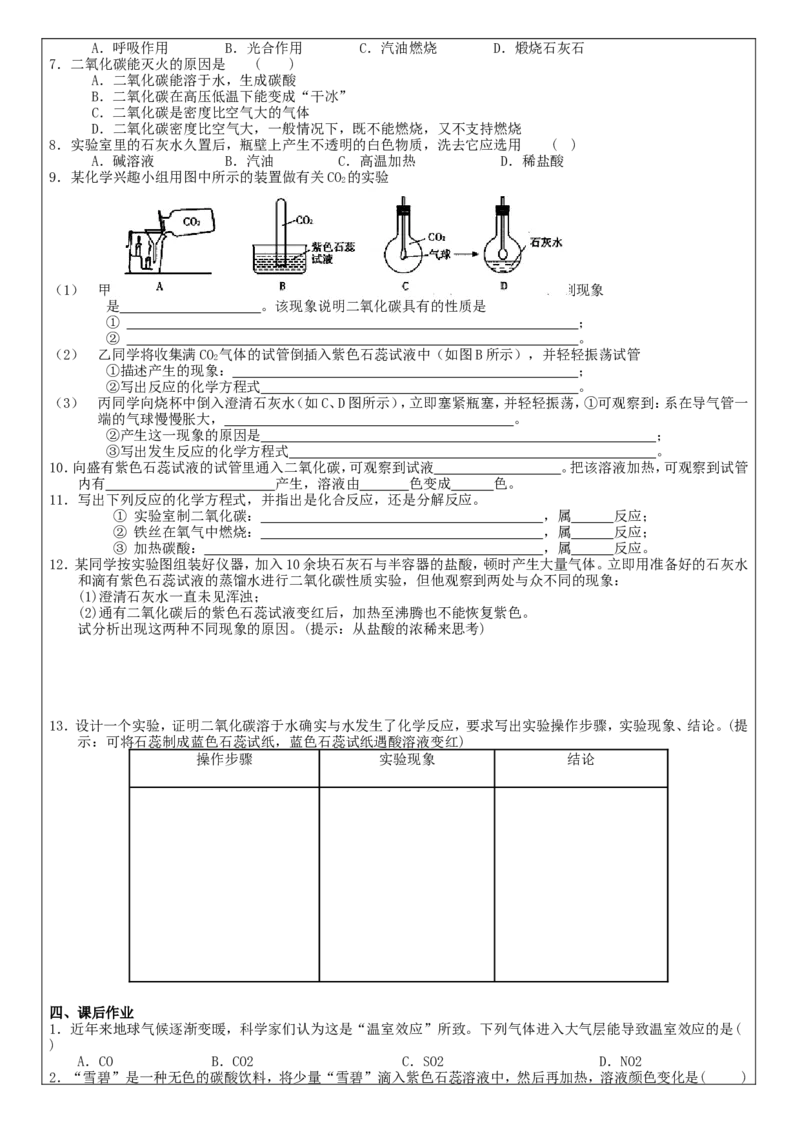
例7.右图是某兴趣小组设计的一套实验装置,装置足以维持实验过程中小白鼠的生命活动。装置气密性良好。经数
小时后,u 形管A、B两处的液面情况是( )
(忽略水蒸气和温度变化对实验 结果的影响)
A.A处上升,B处下降 B.A、B两处都下降
C.A处下降,B处上升 D.A、B两处都不变
例8.写出下列反应化学方程式:
_________________________________________________________
_________________________________________________________
_________________________________________________________
_________________________________________________________
例9.把一瓶二氧化碳气体倒人盛有阶梯形蜡烛的烧杯中,可观察到 ,说明二
氧化碳 ,所以二氧化碳可作 剂。
例10.图为实验室制取二氧化碳的装置图,根据图形回答问题。
⑴ 写出图中标有标号的仪器名称:
a ,b ,c ,d 。
⑵ 该图中选用的药品应为:A ,B ,
其中药品A应从 加入,药品B应从 加入,先加 再加 。
⑶ 指出该图中出现的错误。
① ;
② ;
③ 。
1. 二氧化碳气体本身没有 性,但当空气中的二氧化碳 正常含量时,会对人体产生有害影响。所以在
人群密集的地方,应注意 。在进入一些可能会含有较多二氧化碳气体的地方之前,应该
那里的二氧化碳含量,看是否会威胁到人体的健康。
2. 往盛紫色石蕊溶液的试管里通入二氧化碳,溶液变 色,加热试管,溶液变 色。
3. 下列有关CO 的实验中,只能证明CO 的物理性质的实验是( )
2 2
4.二氧化碳下列用途,只与它的物理性质有关的是 ( )
A.灭火 B.制化肥 C. 制干冰 D.温室肥料
5.实验室制取二氧化碳一般有如下5步:
① 检查装置气密性;② 按要求装配好仪器;③向漏斗中注入稀盐酸;
④向锥形瓶中加几小块大理石;⑤收集气体。
正确的操作顺序是( )
A.①②③④⑤ B.②①④③⑤ C.①④②③⑤ D.②③④①⑤
6.下列过程中不会增加空气中二氧化碳含量的是 ( )A.呼吸作用 B.光合作用 C.汽油燃烧 D.煅烧石灰石
7.二氧化碳能灭火的原因是 ( )
A.二氧化碳能溶于水,生成碳酸
B.二氧化碳在高压低温下能变成“干冰”
C.二氧化碳是密度比空气大的气体
D.二氧化碳密度比空气大,一般情况下,既不能燃烧,又不支持燃烧
8.实验室里的石灰水久置后,瓶壁上产生不透明的白色物质,洗去它应选用 ( )
A.碱溶液 B.汽油 C.高温加热 D.稀盐酸
9.某化学兴趣小组用图中所示的装置做有关CO 的实验
2
(1) 甲同学将集气瓶中二氧化碳沿着漏斗缓缓倒入烧杯中(如A图所示),观察到现象
是 。该现象说明二氧化碳具有的性质是
① ;
② 。
(2) 乙同学将收集满CO 气体的试管倒插入紫色石蕊试液中(如图B所示),并轻轻振荡试管
2
①描述产生的现象: ;
②写出反应的化学方程式 。
(3) 丙同学向烧杯中倒入澄清石灰水(如C、D图所示),立即塞紧瓶塞,并轻轻振荡,①可观察到:系在导气管一
端的气球慢慢胀大, 。
②产生这一现象的原因是 ;
③写出发生反应的化学方程式 。
10.向盛有紫色石蕊试液的试管里通入二氧化碳,可观察到试液 。把该溶液加热,可观察到试管
内有 产生,溶液由 色变成 色。
11.写出下列反应的化学方程式,并指出是化合反应,还是分解反应。
① 实验室制二氧化碳: ,属 反应;
② 铁丝在氧气中燃烧: ,属 反应;
③ 加热碳酸: ,属 反应。
12.某同学按实验图组装好仪器,加入10余块石灰石与半容器的盐酸,顿时产生大量气体。立即用准备好的石灰水
和滴有紫色石蕊试液的蒸馏水进行二氧化碳性质实验,但他观察到两处与众不同的现象:
(1)澄清石灰水一直未见浑浊;
(2)通有二氧化碳后的紫色石蕊试液变红后,加热至沸腾也不能恢复紫色。
试分析出现这两种不同现象的原因。(提示:从盐酸的浓稀来思考)
13.设计一个实验,证明二氧化碳溶于水确实与水发生了化学反应,要求写出实验操作步骤,实验现象、结论。(提
示:可将石蕊制成蓝色石蕊试纸,蓝色石蕊试纸遇酸溶液变红)
操作步骤 实验现象 结论
四、课后作业
1.近年来地球气候逐渐变暖,科学家们认为这是“温室效应”所致。下列气体进入大气层能导致温室效应的是(
)
A.CO B.CO2 C.SO2 D.NO2
2.“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊溶液中,然后再加热,溶液颜色变化是( )A.先变蓝后变紫 B.变红后颜色不再改变
C.先变无色后变红色 D.先变红色后变紫色
3.“吸烟有害健康”,我国政府规定:从2011年5月1日起,公共室内禁止吸烟。烟草燃烧释放的物质中,能与血红
蛋白结合引起中毒的是( )
A.一氧化碳 B.二氧化碳 C.尼古丁 D.焦油
4.下列有关CO的说法正确的是( )
A.一氧化碳是有刺激性气味的有毒气体
B.在炉火上放一盆水,可以避免一氧化碳中毒
C.一氧化碳中含有氧元素和碳元素,所以它属于混合物
D.一氧化碳能与血红蛋白结合,导致人体缺氧
5.下列物质中,不能用来鉴别CO和CO 的是( )
2
A.澄清的石灰水 B.蒸馏水
C.灼热的氧化铜 D.紫色的石蕊试液
6.含有硫的煤在火炉中不完全燃烧时,排放出的下列气体组合中都属于大气污染气体的是( )
A.SO、CO B.CO、CO、SO C.CO、CO D.CO、SO
2 2 2 2 2 2
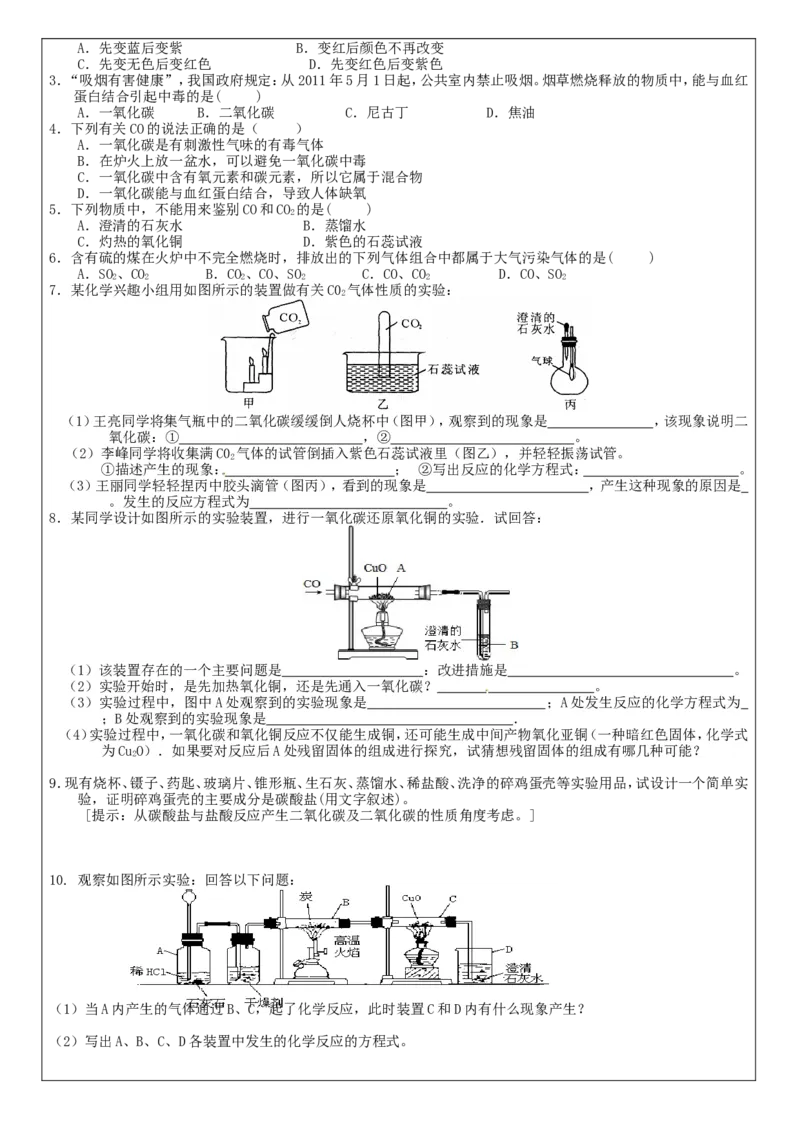
7.某化学兴趣小组用如图所示的装置做有关C0 气体性质的实验:
2
(1)王亮同学将集气瓶中的二氧化碳缓缓倒人烧杯中(图甲),观察到的现象是 ,该现象说明二
氧化碳:① ,② 。
(2)李峰同学将收集满C0 气体的试管倒插入紫色石蕊试液里(图乙),并轻轻振荡试管 。
2
①描述产生的现象: ; ②写出反应的化学方程式: 。
(3)王丽同学轻轻捏丙中胶头滴管(图丙),看到的现象是 ,产生这种现象的原因是
。发生的反应方程式为 。
8.某同学设计如图所示的实验装置,进行一氧化碳还原氧化铜的实验.试回答:
(1)该装置存在的一个主要问题是 :改进措施是 。
(2)实验开始时,是先加热氧化铜,还是先通入一氧化碳? 。
(3)实验过程中,图中A处观察到的实验现象是 ;A处发生反应的化学方程式为
;B处观察到的实验现象是 .
(4)实验过程中,一氧化碳和氧化铜反应不仅能生成铜,还可能生成中间产物氧化亚铜(一种暗红色固体,化学式
为CuO).如果要对反应后A处残留固体的组成进行探究,试猜想残留固体的组成有哪几种可能?
2
9.现有烧杯、镊子、药匙、玻璃片、锥形瓶、生石灰、蒸馏水、稀盐酸、洗净的碎鸡蛋壳等实验用品,试设计一个简单实
验,证明碎鸡蛋壳的主要成分是碳酸盐(用文字叙述)。
[提示:从碳酸盐与盐酸反应产生二氧化碳及二氧化碳的性质角度考虑。]
10. 观察如图所示实验:回答以下问题:
(1)当A内产生的气体通过B、C,起了化学反应,此时装置C和D内有什么现象产生?
(2)写出A、B、C、D各装置中发生的化学反应的方程式。初三化学第六单元综合检测题(A卷)
一、选择题(每小题只有一个正确答案,把正确答案序号填入下表。每小题3分,共45分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案
1.古代一些书法家、画家用墨书写或绘制的字画能够保存很长时间而不变色,这是因为( )
A.纸的质量好 B.碳的化学性质在常温下比较稳定
C.保存方法得当 D.碳在任何条件下都不与其他物质反应
2.下列变化属于物理变化的是( )
A.CO使人中毒 B.澄清石灰水长期露置在空气中
C.干冰变为二氧化碳气体 D.二氧化碳的水溶液使紫色石蕊试液变红
3.为了检验二氧化碳是否充满集气瓶,正确的方法是( )
A.加入澄清石灰水 B.滴入紫色石蕊试液
C.用燃着的木条放在瓶口 D.用燃着的木条迅速伸入瓶底
4.不能用来鉴别CO和CO 两种气体的方法是( )
2
A.通入澄清石灰水 B.观察颜色 C.通入紫色石蕊试液 D.点燃
5.常温下能与二氧化碳发生化合反应的物质是( )
A.水 B.澄清石灰水 C.氧气 D.木炭
6.下列气体既有可燃性又有还原性的化合物是( )
A.氧气 B.一氧化碳 C.二氧化碳 D.氮气
7.要除去二氧化碳中混有的一氧化碳,可把混合气体通过( )
A.水 B.炽热的炭层 C.澄清石灰水 D.灼热的氧化铜
8.下列各组仪器中,不能用来组装实验室制取二氧化碳装置的是( )
A.长颈漏斗、集气瓶、酒精灯 B.长颈漏斗、集气瓶、试管
C.长颈漏斗、锥形瓶、集气瓶 D.平底烧瓶、长颈漏斗、集气瓶
9.将干冰放在空气中,其周围就会产生大量的白雾,因而舞台上常用其制造云雾缭绕的环境。干冰能产生白雾的原
因是( )
A.干冰升华出大量的水蒸气
B.干冰升华发出大量的白色二氧化碳气体
C.干冰被空气中的氧气氧化产生了大量的白色气体
D.干冰升华时吸收大量的热,使周围温度降低,大量的水蒸气凝结成了小液滴
10. 将N、CO、CO 的混合气体依次通入足量石灰水和灼热CuO后,冷却至室温,剩余气体是( )
2 2
A.N、CO B.N C.CO D.N、CO、HO
2 2 2 2 2 2 2
11.下列关于碳单质的说法中,错误的是( )
A.碳元素组成的单质包括一氧化碳和二氧化碳 B.金刚石和石墨都是由碳元素组成的
C.单质碳的化学性质在常温下是不活泼的 D.单质碳在充足的氧气中燃烧生成二氧化碳
12.长期盛放石灰水的试剂瓶内壁有一层白膜,除去这白膜使试剂瓶变得明净的最好方法是( )
A.用蒸馏水冲洗 B.用钢丝刷刷洗 C.用稀盐酸洗涤 D.用热水冲洗
13.如果要除去一氧化碳气体中混有少量二氧化碳,应该采用的方法是( )
A.把混合气体点燃 B.把混合气体通过澄清石灰水
C.把混合气体通过灼热的氧化铜 D.把混合气体由一个容器倾倒到另一个容器里
14. 用一氧化碳在加热的条件下还原氧化铜,发现已制得的铜又很快变黑了,你推测产生这种现象的原因是( )
A.温度太低 B.试管口倾斜了
C.反应开始时,没有把试管内的空气排干净
D.铜没有在一氧化碳气流中冷却而又被空气中氧气所氧化
15. 一种无色气体X与炽热的木炭反应,得到另一种无色气体Y,Y在加热条件下与一种黑色固体反应又得到X和
一种亮红色固体,则气体X和Y是( )
A.X是CO,Y是CO B.X是CO,Y是CO
2 2
C.X是O,Y是CO D.X是O,Y是CO
2 2 2
二、填空题(25分)
16.(8分)家庭小实验:将洗净的碎鸡蛋壳(主要成分是碳酸钙)放入小玻璃杯中,然后加入适量的稀盐酸,观察到鸡
蛋壳表面 ,该反应的化学方程式是 ,立即用蘸有澄清石灰水的
玻璃片盖住,一会儿,便可观察到澄清石灰水 ,该反应的化学方程式是
。
17(. 7分)向盛有紫色石蕊试液的试管中通入适量的CO,紫色石蕊试液的试液变为 色,其反应的化学方程式
2
为: 。将反应后的溶液加热,则石蕊由 色变为 色,其
反应的化学方程式为: 。
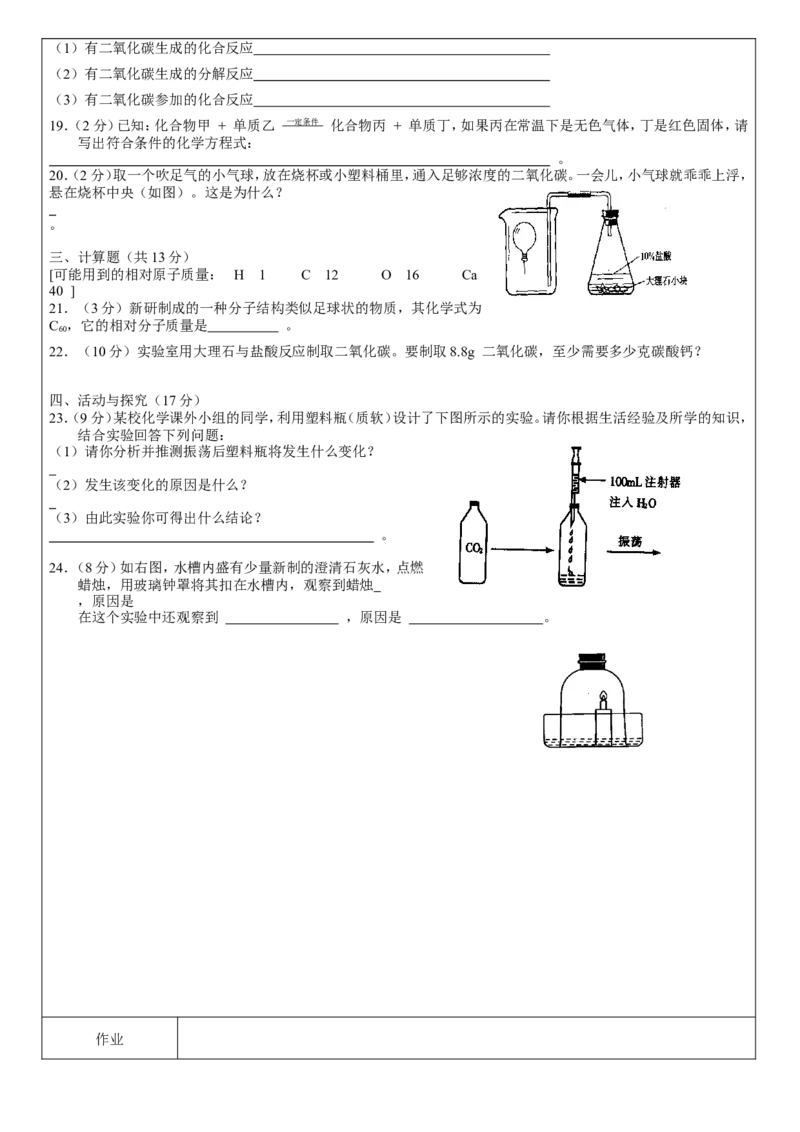
18.(6分)请按照要求写出下列反应的化学方程式(1)有二氧化碳生成的化合反应
(2)有二氧化碳生成的分解反应
(3)有二氧化碳参加的化合反应
19.(2分)已知:化合物甲 + 单质乙 一定条件 化合物丙 + 单质丁,如果丙在常温下是无色气体,丁是红色固体,请
写出符合条件的化学方程式:
。
20.(2分)取一个吹足气的小气球,放在烧杯或小塑料桶里,通入足够浓度的二氧化碳。一会儿,小气球就乖乖上浮,
悬在烧杯中央(如图)。这是为什么?
。
三、计算题(共13分)
[可能用到的相对原子质量: H 1 C 12 O 16 Ca
40 ]
21.(3分)新研制成的一种分子结构类似足球状的物质,其化学式为
C ,它的相对分子质量是 。
60
22.(10分)实验室用大理石与盐酸反应制取二氧化碳。要制取8.8g 二氧化碳,至少需要多少克碳酸钙?
四、活动与探究(17分)
23.(9分)某校化学课外小组的同学,利用塑料瓶(质软)设计了下图所示的实验。请你根据生活经验及所学的知识,
结合实验回答下列问题:
(1)请你分析并推测振荡后塑料瓶将发生什么变化?
(2)发生该变化的原因是什么?
(3)由此实验你可得出什么结论?
。
24.(8分)如右图,水槽内盛有少量新制的澄清石灰水,点燃
蜡烛,用玻璃钟罩将其扣在水槽内,观察到蜡烛
,原因是
在这个实验中还观察到 ,原因是 。
作业教学效果/
课后反思
针对本堂收获和自我表现(对应指数上打√)
学生自评 学生/家长签名
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩