文档内容
《晶体结构与性质》能力提升单元检测
学校:___________姓名:___________班级:___________考号:___________
一、单选题(16小题,每小题3分,共48分)
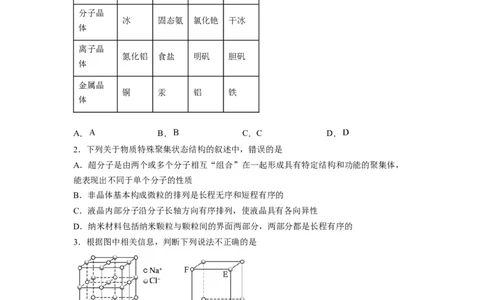
1.下列物质所属晶体类型分类正确的是
选项 A. B. C. D.
共价晶
石墨 生石灰 碳化硅 金刚石
体
分子晶
冰 固态氨 氯化铯 干冰
体
离子晶
氮化铝 食盐 明矾 胆矾
体
金属晶
铜 汞 铝 铁
体
A. B. C.C D.
2.下列关于物质特殊聚集状态结构的叙述中,错误的是
A.超分子是由两个或多个分子相互“组合”在一起形成具有特定结构和功能的聚集体,
能表现出不同于单个分子的性质
B.非晶体基本构成微粒的排列是长程无序和短程有序的
C.液晶内部分子沿分子长轴方向有序排列,使液晶具有各向异性
D.纳米材料包括纳米颗粒与颗粒间的界面两部分,两部分都是长程有序的
3.根据图中相关信息,判断下列说法不正确的是A.在NaCl晶体中,距离Na+最近的Cl-形成正八面体
B.该气态团簇分子的分子式为EF 或FE
4 4 4 4
C.1个Zn的晶胞中含有2个Zn原子
D.KO 晶体中每个K+周围有6个紧邻的K+,每个 周围有6个紧邻的
2
4.下列性质可能符合分子晶体特点的是(深度解析)
①熔点 ,易溶于水,水溶液能导电
②熔点 ,液态不导电,水溶液能导电
③能溶于 ,熔点 ,沸点
④熔点 ,质软,固态能导电,密度为
A.①④ B.②③ C.①② D.②④
5.根据下列性质判断,属于共价晶体的物质是。
A.熔点为2700℃,导电性好,延展性强
B.无色晶体,熔点大于3500℃,不导电,质硬,难溶于水和有机溶剂
C.无色晶体,能溶于水,质硬而脆,熔点为801℃,熔化时能导电
D.沸点为-78℃,微溶于水,硬度小,固态或液态时不导电
6.用 表示阿伏伽德罗常数的值,下列叙述正确的是
A.标准状况下,22.4LHF中HF分子的个数为
B.60g二氧化硅中 键个数为
C.1mol白磷中含有的 键个数为
D. 中含有的氧原子数且为
7.已知: 发生水解反应的机理如图,下列叙述正确的是
A. 的键角与白磷(P )的键角相同
4
B. 脱水后加热分解得到的晶体中每个Si可参与形成12个12元环
C. 和 均属于共价晶体(原子晶体)
D. 不能按照上述机理发生水解反应,原因是C的原子半径小
8.关于晶体的下列说法正确的是
A.任何晶体中,若含有阳离子就一定有阴离子
B.氯化钠溶于水时晶体中的离子键被破坏C.晶体中分子间作用力越大,分子越稳定
D.离子晶体中只含有离子键,不含有共价键
9.下列说法中正确的有
①含有离子的晶体一定是离子晶体;
②离子键是阴、阳离子间的相互吸引作用;
③金属晶体的导电性、导热性均与自由电子有关;
④共价键的强弱决定分子晶体熔、沸点的高低;
⑤共价晶体中一定含有共价键;
⑥分子晶体的熔点一定比金属晶体低;
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6;
⑧硬度由大到小:金刚石>碳化硅>晶体硅
A.2个 B.3个 C.4个 D.5个
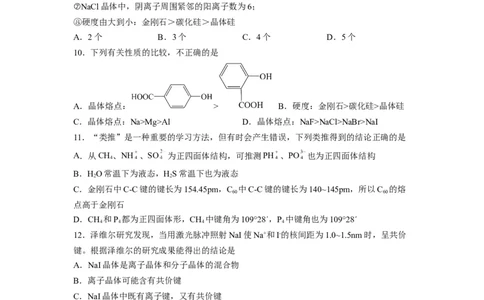
10.下列有关性质的比较,不正确的是
A.晶体熔点: > B.硬度:金刚石>碳化硅>晶体硅
C.晶体熔点:Na>Mg>Al D.晶体熔点:NaF>NaCl>NaBr>NaI
11.“类推”是一种重要的学习方法,但有时会产生错误,下列类推得到的结论正确的是
A.从CH、NH 、SO 为正四面体结构,可推测PH 、PO 也为正四面体结构
4
B.HO常温下为液态,HS常温下也为液态
2 2
C.金刚石中C-C键的键长为154.45pm,C 中C-C键的键长为140~145pm,所以C 的熔
60 60
点高于金刚石
D.CH 和P 都为正四面体形,CH 中键角为109°28ˊ,P 中键角也为109°28ˊ
4 4 4 4
12.泽维尔研究发现,当用激光脉冲照射NaI使Na+和I-的核间距为1.0~1.5nm时,呈共价
键。根据泽维尔的研究成果能得出的结论是
A.NaI晶体是离子晶体和分子晶体的混合物
B.离子晶体可能含有共价键
C.NaI晶体中既有离子键,又有共价键
D.共价键和离子键没有绝对的界限
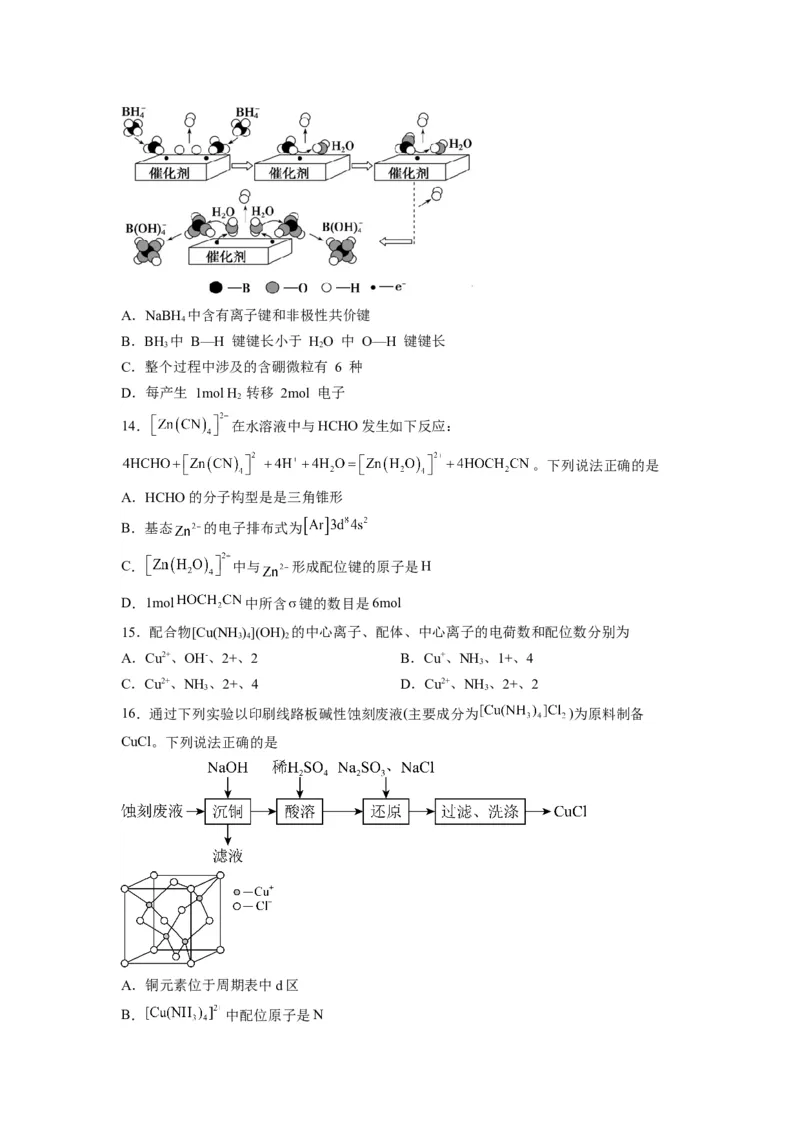
13.硼氢化钠(NaBH )与水在催化剂作用下获得氢气的微观过程如下图所示。下列说法正确
4
的是A.NaBH 中含有离子键和非极性共价键
4
B.BH 中 B—H 键键长小于 HO 中 O—H 键键长
3 2
C.整个过程中涉及的含硼微粒有 6 种
D.每产生 1mol H 转移 2mol 电子
2
14. 在水溶液中与HCHO发生如下反应:
。下列说法正确的是
A.HCHO的分子构型是是三角锥形
B.基态 的电子排布式为
C. 中与 形成配位键的原子是H
D.1mol 中所含 键的数目是6mol
15.配合物[Cu(NH )](OH) 的中心离子、配体、中心离子的电荷数和配位数分别为
3 4 2
A.Cu2+、OH-、2+、2 B.Cu+、NH 、1+、4
3
C.Cu2+、NH 、2+、4 D.Cu2+、NH 、2+、2
3 3
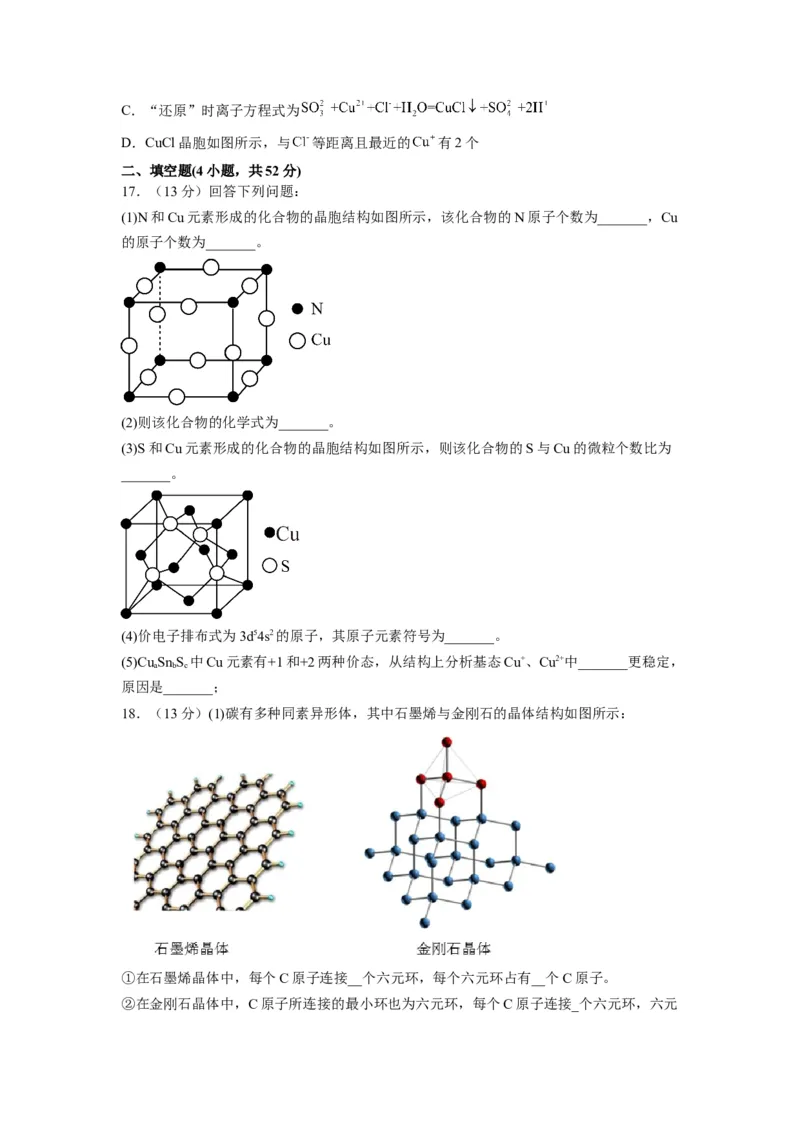
16.通过下列实验以印刷线路板碱性蚀刻废液(主要成分为 )为原料制备
CuCl。下列说法正确的是
A.铜元素位于周期表中d区
B. 中配位原子是NC.“还原”时离子方程式为
D.CuCl晶胞如图所示,与 等距离且最近的 有2个
二、填空题(4小题,共52分)
17.(13分)回答下列问题:
(1)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的N原子个数为_______,Cu
的原子个数为_______。
(2)则该化合物的化学式为_______。
(3)S和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的S与Cu的微粒个数比为
_______。
(4)价电子排布式为3d54s2的原子,其原子元素符号为_______。
(5)CuSn S 中Cu元素有+1和+2两种价态,从结构上分析基态Cu+、Cu2+中_______更稳定,
a b c
原因是_______;
18.(13分)(1)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:
①在石墨烯晶体中,每个C原子连接__个六元环,每个六元环占有__个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接_个六元环,六元环中最多有__个C原子在同一平面。
(2)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以_相结合,其晶胞中共有8
个原子,其中在面心位置贡献__个原子。
(3)如图为S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__。
8
(4)比较下列储卤化物的熔点和沸点,分析其变化规律及原因__。
GeCl GeBr GeI
4 4 4
熔点/℃ -49.5 26 146
沸点/℃ 83.1 186 约400
19.(13分)回答下列问题:
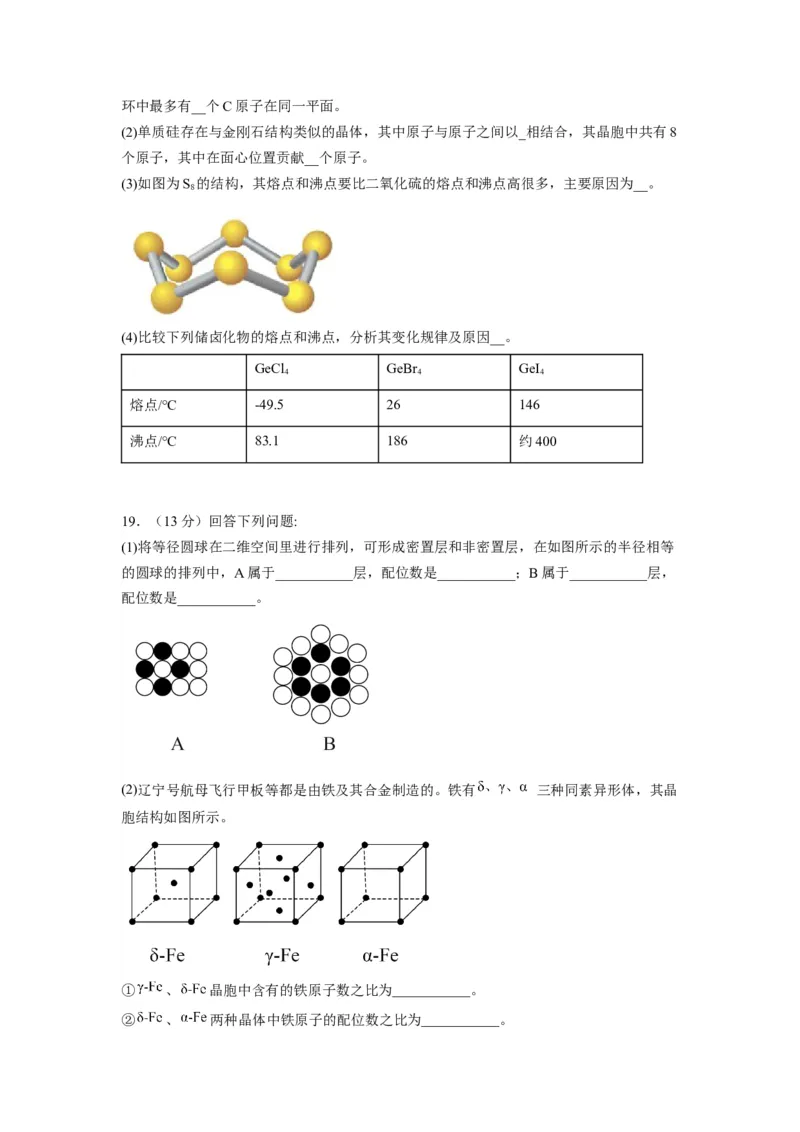
(1)将等径圆球在二维空间里进行排列,可形成密置层和非密置层,在如图所示的半径相等
的圆球的排列中,A属于___________层,配位数是___________;B属于___________层,
配位数是___________。
(2)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有 三种同素异形体,其晶
胞结构如图所示。
① 、 晶胞中含有的铁原子数之比为___________。
② 、 两种晶体中铁原子的配位数之比为___________。③若 晶胞的边长为a cm, 晶胞的边长为b cm,则两种晶体的密度之比为
___________。
20.(13分)配位化学的应用十分广泛,在经济、生产、生活等方面都有重要作用。
(1)在配合物中部分分子或离子与中心离子较紧密地结合在一起,组成在溶液中能够稳定存
在的整体,称为“内界”{书写时用“[ ]”与外界分离}。与中心离子结合不够紧密的离子
则处于“外界”。内界和外界不同,物质的性质也不同,如CoCl 与NH 形成的三种配合
3 3
物A、B、C,Co3+的配位数均为6,但它们的颜色各异,如果各取1molA、B、C溶于水,
加入足量硝酸银溶液,分别产生1mol、2mol、3mol白色沉淀。则它们的化学式分别为A:
_______;B:_______,C:_______,它们的配体分别是A:_______;B:_______;C:
_______。
(2)甲醇和CO合成乙酸时,使用铑羰基化合物[Rh(CO) I]-作为催化剂,使得原本需要高压
2 2
下才能进行的反应在低压下也能进行。其催化机理如图:
①根据Rh的化合价可将I、II、III、IV、V分为:
1)化合价_______价,包含_______;
2)化合价_______价,包含_______;(有几种化合价填几类,可不填满,也可增加)
②上述机理中包括_______步反应,其中一步为氧化加成,该步反应的方程式为_______。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育