文档内容
南充高中高 2025 级高一(上)第一次月考
化学试题
(考试时间:75分钟 试卷总分:100分)
命题:左志红 审题:李忠恒
可能用到的相对原子质量:H1 C12 N14 O16
一、选择题(本题共15个小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.下列变化中,涉及氧化还原反应的是
①易燃物的自燃 ②绿色植物的光合作用 ③钢铁的锈蚀 ④食物的腐败
A.①②③④ B.①②③ C.②③④ D.①③④
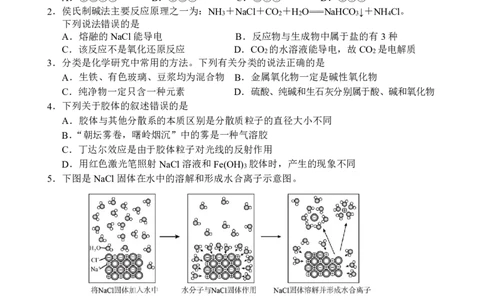
2.侯氏制碱法主要反应原理之一为:NH +NaCl+CO +H O===NaHCO ↓+NH Cl。
3 2 2 3 4
下列说法错误的是
A.熔融的NaCl能导电 B.反应物与生成物中属于盐的有3种
C.该反应不是氧化还原反应 D.CO 的水溶液能导电,故CO 是电解质
2 2
3.分类是化学研究中常用的方法。下列有关分类的说法正确的是
A.生铁、有色玻璃、豆浆均为混合物 B.金属氧化物一定是碱性氧化物
C.纯净物一定只含一种元素 D.硫酸、纯碱和生石灰分别属于酸、碱和氧化物
4.下列关于胶体的叙述错误的是
A.胶体与其他分散系的本质区别是分散质粒子的直径大小不同
B.“朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶
C.丁达尔效应是由于胶体粒子对光线的反射作用
D.用红色激光笔照射NaCl溶液和Fe(OH) 胶体时,产生的现象不同
3
5.下图是NaCl固体在水中的溶解和形成水合离子示意图。
下列说法正确的是
A.固体NaCl中不存在离子,不能导电 B.NaCl溶于水的过程中发生电子转移
C.水合钠离子和水合氯离子中水分子的朝向不同 D.NaCl通电情况下才能电离
6.下列离子方程式书写正确的是
A.用醋酸除水垢:CaCO +2H+===Ca2++H O+CO ↑
3 2 2
B.用Al置换AgNO 溶液中的银:Al+Ag+===Ag+Al3+
3
C.Cu(OH) 与稀硝酸反应:Cu(OH) +2H+===Cu2++2H O
2 2 2
D.Fe (SO ) 溶液中加入足量Ba(OH) 溶液:
2 4 3 2
Fe3++SO2-+Ba2++3OH-===Fe(OH) ↓+BaSO ↓
4 3 4
17.下列各组离子,能在透明溶液中大量共存的是
A.Al3+、NO-、OH-、NH+ B.Na+、Cl-、Cu2+、SO2-
3 4 4
C.H+、K+、NO-、CO2- D.Ca2+、 Na+、NO-、SO2-
3 3 3 4
8.从化合价升降角度分析,下列反应不可能实现的是(方程式均未配平)
A.NO+HNO NO +H O
3 2 2
B.S+NaOH Na SO +Na S+H O
2 3 2 2
C.Fe3++SO+HO Fe2++SO2-+H+
2 2 4
D.Cr O2-+H++Cl Cr3++Cl-+H O
2 7 2 2
9.下列变化需要加入还原剂才能实现的是
A.KMnO MnO B.SO H SO C.HCl Cl D.FeCl Fe
4 2 3 2 4 2 2
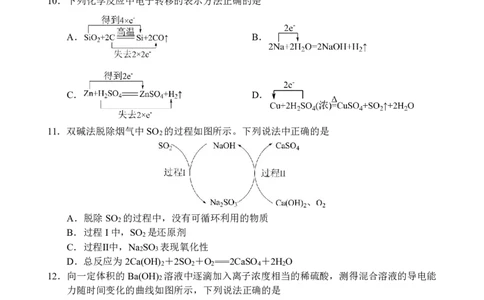
10.下列化学反应中电子转移的表示方法正确的是
A. B.
C. D.
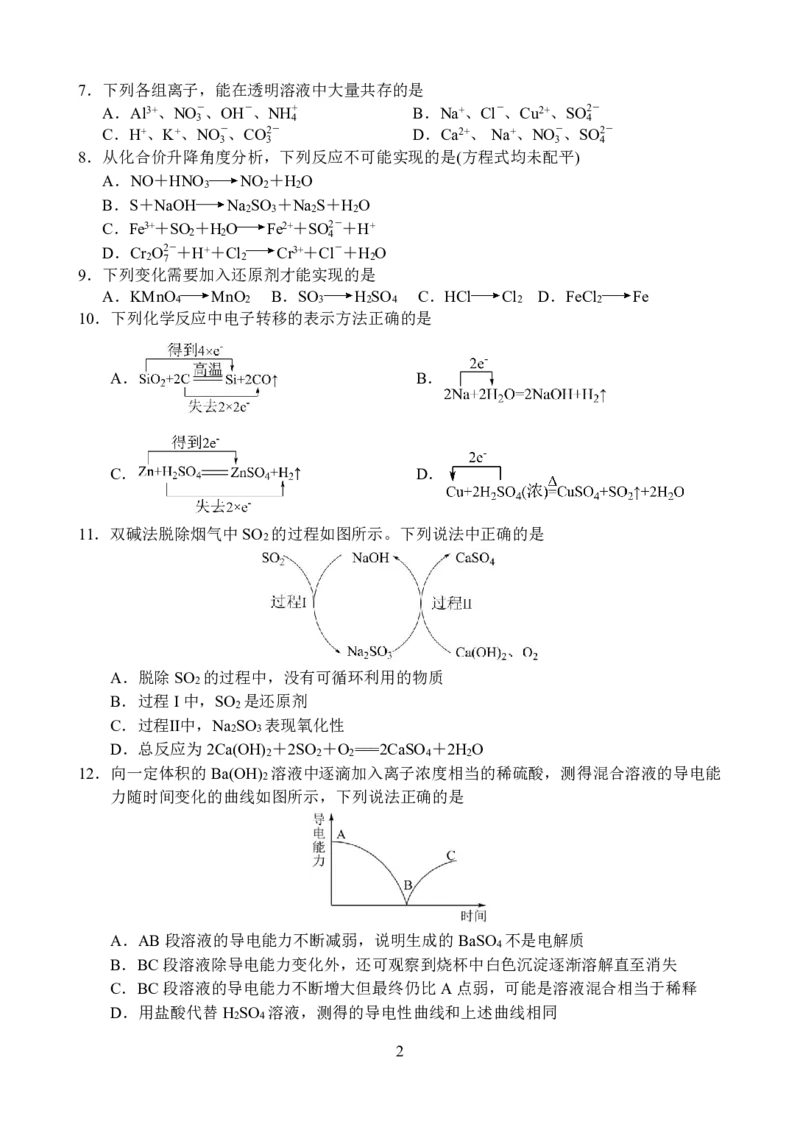
11.双碱法脱除烟气中SO 的过程如图所示。下列说法中正确的是
2
A.脱除SO 的过程中,没有可循环利用的物质
2
B.过程I中,SO 是还原剂
2
C.过程Ⅱ中,Na SO 表现氧化性
2 3
D.总反应为2Ca(OH) +2SO +O ===2CaSO +2H O
2 2 2 4 2
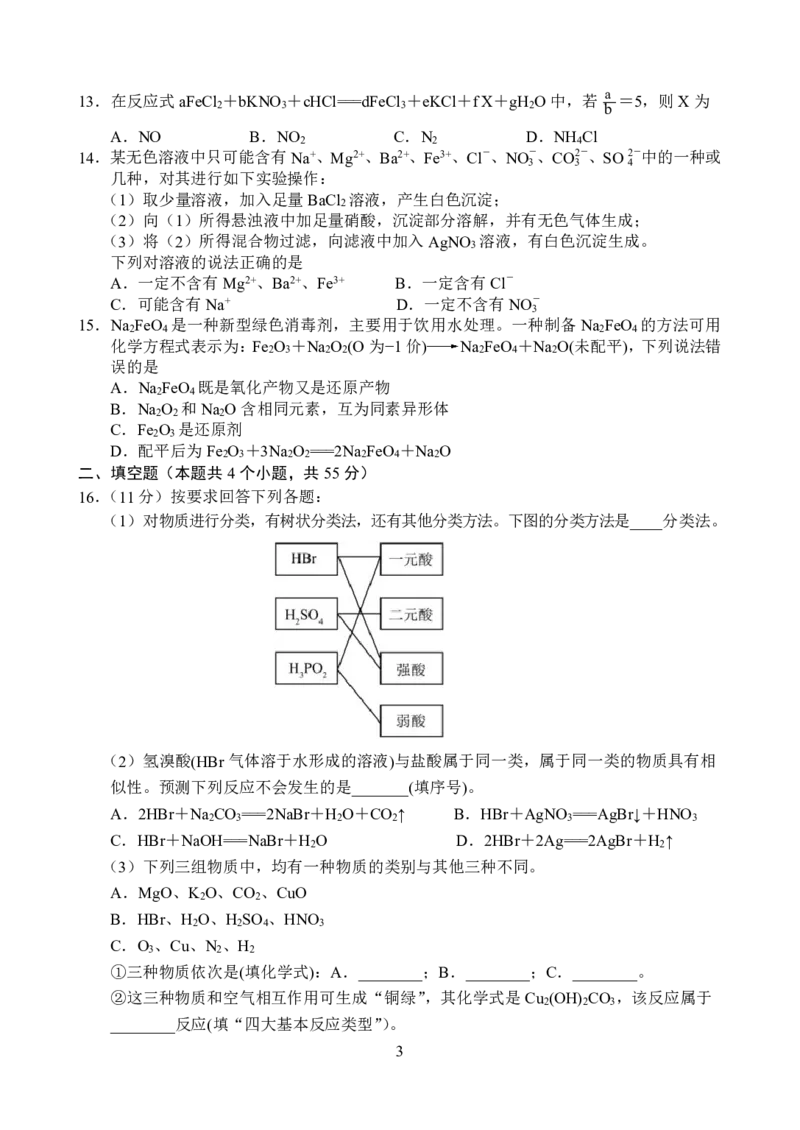
12.向一定体积的Ba(OH) 溶液中逐滴加入离子浓度相当的稀硫酸,测得混合溶液的导电能
2
力随时间变化的曲线如图所示,下列说法正确的是
A.AB段溶液的导电能力不断减弱,说明生成的BaSO 不是电解质
4
B.BC段溶液除导电能力变化外,还可观察到烧杯中白色沉淀逐渐溶解直至消失
C.BC段溶液的导电能力不断增大但最终仍比A点弱,可能是溶液混合相当于稀释
D.用盐酸代替H SO 溶液,测得的导电性曲线和上述曲线相同
2 4
213.在反应式aFeCl
2
+bKNO
3
+cHCl===dFeCl
3
+eKCl+fX+gH
2
O中,若―
b
a =5,则X为
A.NO B.NO C.N D.NH Cl
2 2 4
14.某无色溶液中只可能含有Na+、Mg2+、Ba2+、Fe3+、Cl-、NO-、CO2-、SO2-中的一种或
3 3 4
几种,对其进行如下实验操作:
(1)取少量溶液,加入足量BaCl 溶液,产生白色沉淀;
2
(2)向(1)所得悬浊液中加足量硝酸,沉淀部分溶解,并有无色气体生成;
(3)将(2)所得混合物过滤,向滤液中加入AgNO 溶液,有白色沉淀生成。
3
下列对溶液的说法正确的是
A.一定不含有Mg2+、Ba2+、Fe3+ B.一定含有Cl-
C.可能含有Na+ D.一定不含有NO-
3
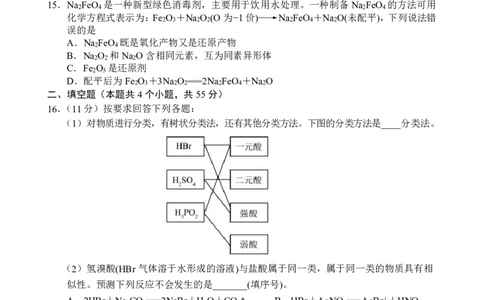
15.Na FeO 是一种新型绿色消毒剂,主要用于饮用水处理。一种制备Na FeO 的方法可用
2 4 2 4
化学方程式表示为:Fe O +Na O (O为−1价) Na FeO +Na O(未配平),下列说法错
2 3 2 2 2 4 2
误的是
A.Na FeO 既是氧化产物又是还原产物
2 4
B.Na O 和Na O含相同元素,互为同素异形体
2 2 2
C.Fe O 是还原剂
2 3
D.配平后为Fe O +3Na O ===2Na FeO +Na O
2 3 2 2 2 4 2
二、填空题(本题共4个小题,共55分)
16.(11分)按要求回答下列各题:
(1)对物质进行分类,有树状分类法,还有其他分类方法。下图的分类方法是____分类法。
(2)氢溴酸(HBr气体溶于水形成的溶液)与盐酸属于同一类,属于同一类的物质具有相
似性。预测下列反应不会发生的是_______(填序号)。
A.2HBr+Na CO ===2NaBr+H O+CO ↑ B.HBr+AgNO ===AgBr↓+HNO
2 3 2 2 3 3
C.HBr+NaOH===NaBr+H O D.2HBr+2Ag===2AgBr+H ↑
2 2
(3)下列三组物质中,均有一种物质的类别与其他三种不同。
A.MgO、K O、CO 、CuO
2 2
B.HBr、H O、H SO 、HNO
2 2 4 3
C.O 、Cu、N 、H
3 2 2
①三种物质依次是(填化学式):A.________;B.________;C.________。
②这三种物质和空气相互作用可生成“铜绿”,其化学式是Cu (OH) CO ,该反应属于
2 2 3
________反应(填“四大基本反应类型”)。
317.(20分)分类是认识和研究物质及其变化的一种常用的科学方法。现有以下物质:
①N O ②H ③Ba(OH) 固体 ④稀硫酸 ⑤酒精 ⑥食盐水 ⑦锌
2 5 2 2
⑧熔融硫酸钡 ⑨NaHSO 固体 ⑩HNO ⑪氢氧化铁胶体
4 3
(1)从物质分类的角度看,①属于_________(填“酸性氧化物”或“碱性氧化物”)。
(2)上述物质中属于电解质的是____(填序号,下同);上述条件下能导电的物质有___。
(3)请写出③在水溶液中的电离方程式:___________。
(4)从上述物质中选出适当物质进行反应,写出制备②的离子方程式:____________。
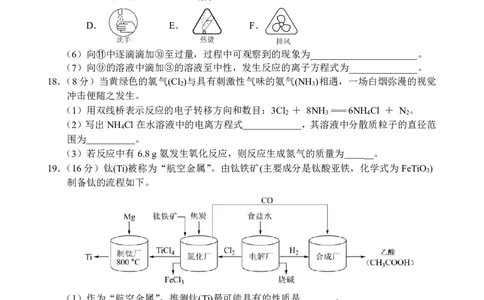
(5)实验室制备⑪,下列实验提示图标不需要用到的是(填序号)______________。
A. B. C.
D. E. F.
(6)向⑪中逐滴滴加⑩至过量,过程中可观察到的现象为______________________。
(7)向⑨的溶液中滴加③的溶液至中性,发生反应的离子方程式为______________。
18.(8分)当黄绿色的氯气(Cl )与具有刺激性气味的氨气(NH )相遇,一场白烟弥漫的视觉
2 3
冲击便随之发生。
(1)用双线桥表示反应的电子转移方向和数目:3Cl + 8NH ===6NH Cl + N 。
2 3 4 2
(2)写出NH Cl在水溶液中的电离方程式 ,其溶液中分散质粒子的直径范
4
围为 。
(3)若反应中有6.8g氨发生氧化反应,则反应生成氮气的质量为 __。
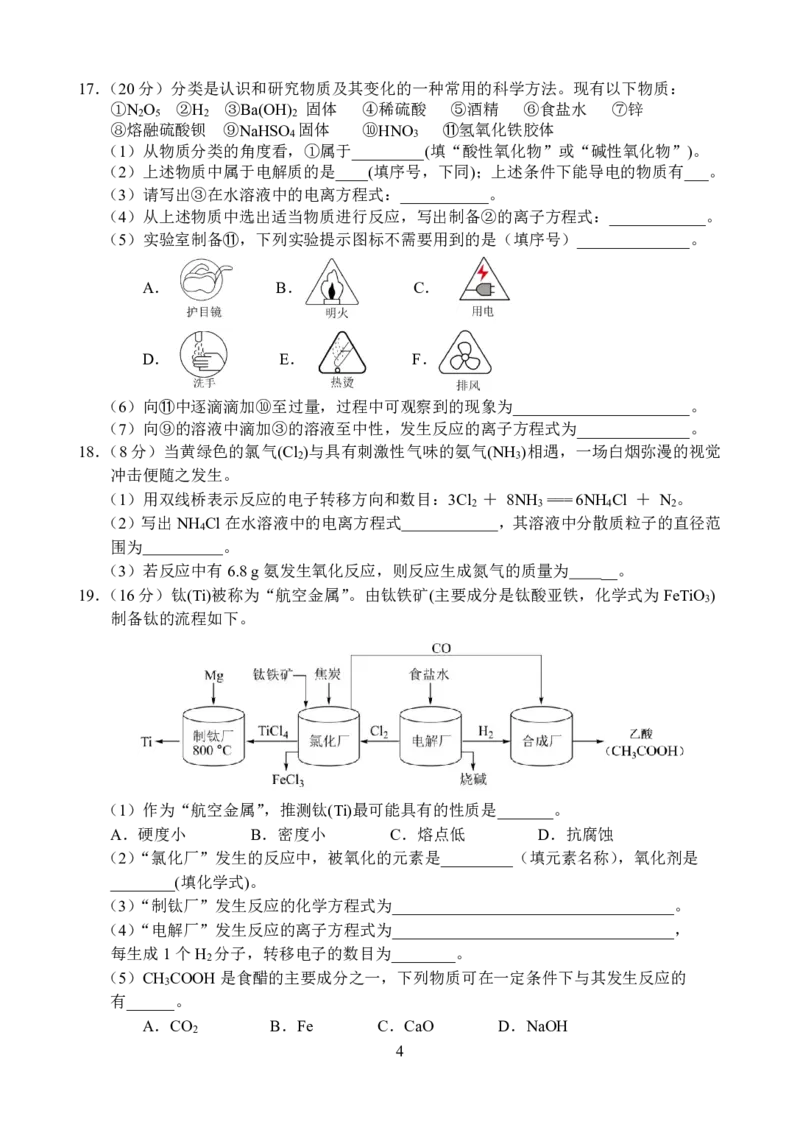
19.(16分)钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为FeTiO )
3
制备钛的流程如下。
(1)作为“航空金属”,推测钛(Ti)最可能具有的性质是_______。
A.硬度小 B.密度小 C.熔点低 D.抗腐蚀
(2)“氯化厂”发生的反应中,被氧化的元素是_________(填元素名称),氧化剂是
________(填化学式)。
(3)“制钛厂”发生反应的化学方程式为___________________________________。
(4)“电解厂”发生反应的离子方程式为___________________________________,
每生成1个H 分子,转移电子的数目为________。
2
(5)CH COOH是食醋的主要成分之一,下列物质可在一定条件下与其发生反应的
3
有______。
A.CO B.Fe C.CaO D.NaOH
2
4