文档内容
溶 液 单元测试
一、选择题:(本题有10小题,每小题2分,共20分。每小题只有一个选项符合题意)
1. 30℃时Ca(OH) 在水中的溶解度为0.16g/100g水。在此温度下,实验小组为制备饱和的
2
澄清石灰水,称取5.6g生石灰,放入1000g水中,充分搅拌后冷却至30℃,过滤得到的澄清石
灰水中溶质的质量
A、等于5.6g B、大于5.6g C、等于1.6g D、小于5.6g
2.某金属加工厂生产过程中的废液含有少量硝酸银和硝酸铜,为回收利用资源和防止污
染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤出的固体中加入少量稀盐
酸,无气体产生。则下列有关说法中,正确的是
A.滤出的固体中一定含有银和铜,一定不含铁
B.滤出的固体中一定含有银,可能含有铜和铁
C.滤液中一定有硝酸亚铁,可能有硝酸银和硝酸铜
D.滤液中一定有硝酸亚铁,一定没有硝酸银和硝酸铜
3.下列实验设计不可行的是
A.加适量稀硫酸以除去硫酸钠溶液中的氢氧化钠
B.将氧气和氢气的混合气体通过灼热的氧化铜以除去氢气
C.用稀盐酸除去铜粉中的镁粉
D.在不用指示剂的情况下,选用CaCO 粉末将含有盐酸的CaCI 溶液调至pH=7
3 2
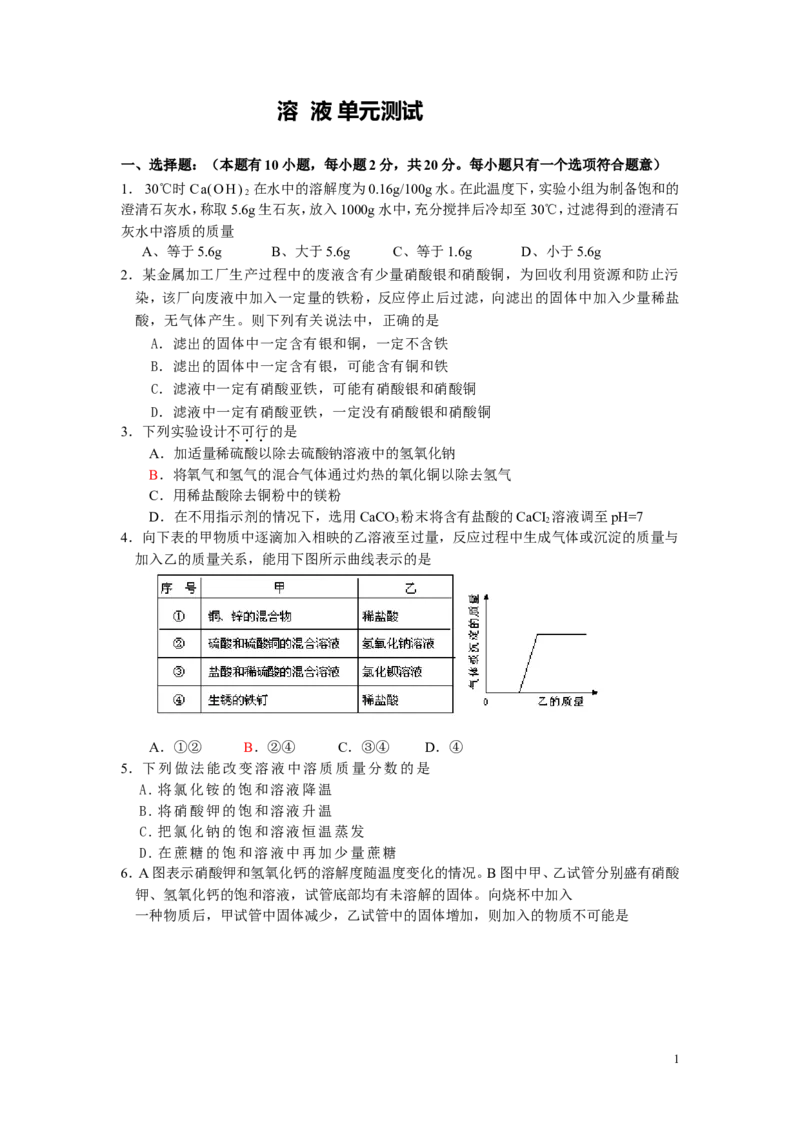
4.向下表的甲物质中逐滴加入相映的乙溶液至过量,反应过程中生成气体或沉淀的质量与
加入乙的质量关系,能用下图所示曲线表示的是
A.①② B.②④ C.③④ D.④
5.下列做法能改变溶液中溶质质量分数的是
A.将氯化铵的饱和溶液降温
B.将硝酸钾的饱和溶液升温
C.把氯化钠的饱和溶液恒温蒸发
D.在蔗糖的饱和溶液中再加少量蔗糖
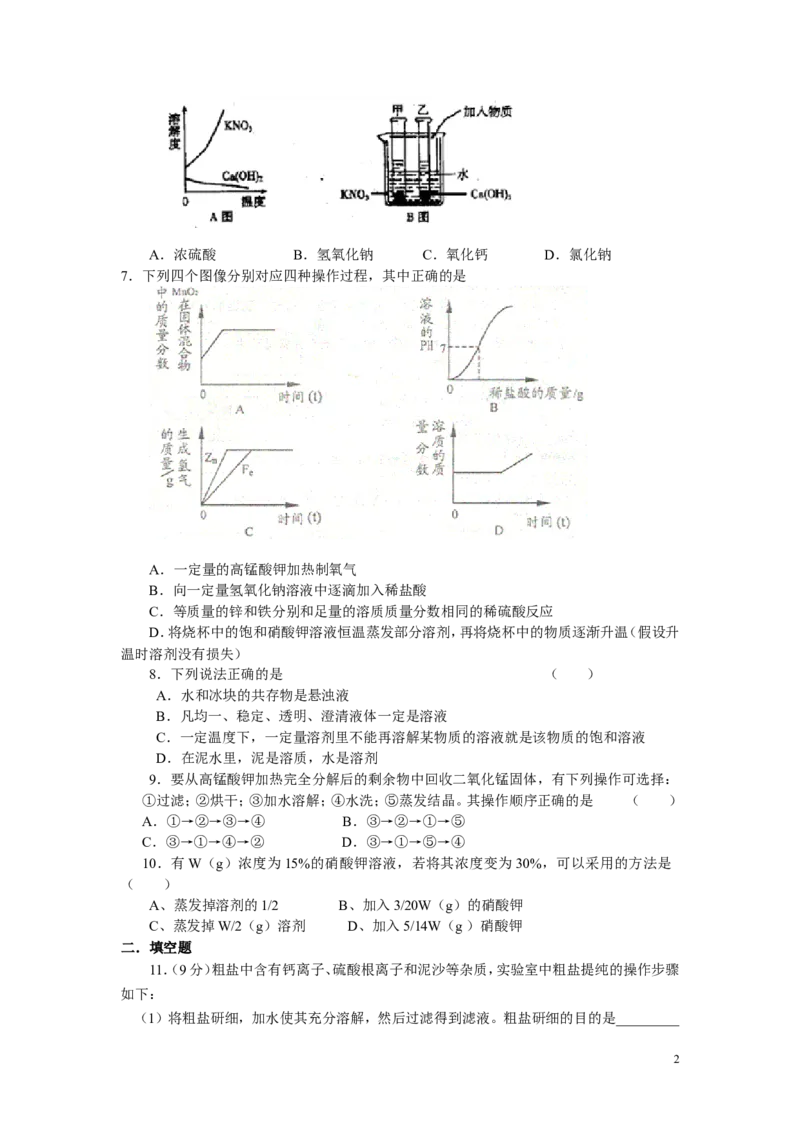
6.A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况。B图中甲、乙试管分别盛有硝酸
钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入
一种物质后,甲试管中固体减少,乙试管中的固体增加,则加入的物质不可能是
1A.浓硫酸 B.氢氧化钠 C.氧化钙 D.氯化钠
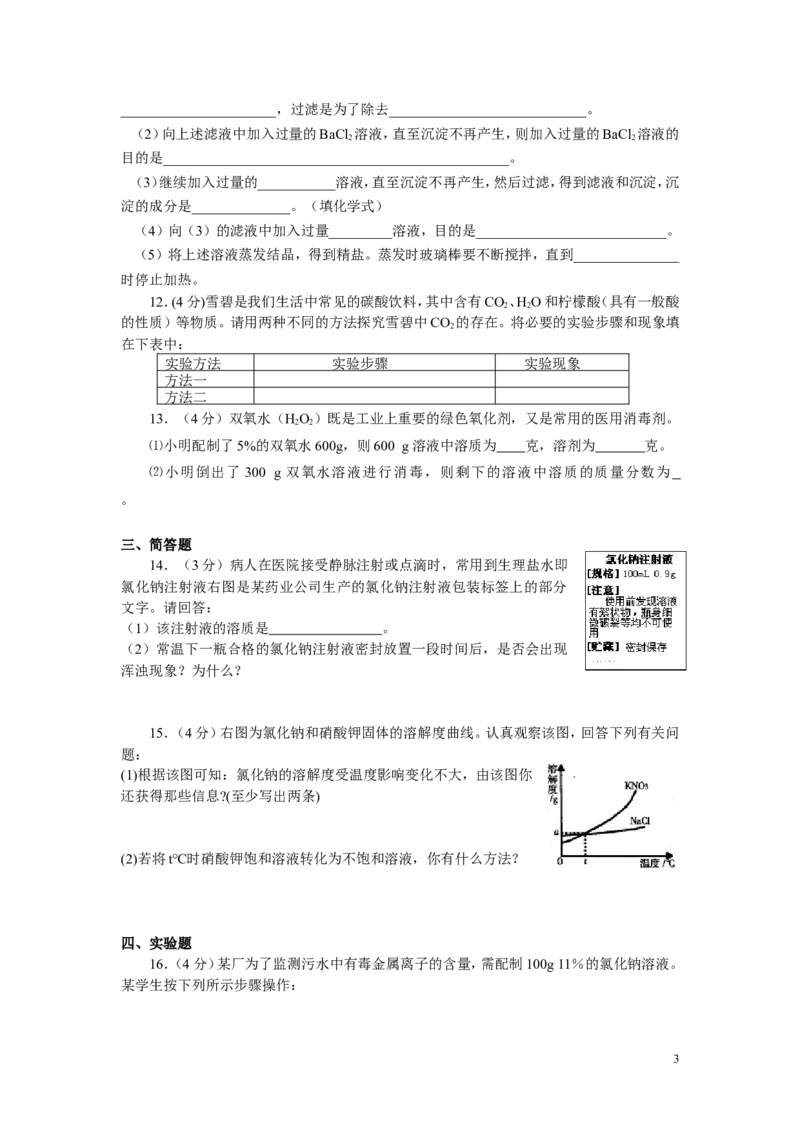
7.下列四个图像分别对应四种操作过程,其中正确的是
A.一定量的高锰酸钾加热制氧气
B.向一定量氢氧化钠溶液中逐滴加入稀盐酸
C.等质量的锌和铁分别和足量的溶质质量分数相同的稀硫酸反应
D.将烧杯中的饱和硝酸钾溶液恒温蒸发部分溶剂,再将烧杯中的物质逐渐升温(假设升
温时溶剂没有损失)
8.下列说法正确的是 ( )
A.水和冰块的共存物是悬浊液
B.凡均一、稳定、透明、澄清液体一定是溶液
C.一定温度下,一定量溶剂里不能再溶解某物质的溶液就是该物质的饱和溶液
D.在泥水里,泥是溶质,水是溶剂
9.要从高锰酸钾加热完全分解后的剩余物中回收二氧化锰固体,有下列操作可选择:
①过滤;②烘干;③加水溶解;④水洗;⑤蒸发结晶。其操作顺序正确的是 ( )
A.①→②→③→④ B.③→②→①→⑤
C.③→①→④→② D.③→①→⑤→④
10.有W(g)浓度为15%的硝酸钾溶液,若将其浓度变为30%,可以采用的方法是
( )
A、蒸发掉溶剂的1/2 B、加入3/20W(g)的硝酸钾
C、蒸发掉W/2(g)溶剂 D、加入5/14W(g )硝酸钾
二.填空题
11.(9分)粗盐中含有钙离子、硫酸根离子和泥沙等杂质,实验室中粗盐提纯的操作步骤
如下:
(1)将粗盐研细,加水使其充分溶解,然后过滤得到滤液。粗盐研细的目的是_________
2______________________,过滤是为了除去____________________________。
(2)向上述滤液中加入过量的BaCl 溶液,直至沉淀不再产生,则加入过量的BaCl 溶液的
2 2
目的是_________________________________________________。
(3)继续加入过量的___________溶液,直至沉淀不再产生,然后过滤,得到滤液和沉淀,沉
淀的成分是______________。(填化学式)
(4)向(3)的滤液中加入过量_________溶液,目的是___________________________。
(5)将上述溶液蒸发结晶,得到精盐。蒸发时玻璃棒要不断搅拌,直到_______________
时停止加热。
12.(4分)雪碧是我们生活中常见的碳酸饮料,其中含有CO、HO和柠檬酸(具有一般酸
2 2
的性质)等物质。请用两种不同的方法探究雪碧中CO 的存在。将必要的实验步骤和现象填
2
在下表中:
实验方法 实验步骤 实验现象
方法一
方法二
13.(4分)双氧水(HO)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂。
2 2
⑴小明配制了5%的双氧水600g,则600 g溶液中溶质为 克,溶剂为 克。
⑵小明倒出了 300 g 双氧水溶液进行消毒,则剩下的溶液中溶质的质量分数为
。
三、简答题
14.(3分)病人在医院接受静脉注射或点滴时,常用到生理盐水即
氯化钠注射液右图是某药业公司生产的氯化钠注射液包装标签上的部分
文字。请回答:
(1)该注射液的溶质是 。
(2)常温下一瓶合格的氯化钠注射液密封放置一段时间后,是否会出现
浑浊现象?为什么?
15.(4分)右图为氯化钠和硝酸钾固体的溶解度曲线。认真观察该图,回答下列有关问
题:
(1)根据该图可知:氯化钠的溶解度受温度影响变化不大,由该图你
还获得那些信息?(至少写出两条)
(2)若将t℃时硝酸钾饱和溶液转化为不饱和溶液,你有什么方法?
四、实验题
16.(4分)某厂为了监测污水中有毒金属离子的含量,需配制100g 11%的氯化钠溶液。
某学生按下列所示步骤操作:
3A B C D E
(1)你认为以上步骤中有错误的是(填序号) ________________;
(2)请你纠正其错误操作:________________________________________________
。
17.(6分)初三(5)班小李想探究哪些因素影响固体物质在水中的溶解度?请帮助他完成
下面的实验探究。
[ 猜 想 ] 因素l:溶质的种类;因素2:温度 。
[实验探究](一) 因素l:溶质的种类
操作步骤:在常温下,用量筒各量取5mL蒸馏水,分别加入①、②、③3支试管中,
再分别加入NaCl、KNO、Ca(OH) 各2g,振荡,观察各物质的溶解情况。
3 2
实验现象: 。
实验结论: 。
(二)因素2:温度(以KN0 为例)
3
操作步骤:用量筒各量取5ml蒸馏水,分别加入①、②、③3支试管中,再各加入
5g KN0 晶体,将试管①保持在常温下,将试管②加热并保持在40℃,将试管③加
3
热并保持在60℃,振荡,观察各试管中KN0 的溶解情况。
3
实验现象: 。
实验结论: 。
四.计算题:(6分)
18.右图是某工业盐产品质量指标。为了测定该工业
盐中氯化钠的质量分数,取100g该工业盐进行实验: (工业盐)
氯化钠(%)≥95.5
①用碳酸钠来测定杂质氯化钙的质量分数,得到1g沉淀。
水分(%)≤3.4
②实际测得水的质量分数为3.3%: 氯化钙(%)≤1.1
求:(1)100g该工业盐中含氯化钙的质量分数。
(2)通过计算,判断此工业盐中氯化钠的质量分数是否符合产品质量指标?
4