文档内容
第三章 铁 金属材料
单元检测
一、选择题(本题包括16小题,每小题3分,共48分,每小题只有一个选项符合题意。)
1.(2022·新疆生产建设兵团第三师图木舒克市第二中学高一期末)下列生活中的物质与其有效成分的化
学式、用途的对应关系中,不正确的是
选项 A. B. C. D.
生活中的物质 铁红 漂白液 小苏打 复方氢氧化铝片
有效成分的化学式 Fe O NaClO NaHCO Al(OH)
3 4 3 3
用途 做红色颜料 做杀菌漂白剂 做发酵粉 做抗酸药
A.A B.B C.C D.D
【答案】A
【详解】A.铁红是Fe O 的俗称,故A错误;
2 3
B.漂白液的有效成分为NaClO,具有强氧化性,常用来做消毒剂,故B正确;
C.小苏打是碳酸氢钠的俗称,加热易分解放出二氧化碳,可以做发酵粉,故C正确;
D.复方氢氧化铝片的主要成分为氢氧化铝,能够和盐酸反应,可以做抗酸药,故D正确;
故选A。
2.(2022·全国·高一单元测试)下列关于新型合金材料说法不正确的是
A.镧镍合金能大量吸收H 形成金属氢化物,可作储氢材料
2
B.钛合金生物相容性好,强度大,可作人造骨骼
C.生铁和钢是含碳量不同的两种铁碳合金,生铁的含碳量比钢的含碳量高
D.合金的熔点比其成分金属的熔点高
【答案】D
【详解】A.镧镍合金能大量吸收H ,并与H 结合成金属氢化物,金属氢化物稍稍加热又容易分解,所
2 2
以可用作储氢材料,故A正确;
B.钛合金生物相容性好,强度大,常用作人造骨骼,故B正确;
C.生铁是含碳量大于2%的铁碳合金,钢是对含碳量在0.02%~2%之间的铁碳合金的统称,生铁的含碳量
比钢高,故C正确;
D.合金的熔点比其成分金属的熔点低,故D错误;
答案为D。
3.(2022·辽宁·渤海大学附属高级中学高一期末)下列有关物质的性质与用途的描述错误的是
A.Al具有良好的延展性,故铝可用于制作铝金属制品
B.镁铝合金的密度大、强度高,是制造飞机和宇宙飞船的理想材料
C.Al、Al O 均能与酸、碱反应,因此铝制炊具不宜用来蒸煮酸性或碱性食物
2 3
学科网(北京)股份有限公司D.“蛟龙号”载人潜水器的耐压球壳是用钛合金制造的,合金具有硬度大等优点
【答案】B
【详解】A.铝常用于制作铝金属制品,主要是Al具有良好的延展性,故A正确;
B.镁铝合金的密度小、强度高,是制造飞机和宇宙飞船的理想材料,故B错误;
C.Al、Al O 均能与酸、碱反应,因此铝制炊具不宜用来蒸煮和长时间盛放酸性或碱性食物,故C正确;
2 3
D.“蛟龙号”载人潜水器的耐压球壳是用钛合金制造的,说明钛合金具有硬度大等优点,故D正确。
综上所述,答案为B。
4.(2022·全国·高一课时练习)下列关于金属铝的叙述中,不正确的是
A.铝的化学性质很活泼,但在空气中不易锈蚀
B.铝箔在空气中受热可以熔化,且发生剧烈燃烧
C.铝是比较活泼的金属,常温下能与盐酸、NaOH溶液等发生反应
D.相同质量的铝分别与足量的盐酸和氢氧化钠反应,产生氢气的量相同
【答案】B
【详解】A..铝的化学性质很活泼,在空气中易形成氧化膜,很稳定不易锈蚀,故A正确;
B.铝箔在空气中受热可以熔化形成小球,表面生成氧化铝,氧化铝熔点很高,不能发生剧烈燃烧反应,
故B错误;
C.铝是比较活泼的金属,常温下能与盐酸、NaOH溶液等发生氧化还原反应,故C正确;
D.铝分别与盐酸和氢氧化钠反应,都能产生氢气,因为是足量的盐酸和氢氧化钠,铝的质量相同,所以
产生氢气的量相同,故D正确;
故答案:B。
5.(2022·全国·高一单元测试)下列有关铁及其化合物的叙述中正确的是
A.赤铁矿的主要成分为
B. 与 溶液反应生成血红色沉淀
C.氢氧化亚铁是白色固体,置于空气中迅速变成灰绿色,最终变成红褐色
D.为了除去 溶液中的 杂质,可向溶液中通入过量
【答案】C
【详解】A.赤铁矿的主要成分为 ,磁铁矿的主要成分为 ,A错误;
B. 与 溶液反应生成 ,是血红色溶液,B错误;
C.氢氧化亚铁是白色固体,易被氧化为氢氧化铁,故置于空气中迅速变成灰绿色,最终变成红褐色,C
正确;
D.氯气能与氯化亚铁溶液反应生成氯化铁,铁能与氯化铁溶液反应生成氯化亚铁,为了除去 溶液
中的 杂质,不能向溶液中通入过量 ,应加入铁粉,D错误;
答案选C。
6.(2022·全国·高一课时练习)下列有关除杂的操作中不正确的是
A. 溶液中含少量 杂质:加入过量的 粉,过滤
学科网(北京)股份有限公司B.除去 溶液中少量的 :加入新制氯水
C.除 溶液中少量的 杂质可以向溶液中加入过量铁粉,然后过滤
D.除 溶液中的 杂质可以向溶液中加入过量铁粉
【答案】D
【详解】A.加入过量的铁粉,发生反应 ,再经过过滤,能够除去杂质,A正确;
B.新制氯水与 反应: ,可以除去杂质,B正确;
C.向含有少量 的 溶液中加入过量 粉: ,过滤即可除杂,C正确;
D. 与氯化铁反应,将原物质除去,不能除杂,应向该溶液中通入足量的氯气,D错误;
故选D。
7.(2022·全国·高一课时练习)验证Fe3+与Fe2+能够相互转化。
按下列顺序实验 对应现象
①向FeCl 溶液中加入过量铁 i.溶液由黄色变成浅绿
3
粉 色
②滴加KSCN溶液 ii.溶液无明显变化
③再滴加几滴氯水 iii.溶液变红
下列分析不合理的是A.解释现象i的反应:2Fe3++Fe=3Fe2+
B.实验②与③可以调换顺序
C.溶液变红涉及的反应:Cl +2Fe2+=2Cl-+2Fe3+
2
D.氧化性:Cl >Fe3+>Fe2+
2
【答案】B
【详解】A.①向FeCl 溶液中加入过量铁粉,溶液由黄色变成浅绿色,这是由于FeCl 与Fe发生反应产生
3 3
FeCl ,该反应的离子方程式为:2Fe3++Fe=3Fe2+,A正确;
2
B.实验②证明反应后的溶液中不存在Fe3+,实验③证明Fe2+被氧化成Fe3+;若二者调换,无法证明该转化
关系,所以实验②与③不能调换顺序,B错误;
C.溶液变红,说明Fe2+被氯水氧化成Fe3+,发生反应为:Cl +2Fe2+=2Cl-+2Fe3+,C正确;
2
D.在氧化还原反应中,微粒的氧化性:氧化剂>氧化产物。根据反应2Fe3++Fe=3Fe2+可知物质的氧化性:
Fe3+>Fe2+,根据Cl +2Fe2+=2Cl-+2Fe3+可知微粒的氧化性:Cl >Fe3+,所以氧化性:Cl >Fe3+>Fe2+,D正确;
2 2 2
故合理选项是B。
8.(2022·全国·高一单元测试)对实验I~IV的实验操作现象判断正确的是
学科网(北京)股份有限公司A.实验I:产生红褐色沉淀 B.实验II:溶液颜色变红
C.实验III:放出大量气体 D.实验IV:铜片表面有黑色固体生成
【答案】C
【详解】A.将氯化铁饱和溶液加入到沸水中加热至溶液呈红褐色可得到氢氧化铁胶体,不是氢氧化铁红
褐色沉淀,故A错误;
B.三价铁离子与硫氰化钾溶液反应生成硫氰合铁,溶液变红色,与二价铁离子不反应,溶液不变色,故
B错误;
C.铝与氢氧化钠溶液反应生成NaAlO 和氢气,有大量气体生成,故C正确;
2
D.硫酸铁与铜单质反应生成硫酸亚铁和硫酸铜,不会有黑色固体生成,故D错误;
故选C。
9.(2022·广东汕头·高一期末)金属及其化合物的转化关系是化学学习的重要内容之一。下列各组物质
的转化关系,不能均由一步反应实现的是
A.
B.
C.
D.
【答案】C
【详解】A.Na与H O反应生成NaOH,NaOH与CO 反应生成Na CO ,Na CO 与HCl反应生成NaCl,A不
2 2 2 3 2 3
符合题意;
B.Mg与氯气或HCl反应生成MgCl ,MgCl 与NaOH溶液反应生成Mg(OH) 沉淀,Mg(OH) 与H SO 反应生
2 2 2 2 2 4
成MgSO ,B不符合题意;
4
C.Al与O 反应生成Al O ,Al O 与水不反应,故不能一步转化为Al(OH) ,C符合题意;
2 2 3 2 3 3
D.Fe与HCl反应生成FeCl ,FeCl 与碱反应生成Fe(OH) ,Fe(OH) 可被O 氧化为Fe(OH) ,D不符合题意;
2 2 2 2 2 3
故答案选C。
10.(2022·四川·宁南中学高一开学考试)下列各组离子在给定条件的溶液中可能大量共存的是
A.加入铝片有大量氢气产生的溶液中:Mg2+、K+、SO 、Cl-
B.碱性无色溶液中:Na+、K+、MnO 、NO
C.在0.1mol/L的盐酸中:Ca2+、Fe2+、Na+、ClO-
D.在强碱性溶液中:Ca2+、K+、NH 、Cl-
【答案】A
学科网(北京)股份有限公司【详解】A.加入铝片有大量氢气产生的溶液可能是强酸也可能是强碱,强酸溶液中有大量的H+,H+、
Mg2+、K+、SO 、Cl-能够大量共存,强碱溶液中有大量的OH-,OH-与Mg2+不能大量共存,A符合题意;
B.无色溶液中不可能含有大量的MnO ,B不合题意;
C.在0.1mol/L的盐酸中有大量的H+,H+、Fe2+、ClO-因发生氧化还原反应而不能大量共存,C不合题意;
D.在强碱性溶液中有大量的OH-,OH-、NH 不能大量共存,D不合题意;
故答案为:A。
11.(2022·全国·高一单元测试)下列实验操作、现象或结论均正确的是
选项 实验操作 现象或结论
A 用酒精灯点燃铝箔 铝箔剧烈燃烧,产生白烟
B 焰色反应时直接观察火焰颜色 未观察到紫色火焰,说明不含
C 向某溶液中先通Cl ,再滴加KSCN溶液 溶液变红,说明溶液中含有
2
D 使用胶头滴管伸入NaOH溶液中滴加FeSO 溶液 先看到白色絮状沉淀
4
A.A B.B C.C D.D
【答案】D
【详解】A.铝箔受热时表明生成熔点很高的氧化铝,所以铝箔燃烧的现象是熔而不滴,A错误;
B.观察K的焰色反应应透过蓝色钴玻璃,B错误;
C.为了确定原溶液中是否含有Fe2+,应先滴加KSCN溶液再通Cl ,C错误;
2
D.使用胶头滴管伸入NaOH溶液中滴加FeSO 溶液,在底部生成Fe(OH) 沉淀,为白色絮状沉淀,D正确;
4 2
综上所述答案为D。
12.(2022·全国·高一课时练习)易拉罐的主要成分为铝合金,其中以铝铁合金和铝镁合金最为常见。为
确定铝合金中金属的成分,现取几小块易拉罐碎片进行下列实验,其中实验方案、现象与结论均正确的
是
选项 实验方案 现象与结论
A 加入盐酸 产生无色气体,含铝、铁、镁三种金属
B 加入NaOH溶液 有无色气体产生,含有镁、铝两种金属
C 加入盐酸后,向所得溶液中再加入少量NaOH溶液 产生白色沉淀,一定只含有镁
D 用盐酸溶解并放置一会儿后,加入KSCN溶液 溶液呈血红色,含有铁
A.A B.B C.C D.D
【答案】D
【详解】A.因铝、铁、镁都能和盐酸反应产生气体,故不能确定含有铝、铁、镁三种金属,A项错误;
B.铝、铁镁中只有铝可与 溶液反应生成无色气体,不能证明含有 ,B项错误;
学科网(北京)股份有限公司C.加入盐酸后,向所得溶液中再加入少量 溶液产生白色沉淀,则合金中可能含有镁,也可能含有
铝,C项错误;
D.铁单质与盐酸反应生成亚铁离子,在空气中放置一会儿,亚铁离子易被氧化为铁离子,在溶液中滴加
溶液,溶液呈血红色,D项正确;
综上所述,答案为D。
13.(2022·全国·高一单元测试)元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模
型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为
铁元素的“价一类”二维图,箭头表示部分物质间的转化关系,下列说法正确的是
A.铁与水蒸气在高温条件下反应可实现转化①
B.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成黑色粉末
C.由图可预测:高铁酸钠(Na FeO )具有强氧化性,可用于消毒
2 4
D.加热Fe(OH) ,发生转化⑥,加水可溶解Fe(OH)
3 3
【答案】C
【详解】A.①表示铁单质缓慢氧化转化为Fe O ,高温下铁与水蒸气生成四氧化三铁,不能实现上述转
2 3
化①,A错误;
B.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化四氧化三铁,不能发生转化②,B错误;
C.据图可知处于高价态的物质具有强氧化性,高铁酸钠中铁为+6价,处于高价态,具有强氧化性,C正
确;
D.Fe(OH) 难溶于水,加水不溶解,D错误;
3
综上所述答案为C。
14.(2022·全国·高一单元测试)某同学对铁的氧化物产生浓厚兴趣,查阅资料后制成以下卡片:
下列说法正确的是
A.FeO、Fe O 和Fe O 均为黑色固体
2 3 3 4
B.反应②的温度比反应③的温度高
学科网(北京)股份有限公司C.热稳定性顺序:FeO>Fe O
2 3
D.四氧化三铁中铁元素的化合价复杂,若写成氧化物的形式,则化学式可写为FeO·Fe O
2 3
【答案】D
【详解】A.Fe O 为红色固体,A错误;
2 3
B.根据题意可知Fe在500℃时生成Fe O ,继续升高温度生成Fe O ,而在1400℃时Fe O 转化为Fe O ,
3 4 2 3 2 3 3 4
所以反应②的温度比反应③的温度低,B错误;
C.FeO不稳定,在空气中会被迅速氧化为Fe O ,C错误;
3 4
D.四氧化三铁中Fe为+2价和+3价,个数比为1:2,化学式可写为FeO·Fe O ,D正确;
2 3
综上所述答案为D。
15.(2022·江西·丰城九中高一期末)工业废弃物的资源化回收再利用,可以更大限度地发挥原材料的价
值。下图是工业生产纳米磁性氧化铁的流程:
下列说法不正确的是
A.用 溶液浸泡是为了除去废铁屑表面的铁锈
B.若生产中不通入 ,暴露在空气中生产,将不能得到高纯度产品
C.加适量的 是为了将部分 氧化为 ,涉及反应:
D.溶液A中 和 的浓度比为1:2
【答案】A
【分析】用 溶液浸泡废铁屑除去废铁屑表面的油污,用硫酸溶液铁,加入过氧化氢将部分 氧
化为 ,加入氢氧化钠、在隔绝空气的条件下加热生成纳米四氧化三铁。
【详解】A.用 溶液浸泡废铁屑是为了除去废铁屑表面的油污,故A错误;
B.若生产中不通入 ,暴露在空气中生产, 被氧气氧化为 ,不能得到高纯度产品,故B正确;
C.四氧化三铁中含有+2价和+3价的铁, 具有氧化性,加适量的 是为了将部分 氧化为
,涉及反应: ,故C正确;
D.四氧化三铁中+2价和+3价的铁物质的量比为1:2,所以溶液A中 和 的浓度比为1:2,故D正
确;
选A
16.(2022·江西·临川一中高一阶段练习)13.6gFe和Fe O 的混合物,加入150mL足量的稀硫酸,在标准
2 3
状况下收集到1.12LH ,向反应后的溶液中滴加KSCN溶液不变红。为中和过量的稀硫酸,并使Fe元素全
2
部转化为Fe(OH) 沉淀,恰好消耗了200mL3mol/L的NaOH溶液,则该稀H SO 的物质的量浓度为
2 2 4
A.2.25mol/L B.2mol/L C.3mol/L D.0.6mol/L
【答案】B
学科网(北京)股份有限公司【详解】根据题干信息可知,涉及反应有:Fe+H SO =FeSO +H ↑、Fe O +3H SO =Fe (SO ) +3H O、
2 4 4 2 2 3 2 4 2 4 3 2
Fe+Fe (SO ) =3FeSO 、FeSO +2NaOH=Fe(OH) ↓+Na SO 、2NaOH+H SO =Na SO +2H O,即反应最后铁元素完
2 4 3 4 4 2 2 4 2 4 2 4 2
全沉淀后,溶液中的溶质只剩下Na SO ,根据Na+和 守恒可得:n(Na+)=n(NaOH)=2n(
2 4
)=2n(H SO ),即n(NaOH)=2n(H SO ),则0.2L×3mol/L=2×0.15L×c(H SO ),解得c(H SO )=2mol/L,故答案为:
2 4 2 4 2 4 2 4
B。
二、非选择题(本题包括4小题,共52分)
17.(2022·全国·高一单元测试)铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问
题。
(1)所含铁元素既有氧化性又有还原性的物质是___________(填字母代号)。
A.Fe B.FeCl C.FeSO D.Fe O
2 4 2 3
(2)向沸水中逐滴滴加lmol/LFeCl 溶液﹐至液体呈透明的红褐色,该分散系中粒子直径的范围是
3
___________nm。
(3)电子工业需要用30%的FeCl 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl 溶液与铜反应
3 3
的离子方程式:___________。某校同学为测定FeCl 腐蚀铜后所得溶液的组成,进行了如下实验:首先取
3
少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是___________,在此基础上,又进
行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO 溶液,得白色沉淀,
3
___________(填实验操作,下同)、___________、干燥,称量沉淀质量为43.05g。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是___________(填字母代号)。
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
【答案】(1)BC
(2)1~100
(3) Fe3+ 过滤 洗涤
(4)B
【解析】(1)
当元素处于最高价态时只有氧化性,当元素处于最低价态时只有还原性,当元素处于中间价态时既有氧
化性又有还原性, Fe只有还原性,FeCl 既有氧化性又有还原性, FeSO 既有氧化性又有还原性,Fe O
2 4 2 3
只有氧化性,故选BC;
(2)
向沸水中逐滴滴加lmol/LFeCl 溶液﹐至液体呈透明的红褐色,得到氢氧化铁胶体,该分散系中粒子直径
3
的范围是1~100nm。
(3)
FeCl 溶液与铜反应生成氯化亚铁和氯化铜,反应的离子方程式是 。Fe3+遇KSCN溶
3
液变为血红色,取少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是Fe3+;取50.0mL
学科网(北京)股份有限公司待测溶液,向其中加入足量的AgNO 溶液,得白色氯化银沉淀,过滤、洗涤、干燥,称量沉淀质量。
3
(4)
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe3+,故A错误;
B.Fe2+能使酸性高锰酸钾溶液褪色,向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有
Fe2+,故B正确;
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,溶液显红色,可能原溶液中含有Fe3+,故C错误;
选B。
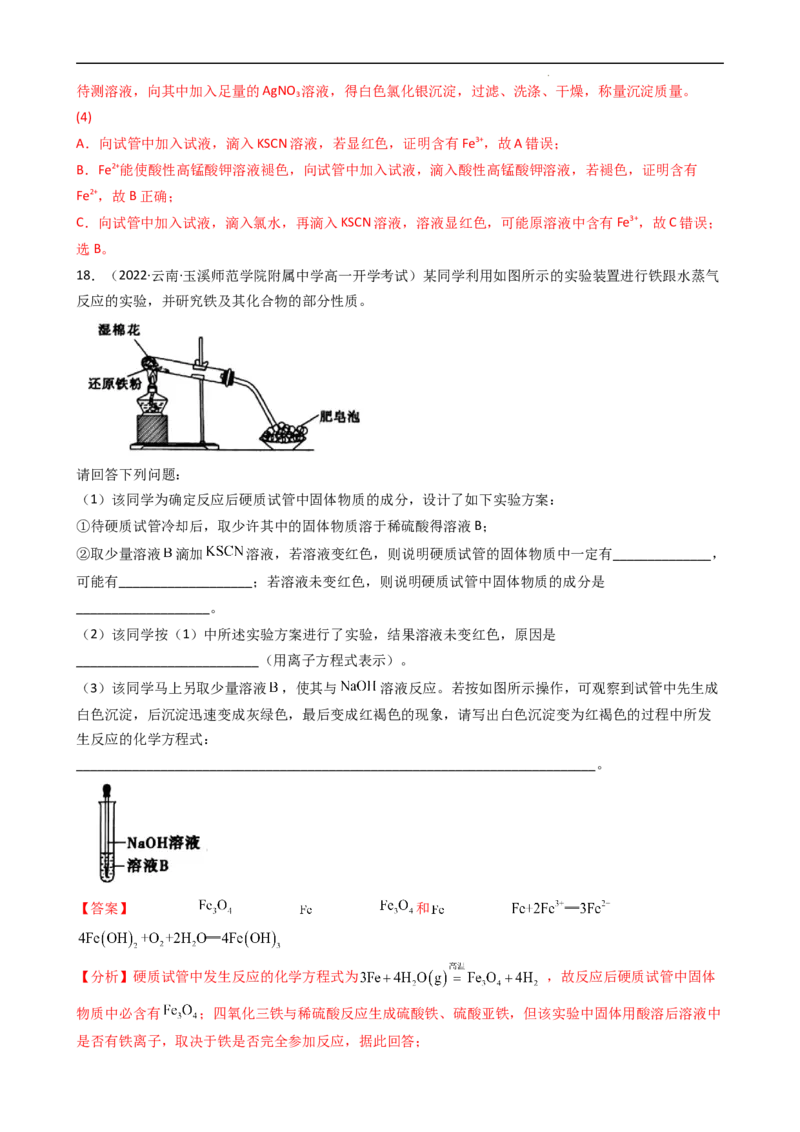
18.(2022·云南·玉溪师范学院附属中学高一开学考试)某同学利用如图所示的实验装置进行铁跟水蒸气
反应的实验,并研究铁及其化合物的部分性质。
请回答下列问题:
(1)该同学为确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液 滴加 溶液,若溶液变红色,则说明硬质试管的固体物质中一定有______________,
可能有___________________;若溶液未变红色,则说明硬质试管中固体物质的成分是
___________________。
(2)该同学按(1)中所述实验方案进行了实验,结果溶液未变红色,原因是
__________________________(用离子方程式表示)。
(3)该同学马上另取少量溶液 ,使其与 溶液反应。若按如图所示操作,可观察到试管中先生成
白色沉淀,后沉淀迅速变成灰绿色,最后变成红褐色的现象,请写出白色沉淀变为红褐色的过程中所发
生反应的化学方程式:
__________________________________________________________________________。
【答案】 和
【分析】硬质试管中发生反应的化学方程式为 ,故反应后硬质试管中固体
物质中必含有 ;四氧化三铁与稀硫酸反应生成硫酸铁、硫酸亚铁,但该实验中固体用酸溶后溶液中
是否有铁离子,取决于铁是否完全参加反应,据此回答;
学科网(北京)股份有限公司【详解】(1)取②中少量溶液 滴加 溶液,若溶液变红色,说明有 , 由反应产物 转化
而来,说明硬质试管的固体物质中一定有 ,可能有少量未反应的Fe,因为少量铁剩余不影响上述现
象;若溶液未变红色,说明无 ,则固体物质的成分为 和 ,残渣在用酸溶解时因为铁较多而使
消耗完,溶液中存在着的是 ;
(2)结合(1)的分析,可知溶液未变红色的原因是铁和铁离子反应生成了亚铁离子,铁离子消耗完了,离子
方程式为: ;
(3)另取少量溶液 ,与 溶液反应,可观察到试管中先生成白色沉淀,则溶液B中含FeSO 、不含
4
Fe (SO ) ,若按如图所示操作,FeSO 与 溶液发生复分解反应,产生白色Fe(OH) 沉淀,Fe(OH) 沉淀
2 4 3 4 2 2
被溶解氧或接触空气中氧气后被氧化,沉淀迅速变成灰绿色,最后变成红褐色的现象,故发生反应的化
学方程式: 。
19.(2022·湖南·长郡中学高一期末)根据下图的化学反应框图解图。
已知:粉末化合物A是红棕色,粉末单质B是金属单质
(1)单质F是________,溶液E加入氢氧化钠溶液的现象是_____________________;
(2)写出下列反应的化学方程式:
A+B→C+D_____________________________________;
D→H:_________________________________。
(3)写出下列反应的离子方程式:
E+Cl →G:__________________;
2
G+C→E:________________________;
B→F+H:__________________________。
【答案】 H (氢气) 生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色 2Al +
2
Fe O 2Fe + Al O Al O + 2NaOH=2NaAlO +H O 2Fe2+ +Cl =2Fe3+ +2Cl- 2Fe3+ + Fe = 3Fe2+ 2Al +
2 3 2 3 2 3 2 2 2
2OH- + 2H O = 2 + 3H ↑
2 2
【分析】粉末化合物A是红棕色,粉末单质B是金属单质,粉状单质B能与强碱溶液反应产生单质F说明
B为铝,F为氢气,结合转化关系可知,A为Fe O ,C为Fe,D为Al O ,E为FeCl ,G为FeCl ,H为
2 3 2 3 2 3
学科网(北京)股份有限公司NaAlO ,据此解答。
2
【详解】粉末化合物A是红棕色,粉末单质B是金属单质,粉状单质B能与强碱溶液反应产生单质F说明
B为铝,F为氢气,结合转化关系可知,A为Fe O ,C为Fe,D为Al O ,E为FeCl ,G为FeCl ,H为
2 3 2 3 2 3
NaAlO ,
2
(1) 由上述分析可知,单质F是H (氢气),溶液E为FeCl 溶液,向FeCl 溶液中加入氢氧化钠溶液先生成氢
2 2 2
氧化亚铁,后迅速被氧化为氢氧化铁,现象是生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色;
故答案为H (氢气);生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色;
2
(2)A+B→C+D的反应为铝热反应,化学方程式为:2Al + Fe O 2Fe + Al O ;
2 3 2 3
D→H的化学方程式:Al O + 2NaOH=2NaAlO +H O;
2 3 2 2
故答案为2Al + Fe O 2Fe + Al O ;Al O + 2NaOH=2NaAlO +H O;
2 3 2 3 2 3 2 2
(3)E+Cl →G的离子方程式:2Fe2+ +Cl =2Fe3+ +2Cl-;
2 2
G+C→E的离子方程式:2Fe3+ + Fe = 3Fe2+;
B→F+H:2Al + 2OH- + 2H O = 2 + 3H ↑,
2 2
故答案为2Fe2+ +Cl =2Fe3+ +2Cl-;2Fe3+ + Fe = 3Fe2+;2Al + 2OH- + 2H O = 2 + 3H ↑。
2 2 2
【点睛】本题考查无机物推断,涉及Al、Fe元素单质化合物的性质,物质的颜色是推断突破口,注意对
基础知识的掌握。
20.(2021·四川省绵阳南山中学高一期中)把 含镁、铝、铜的合金粉末分为两等份,一份放入过量
氢氧化钠溶液中,得到 (标准状况),另一份放入过量盐酸中,得到 (标准状况)。试计算:
(1)该合金中铝的质量为_______g。
(2)该合金中镁、铝、铜的物质的量之比为多少?_____(无解题过程不给分)
【答案】
(1)
(2)
【解析】
(1)标准状况, 的物质的量是 ,设一份合金中铝的物质的量是xmol,
,x=0.2mol;
所以该合金中铝的质量为0.2mol×27g/mol×2=10.8g。
(2)铝和镁都能与盐酸反应放出氢气,另一份放入过量盐酸中,得到 (标准状况),则镁与盐酸
学科网(北京)股份有限公司反应放出氢气的体积是(8.96-6.72)L=2.24L(标准状况),氢气的物质的量是 ;设一份合
金中镁的物质的量是ymol
,y=0.1mol,则一份合金中镁的质量是0.1mol×24g/mol=2.4g,铜的质量是
11g-2.4g-0.2mol×27g/mol=3.2g,铜的物质的量是 ;该合金中镁、铝、铜的物质的量之
比为0.1:0.2:0.05=2:4:1。
学科网(北京)股份有限公司学科网(北京)股份有限公司