文档内容
第三章 铁 金属材料
单元检测
一、选择题(本题包括16小题,每小题3分,共48分,每小题只有一个选项符合题意。)
1.(2022·新疆生产建设兵团第三师图木舒克市第二中学高一期末)下列生活中的物质与其有效成分的化
学式、用途的对应关系中,不正确的是
选项 A. B. C. D.
生活中的物质 铁红 漂白液 小苏打 复方氢氧化铝片
有效成分的化学式 Fe O NaClO NaHCO Al(OH)
3 4 3 3
用途 做红色颜料 做杀菌漂白剂 做发酵粉 做抗酸药
A.A B.B C.C D.D
2.(2022·全国·高一单元测试)下列关于新型合金材料说法不正确的是
A.镧镍合金能大量吸收H 形成金属氢化物,可作储氢材料
2
B.钛合金生物相容性好,强度大,可作人造骨骼
C.生铁和钢是含碳量不同的两种铁碳合金,生铁的含碳量比钢的含碳量高
D.合金的熔点比其成分金属的熔点高
3.(2022·辽宁·渤海大学附属高级中学高一期末)下列有关物质的性质与用途的描述错误的是
A.Al具有良好的延展性,故铝可用于制作铝金属制品
B.镁铝合金的密度大、强度高,是制造飞机和宇宙飞船的理想材料
C.Al、Al O 均能与酸、碱反应,因此铝制炊具不宜用来蒸煮酸性或碱性食物
2 3
D.“蛟龙号”载人潜水器的耐压球壳是用钛合金制造的,合金具有硬度大等优点
4.(2022·全国·高一课时练习)下列关于金属铝的叙述中,不正确的是
A.铝的化学性质很活泼,但在空气中不易锈蚀
B.铝箔在空气中受热可以熔化,且发生剧烈燃烧
C.铝是比较活泼的金属,常温下能与盐酸、NaOH溶液等发生反应
D.相同质量的铝分别与足量的盐酸和氢氧化钠反应,产生氢气的量相同
5.(2022·全国·高一单元测试)下列有关铁及其化合物的叙述中正确的是
A.赤铁矿的主要成分为
B. 与 溶液反应生成血红色沉淀
C.氢氧化亚铁是白色固体,置于空气中迅速变成灰绿色,最终变成红褐色
D.为了除去 溶液中的 杂质,可向溶液中通入过量
6.(2022·全国·高一课时练习)下列有关除杂的操作中不正确的是
A. 溶液中含少量 杂质:加入过量的 粉,过滤
学科网(北京)股份有限公司B.除去 溶液中少量的 :加入新制氯水
C.除 溶液中少量的 杂质可以向溶液中加入过量铁粉,然后过滤
D.除 溶液中的 杂质可以向溶液中加入过量铁粉
7.(2022·全国·高一课时练习)验证Fe3+与Fe2+能够相互转化。
按下列顺序实验 对应现象
①向FeCl 溶液中加入过量铁 i.溶液由黄色变成浅绿
3
粉 色
②滴加KSCN溶液 ii.溶液无明显变化
③再滴加几滴氯水 iii.溶液变红
下列分析不合理的是A.解释现象i的反应:2Fe3++Fe=3Fe2+
B.实验②与③可以调换顺序
C.溶液变红涉及的反应:Cl +2Fe2+=2Cl-+2Fe3+
2
D.氧化性:Cl >Fe3+>Fe2+
2
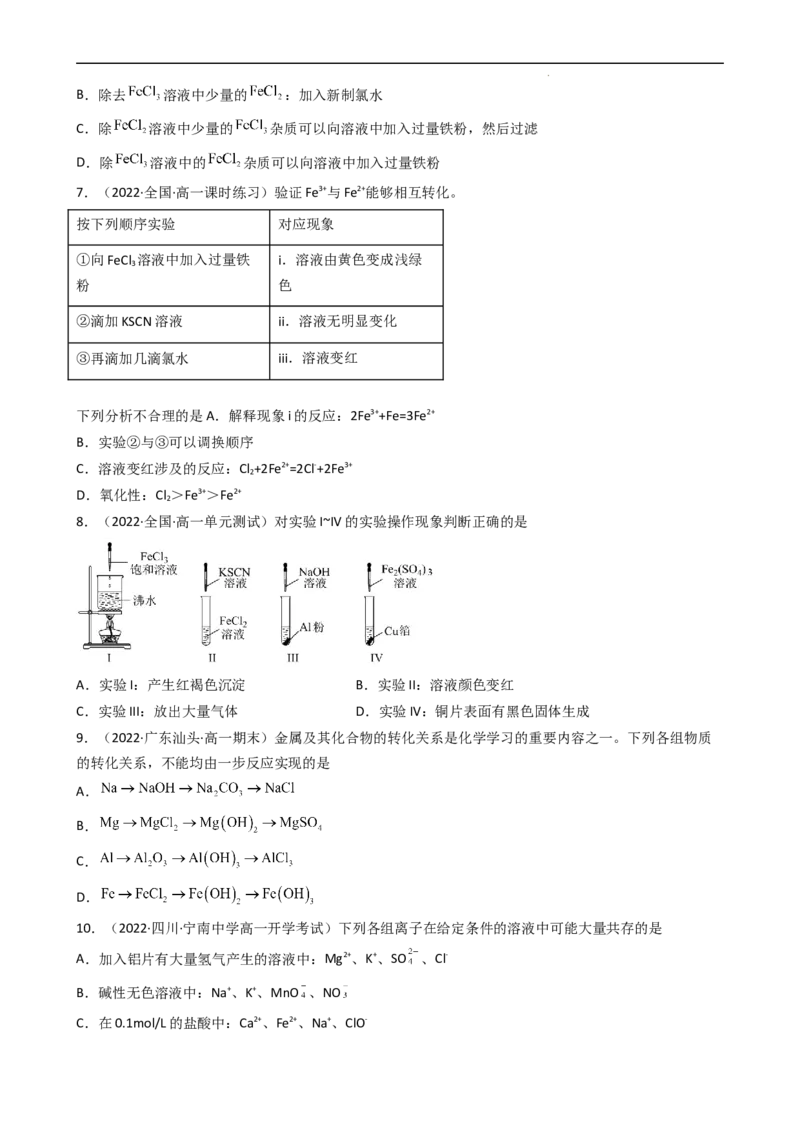
8.(2022·全国·高一单元测试)对实验I~IV的实验操作现象判断正确的是
A.实验I:产生红褐色沉淀 B.实验II:溶液颜色变红
C.实验III:放出大量气体 D.实验IV:铜片表面有黑色固体生成
9.(2022·广东汕头·高一期末)金属及其化合物的转化关系是化学学习的重要内容之一。下列各组物质
的转化关系,不能均由一步反应实现的是
A.
B.
C.
D.
10.(2022·四川·宁南中学高一开学考试)下列各组离子在给定条件的溶液中可能大量共存的是
A.加入铝片有大量氢气产生的溶液中:Mg2+、K+、SO 、Cl-
B.碱性无色溶液中:Na+、K+、MnO 、NO
C.在0.1mol/L的盐酸中:Ca2+、Fe2+、Na+、ClO-
学科网(北京)股份有限公司D.在强碱性溶液中:Ca2+、K+、NH 、Cl-
11.(2022·全国·高一单元测试)下列实验操作、现象或结论均正确的是
选项 实验操作 现象或结论
A 用酒精灯点燃铝箔 铝箔剧烈燃烧,产生白烟
B 焰色反应时直接观察火焰颜色 未观察到紫色火焰,说明不含
C 向某溶液中先通Cl ,再滴加KSCN溶液 溶液变红,说明溶液中含有
2
D 使用胶头滴管伸入NaOH溶液中滴加FeSO 溶液 先看到白色絮状沉淀
4
A.A B.B C.C D.D
12.(2022·全国·高一课时练习)易拉罐的主要成分为铝合金,其中以铝铁合金和铝镁合金最为常见。为
确定铝合金中金属的成分,现取几小块易拉罐碎片进行下列实验,其中实验方案、现象与结论均正确的
是
选项 实验方案 现象与结论
A 加入盐酸 产生无色气体,含铝、铁、镁三种金属
B 加入NaOH溶液 有无色气体产生,含有镁、铝两种金属
C 加入盐酸后,向所得溶液中再加入少量NaOH溶液 产生白色沉淀,一定只含有镁
D 用盐酸溶解并放置一会儿后,加入KSCN溶液 溶液呈血红色,含有铁
A.A B.B C.C D.D
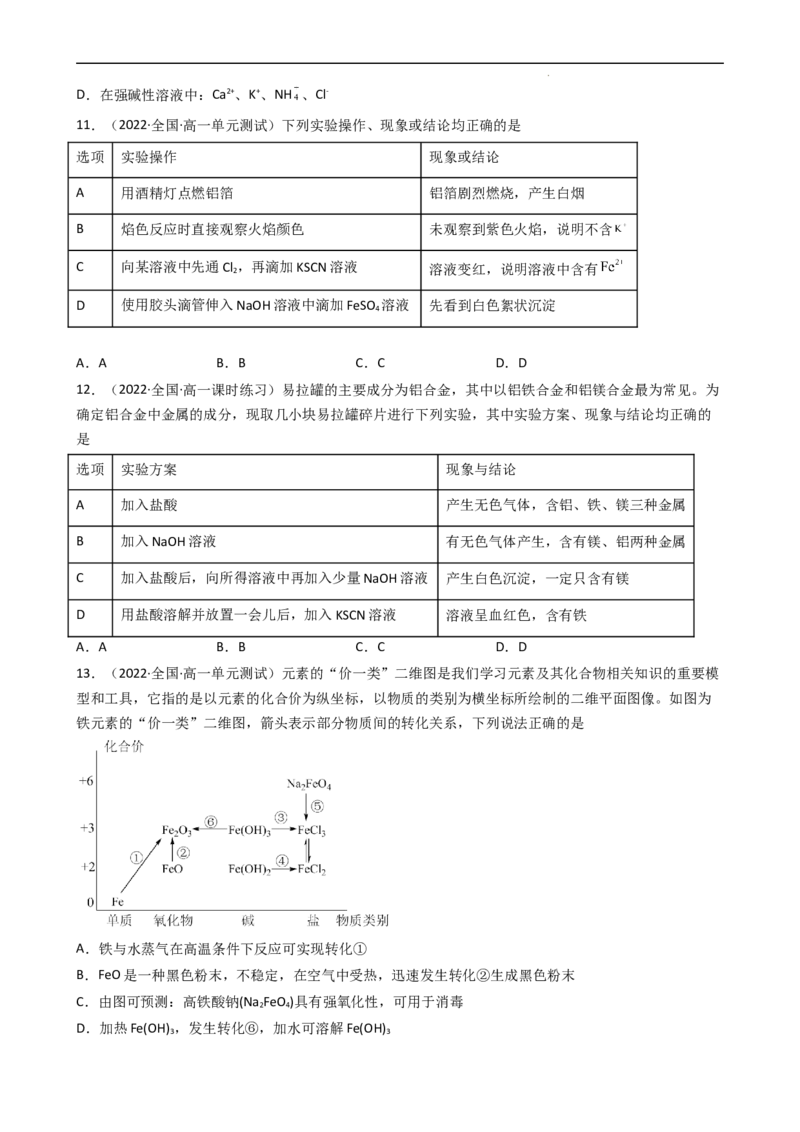
13.(2022·全国·高一单元测试)元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模
型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为
铁元素的“价一类”二维图,箭头表示部分物质间的转化关系,下列说法正确的是
A.铁与水蒸气在高温条件下反应可实现转化①
B.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成黑色粉末
C.由图可预测:高铁酸钠(Na FeO )具有强氧化性,可用于消毒
2 4
D.加热Fe(OH) ,发生转化⑥,加水可溶解Fe(OH)
3 3
学科网(北京)股份有限公司14.(2022·全国·高一单元测试)某同学对铁的氧化物产生浓厚兴趣,查阅资料后制成以下卡片:
下列说法正确的是
A.FeO、Fe O 和Fe O 均为黑色固体
2 3 3 4
B.反应②的温度比反应③的温度高
C.热稳定性顺序:FeO>Fe O
2 3
D.四氧化三铁中铁元素的化合价复杂,若写成氧化物的形式,则化学式可写为FeO·Fe O
2 3
15.(2022·江西·丰城九中高一期末)工业废弃物的资源化回收再利用,可以更大限度地发挥原材料的价
值。下图是工业生产纳米磁性氧化铁的流程:
下列说法不正确的是
A.用 溶液浸泡是为了除去废铁屑表面的铁锈
B.若生产中不通入 ,暴露在空气中生产,将不能得到高纯度产品
C.加适量的 是为了将部分 氧化为 ,涉及反应:
D.溶液A中 和 的浓度比为1:2
16.(2022·江西·临川一中高一阶段练习)13.6gFe和Fe O 的混合物,加入150mL足量的稀硫酸,在标准
2 3
状况下收集到1.12LH ,向反应后的溶液中滴加KSCN溶液不变红。为中和过量的稀硫酸,并使Fe元素全
2
部转化为Fe(OH) 沉淀,恰好消耗了200mL3mol/L的NaOH溶液,则该稀H SO 的物质的量浓度为
2 2 4
A.2.25mol/L B.2mol/L C.3mol/L D.0.6mol/L
二、非选择题(本题包括4小题,共52分)
17.(2022·全国·高一单元测试)铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问
题。
(1)所含铁元素既有氧化性又有还原性的物质是___________(填字母代号)。
A.Fe B.FeCl C.FeSO D.Fe O
2 4 2 3
(2)向沸水中逐滴滴加lmol/LFeCl 溶液﹐至液体呈透明的红褐色,该分散系中粒子直径的范围是
3
___________nm。
(3)电子工业需要用30%的FeCl 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl 溶液与铜反应
3 3
的离子方程式:___________。某校同学为测定FeCl 腐蚀铜后所得溶液的组成,进行了如下实验:首先取
3
少量待测溶液﹐滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是___________,在此基础上,又进
行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO 溶液,得白色沉淀,
3
学科网(北京)股份有限公司___________(填实验操作,下同)、___________、干燥,称量沉淀质量为43.05g。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是___________(填字母代号)。
A.向试管中加入试液,滴入KSCN溶液,若显红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
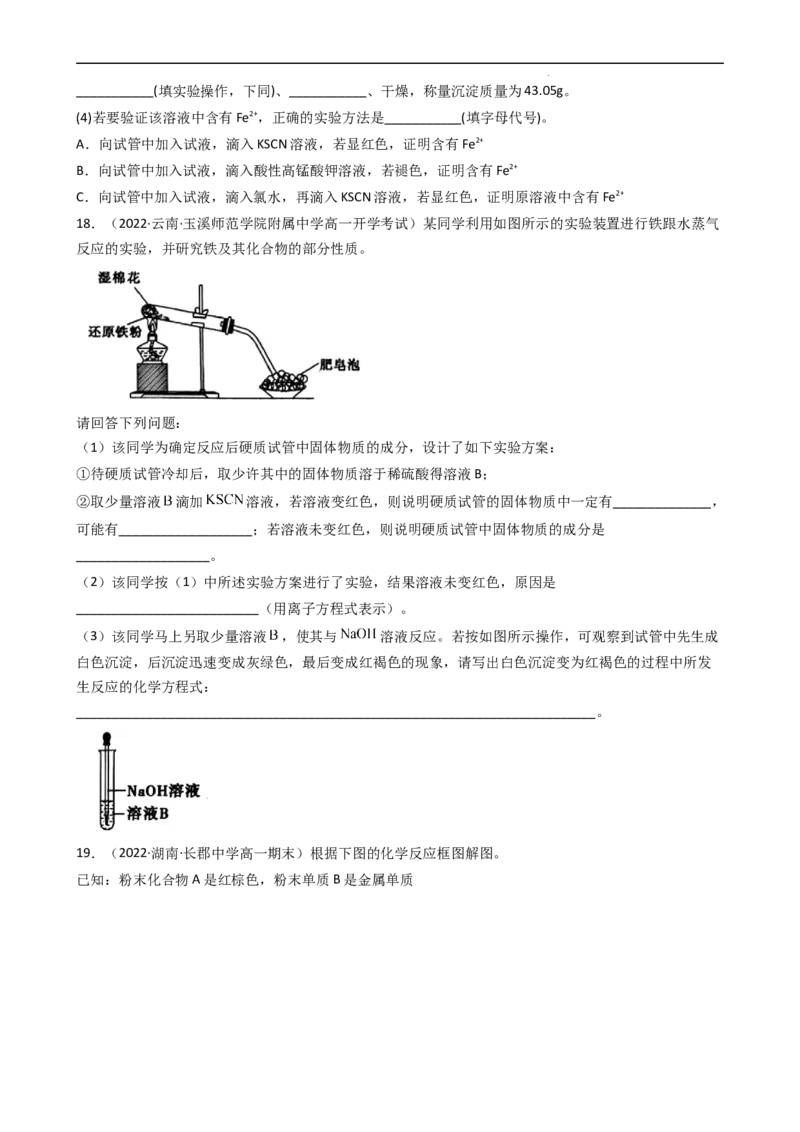
18.(2022·云南·玉溪师范学院附属中学高一开学考试)某同学利用如图所示的实验装置进行铁跟水蒸气
反应的实验,并研究铁及其化合物的部分性质。
请回答下列问题:
(1)该同学为确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液 滴加 溶液,若溶液变红色,则说明硬质试管的固体物质中一定有______________,
可能有___________________;若溶液未变红色,则说明硬质试管中固体物质的成分是
___________________。
(2)该同学按(1)中所述实验方案进行了实验,结果溶液未变红色,原因是
__________________________(用离子方程式表示)。
(3)该同学马上另取少量溶液 ,使其与 溶液反应。若按如图所示操作,可观察到试管中先生成
白色沉淀,后沉淀迅速变成灰绿色,最后变成红褐色的现象,请写出白色沉淀变为红褐色的过程中所发
生反应的化学方程式:
__________________________________________________________________________。
19.(2022·湖南·长郡中学高一期末)根据下图的化学反应框图解图。
已知:粉末化合物A是红棕色,粉末单质B是金属单质
学科网(北京)股份有限公司(1)单质F是________,溶液E加入氢氧化钠溶液的现象是_____________________;
(2)写出下列反应的化学方程式:
A+B→C+D_____________________________________;
D→H:_________________________________。
(3)写出下列反应的离子方程式:
E+Cl →G:__________________;
2
G+C→E:________________________;
B→F+H:__________________________。
20.(2021·四川省绵阳南山中学高一期中)把 含镁、铝、铜的合金粉末分为两等份,一份放入过量
氢氧化钠溶液中,得到 (标准状况),另一份放入过量盐酸中,得到 (标准状况)。试计算:
(1)该合金中铝的质量为_______g。
(2)该合金中镁、铝、铜的物质的量之比为多少?_____(无解题过程不给分)
学科网(北京)股份有限公司学科网(北京)股份有限公司