文档内容
第三章 铁 金属材料
单元复习检测
1.(2020·江苏省如皋中学高一月考)下列关于合金的说法中不正确的是
A.生铁和钢都属于铁合金 B.铝合金是目前用途广泛的合金之一
C.稀土金属可以用于生产合金 D.在我国使用最早的合金是钢
【答案】D
【详解】
A.生铁为含碳量>2%的铁合金,而钢为含碳量为0.02~2.11%的铁合金,都属于铁合
金,A说法正确;
B.铝在地壳中的含量较高,且化学性质稳定,则铝合金是目前用途广泛的合金之一,
B说法正确;
C.在青铜和黄铜冶炼中添加少量的稀土金属能提高合金的强度、延伸率、耐热性和导
电性,稀土金属可以用于生产合金,C说法正确;
D.在我国使用最早的合金是青铜,D说法错误;
答案为D。
2.(2020·安达市第七中学高一月考)现有
①NaO ②Fe O ③FeCl ④FeCl ⑤Fe(OH) 五种物质,下列说法正确的是
2 2 3 4 2 3 3
A.均能通过化合反应生成
B.只有①②④能通过化合反应生成
C.过量的铁在氯气中燃烧可以生成③
D.将1mol①投入含有1mol③的溶液中,生成白色絮状沉淀并有气泡冒出
【答案】A
【详解】
A. Na和O 在点燃条件下生成NaO,Fe和O 在点燃条件下生成Fe O,Fe和FeCl 反
2 2 2 2 3 4 3
应生成FeCl ,Fe在Cl 中燃烧生成FeCl ,Fe(OH) 和O、HO反应生成Fe(OH) ,均
2 2 3 2 2 2 3
为化合反应,故A正确;
B. 由A项分析可知,五种物质均能通过化合反应生成,故B错误;
C. 氯气的氧化性强,无论铁是否过量,在氯气中燃烧时只能生成FeCl ,铁和氯化铁
3
反应生成氯化亚铁需要在水溶液中才能发生,故C错误;
D. Na O 具有强氧化性,将NaO 投入FeCl 溶液中,生成红褐色Fe(OH) 沉淀并有气
2 2 2 2 2 3泡(O )冒出,故D错误;
2
答案选A。
3.(2020·安达市第七中学高一月考)下列生活或工业中的物质与其成分、性质和用
途的对应关系中,正确的是
选项 物质及成分 性质 用途
A 小苏打(Na CO) 与酸反应产生二氧化碳 作发酵粉
2 3
B 磁性氧化铁(Fe O) 难溶于水,红色 制造红色涂料
2 3
C 蓝矾(CuSO ·5H O) 蓝色 检验水蒸气
4 2
漂白织物、麦杆、羽毛
D 过氧化钠(Na O) 强氧化性
2 2 等
【答案】D
【详解】
A.小苏打的成分是NaHCO ,故A错误;
3
B.磁性氧化铁的成分是Fe O,故B错误;
3 4
C.蓝矾的成分是CuSO ·5H O,固体呈蓝色,通常用CuSO 检验水蒸气,CuSO 遇水
4 2 4 4
蒸气生成CuSO ·5H O,现象是白色固体变蓝色,故C错误;
4 2
D.过氧化钠的成分是NaO,具有强氧化性、漂白性,可以用来漂白织物、麦杆、羽
2 2
毛等,故D正确;
答案选D。
4.(2020·东城区·北京一七一中高一期中)纳米级 Fe O 可用于以太阳能为热源分解
3 4
水制H,过程如下图所示。下列说法正确的是:
2
A.过程Ⅰ的反应为:6FeO+O 2Fe O
2 3 4
B.过程Ⅱ中H 为还原剂
2
C.整个过程的总反应为:2HO 2H↑+O ↑
2 2 2
D.FeO 是过程Ⅰ的氧化产物【答案】C
【详解】
A.据图可知过程Ⅰ为Fe O 在太阳光照射下分解生成FeO与O,反应方程式为:
3 4 2
2Fe O 6FeO+O,故A错误;
3 4 2
B.过程Ⅱ为FeO与水反应生成H 和Fe O,氢气为还原产物,故B错误;
2 3 4
C.过程I方程式为:2Fe O 6FeO+O↑;过程II方程式为:
3 4 2
3FeO+HO=H↑+Fe O,将I+II×2可得总反应为2HO 2H↑+O ↑,故C正确;
2 2 3 4 2 2 2
D.过程I中Fe O 转化为FeO的过程中Fe元素化合价降低,所以FeO为还原产物,
3 4
故D错误;
综上所述答案为C。
5.(2020·浙江高一月考)在Fe、FeO和Fe O 组成的混合物中加入100mL2mol/L的
2 3
盐酸,恰好使混合物完全溶解,并放出448mL气体(标准状况),在反应后溶液中加入
NH SCN溶液,无明显现象。下列判断正确的是( )
4
A.混合物中三种物质反应时消耗盐酸的物质的量之比为1:1:3
B.反应后所得溶液中的Fe2+离子与Cl-离子的物质的量浓度之比为1:3
C.混合物中,FeO的物质的量无法确定,但Fe比Fe O 的物质的量多
2 3
D.混合物中,Fe O 的物质的量无法确定,但Fe比FeO的物质的量多
2 3
【答案】C
【分析】
混合物恰好完全溶解,且在反应后溶液中加入NH SCN溶液,无明显现象,说明无
4
Fe3+,故溶液中溶质为FeCl ,n(HCl)=0.2mol,n(H )=0.448L÷22.4L/mol=0.02mol,
2 2
n(Fe2+)=0.1mol,由反应2Fe3++Fe=3Fe2+知Fe比Fe O 的物质的量多,但FeO的物质的
2 3
量无法确定,据此分析解答。
【详解】
A.根据以上分析知Fe比Fe O 的物质的量多,但FeO的物质的量无法确定,故无法
2 3
确定混合物里三种物质反应时消耗盐酸的物质的量之比,A错误;
B.反应后所得溶液为FeCl 溶液,阳离子与阴离子的物质的量浓度之比为1:2,B错
2误;
C.混合物恰好完全溶解,且无Fe3+,故溶液中溶质为FeCl ,由铁与酸反应生成氢气
2
及反应2Fe3++Fe=3Fe2+知Fe比Fe O 的物质的量多,但FeO的物质的量无法确定,C正
2 3
确;
D.FeO的物质的量无法确定,不能确定Fe与FeO的物质的量的关系,D错误;
答案选C。
6.(2020·江苏省如皋中学高一月考)下列图示方法能完成相应实验的是
A.用图①配制一定物质的量浓度的NaOH溶液
B.用图②在实验室制取Cl
2
C.用图③探究碳酸氢钠和碳酸钠的热稳定性
D.用图④制备少量Fe(OH) 并能较长时间看到其白色
2
【答案】D
【详解】
A.容量瓶中不能溶解固体物质,则不能用图①配制一定物质的量浓度的NaOH溶液,
A与题意不符;
B.用二氧化锰与浓盐酸共热制备氯气,则不能用图②在实验室制取Cl,B与题意不
2
符;
C.外试管加热的温度高于内试管,且碳酸钠受热不分解,则不能用图③探究碳酸氢钠
和碳酸钠的热稳定性,C与题意不符;
D.硫酸与铁反应生成氢气,氢气能把装置A中生成的硫酸亚铁压入装置B,且氢气
能排净装置内的空气,可防止氢氧化亚铁被氧化,则用图④制备少量Fe(OH) 并能较
2
长时间看到其白色,D符合题意;
答案为D。
7.(2020·浙江高一期中)如图所示装置中能较长时间看到Fe(OH) 白色沉淀的是
2A.①② B.①②④ C.①④ D.②③④
【答案】B
【分析】
实验中生成的Fe(OH) 容易发生氧化,要能较长时间看到Fe(OH) 白色沉淀就要防止其
2 2
发生氧化。,
【详解】
①Fe与稀硫酸反应生成的氢气将装置内空气排出,可防止生成的氢氧化亚铁被氧化,
①符合题意;
②Fe与稀硫酸反应生成的氢气将装置内空气排出,且利用氢气的压力使硫酸亚铁与
NaOH接触而反应,可防止生成的氢氧化亚铁被氧化,②符合题意;
③生成的氢氧化亚铁能够与空气中氧气发生反应4Fe(OH) +O +2H O=4Fe(OH) ,导致
2 2 2 3
不能长时间观察到氢氧化亚铁,③不符题意;
④苯隔绝空气,可防止生成的氢氧化亚铁被氧化,③符合题意;
所以上述装置中能较长时间看到Fe(OH) 白色沉淀的是①②④,答案选B。
2
8.(2020·湖南高一月考)高铁酸钠(Na FeO)是一种新型绿色消毒剂,主要用于饮用
2 4
水处理。工业制备高铁酸钠的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-
=2FeO +3Cl - +5H O。下列有关说法错误的是
2
A.高铁酸钠中铁的化合价为+6 价
B.由上述反应可知,ClO-的氧化性强于FeO
C.上述反应中氧化剂和还原剂的物质的量之比为 2∶3
D.NaFeO 处理水时,不仅能消毒,而且生成的 Fe3+与水反应形成 Fe(OH) 胶体能
2 4 3
吸附水中的悬浮杂质
【答案】C
【详解】
A.高铁酸根中氧元素为-2 价,设 Fe 元化合价为 x,则 x+(-2)×4=-2,解得 x=+6,
故 A 正确;
B.该反应中 ClO-为氧化剂,FeO 为氧化产物,所以ClO-的氧化性强于FeO ,故
B 正确;
C.该反应中 ClO-为氧化剂,Cl 元素化合价由-1 价变为-2 价,Fe(OH) 为还原剂,
3
Fe 元素化合价由+3 价变为+6 价, 根据化合价升降平衡可知氧化剂和还原剂的物质
的量之比为 3∶2,故C 错误;D.NaFeO 具有氧化性所以能杀菌,高铁酸钾被还原为 Fe3+,Fe3+水解生成的
2 4
Fe(OH) (胶体)具有净水作用,故D 正确;
3
综上所述答案为C。
9.(2020·浙江高一月考)下列说法正确的是( )
A.新制氯水放在棕色广口试剂瓶中
B.溧白粉能长期放置于敞口烧杯中
C.配制FeCl 溶液时,要加入少量铁粉
2
D.可用氯气除去Fe (SO ) 溶液中少量的Fe2+
2 4 3
【答案】C
【详解】
A.新制氯水呈液态,其中的HClO光照易分解,因此一般要放在棕色细口试剂瓶中,
A错误;
B.溧白粉的有效成分Ca(ClO) 容易与空气中的CO 发生反应导致变质,因此不能长
2 2
期放置于敞口烧杯中,要密封保存,B错误;
C.FeCl 具有还原性,容易被氧气氧化变为氯化铁,为防止其氧化变质,在配制FeCl
2 2
溶液时,要加入少量铁粉,C正确;
D.除去Fe (SO ) 溶液中少量的Fe2+时,不能引入新的杂质,应该使用绿色氧化物
2 4 3
HO,若使用氯气,会引入杂质Cl-,D错误;
2 2
故合理选项是C。
10.(2020·浙江高一期中)用FeCl 溶液腐蚀印刷电路板上的铜,所得的溶液中加入
3
铁粉。对加入铁粉充分反应后的溶液分析合理的是( )
A.若无固体剩余,则溶液中一定有Fe3+
B.若溶液中有Fe2+,则一定有Cu析出
C.若溶液中有Cu2+,则一定没有固体析出
D.若有固体存在,则溶液中一定有Fe2+
【答案】D
【详解】
已知:氧化性是Fe3+>Cu2+>Fe2+,还原性是Fe>Cu,则
A.若无固体剩余,这说明铁粉完全被氧化,但此时溶液中不一定还有Fe3+,A错误;
B.若溶液中有Fe2+,但如果溶液铁离子过量,则不一定有Cu析出,B错误;
C.若溶液中有Cu2+,则也可能有部分铜已经被置换出来,因此不一定没有固体析出,
C错误;
D.若有固体存在,则固体中一定有铜,可能还有铁,因此溶液中一定有Fe2+,D正确;
答案选D。
11.(2020·东台市创新学校高二学业考试)在CuO中混有少量的Al O 杂质,欲将杂
2 3
质除去可选用的试剂是
A.稀硫酸 B.浓氨水 C.稀盐酸 D.氢氧化钾溶液
【答案】D
【详解】
A.稀硫酸与二者均能反应,CuO+HSO =CuSO+H O,
2 4 4 2
Al O+3H SO =Al(SO )+3H O,A不合题意;
2 3 2 4 2 4 3 2
B.浓氨水与二者均不能反应,无法除杂,B不合题意;
C.稀盐酸与二者均能反应,CuO+2HCl=CuCl +H O,Al O+6HCl=2AlCl +3H O,C不
2 2 2 3 3 2
合题意;
D.氢氧化钾溶液与Al O 反应转化为可溶性NaAlO ,Al O+2NaOH=2NaAlO +H O,
2 3 2 2 3 2 2
而CuO不能,故能用于除杂,D符合题意;
故答案为:D。
12.(2020·浙江高二期中)实验室中,要使AlCl 溶液中的Al3+离子全部沉淀出来,
3
适宜用的试剂是( )
A.NaOH溶液 B.Ba(OH) 溶液 C.盐酸 D.氨水
2
【答案】D
【详解】
A.当NaOH溶液过量时,会生成偏铝酸钠,不能将A13+完全沉淀出来,故不选A项;
B.当Ba(OH) 溶液过量时,会生成偏铝酸钠,不能将A13+完全沉淀出来,,故不选B
2
项;
C.盐酸与AlCl 溶液不反应,故不选C项;
3
D.Al3++3NH·H O=Al(OH) ↓+3NH ,且氨水不与Al(OH) 发生反应,故可将Al3+完全
3 2 3 3
沉淀,故选D项;
故答案为D 。
13.(2020·青铜峡市高级中学高一月考)下列关于金属性质的描述中不正确的是
( )
A.铝能稳定存在的是因为铝表面形成致密的氧化膜
B.铝箔在空气中受热时只熔化不滴落
C.铁不论在空气中还是纯氧中都不会燃烧D.常温下,Fe与HO不反应,但在空气中的O、HO共同作用下能发生反应
2 2 2
【答案】C
【详解】
A.铝在空气中稳定存在的原因是在常温下Al与氧气反应,铝表面能形成致密的氧化
膜,故A正确;
B.铝箔在空气中受热,表面生成氧化铝,氧化铝的熔点高,包裹在Al的外面,则熔
化的Al 并不滴落,故B正确;
C.铁在纯氧气中燃烧生成四氧化三铁,在空气中不能燃烧,故C错误;
D.常温下,Fe与HO不反应;Fe中含有C元素,Fe、C与电解质溶液能形成原电池,
2
所以在空气中Fe与O、HO能发生反应,故D正确;
2 2
故选C。
14.(2020·肇庆市第一中学高一月考)下列实验报告中,完全正确的是( )
序号 实验操作 现象 结论
A 向溶液中滴加用盐酸酸化的BaCl 溶液 有白色沉淀 原溶液中含
2
B 向溶液中滴加氯水后,再滴入KSCN溶液 溶液变红色 原溶液中含Fe3+
向装有NaO 的试管中加入水后,立即滴加 溶液先变红后褪
C 2 2 NaO 有漂白性
酚酞试液 色 2 2
观察到有紫色火
D 用洁净的玻璃棒蘸取溶液进行焰色反应 原溶液中有K+
焰
【答案】C
【详解】
A.向溶液中滴加用盐酸酸化的BaCl 溶液,沉淀可能为AgCl或BaSO,原溶液可能
2 4
含银离子,应先加盐酸排除其它离子的干扰,再滴加氯化钡溶液,故A不符合题意;
B.向溶液中滴加氯水后,再滴入KSCN溶液,溶液变红色,溶液中可能含亚铁离子,
亚铁离子被氧化成铁离子,铁离子遇KSCN溶液变红;检验铁离子,不需要氯水,直
接加KSCN溶液,若溶液变红,则含有铁离子,故B不符合题意;
C.酚酞遇碱变红,过氧化钠和水反应生成NaOH,溶液显碱性,溶液会变红;过量的
过氧化钠,具有漂白性,则溶液先变红后褪色,故C符合题意;
D.观察K的焰色反应需要透过蓝色的钴玻璃片,滤去黄光的干扰,故D不符合题意;
答案选C。
15.(2020·洮南市第一中学高一月考)如图所示,在杠杆的两端分别挂着质量相同的
铝球和铁球,此时杠杆平衡,然后将两球分别浸没在足量的质量相等的烧碱溶液和硫
酸铜溶液中一段时间。下列说法正确的是(忽略溶液对两球的浮力)( )A.铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡
B.铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,溶液蓝色变浅,杠杆
向右倾斜
C.反应后去掉两烧杯,杠杆仍平衡
D.右边球上出现红色,左边溶液的c(OH-)增大
【答案】B
【分析】
质量相同的铝球和铁球,此时杠杆平衡,然后左烧杯中发生
2Al+2NaOH+2H O=2NaAlO +3H ↑,右烧杯中发生Fe+CuSO=Cu+FeSO ,则左烧杯中
2 2 2 4 4
溶液质量增大,右烧杯中溶液质量减小,以此来解答。
【详解】
A.左烧杯中发生2Al+2NaOH+2H O=2NaAlO +3H ↑,不生成沉淀,故A错误;
2 2 2
B.左烧杯中发生2Al+2NaOH+2H O=2NaAlO +3H ↑,右烧杯中发生
2 2 2
Fe+CuSO=Cu+FeSO ,观察到铝球表面有气泡产生,溶液澄清,而铁球表面有红色物
4 4
质析出,溶液蓝色变浅,由反应可知左烧杯中Al的质量变小,右烧杯中Fe球上生成
Cu质量变大,杠杆右边下沉,故B正确;
C.由选项B的分析可知,反应后去掉两烧杯,杠杆不能平衡,故C错误;
D.右边球上生成Cu,则出现红色,而左边溶液中消耗NaOH,则c(OH-)减小,故D
错误。
答案选B。
【点睛】
本题考查铝的化学性质,把握习题中的信息及发生的反应为解答的关键,侧重分析与
应用能力的考查,注意利用差量法分析质量变化。
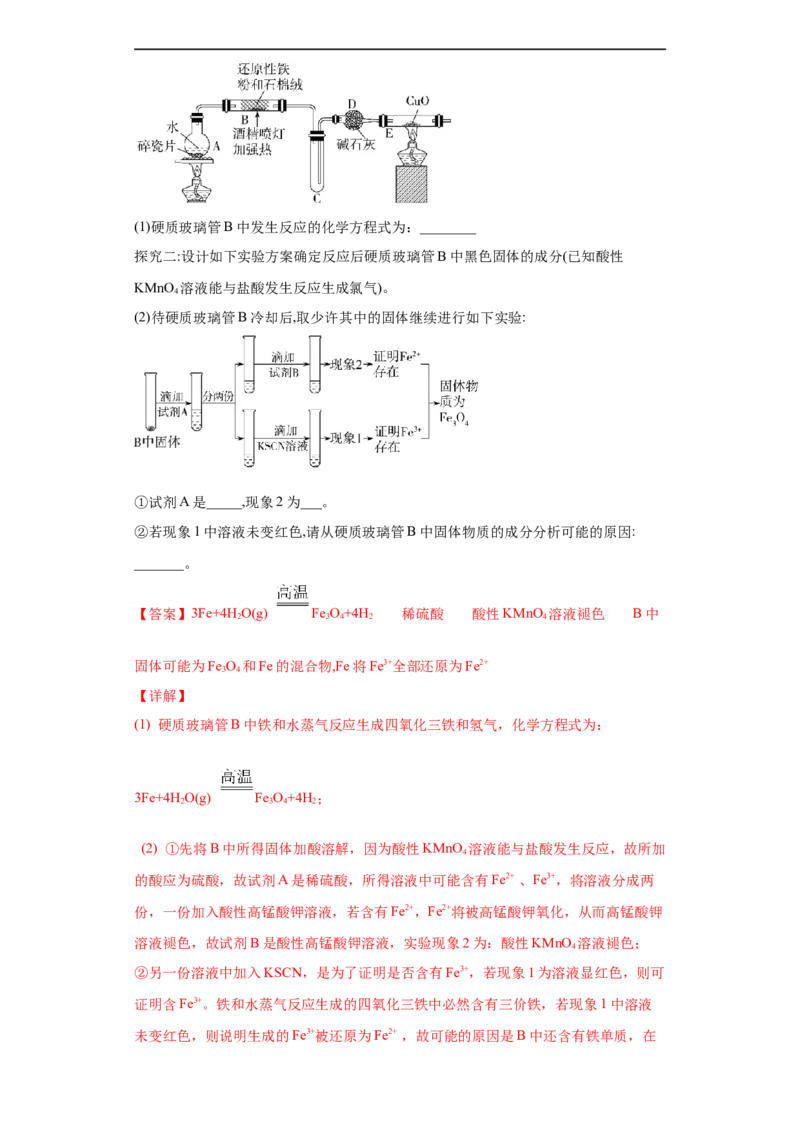
16.(2020·金华市云富高级中学高一期中)某研究性学习小组请你参与“研究铁与水
蒸气反应所得固体物质的成分、性质及再利用”实验探究,并回答下列问题:
(查阅资料)含有Fe3+的盐溶液遇到KSCN溶液时变成红色,含有Fe2+的盐溶液遇到
KSCN溶液时不变色。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。(1)硬质玻璃管B中发生反应的化学方程式为:________
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分(已知酸性
KMnO 溶液能与盐酸发生反应生成氯气)。
4
(2)待硬质玻璃管B冷却后,取少许其中的固体继续进行如下实验:
①试剂A是_____,现象2为___。
②若现象1中溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因:
_______。
【答案】3Fe+4H O(g) Fe O+4H 稀硫酸 酸性KMnO 溶液褪色 B中
2 3 4 2 4
固体可能为Fe O 和Fe的混合物,Fe将Fe3+全部还原为Fe2+
3 4
【详解】
(1) 硬质玻璃管B中铁和水蒸气反应生成四氧化三铁和氢气,化学方程式为:
3Fe+4H O(g) Fe O+4H ;
2 3 4 2
(2) ①先将B中所得固体加酸溶解,因为酸性KMnO 溶液能与盐酸发生反应,故所加
4
的酸应为硫酸,故试剂A是稀硫酸,所得溶液中可能含有Fe2+ 、Fe3+,将溶液分成两
份,一份加入酸性高锰酸钾溶液,若含有Fe2+,Fe2+将被高锰酸钾氧化,从而高锰酸钾
溶液褪色,故试剂B是酸性高锰酸钾溶液,实验现象2为:酸性KMnO 溶液褪色;
4
②另一份溶液中加入KSCN,是为了证明是否含有Fe3+,若现象1为溶液显红色,则可
证明含Fe3+。铁和水蒸气反应生成的四氧化三铁中必然含有三价铁,若现象1中溶液
未变红色,则说明生成的Fe3+被还原为Fe2+ ,故可能的原因是B中还含有铁单质,在溶液中,铁单质与Fe3+发生了反应,故B中固体物质的成分分析可能的原因是:B中
固体可能为Fe O 和Fe的混合物,Fe将Fe3+全部还原为Fe2+。
3 4
17.用下面两种方法可以制得白色的 沉淀。
Ⅰ.方法一:用 溶液与不含 的蒸馏水配制的NaOH溶液反应制备 。
(1)除去蒸馏水中溶解的 常采用的________方法。
(2)生成白色 沉淀的操作是用长胶头滴管吸取不含 的NaOH溶液,插入
溶液液面下,再挤出NaOH溶液。这样操作的理由是________________。
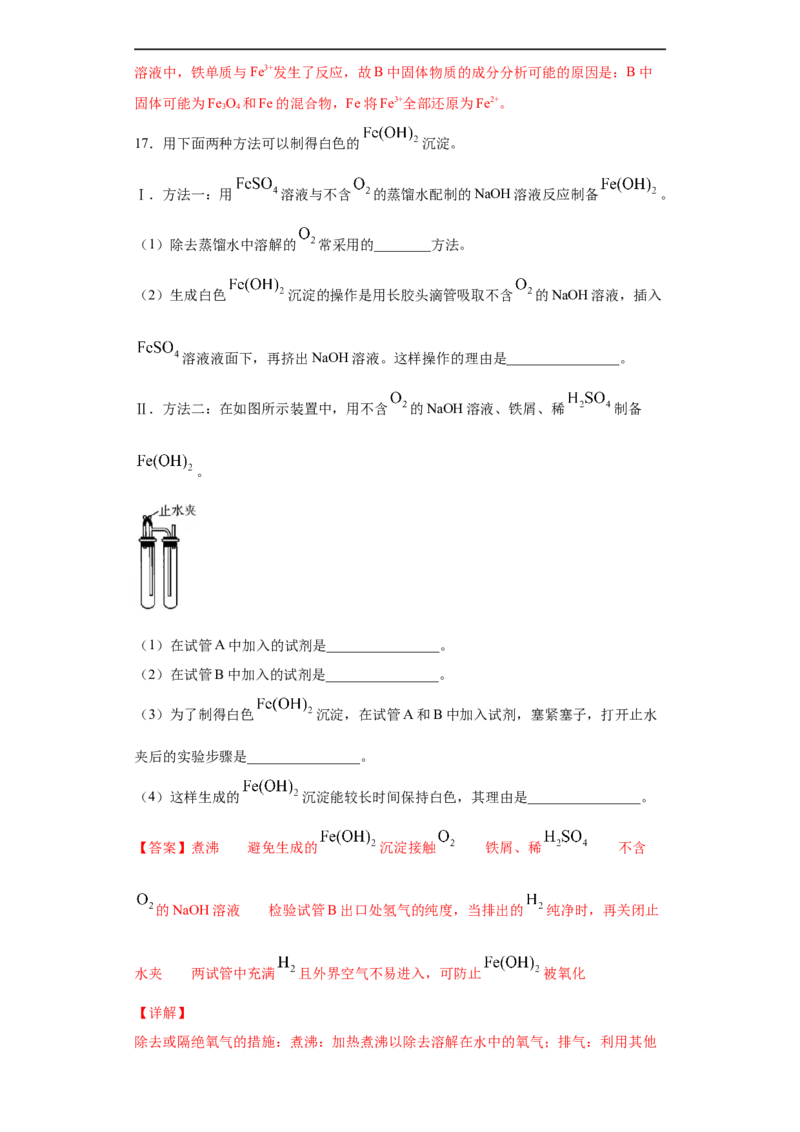
Ⅱ.方法二:在如图所示装置中,用不含 的NaOH溶液、铁屑、稀 制备
。
(1)在试管A中加入的试剂是________________。
(2)在试管B中加入的试剂是________________。
(3)为了制得白色 沉淀,在试管A和B中加入试剂,塞紧塞子,打开止水
夹后的实验步骤是________________。
(4)这样生成的 沉淀能较长时间保持白色,其理由是________________。
【答案】煮沸 避免生成的 沉淀接触 铁屑、稀 不含
的NaOH溶液 检验试管B出口处氢气的纯度,当排出的 纯净时,再关闭止
水夹 两试管中充满 且外界空气不易进入,可防止 被氧化
【详解】
除去或隔绝氧气的措施:煮沸:加热煮沸以除去溶解在水中的氧气;排气:利用其他气体排尽装置中的氧气;覆盖:在液面上覆盖一层苯或煤油等,隔绝氧气。
Ⅰ.(1)常采用煮沸的方法除去蒸馏水中的 ;
(2)因为 在空气中易被 氧化为 ,所以在制备 时,若
向 溶液中直接滴加NaOH溶液,会带入空气使制取的 被氧化;若将
盛有NaOH溶液的长胶头滴管插入 溶液液面下,再挤出NaOH溶液,可以防止
滴加NaOH溶液时带入空气,避免生成的 接触 ;
Ⅱ.(1)在试管A中加入的试剂是铁屑、稀 ;
(2)在试管B中加入的试剂是不含 的NaOH溶液;
(3)为了制得白色 沉淀,在试管A和B中加入试剂,塞紧塞子,打开止水
夹后的实验步骤是检验试管B出口处氢气的纯度,当排出的 纯净时,再关闭止水夹;
(4)制备 时利用Fe与 反应产生的 排尽装置中的空气,收集氢气
验纯后,关闭止水夹,试管A中产生 ,压强增大,将A中溶液压入B中与NaOH
溶液反应制备 , 沉淀在 的氛围中不易被氧化,能较长时间保持
白色。
18.(2018·福州金山中学高二学业考试)实验室用硫铁矿烧渣(主要成分为Fe O、
2 3
FeO、SiO)为原料制备硫酸亚铁晶体,设计流程如下:
2
(1)步骤(I)中分离溶液和沉淀的操作是___________,该操作中用到的玻璃仪器有玻璃棒、
烧杯和___________;(2)沉淀A的主要成分是___________;
(3)滤液B中的阳离子有H+、Fe3+和___________;
(4)写出步骤(Ⅱ)中Fe3+和Fe反应生成Fe2+的离子方程式:___________。
【答案】过滤 漏斗 SiO Fe2+ 2Fe3++Fe=3Fe2+
2
【分析】
硫铁矿烧渣(主要成分为Fe O、FeO、SiO)加入过量稀硫酸进行酸浸,氧化铁、氧化
2 3 2
亚铁与稀硫酸反应生成硫酸铁、硫酸亚铁进入滤液B,SiO 难溶于稀硫酸为沉淀A;
2
滤液B中加入过量铁粉将铁离子还原成Fe2+,同时除去过量的稀硫酸,过滤分离过量
的铁粉和硫酸亚铁溶液,控制一定条件得到硫酸亚铁晶体。
【详解】
(1)步骤(I)中分离溶液和沉淀的操作为过滤;过滤需要的玻璃仪器为玻璃棒、烧杯和漏
斗;
(2)根据分析可知沉淀A的主要成分为难溶于稀硫酸的SiO;
2
(3)根据分析可知滤液B中的阳离子有H+、Fe3+和Fe2+;
(4)步骤(Ⅱ)中Fe3+和Fe反应生成Fe2+的离子方程式为2Fe3++Fe=3Fe2+。
19.镁铝合金是飞机制造、化工生产等行业的重要材料。某研究性学习小组的同学为
测定某含镁3%~5%的镁铝合金(不含其他元素)中镁的质量分数,设计了下列两种不
同的实验方案进行探究。
回答下列问题:
(方案一)
(实验方案)将一定质量的镁铝合金与足量NaOH溶液反应,测定剩余固体的质量。
实验中发生反应的化学方程式为
_________________________________________________________。
(实验步骤)
(1)称取10.8g镁铝合金样品,溶于体积为V、物质的量浓度为4.0mol/LNaOH溶液
中,充分反应。则V≥_____________mL。
(2)过滤、洗涤、干燥、称量剩余固体。该步骤中若未洗涤剩余固体,则测得镁的质
量分数将______________________(填“偏高”“偏低”或“不受影响”)。
(方案二)
(实验方案)将一定质量的镁铝合金与足量稀硫酸反应,测定生成气体的体积。
(实验装置)
(1)同学们拟选用如图所示实验装置完成实验:你认为最简易的实验装置的连接顺序是A接(________),(________)接
(________),(________)接(________)(填接口字母,可不填满)。
(2)仔细分析实验装置后,同学们经讨论认为有两点会引起较大误差;稀硫酸滴入锥
形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气的体积偏大;实验结束
时,连接盛水试剂瓶和量筒的导管中有少量水存在,使所测氢气的体积偏小。于是他
们设计了如图所示的实验装置。
①装置中导管a的作用是_______________________________________。
②若需确定产生氢气的物质的量,还需测定的数据是____________________。
【答案】2Al+2NaOH+2H O=2NaAlO +3H ↑ 97 偏高 E D G
2 2 2
使分液漏斗内气体压强与锥形瓶内气体压强相等 打开分液漏斗活塞时,稀硫酸能
顺利滴下 滴入锥形瓶的稀硫酸的体积等于进入分液漏斗的气体的体积,从而消除
由于加入稀硫酸而引起的测定氢气体积的误差 实验时的温度和压强
【分析】
方案一:将镁铝合金与足量NaOH溶液反应,镁不和NaOH溶液反应,铝与NaOH溶
液发生反应2Al+2NaOH+2H O=2NaAlO +3H ↑;
2 2 2
方案二:镁铝合金与稀硫酸反应产生氢气,用排水量气法测定氢气的体积,其中氢气
通过盛水的试剂瓶时一定要短进长出,利用增大压强的原理将水排入量筒中,量筒中
水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部。
【详解】
方案一:(1)等质量的镁铝合金中,镁的质量分数最小时,铝的质量最大,需要的
NaOH溶液的体积最大,则实际需要的NaOH溶液的体积应大于或等于该最大值,假
设镁铝合金中镁的质量分数最小为3%,则10.8g镁铝合金样品中含有铝的质量为10.8g×(1-3%)=10.476g,其物质的量为 =0.388mol,根据反应
2Al+2NaOH+2H O=2NaAlO +3H ↑可知,需要清耗的NaOH的物质的量
2 2 2
n(NaOH)=n(Al)=0.388mol,其溶液的体积为 =0.097L=97mL,故V≥97mL。
(2)过滤后,金属镁的表面会残留偏铝酸钠等物质,如果未洗涤,测得剩余固体的质量
将大于镁的实际质量,所测得镁的质量分数将偏高。
方案二:(1)镁铝合金与稀硫酸反应产生氢气,用排水量气法测定氢气的体积,其中氢
气通过盛水的试剂瓶时一定要短进长出,利用增大压强的原理将水排入量筒中,量筒
中水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部,故连接顺序为A接
E,D接G。
(2)①装置中导管a的作用是保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开
分液漏斗活塞时,稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸的体积等于进入分液漏斗
的气体的体积,从而消除由于加入稀硫酸而引起的测定氢气体积的误差。
②气体体积受温度和压强影响,因此若需确定产生氨气的物质的量,还需测定实验时
的温度和压强。
20.(2019·江苏广陵区·扬州中学高一期末)已知:①铜矿石中含有Cu (OH) CO 及含
2 2 3
铁元素的杂质;
②黄铵铁矾的化学式为(NH )xFey(SO )m(OH)n,其中铁为+3价。
4 4
某兴趣小组利用该铜矿石制黄铵铁矾的流程如下:
(1)Cu (OH) CO 与稀硫酸反应时离子方程式___________。
2 2 3
(2)黄铵铁矾高温下分解可得到一种红棕色固体,该红棕色固体的化学式为___________。
(3)H O 可以将Fe2+转化成Fe3+。但温度过高时,Fe2+转化率下降,其原因___________。
2 2
(4)该小组为测定黄铵铁矾的组成,进行了如下实验:
a.称取mg样品,加盐酸完全溶解后,将所得溶液分为两等份;
b.向一份中加入足量NaOH溶液并加热,收集到标准状况下112mL的气体(发生反应:
+OH- NH ↑+HO,假设气体全部逸出);将所得沉淀过滤、洗涤、灼烧至恒重,
3 2得到红棕色粉末0.60g;
c.向另一份中加足量BaCl 溶液充分反应后,过滤、洗涤、干燥得沉淀2.33g。
2
①黄铵铁矾中 与 的个数比为___________;
②通过计算确定黄铵铁矾的化学式___________。(写出必要的计算过程,否则不得分)
【答案】Cu (OH) CO+4H+=2Cu2++CO ↑+3H O Fe O 过氧化氢高温下易分解
2 2 3 2 2 2 3
1:2 (NH )Fe (SO )(OH)
4 2 3 4 4 3
【分析】
由流程可知,铜矿与硫酸反应,过滤除去不溶物,溶液A中含有Cu2+、Fe2+、Fe3+,调
节溶液pH、加入过氧化氢将Fe2+氧化为Fe3+,再加入硫酸铵得到硫酸铜与黄铵铁矾,
以此来解答。
【详解】
(1)Cu (OH) CO 与稀硫酸反应时离子方程式为Cu (OH) CO+4H+=2Cu2++CO ↑+3H O,
2 2 3 2 2 3 2 2
故答案为:Cu (OH) CO+4H+=2Cu2++CO ↑+3H O;
2 2 3 2 2
(2)黄铵铁矶高温下分解可得到一种红棕色固体,该红棕色固体的化学式为Fe O,故答
2 3
案为:Fe O;
2 3
(3)H O 可以将Fe2+转化成Fe3+,但温度过高时,Fe2+转化率下降,其原因为过氧化氢高
2 2
温下分解,故答案为:过氧化氢高温下易分解;
(4)由信息可知,NH 为 =0.005mol,则n(NH )=0.005mol,Fe O 的物质的
3 2 3
量为 =0.00375mol,则n(Fe3+)=2×0.00375mol=0.0075mol,硫酸钡物质的量为
=0.01mol,则n(SO )=0.01mol,由电荷守恒,则
n(OH−)=0.005mol+0.0075mol×3−0.01mol×2=0.0075mol,
①黄铵铁矾中NH 与SO 的个数比为0.005mol:0.01mol=1:2,故答案为:1:2;
②黄铵铁矾中n(NH ):n(Fe3+):n(SO
):n(OH−)=0.005mol:0.0075mol:0.01mol:0.0075mol=2:3:4:3,故黄铵铁矾的化学式为
(NH )Fe (SO )(OH) ,故答案为:(NH )Fe (SO )(OH) 。
4 2 3 4 4 3 4 2 3 4 4 3