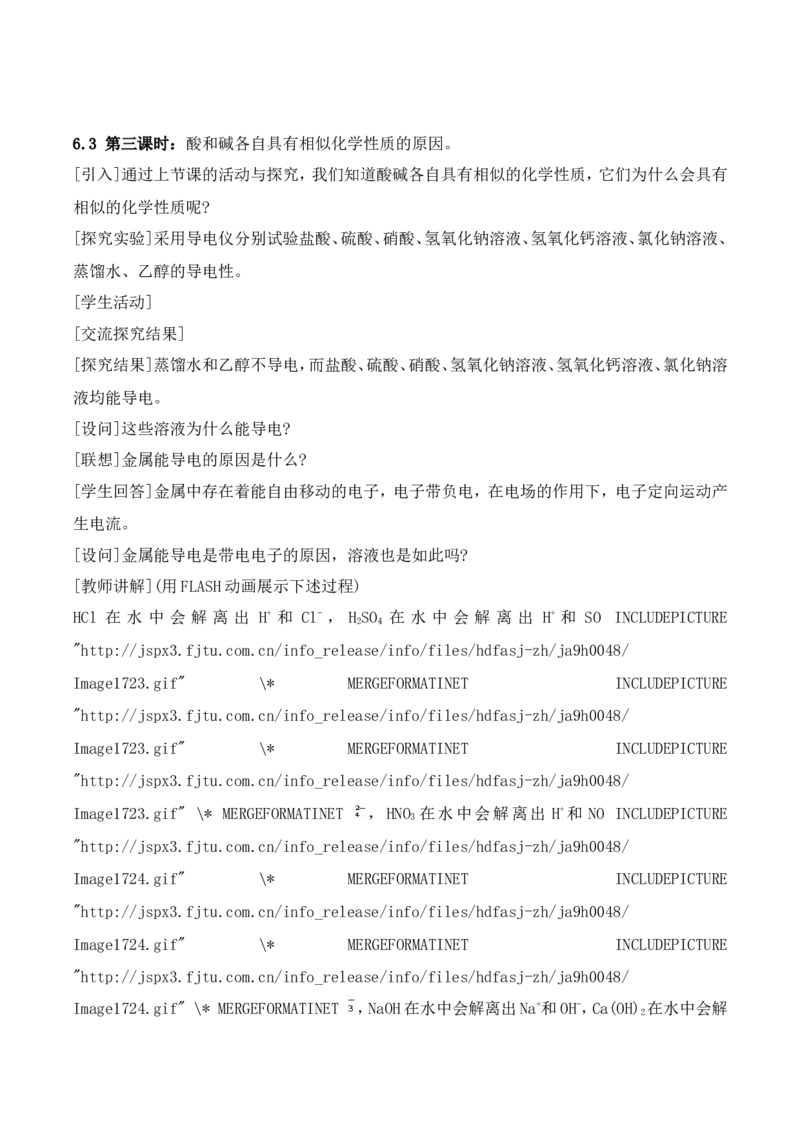文档内容
第十单元 课题1 常见的酸和碱
(参考课时:3课时)
1 教学目标
1.1 知识与技能:
(1)知道几种常见酸和碱的主要性质和用途。
(2)会用酸碱指示剂检验溶液的酸碱性。
(3)认识酸和碱的腐蚀性及使用时的安全注意事项。
(4)能完成简单的探究实验。
1.2 过程与方法:
(1)进一步认识和体验科学探究的过程。
(2)运用实验的方法获取信息,运用比较概括等方法对获取的信息进行加工。
(3)增强对化学现象的探究欲,发展善于合作、勤于思考的科学精神。
1.3 情感态度与价值观 :
进一步增强探究物质的好奇心和求知欲。
2 教学重点/难点/易考点
2.1 教学重点
(1)运用酸碱指示剂检验溶液的酸碱性。
[来源:www.shul
(2)酸碱各自相似的化学性质。
2.2 教学难点
酸和碱各自具有相似化学性质的原因。
3 专家建议
本节从学生亲身体验入手引出问题,较好的激起了学生的学习兴趣,为学好本节打好基础
本节课学习难度不是很大,学生可以亲自设计实验、动手探究,方便易操作现象明显的实
验,亲自体验当魔术师的感觉,尝试合作的力量,体验解决困惑后的喜悦。通过实验探究,初步
学会用酸碱指示剂识别酸和碱,并通过对比学习浓盐酸和浓硫酸的物理性质和它们的特性,也
是为以后学习酸碱做好辅垫。
授课过程中,利用食物味道和回忆感觉为学生提供丰富的感性材料,从而获取对酸和碱的
感性认识;用小魔术形式激发学生学习的积极性和参与的热情,体验到收获的喜悦。从而到出
酸碱指示剂,并会用指示剂区分酸碱溶液;通过实验探究和图片的展示,帮助学生推理出浓盐酸和浓硫酸的特性,同时在使用浓硫酸时,注意它的强烈的腐蚀性,从而提高学生观察分析,应
用知识解决问题的能力,培养了学生辩证思维的方法。教学效果比较好。
4 教学方法
复习、总结、联系实际、实验探究、巩固练习。
5 教学用具
教师用具:仪器:烧杯、玻璃棒、锥形瓶、双孔塞、分液漏斗、短玻璃导管、镊子、投影仪;
药品:浓硫酸、鸡爪、NaOH溶液(20%)。
学生用具:仪器:滴管、研钵,烧杯、纱布、纸、小木棍、布、玻璃片、玻璃棒、点滴板、镊子、表面皿、
蒸发皿、溶液导电性实验仪器;
药品:食醋、稀盐酸、稀硝酸、稀硫酸、食盐水、石灰水、氢氧化钠溶液、紫色石蕊试液、无色酚酞
试液、酒精、花(果实)、浓盐酸、浓硫酸、生锈的铁钉、NaOH固体、生石灰、蒸馏水。
6 教学过程
6.1 第一课时:酸和碱溶液与酸碱指示剂的反应。
[回忆]在生活中,你接触过、听说过哪些酸和碱?
[学生发言]如:酸有醋酸、盐酸、硫酸、硝酸、果酸,碱有石灰水中的溶质、氢氧化钠。
[设问]我们如何确定这些物质是酸还是碱?
[回想]二氧化碳通入紫色的石蕊试液中,溶液颜色有什么变化?是什么物质使溶液改变了颜色?
[学生回答]1.溶液由紫色变成红色。
2.二氧化碳溶于水生成了碳酸,是碳酸改变了溶液的颜色。
[讨论]根据以上知识,试讨论确定物质是酸还是碱的方法。
[学生发言]取各物质的溶液各少量,分别滴入几滴石蕊试液,若试液由紫色变为红色,则被测
溶液是酸溶液,否则为碱溶液。
[引导]好,通过下面的活动与探究即可验证你设想的正确与否。
[活动与探究](投影展示)
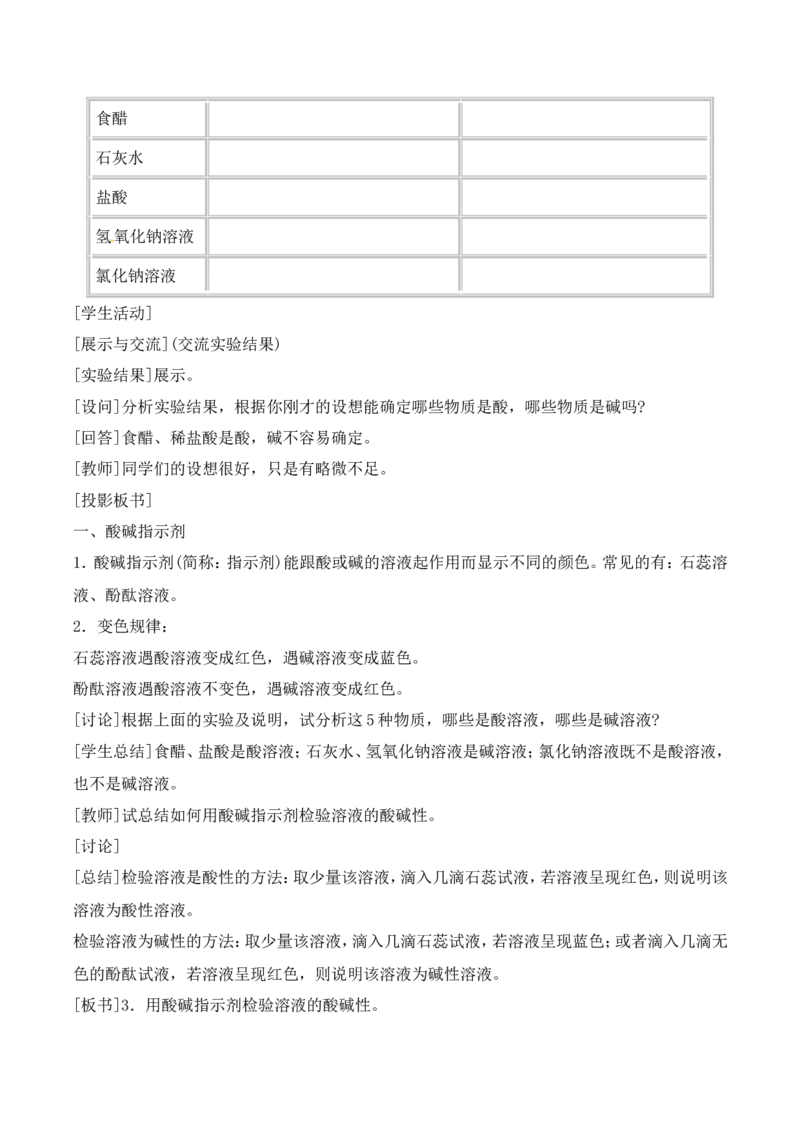
将10支试管分成两组,每组的5支试管中分别加入少量食醋、石灰水、盐酸、氢氧化钠溶液、氯
化钠溶液。向其中一组试管中滴入紫色石蕊试液2—3滴,向另一组试管中滴入2~3滴无色酚
酞溶液,观察现象。
加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化食醋
石灰水
盐酸
氢氧化钠溶液
氯化钠溶液 t]
[学生活动]
[展示与交流](交流实验结果)
[实验结果]展示。
[设问]分析实验结果,根据你刚才的设想能确定哪些物质是酸,哪些物质是碱吗?
[回答]食醋、稀盐酸是酸,碱不容易确定。
[教师]同学们的设想很好,只是有略微不足。
[投影板书]
一、酸碱指示剂
1.酸碱指示剂(简称:指示剂)能跟酸或碱的溶液起作用而显示不同的颜色。常见的有:石蕊溶
液、酚酞溶液。
2.变色规律:
石蕊溶液遇酸溶液变成红色,遇碱溶液变成蓝色。
酚酞溶液遇酸溶液不变色,遇碱溶液变成红色。
[讨论]根据上面的实验及说明,试分析这5种物质,哪些是酸溶液,哪些是碱溶液?
[学生总结]食醋、盐酸是酸溶液;石灰水、氢氧化钠溶液是碱溶液;氯化钠溶液既不是酸溶液,
也不是碱溶液。
[教师]试总结如何用酸碱指示剂检验溶液的酸碱性。
[讨论]
[总结]检验溶液是酸性的方法:取少量该溶液,滴入几滴石蕊试液,若溶液呈现红色,则说明该
溶液为酸性溶液。
检验溶液为碱性的方法:取少量该溶液,滴入几滴石蕊试液,若溶液呈现蓝色;或者滴入几滴无
色的酚酞试液,若溶液呈现红色,则说明该溶液为碱性溶液。[来
[板书]3.用酸碱指示剂检验溶液的酸碱性。[过渡]酸碱指示剂的种类很多,不只是石蕊试液和酚酞试液。在日常生活中指示剂随处可见,
同学们可通过下面的活动体验一下。
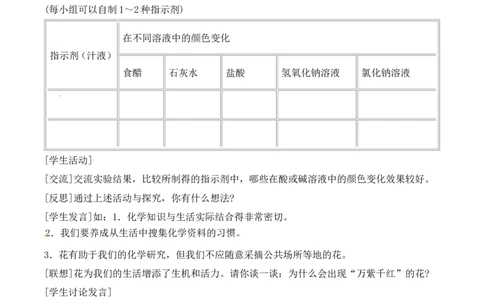
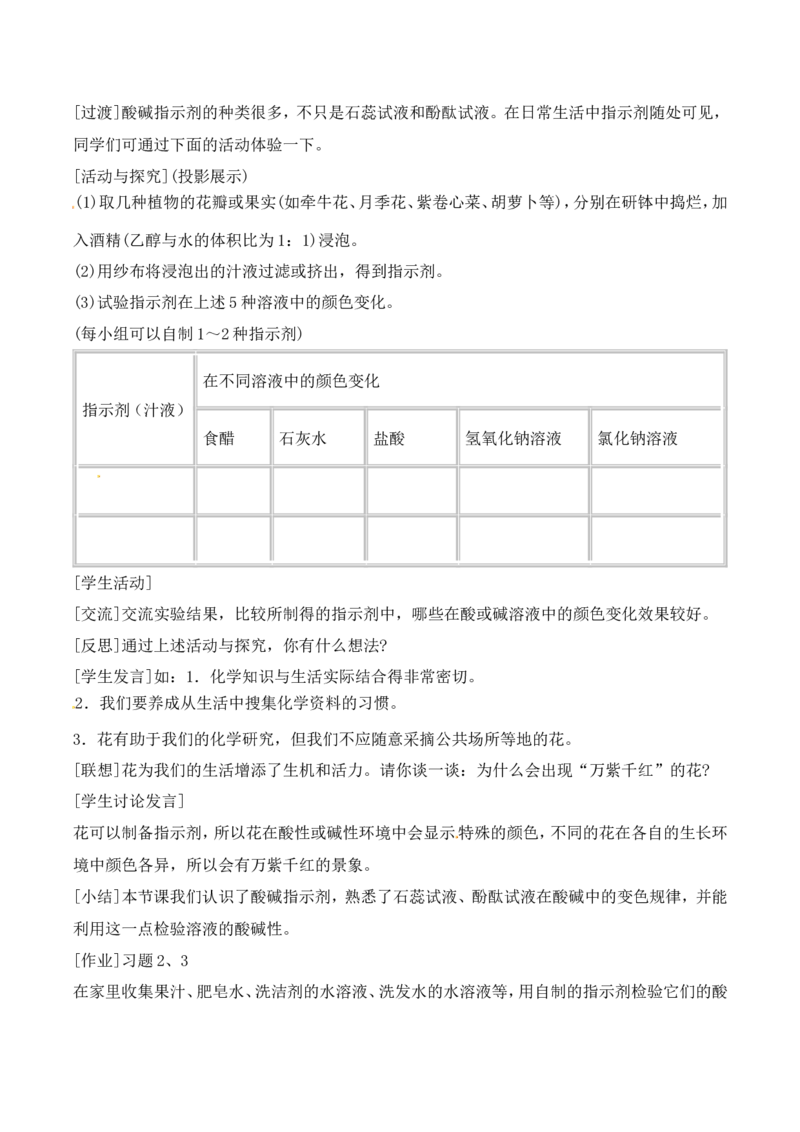
[活动与探究](投影展示)
(1)取几种植物的花瓣或果实(如牵牛花、月季花、紫卷心菜、胡萝卜等),分别在研钵中捣烂,加
入酒精(乙醇与水的体积比为1:1)浸泡。
(2)用纱布将浸泡出的汁液过滤或挤出,得到指示剂。
(3)试验指示剂在上述5种溶液中的颜色变化。
(每小组可以自制1~2种指示剂)
在不同溶液中的颜色变化
指示剂(汁液)
食醋 石灰水 盐酸 氢氧化钠溶液 氯化钠溶液
[学生活动]
[交流]交流实验结果,比较所制得的指示剂中,哪些在酸或碱溶液中的颜色变化效果较好。
[反思]通过上述活动与探究,你有什么想法?
[学生发言]如:1.化学知识与生活实际结合得非常密切。
2.我们要养成从生活中搜集化学资料的习惯。
3.花有助于我们的化学研究,但我们不应随意采摘公共场所等地的花。
[联想]花为我们的生活增添了生机和活力。请你谈一谈:为什么会出现“万紫千红”的花?
[学生讨论发言]
花可以制备指示剂,所以花在酸性或碱性环境中会显示特殊的颜色,不同的花在各自的生长环
境中颜色各异,所以会有万紫千红的景象。
[小结]本节课我们认识了酸碱指示剂,熟悉了石蕊试液、酚酞试液在酸碱中的变色规律,并能
利用这一点检验溶液的酸碱性。
[作业]习题2、3
在家里收集果汁、肥皂水、洗洁剂的水溶液、洗发水的水溶液等,用自制的指示剂检验它们的酸碱性。
6.2 第二课时:几种常见酸和碱的主要性质和用途。
[引入]上节课我们学习了酸碱指示剂,并熟悉了几种酸和碱,这节课我们重点探讨几种酸和碱
的性质和用途。
[板书]二、几种常见的酸
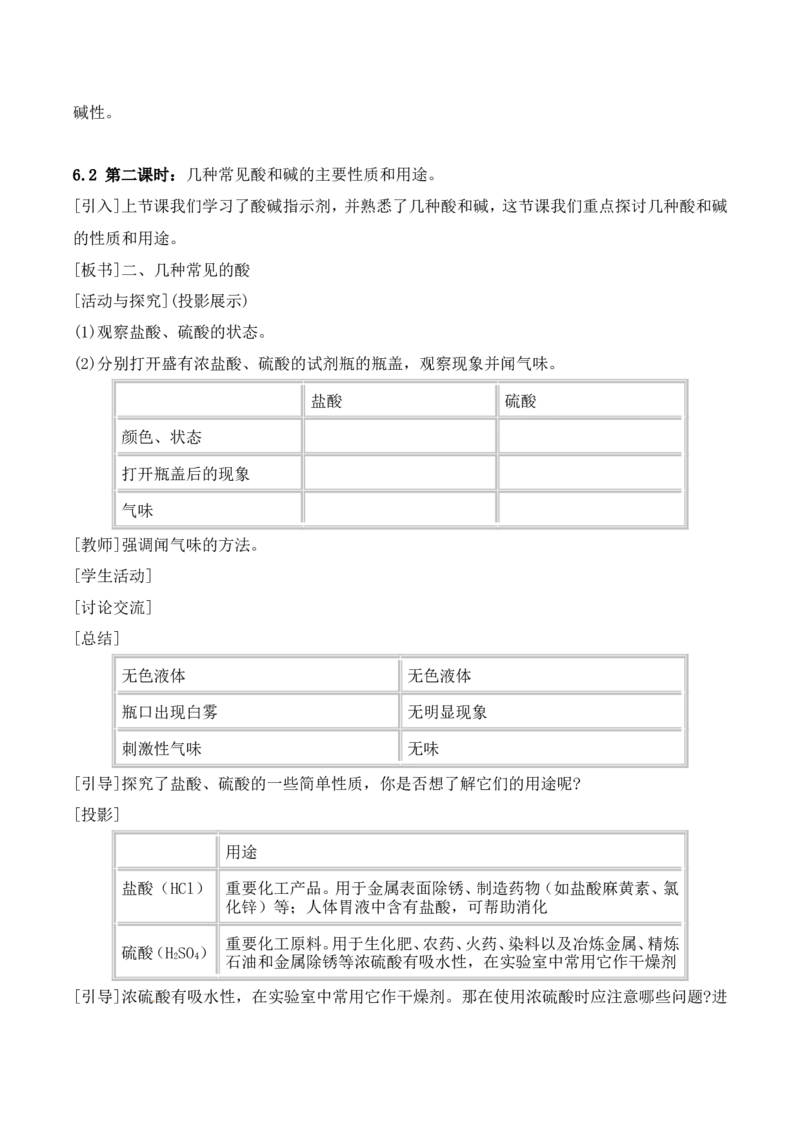
[活动与探究](投影展示)
(1)观察盐酸、硫酸的状态。
(2)分别打开盛有浓盐酸、硫酸的试剂瓶的瓶盖,观察现象并闻气味。
盐酸 硫酸
颜色、状态 [来源:数理化网]
打开瓶盖后的现象
气味
[教师]强调闻气味的方法。
[学生活动]
[讨论交流]
[总结]
无色液体 无色液体
瓶口出现白雾 无明显现象
刺激性气味 无味
[引导]探究了盐酸、硫酸的一些简单性质,你是否想了解它们的用途呢?
[投影]
用途
盐酸(HCl) 重要化工产品。用于金属表面除锈、制造药物(如盐酸麻黄素、氯
[来源: 化锌)等;人体胃液中含有盐酸,可帮助消化
重要化工原料。用于生化肥、农药、火药、染料以及冶炼金属、精炼
硫酸(H SO )
2 4 石油和金属除锈等浓硫酸有吸水性,在实验室中常用它作干燥剂
[引导]浓硫酸有吸水性,在实验室中常用它作干燥剂。那在使用浓硫酸时应注意哪些问题?进行完下面的活动与探究,你就会明白使用浓硫酸的注意事项。
[活动与探究](投影展示)
将纸、小木棍、布放在玻璃片上做实验:
实验 放置一会儿后的现象
用玻璃棒蘸浓酸在纸上写字
用小木棍蘸少量浓硫酸
将浓酸滴到一小块布上
[教师]提醒学生注意安全,不要将浓硫酸沾到皮肤和衣服上。
[学生活动](教师注意学生安全)
[交流]纸上留下黑色的字迹;小木棍上被浓硫酸触及的部位变黑;布料上滴有浓硫酸的部位已
破烂。
[反思]通过上面的活动与探究,你有什么想法?
[学生发言]使用浓硫酸时,必须十分小心,切不可将浓硫酸滴在皮肤和衣服上。
[教师讲解]浓硫酸具有强腐蚀性。它能夺取纸张、木材、布料、皮肤(都由含碳、氢、氧等元素的
化合物组成)里的水分,生成黑色的炭。
[引导]浓硫酸有吸水性,那浓硫酸与水作用时还会出现哪些问题?
[教师演示]将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里,用玻璃棒不断搅动,并让学生用手
接触烧杯外壁。
[分析讨论]手有什么感觉?这说明了什么?
[学生]用手接触烧杯外壁,感到比较烫。这说明浓硫酸溶于水时放出大量的热。
[设问]能否将上述实验稍作调整,将水注入浓硫酸里?
[学生发言]能;不能。
[教师演示]在500mL锥形瓶中盛约25 mL浓硫酸,锥形瓶双孔塞的一孔中装分液漏斗(盛有水)
另一孔装短玻璃导管。将分液漏斗中的少量水缓慢滴入锥形瓶,观察现象。
[学生描述现象]
水立刻沸腾,液滴向四周飞溅。
[设问]四周飞溅的液滴若接触了人的皮肤,后果会怎样?能否将第1个演示实验中的水、浓硫酸
对调?
[学生回答]1.皮肤立即被腐蚀,生成黑色的炭。2.不能将水沿烧杯壁缓慢地注入浓硫酸里。
[教师]水的密度较小,浮在浓硫酸上面,溶解时放出的热会使水立刻沸腾,使硫酸液滴向四周
飞溅。
稀释浓硫酸的正确操作:如演示实验1。
[小结并板书]1.浓硫酸:(1)有吸水性,在实验室中常用它作干燥剂。
(2)浓硫酸具有强腐蚀性,使用时必须十分小心。
(3)稀释浓硫酸的正确操作:将浓硫酸沿着烧杯壁缓慢地注入盛有水的烧杯里,用玻璃棒不断
搅动。
(4)如果不慎将浓硫酸沾到皮肤或衣服上,应立即用布擦掉,再用大量水冲洗,然后涂上3%~
5%的碳酸氢钠溶液。
[思考]如果将稀硫酸沾到皮肤或衣服上,是否也要进行类似浓硫酸的操作?为什么?
[学生思考后发言]1.稀硫酸没有强腐蚀性,不必采取处理浓硫酸的操作。
2.应该采取同样的操作。因为稀硫酸中的水会慢慢蒸发,日久后会变成浓硫酸,同样会腐蚀皮
肤、衣服。
[过渡]前面我们探究了几种酸的物理性质,下面来探究它们的化学性质。
[活动与探究](投影展示)
(1)如下图所示,在白色点滴板上进行实验,并观察现象。
加紫色石蕊溶液 加无色酚酞溶液
稀盐酸
稀硫酸
(2)回忆第八单元所学的几种金属分别与稀盐酸或稀
硫酸的反应,写出化学方程式。
与稀盐酸反应 与稀硫酸反应
镁 [来源:数理化网]
锌
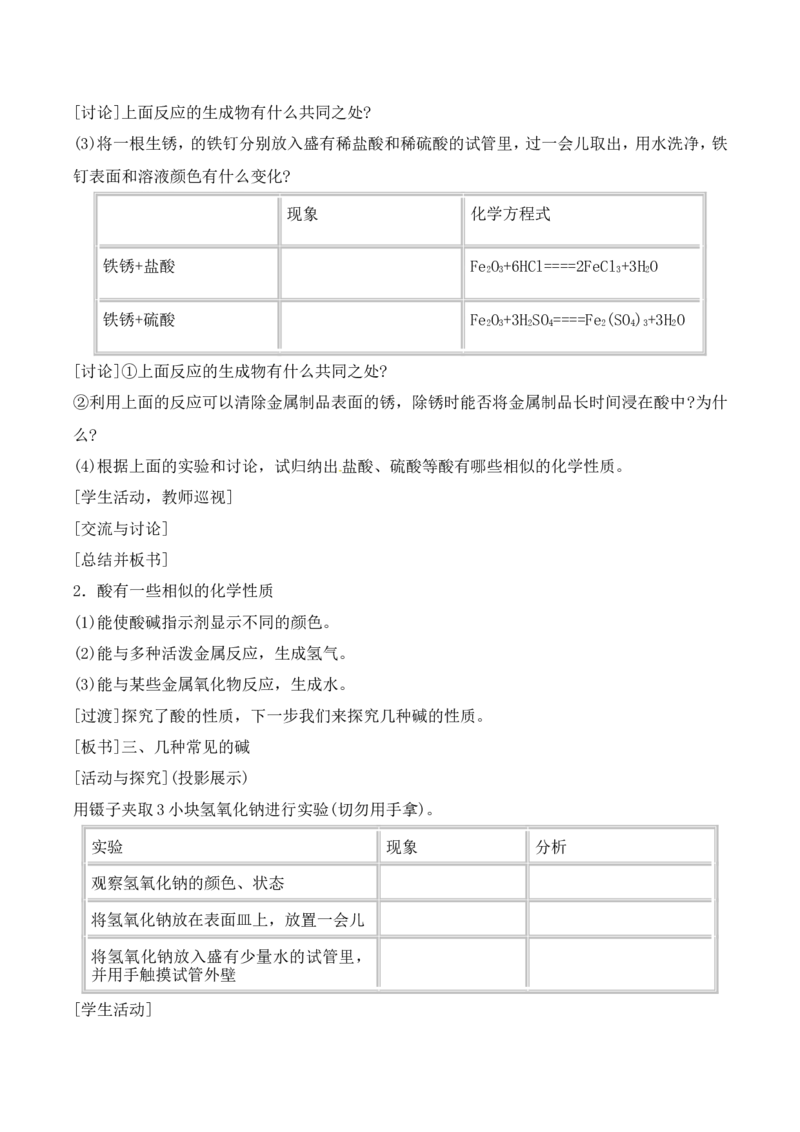
铁[讨论]上面反应的生成物有什么共同之处?
(3)将一根生锈,的铁钉分别放入盛有稀盐酸和稀硫酸的试管里,过一会儿取出,用水洗净,铁
钉表面和溶液颜色有什么变化?
现象 化学方程式
铁锈+盐酸 Fe O +6HCl====2FeCl +3H O
2 3 3 2
铁锈+硫酸 Fe O +3H SO ====Fe (SO ) +3H O
2 3 2 4 2 4 3 2
[讨论]①上面反应的生成物有什么共同之处?
②利用上面的反应可以清除金属制品表面的锈,除锈时能否将金属制品长时间浸在酸中?为什
么?
(4)根据上面的实验和讨论,试归纳出盐酸、硫酸等酸有哪些相似的化学性质。
[学生活动,教师巡视]
[交流与讨论]
[总结并板书]
2.酸有一些相似的化学性质
(1)能使酸碱指示剂显示不同的颜色。
(2)能与多种活泼金属反应,生成氢气。
(3)能与某些金属氧化物反应,生成水。
[过渡]探究了酸的性质,下一步我们来探究几种碱的性质。
[板书]三、几种常见的碱
[活动与探究](投影展示)
用镊子夹取3小块氢氧化钠进行实验(切勿用手拿)。
实验 现象 分析
观察氢氧化钠的颜色、状态
将氢氧化钠放在表面皿上,放置一会儿
将氢氧化钠放入盛有少量水的试管里,
并用手触摸试管外壁
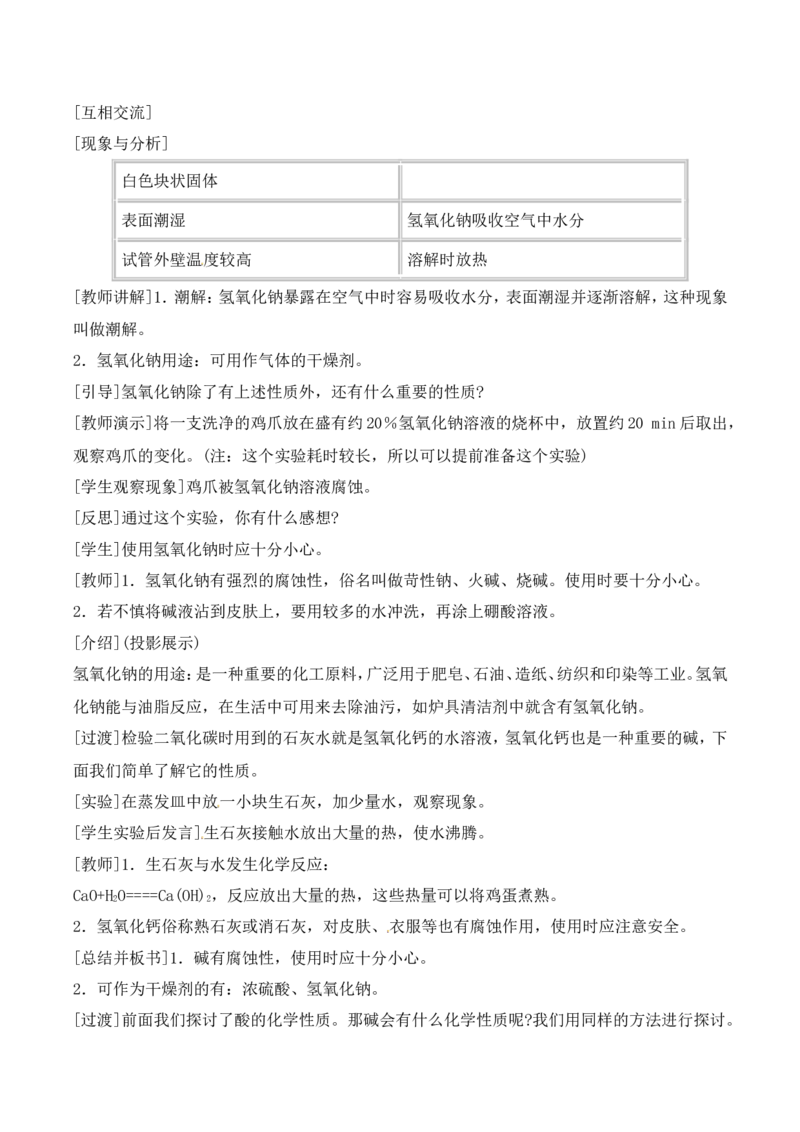
[学生活动][互相交流]
[现象与分析]
白色块状固体
表面潮湿 氢氧化钠吸收空气中水分
试管外壁温度较高 溶解时放热
[教师讲解]1.潮解:氢氧化钠暴露在空气中时容易吸收水分,表面潮湿并逐渐溶解,这种现象
叫做潮解。
2.氢氧化钠用途:可用作气体的干燥剂。
[引导]氢氧化钠除了有上述性质外,还有什么重要的性质?
[教师演示]将一支洗净的鸡爪放在盛有约20%氢氧化钠溶液的烧杯中,放置约20 min后取出,
观察鸡爪的变化。(注:这个实验耗时较长,所以可以提前准备这个实验)
[学生观察现象]鸡爪被氢氧化钠溶液腐蚀。
[反思]通过这个实验,你有什么感想?
[学生]使用氢氧化钠时应十分小心。
[教师]1.氢氧化钠有强烈的腐蚀性,俗名叫做苛性钠、火碱、烧碱。使用时要十分小心。
2.若不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液。
[介绍](投影展示)
氢氧化钠的用途:是一种重要的化工原料,广泛用于肥皂、石油、造纸、纺织和印染等工业。氢氧
化钠能与油脂反应,在生活中可用来去除油污,如炉具清洁剂中就含有氢氧化钠。
[过渡]检验二氧化碳时用到的石灰水就是氢氧化钙的水溶液,氢氧化钙也是一种重要的碱,下
面我们简单了解它的性质。
[实验]在蒸发皿中放一小块生石灰,加少量水,观察现象。
[学生实验后发言]生石灰接触水放出大量的热,使水沸腾。
[教师]1.生石灰与水发生化学反应:
CaO+H O====Ca(OH) ,反应放出大量的热,这些热量可以将鸡蛋煮熟。
2 2
2.氢氧化钙俗称熟石灰或消石灰,对皮肤、衣服等也有腐蚀作用,使用时应注意安全。
[总结并板书]1.碱有腐蚀性,使用时应十分小心。
2.可作为干燥剂的有:浓硫酸、氢氧化钠。
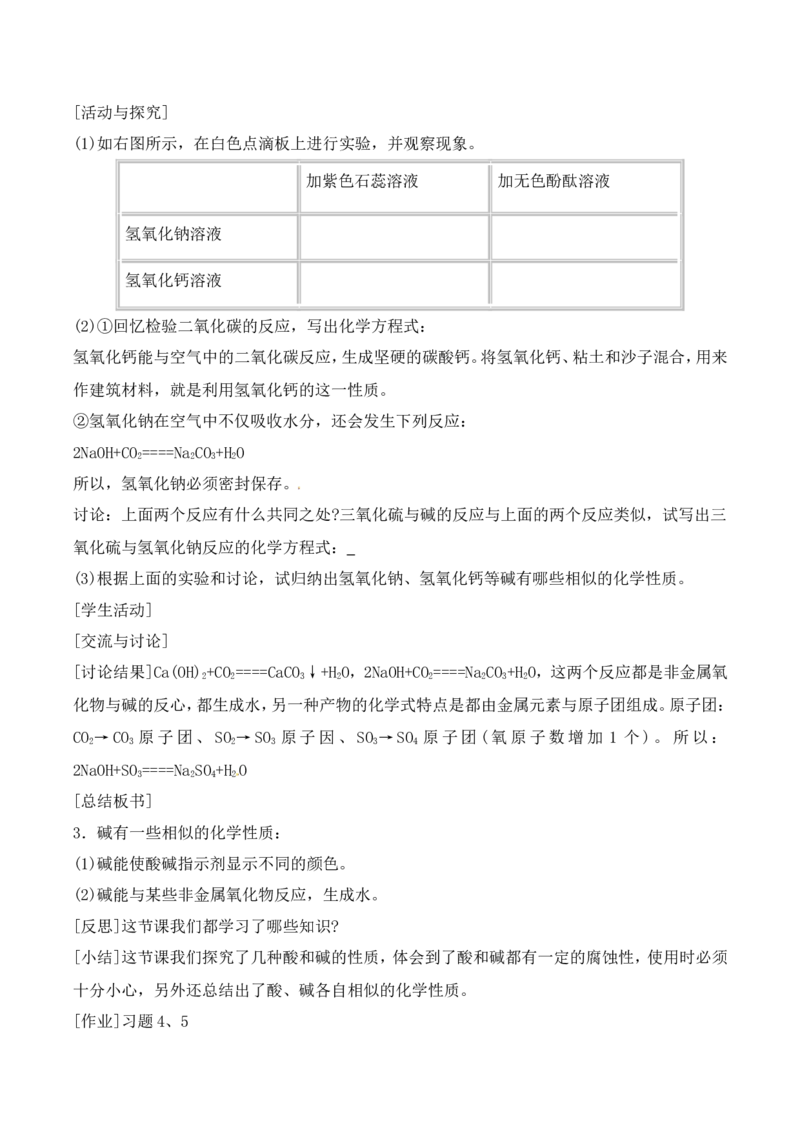
[过渡]前面我们探讨了酸的化学性质。那碱会有什么化学性质呢?我们用同样的方法进行探讨。[活动与探究]
(1)如右图所示,在白色点滴板上进行实验,并观察现象。
加紫色石蕊溶液 加无色酚酞溶液
氢氧化钠溶液 [来源:]
氢氧化钙溶液
(2)①回忆检验二氧化碳的反应,写出化学方程式:
氢氧化钙能与空气中的二氧化碳反应,生成坚硬的碳酸钙。将氢氧化钙、粘土和沙子混合,用来
作建筑材料,就是利用氢氧化钙的这一性质。
②氢氧化钠在空气中不仅吸收水分,还会发生下列反应:
2NaOH+CO ====Na CO +H O
2 2 3 2
所以,氢氧化钠必须密封保存。
讨论:上面两个反应有什么共同之处?三氧化硫与碱的反应与上面的两个反应类似,试写出三
氧化硫与氢氧化钠反应的化学方程式:
(3)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙等碱有哪些相似的化学性质。
[学生活动]
[交流与讨论]
[讨论结果]Ca(OH) +CO ====CaCO ↓+H O,2NaOH+CO ====Na CO +H O,这两个反应都是非金属氧
2 2 3 2 2 2 3 2
化物与碱的反心,都生成水,另一种产物的化学式特点是都由金属元素与原子团组成。原子团:
CO →CO 原子团、SO →SO 原子因、SO →SO 原子团(氧原子数增加 1 个)。所以:
2 3 2 3 3 4
2NaOH+SO ====Na SO +H O
3 2 4 2
[总结板书]
3.碱有一些相似的化学性质:
(1)碱能使酸碱指示剂显示不同的颜色。
(2)碱能与某些非金属氧化物反应,生成水。
[反思]这节课我们都学习了哪些知识?
[小结]这节课我们探究了几种酸和碱的性质,体会到了酸和碱都有一定的腐蚀性,使用时必须
十分小心,另外还总结出了酸、碱各自相似的化学性质。
[作业]习题4、56.3 第三课时:酸和碱各自具有相似化学性质的原因。
[引入]通过上节课的活动与探究,我们知道酸碱各自具有相似的化学性质,它们为什么会具有
相似的化学性质呢?
[探究实验]采用导电仪分别试验盐酸、硫酸、硝酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液、
蒸馏水、乙醇的导电性。
[学生活动]
[交流探究结果]
[探究结果]蒸馏水和乙醇不导电,而盐酸、硫酸、硝酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶
液均能导电。
[设问]这些溶液为什么能导电?
[联想]金属能导电的原因是什么?
[学生回答]金属中存在着能自由移动的电子,电子带负电,在电场的作用下,电子定向运动产
生电流。[来t]
[设问]金属能导电是带电电子的原因,溶液也是如此吗?
[教师讲解](用FLASH动画展示下述过程)
HCl 在 水 中 会 解 离 出 H+ 和 Cl- , H SO 在 水 中 会 解 离 出 H+ 和 SO INCLUDEPICTURE
2 4
"http://jspx3.fjtu.com.cn/info_release/info/files/hdfasj-zh/ja9h0048/
Image1723.gif" \* MERGEFORMATINET INCLUDEPICTURE
"http://jspx3.fjtu.com.cn/info_release/info/files/hdfasj-zh/ja9h0048/
Image1723.gif" \* MERGEFORMATINET INCLUDEPICTURE
"http://jspx3.fjtu.com.cn/info_release/info/files/hdfasj-zh/ja9h0048/
Image1723.gif" \* MERGEFORMATINET ,HNO 在水中会解离出 H+和 NO INCLUDEPICTURE
3
"http://jspx3.fjtu.com.cn/info_release/info/files/hdfasj-zh/ja9h0048/
Image1724.gif" \* MERGEFORMATINET INCLUDEPICTURE
"http://jspx3.fjtu.com.cn/info_release/info/files/hdfasj-zh/ja9h0048/
Image1724.gif" \* MERGEFORMATINET INCLUDEPICTURE
"http://jspx3.fjtu.com.cn/info_release/info/files/hdfasj-zh/ja9h0048/
Image1724.gif" \* MERGEFORMATINET ,NaOH在水中会解离出Na+和OH-,Ca(OH) 在水中会解
2离出Ca2+和OH-,NaCl在水中会解离出Na+和Cl-。这些带电的阴阳离子在溶液中可以自由移动,
在电场的作用下,会定向运动产生电流。
[分析]比较上述物质的解离情况,试分析酸碱各自具有相似化学性质的原因。
[学生思考、讨论、总结]
[归纳]盐酸、硫酸、硝酸在水溶液中都解离出H+和酸根离子,即在不同的酸溶液中都含有相同
的H+,所以酸有一些相似的性质。我们把在水溶液中能电离出唯一的阳离子(H+)的化合物叫做
酸。
氢氧化钠、氢氧化钙这些碱,在水溶液中都能解离出金属离子和OH-,即在不同的碱溶液中都含
有相同的OH-,所以碱具有一些相似的性质。我们把在水溶液中能电离出唯一的阴离子(OH-)的
化合物叫做碱。(对于碱的概念的探究描述,可由学生仿照酸的探究方式自主总结)
[板书]四、酸、碱的概念[]
酸:在水溶液中能电离出唯一的阳离子(H+)的化合物。
碱:在水溶液中能电离出唯一的阴离子(OH-)的化合物。
[反思]通过本节课的学习,你认为我们的探究思路是什么?
[学生思考、讨论]
[总结]探究思路:实验探究→发现共性→设想共性的原因→再实验探究→理论解释→总结出酸
碱的概念。
[反思]学习了本节课,你们有什么收获?
[学生发言]如:1.理解了酸、碱各自具有相似化学性质的原因。
2.初步认识了酸、碱,能简述它们的概念。
3.明白了溶液导电的原因是因为存在自由移动的离子,不同于金属。
4.又学习了一种化学探究的方法。
[作业]实验探究中,氯化钠溶液也能导电,但氯化钠既不是酸,又不是碱,它属哪类物质,请同
学们查阅资料。[来
7 板书设计
第十单元 酸和碱
课题1 常见的酸和碱
第一课时一、酸碱指示剂
1.酸碱指示剂(简称:指示剂)能跟酸或碱的溶液起作用而显示不同的颜色。常见的有:石蕊溶
液、酚酞溶液。
2.变色规律;
石蕊溶液遇酸溶液变成红色,遇碱溶液变成蓝色。
酚酞溶液遇酸溶液不变色,遇碱溶液变成红色。
3.用酸碱指示剂可以检验溶液的酸碱性。
第二课时
二、几种常见的酸
1.浓硫酸
(1)吸水性
(2)强腐蚀性
(3)稀释操作
(4)不慎沾到皮肤或衣服上后的处理方法
2.酸有一些相似的化学性质
(1)能使酸碱指示剂显示不同的颜色。
(2)能与多种活泼金属反应,生成氢气。
(3)能与某些金属氧化物反应,生成水。
三、几种常见的碱
1. 碱有腐蚀性,使用时应十分小心。
2.可作为干燥剂的有:浓硫酸、氢氧化钠。
3.碱有一些相似的化学性质:
(1)碱能使酸碱指示剂显示不同的颜色。
(2)碱能与某些非金属氧化物反应,生成水。
第三课时
四、酸、碱的概念
酸:在水溶液中能电离出唯一的阳离子(H+)的化合物。
碱:在水溶液中能电离出唯一的阴离子(OH-)的化合物。