文档内容
《化学反应与能量》检测题
一、单选题
1.下列有关热化学方程式的表示及说法正确的是 ( )
A.已知c(石墨,s)=c(金刚石,s);△H>0,则石墨比金刚石稳定
B.若2C(s)+O (g)=2CO(g) △H=−221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol
2
C.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H SO 和Ba(OH) 反应的中和热△H=2×
2 4 2
(-57.3)kJ/mol
D.已知H (g)+F (g)=2HF(g);△H=-270kJ/mol,则2L氟化氢气体分解成1L氢气和
2 2
1L氟气吸收270kJ热量
2.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
( )
A.碱性锌锰干电池的负极反应式为:MnO +2H O-2e−=Mn(OH) +2OH−
2 2 2
B.铅蓄电池放电时,正极反应式为PbO +4H++SO 2−+2e−=PbSO +2H O
2 4 4 2
C.NaHS水解反应方程式:HS−+H O H O++S2−
2 3
D.过量的SO 通入到漂白粉溶液中,反应方程式:ClO−+SO +H O=HClO+HSO −
2 2 2 3
3.在一体积固定的密闭容器中加入反应物A、B,发生如下反应: 。反应过程中
的部分数据如下表所示:
0 1.0 1.2 0
2 0.6
4 0.7
6 0.6
下列说法正确的是( )
A.第 时,反应刚好达到平衡状态
B.当 时说明该反应达到平衡状态
C.当该反应达平衡状态后,反应不再进行,各物质浓度保持不变
D.达平衡状态时C的物质的量浓度
4.在一个绝热容积不变的密闭容器中发生 下列各项能说明该反应已经达到化学平衡状态的是
A.容器内气体的总质量保持不变 B.容器中 的浓度保持不变
C.断裂 键的同时断裂 键 D. 和 的质量比14:3
5.氧气(O )和臭氧(O )是氧元素的两种同素异形体,已知热化学方程式:
2 3
4Al(s)+3O (g)=2Al O (s) ΔH ;
2 2 3 1
4Al(s)+2O (g)=2Al O (s) ΔH ;
3 2 3 2
3O (g)=2O (g) ΔH 。
2 3 3
则下列关系式正确的是( )
A.ΔH -ΔH =ΔH B.ΔH +ΔH =ΔH
1 2 3 1 2 3
C.ΔH -ΔH =ΔH D.ΔH +ΔH +ΔH =0
2 1 3 2 1 3
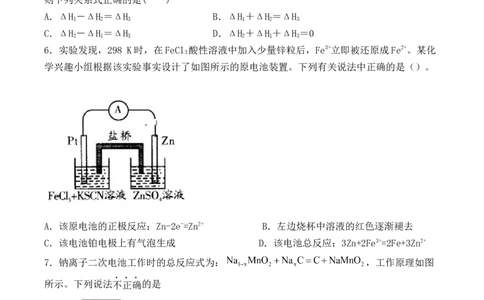
6.实验发现,298 K时,在FeCl 酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化
3
学兴趣小组根据该实验事实设计了如图所示的原电池装置。下列有关说法中正确的是()。
A.该原电池的正极反应:Zn-2e-=Zn2+ B.左边烧杯中溶液的红色逐渐褪去
C.该电池铂电极上有气泡生成 D.该电池总反应:3Zn+2Fe3+=2Fe+3Zn2+
7.钠离子二次电池工作时的总反应式为: ,工作原理如图
所示。下列说法不正确的是
A.钠离子电池的负极是Na-C复合材料
B.电池工作时电流从正极流出,经过负载流到负极,再经电解质流回正极
C.电解质可以是含Na+的导电有机聚合物或能传导Na+的固体钠盐D.电池正极的电极反应式为:
8.对于反应:X(g)+Y(g) ⇌2Z(g) ΔH<0的反应,某一时刻改变外界条件,其速率随时间
的变化图像如图所示。则下列说法符合该图像的是( )
A.t 时刻,增大了X的浓度 B.t 时刻,升高了体系温度
1 1
C.t 时刻,降低了体系温度 D.t 时刻,使用了催化剂
1 1
9.一定量的稀H SO 与过量铁粉反应时,为了加快反应速率,且又不影响生成的氢气的总量,
2 4
可向稀H SO 溶液中加入( )
2 4
A.CuSO 固体 B.NaOH固体 C.CH COONa固体 D.NH C1固体
4 3 4
10.4NH +5O 4NO+6H O,若反应速率分别用v(NH )、v(O )、v(NO)、v(H O)表示,
3 2 2 3 2 2
则下列关系表示正确的是 ()
A.5v(NH )=6v(O ) B.5v(O )=6v(H O)
3 2 2 2
C.2v(NH )=2v(H O) D.4v(O )=5v(NO)
3 2 2
11.在一定条件下,反应2A(g)+2B(g) 3C(g)+D(g)在恒容容器中进行,达到化
学平衡的标志是( )
A.单位时间内生成2n molB,同时消耗3n molCB.容器内压强不随时间变化
C.混合气体的密度不随时间变化 D.B物质的百分含量不变
12.1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖。哈
伯法合成氨需要20﹣50Mpa的高压和500℃的高温下,用铁作催化剂,且氨的产率为10%~
15%。2005年美国俄勒冈大学的化学家使用了一种名为transFe(DMeOPrPE) Cl 的铁化合物作
2 2
催化剂,在常温常压下合成出氨,反应可表示为N +3H =2NH ,下列有关说法正确的是
2 2 3
( )
A.不同的催化剂对化学反应速率的影响均相同
B.哈伯法合成氨是吸热反应,新法合成氨是放热反应
C.新法合成能在常温下进行是因为不需要断裂化学键
D.新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展愿景
13.化学反应A(g)+3B(g) 2C(g)+2D(g),在下列四个选项中是不同的情况下测得的不同物
质的反应速率,其中表示该化学反应的反应速率最慢的是( )
A.v(A)=0.20 mol·(L·min)-1 B.v(B)=0.45 mol·(L·s)-1
C.v(C)=0.30 mol·(L·min)-1 D.v(D)=0.35 mol·(L·min)-1
二、实验题
14.某研究性学习小组向一定量的NaHSO 溶液(加入少量淀粉)中加入稍过量的KIO 溶液,一
3 3段时间后,溶液突然变蓝色。通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影
响,记录如下。
溶液变蓝
0.01mol/LNaHSO 溶 0.01mol/L KIO 溶 反应温
3 3
编号 H O/mL 所用时间
2
液/mL 液/mL 度/°C
t/s
① 6.0 10.0 4.0 15 t
1
② 6.0 14.0 0 15 t
2
③ 6.0 a b 25 t
3
(1)实验①②是探究_______________对反应速率的影响,表中t _________t (填“>”、
1 2
“=”或“<”);实验①③是探究温度对反应速率的影响,表中a=_________,
b=_________。
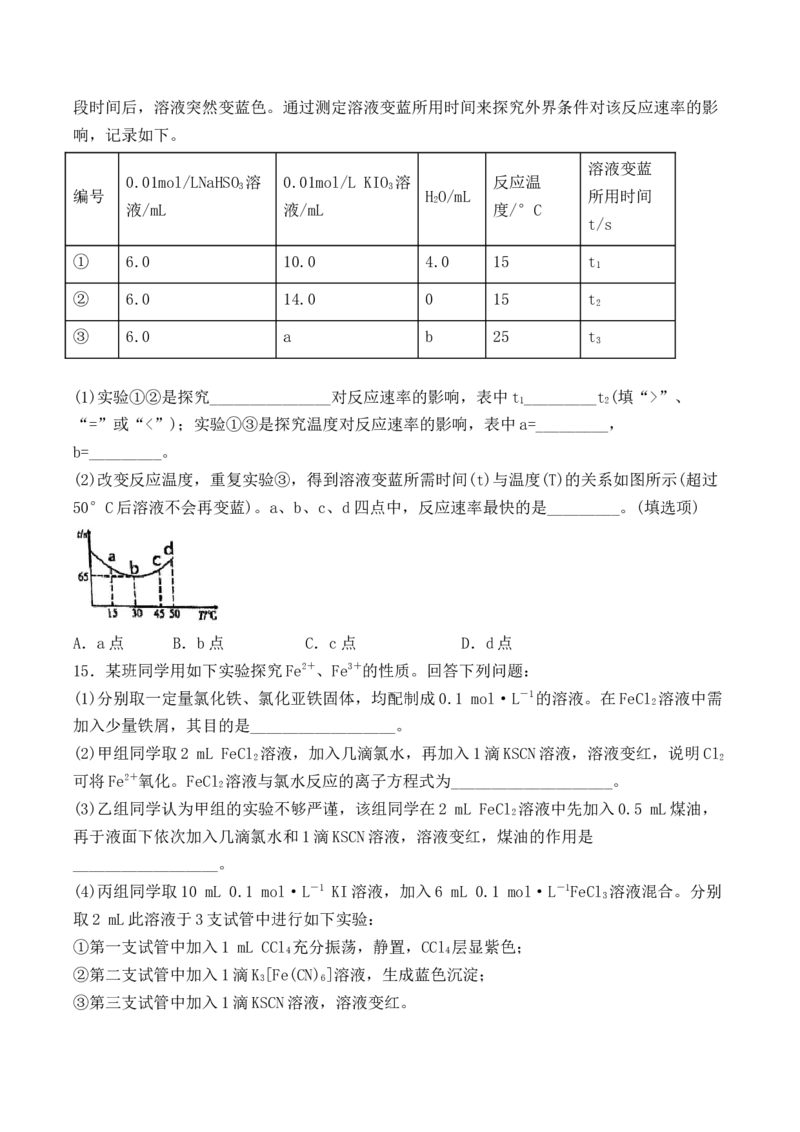
(2)改变反应温度,重复实验③,得到溶液变蓝所需时间(t)与温度(T)的关系如图所示(超过
50°C后溶液不会再变蓝)。a、b、c、d四点中,反应速率最快的是_________。(填选项)
A.a点 B.b点 C.c点 D.d点
15.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl 溶液中需
2
加入少量铁屑,其目的是__________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl
2 2
可将Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为____________________。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL煤油,
2
再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
__________________。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入6 mL 0.1 mol·L-1FeCl 溶液混合。分别
3
取2 mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡,静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K [Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中
仍含有Fe3+,由此可以证明该氧化还原反应为________________反应。(填可逆不可逆)。
(5)丁组同学向盛有H O 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色, 一段时
2 2 2
间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是___。
三、推断题
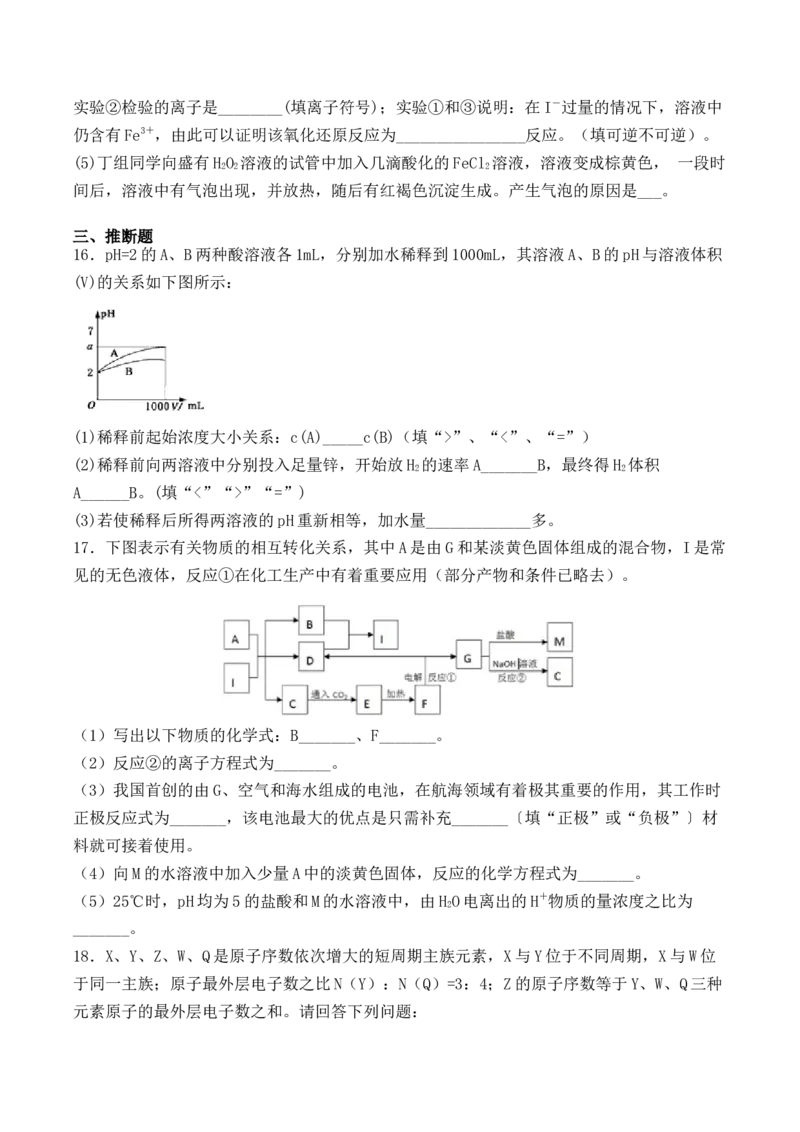
16.pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液A、B的pH与溶液体积
(V)的关系如下图所示:
(1)稀释前起始浓度大小关系:c(A)_____c(B)(填“>”、“<”、“=”)
(2)稀释前向两溶液中分别投入足量锌,开始放H 的速率A_______B,最终得H 体积
2 2
A______B。(填“<”“>”“=”)
(3)若使稀释后所得两溶液的pH重新相等,加水量_____________多。
17.下图表示有关物质的相互转化关系,其中A是由G和某淡黄色固体组成的混合物,I是常
见的无色液体,反应①在化工生产中有着重要应用(部分产物和条件已略去)。
(1)写出以下物质的化学式:B_______、F_______。
(2)反应②的离子方程式为_______。
(3)我国首创的由G、空气和海水组成的电池,在航海领域有着极其重要的作用,其工作时
正极反应式为_______,该电池最大的优点是只需补充_______〔填“正极”或“负极”〕材
料就可接着使用。
(4)向M的水溶液中加入少量A中的淡黄色固体,反应的化学方程式为_______。
(5)25℃时,pH均为5的盐酸和M的水溶液中,由H O电离出的H+物质的量浓度之比为
2
_______。
18.X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,X与Y位于不同周期,X与W位
于同一主族;原子最外层电子数之比N(Y):N(Q)=3:4;Z的原子序数等于Y、W、Q三种
元素原子的最外层电子数之和。请回答下列问题:(1)Y元素在周期表中的位置是______________;QX 的电子式为_____________。
4
(2)一种名为“PowerTrekk”的新型充电器是以化合物W Q和X Z为原料设计的,这两种化
2 2
合物相遇会反应生成W QZ 和气体X ,利用气体X 组成原电池提供能量。
2 3 2 2
①写出W Q和X Z反应的化学方程式:______________。
2 2
②以稀硫酸为电解质溶液,向两极分别通入气体X 和Z 可形成原电池,其中通入气体X 的一
2 2 2
极是_______(填“正极”或“负极”)。
③若外电路有3mol电子转移,则理论上需要W Q的质量为_________。
2
四、计算题
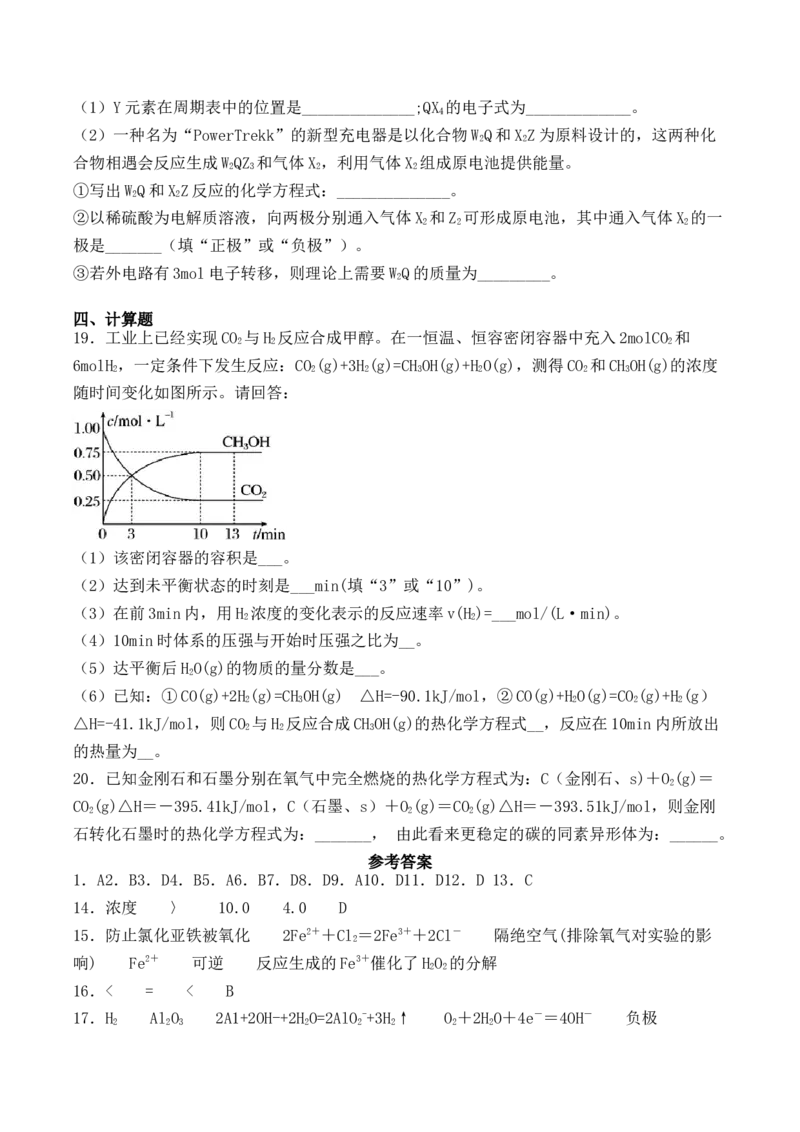
19.工业上已经实现CO 与H 反应合成甲醇。在一恒温、恒容密闭容器中充入2molCO 和
2 2 2
6molH ,一定条件下发生反应:CO (g)+3H (g)=CH OH(g)+H O(g),测得CO 和CH OH(g)的浓度
2 2 2 3 2 2 3
随时间变化如图所示。请回答:
(1)该密闭容器的容积是___。
(2)达到未平衡状态的时刻是___min(填“3”或“10”)。
(3)在前3min内,用H 浓度的变化表示的反应速率v(H )=___mol/(L·min)。
2 2
(4)10min时体系的压强与开始时压强之比为__。
(5)达平衡后H O(g)的物质的量分数是___。
2
(6)已知:①CO(g)+2H (g)=CH OH(g) △H=-90.1kJ/mol,②CO(g)+H O(g)=CO (g)+H (g)
2 3 2 2 2
△H=-41.1kJ/mol,则CO 与H 反应合成CH OH(g)的热化学方程式__,反应在10min内所放出
2 2 3
的热量为__。
20.已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(金刚石、s)+O (g)=
2
CO (g)△H=-395.41kJ/mol,C(石墨、s)+O (g)=CO (g)△H=-393.51kJ/mol,则金刚
2 2 2
石转化石墨时的热化学方程式为:_______, 由此看来更稳定的碳的同素异形体为:______。
参考答案
1.A2.B3.D4.B5.A6.B7.D8.D9.A10.D11.D12.D 13.C
14.浓度 〉 10.0 4.0 D
15.防止氯化亚铁被氧化 2Fe2++Cl =2Fe3++2Cl- 隔绝空气(排除氧气对实验的影
2
响) Fe2+ 可逆 反应生成的Fe3+催化了H O 的分解
2 2
16.< = < B
17.H Al O 2A1+2OH-+2H O=2AlO -+3H ↑ O +2H O+4e-=4OH- 负极
2 2 3 2 2 2 2 24AlCl +6Na O +6H O=4Al〔OH〕 ↓+12NaCl+3O ↑ 1∶104
3 2 2 2 3 2
18.第二周期第ⅢA族 负极 37g
19.2L 3 0.225 mol/(L·min) 30% CO (g)+3H (g)=CH OH(g)+H O(g)
2 2 3 2
△H =-49 kJ/mol 98 kJ
20.C( 金刚石,s )=C( 石墨,s ) △ H=-1.9kJ/mol 石墨